МИНИСТЕРСТВО ОБРАЗОВАНИЯ И НАУКИ УКРАИНЫ Национальный технический университет Украины Факультет биотехнологии и биотехники;
Содержание
- 2. Фенилкетонурия Одним из наиболее распространенных наследственных заболеваний является фенилкетонурия В Украине на 8300 новорожденных один ребенок
- 3. Фенилаланингидроксилаза катализирует реакцию преобразования фенилаланин + О2 + тетрагидробиоптерин ↓ тирозин + вода + окисленный биоптерин
- 4. Цель работы Провести ДНК-анализ мутаций и полиморфизма гена ФАГ и оптимизировать технологию проведения полимеразной цепной реакции
- 5. Для достижения цели были поставлены основные задачи исследования: ДНК-анализ мутаций R408W, R158Q, Y414C, IVS10nt546, IVS12nt1 гена
- 6. Объект и предмет исследования Объект исследования - ДНК человека полученная из лейкоцитов периферической крови Предмет исследования
- 7. Методы: Выделение и очистка ДНК; амплификация in vitro последовательностей гена ФАГ методом полимеразной цепной реакции; рестрикционный
- 8. Этапы ДНК-анализа: Выделение геномной ДНК из образцов венозной крови методом фенольной экстракции; Амплификация in vitro фрагмента
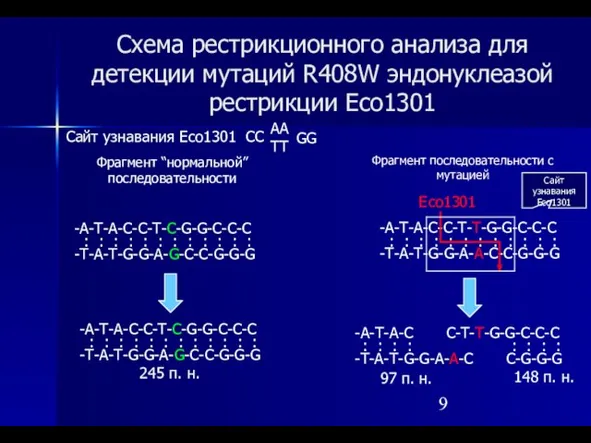
- 9. Схема рестрикционного анализа для детекции мутаций R408W эндонуклеазой рестрикции Eco1301 Сайт узнавания Eco1301 CC -A-T-A-C-C-T-C-G-G-C-C-C -T-A-T-G-G-A-G-C-C-G-G-G
- 10. Анализ мутации R408W. 1 2 3 4 1, 2 – R408W/норма, 3 – норма/норма, 4 –
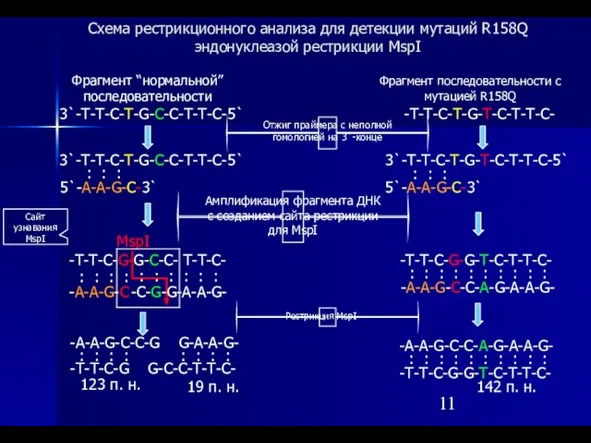
- 11. : : : : 19 п. н. Фрагмент “нормальной” последовательности Фрагмент последовательности с мутацией R158Q -A-A-G-C
- 12. Анализ мутации R158Q. 123 п.н. 119 п.н. 1 2 3 4 1, 2 - R158Q/норма; 3,
- 13. На первом этапе мы рассматривали четыре паралельно протикающие реакции: ДНК+Pr →ДНК.Pr Образование комплекса ДНК.Pr ДНК.Pr →ДНК+Pr
- 14. Концентрации реагентов описываются системой диф. уравнений: Решив данную систему мы получили:
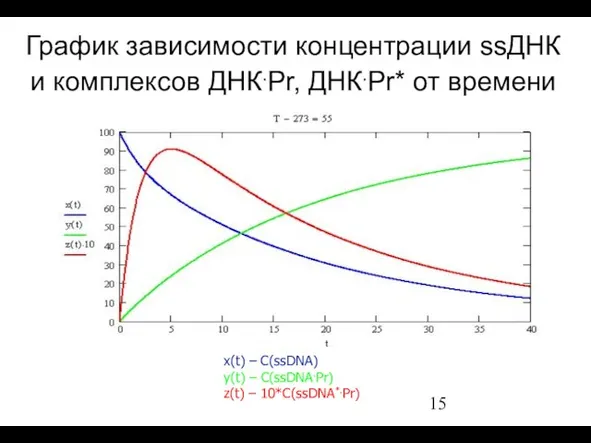
- 15. График зависимости концентрации ssДНК и комплексов ДНК.Pr, ДНК.Pr* от времени x(t) – C(ssDNA) y(t) – C(ssDNA.Pr)
- 16. На втором этапе мы рассматривали шесть паралельно протикающие реакции: ДНК+Pr →ДНК.Pr Образование комплекса ДНК.Pr ДНК.Pr →ДНК+Pr
- 17. Данные процессы описываются системой диф. уравнений:
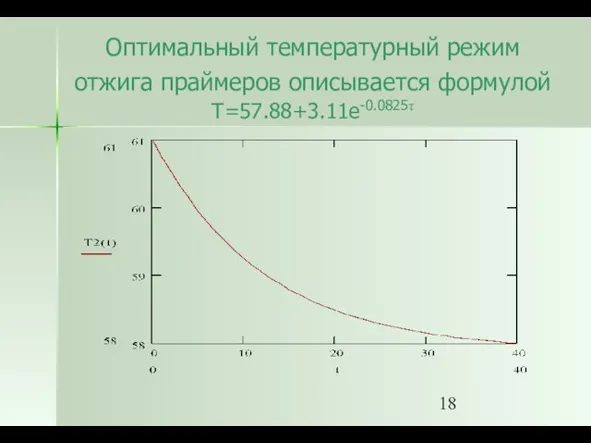
- 18. Оптимальный температурный режим отжига праймеров описывается формулой T=57.88+3.11e-0.0825τ
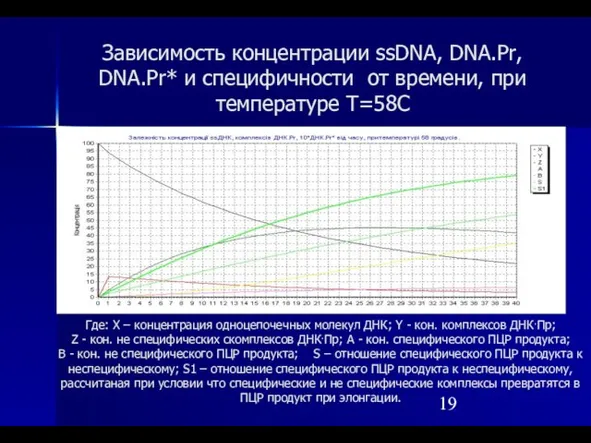
- 19. Зависимость концентрации ssDNA, DNA.Pr, DNA.Pr* и специфичности от времени, при температуре T=58С Где: X – концентрация
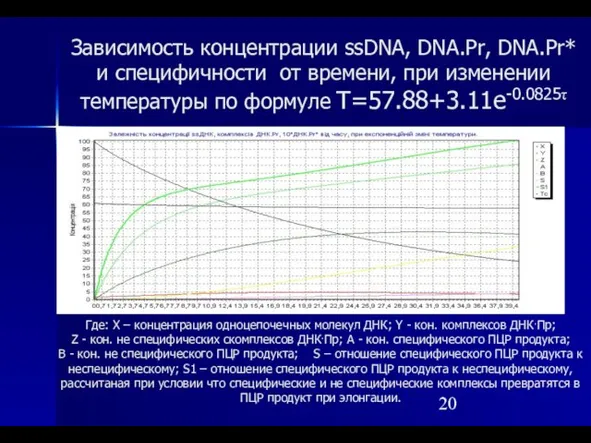
- 20. Зависимость концентрации ssDNA, DNA.Pr, DNA.Pr* и специфичности от времени, при изменении температуры по формуле T=57.88+3.11e-0.0825τ Где:
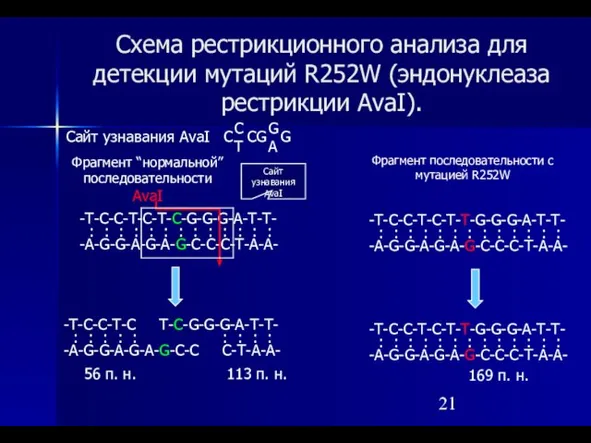
- 21. Схема рестрикционного анализа для детекции мутаций R252W (эндонуклеаза рестрикции AvaI). -T-C-C-T-C-T-C-G-G-G-A-T-T- -A-G-G-A-G-A-G-C-C-C-T-A-A- : : : :
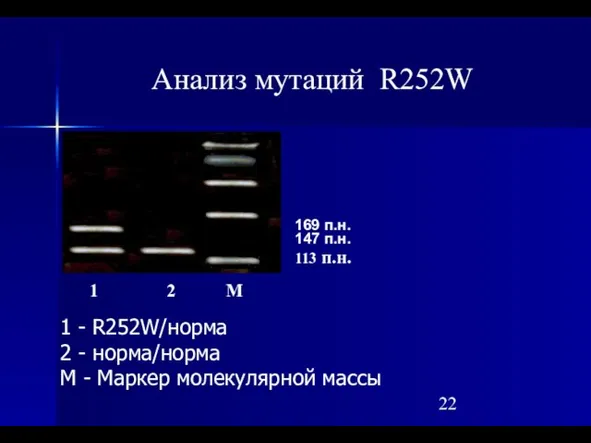
- 22. Анализ мутаций R252W 1 - R252W/норма 2 - норма/норма М - Маркер молекулярной массы
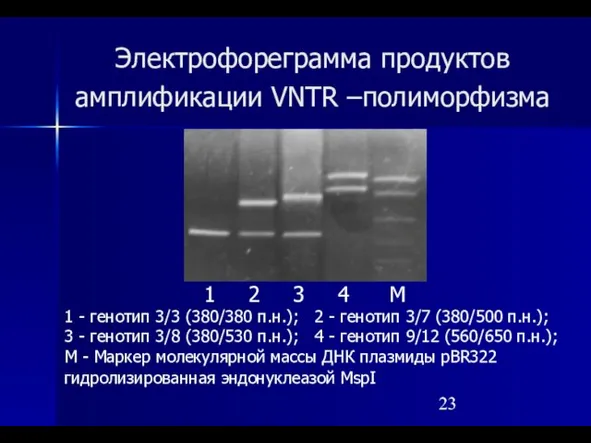
- 23. Электрофореграмма продуктов амплификации VNTR –полиморфизма 1 2 3 4 М 1 - генотип 3/3 (380/380 п.н.);
- 24. Выводы 1. Проведен ДНК-анализ мутаций R408W, IVS12nt1, R158Q, Y414C, IVS10nt546 гена ФАГ в 68 образцах. Двадцать
- 26. Скачать презентацию














 Describing your house
Describing your house Схема монтажа перекрытия СПМ-350 на несущих стенах
Схема монтажа перекрытия СПМ-350 на несущих стенах несеп тас.срс
несеп тас.срс Основы английского языка
Основы английского языка Рекомендации по оформлению и защите научноисследовательской работы. Оформление сопроводительных документов
Рекомендации по оформлению и защите научноисследовательской работы. Оформление сопроводительных документов Идиостиль автора: квантитативный анализ и его филологическая интерпретация
Идиостиль автора: квантитативный анализ и его филологическая интерпретация Тесто для пельменей, вареников и домашней лапши
Тесто для пельменей, вареников и домашней лапши Литература Великобритании XX века
Литература Великобритании XX века Правила санитарии, гигиены и безопасной работы
Правила санитарии, гигиены и безопасной работы Лимфангит лимфаденит абсцесс флегмона
Лимфангит лимфаденит абсцесс флегмона Презентация на тему Фольклор урок
Презентация на тему Фольклор урок  Комитет по взаимодействию с миноритарными акционерами Сбербанка России
Комитет по взаимодействию с миноритарными акционерами Сбербанка России Ассирийская держава
Ассирийская держава Материальная часть стрелкового оружия
Материальная часть стрелкового оружия Наука в политехническом
Наука в политехническом Презентация на тему Внутренние воды Австралии
Презентация на тему Внутренние воды Австралии  Фотоэксперименты
Фотоэксперименты Игрушки и сувениры из Сергиева Посада и англоязычных стран
Игрушки и сувениры из Сергиева Посада и англоязычных стран Основные методики оценки закрытых компаний
Основные методики оценки закрытых компаний Presentation Mali-Russia
Presentation Mali-Russia Основы мировых религиозных культур
Основы мировых религиозных культур Возможности роста финансирования для компаний на ежегодном этапе L.N Innovative Technologies Ltd.Haifa, Israel
Возможности роста финансирования для компаний на ежегодном этапе L.N Innovative Technologies Ltd.Haifa, Israel Деньги–оплатники. Фальшивые деньги – ложники
Деньги–оплатники. Фальшивые деньги – ложники Доказывание и доказательства
Доказывание и доказательства СКАЗКА О ЛЮБОПЫТНОМ ДУХЕ
СКАЗКА О ЛЮБОПЫТНОМ ДУХЕ Библейские сказания в искусстве
Библейские сказания в искусстве Зачем нужны обращения
Зачем нужны обращения Влияние музыки на детей
Влияние музыки на детей