Содержание
- 2. Современная фармакотерапия: высокоактивная («агрессивная», но много ОТС), обезличенная (официнальная, «перегрузка» MR), вариабельная (старение популяции, экофакторы), комбинированная
- 3. Масштаб проблем безопасности ЛС оценивается результатами фармако-эпидемиологических исследований: В США: 3,5-8,8 млн. пациентов ежегодно госпитализируется вследствие
- 4. Контроль безопасности ЛС – это выявление, анализ и предупреждение любых возможных проблем, связанных с ЛС (медицинских
- 5. Медицинские проблемы, связанные с ЛС. 1. Нежелательные побочные реакции (НПР). 2. Off-label (не по инструкции); и
- 6. Типы НПР (классификация ВОЗ)
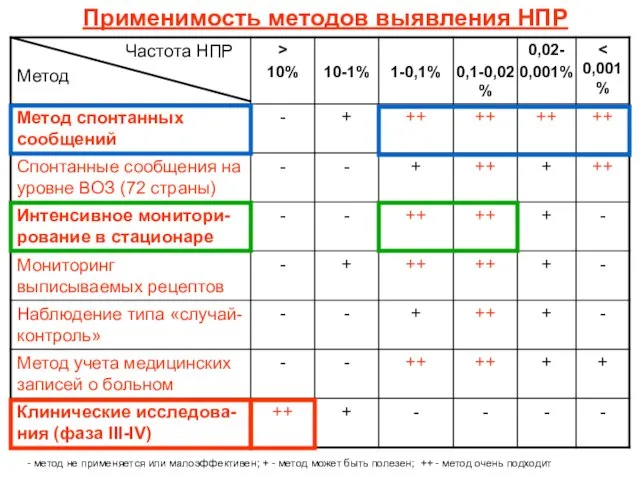
- 7. Применимость методов выявления НПР - метод не применяется или малоэффективен; + - метод может быть полезен;
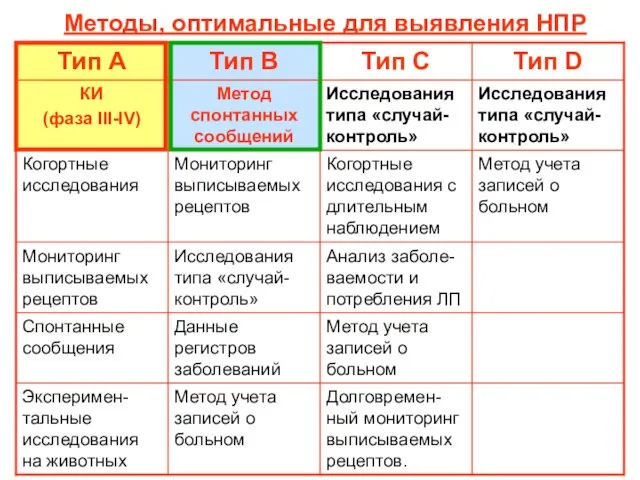
- 8. Методы, оптимальные для выявления НПР
- 9. Цель системы контроля безопасности – это снижение заболеваемости и смертности, вызываемых ЛС. Безопасность ЛП должна изучаться
- 10. Этапы исследования безопасности ЛС: ДКИ (вероятность предсказания переносимости человеком – 65-70%) КИ (выявляют риск НПР ⊇1%)
- 11. Для чего нужна фаза-4 ? В связи с тем, что ДКИ и КИ не позволяют выявить
- 12. Развитие систем контроля безопасности ЛС США: 1906 г. - Харли Вашингтон Вайли - “Бюро Химии” (с
- 13. Национальные центры контроля безопасности Включенные в структуру контрольно-разрешительных систем, регламентирующих обращение ЛС: США, Канада, Австралия, ФРГ,
- 14. Международное сотрудничество в области контроля безопасности ЛС 1962 г. (через 9 месяцев после выявления «талидомидовой эпидемии»)
- 15. Рекомендации по совершенствованию службы контроля безопасности ЛП Повышение уровня компетенции мед.и фарм.работников – введение в программы
- 17. Скачать презентацию












 Федерализм
Федерализм Молоко
Молоко Производная и её геометрический смысл
Производная и её геометрический смысл Инвестиционно-финансовая группа
Инвестиционно-финансовая группа Беспроводная передача электричества
Беспроводная передача электричества Презентация на тему Кодирование графической информации
Презентация на тему Кодирование графической информации Использование деятельного подхода в ОД при формировании ОБЖ
Использование деятельного подхода в ОД при формировании ОБЖ Он-лайн система управленческого учета
Он-лайн система управленческого учета Типы реакций
Типы реакций Энергия солнца в Вашем Доме!
Энергия солнца в Вашем Доме! Московские лабораторииэкономики и технологии знанийпредставляют
Московские лабораторииэкономики и технологии знанийпредставляют Электроёмкость. Конденсаторы
Электроёмкость. Конденсаторы Измерение высоты здания разными способами
Измерение высоты здания разными способами Словообразования
Словообразования Восточная Европа
Восточная Европа Презентация на тему Инвестиции
Презентация на тему Инвестиции Получение наличных средств в сети круглосуточных банкоматов Сбербанка России и других банков по всему миру Безналичная оплата то
Получение наличных средств в сети круглосуточных банкоматов Сбербанка России и других банков по всему миру Безналичная оплата то Предпосылки петровских преобрахований
Предпосылки петровских преобрахований Люблю я Кавказ
Люблю я Кавказ Принцип построения сети ОКС №7. Режимы сигнализации
Принцип построения сети ОКС №7. Режимы сигнализации Программы обучения онлайн 2020
Программы обучения онлайн 2020 Дорогие ребята! Мы шагаем в проект «Среди миров»
Дорогие ребята! Мы шагаем в проект «Среди миров» Кашира
Кашира International Corporate Match Race 10-11 September 2011 Yacht Club of Greece
International Corporate Match Race 10-11 September 2011 Yacht Club of Greece Уголовный процесс Чешской республики
Уголовный процесс Чешской республики Парад студенчества 2018
Парад студенчества 2018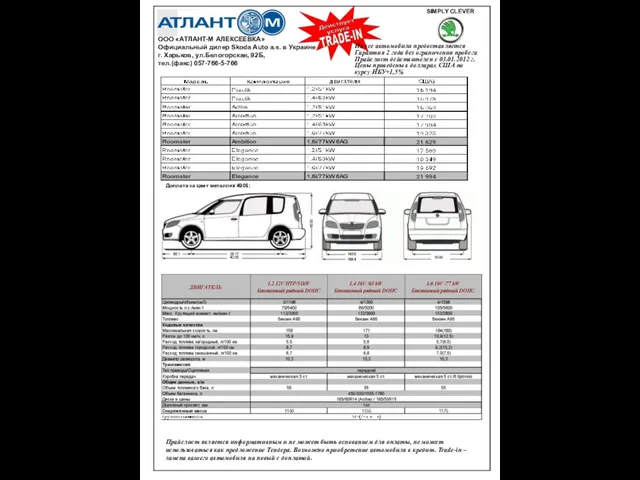 На все автомобили предоставляется Гарантия 2 года без ограничения пробега Прайслист действителен с 03.01.2012 г. Цены приведены в долла
На все автомобили предоставляется Гарантия 2 года без ограничения пробега Прайслист действителен с 03.01.2012 г. Цены приведены в долла О создании Восточно-Сибирского научно образовательного инновационного комплекса в Республике Бурятия
О создании Восточно-Сибирского научно образовательного инновационного комплекса в Республике Бурятия