Содержание
- 2. Углубить и обобщить знания о состоянии химического равновесия, условиях его смещения. Дать понятие о константе равновесия.
- 3. Какие из химических реакций являются обратимыми? 1. NaOH + HCl ? NaCl + H2O 2. N2
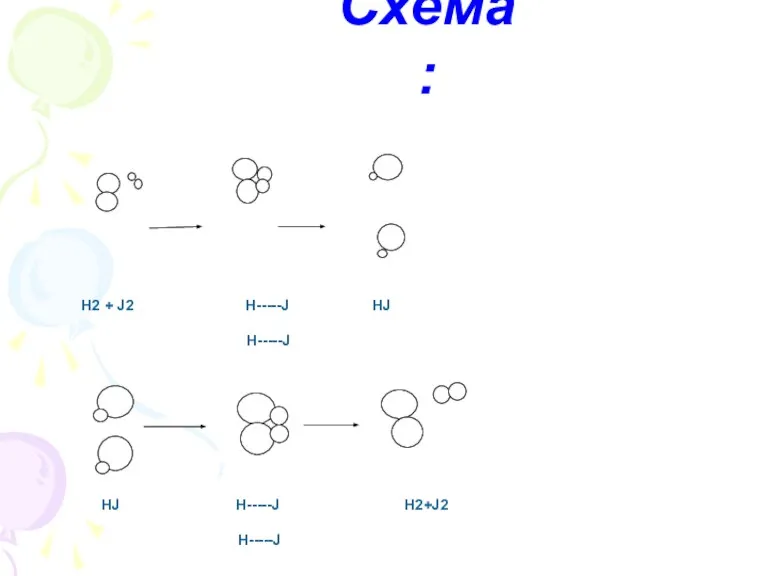
- 4. Схема: Н2 + J2 Н-----J HJ Н-----J HJ Н-----J H2+J2 Н-----J
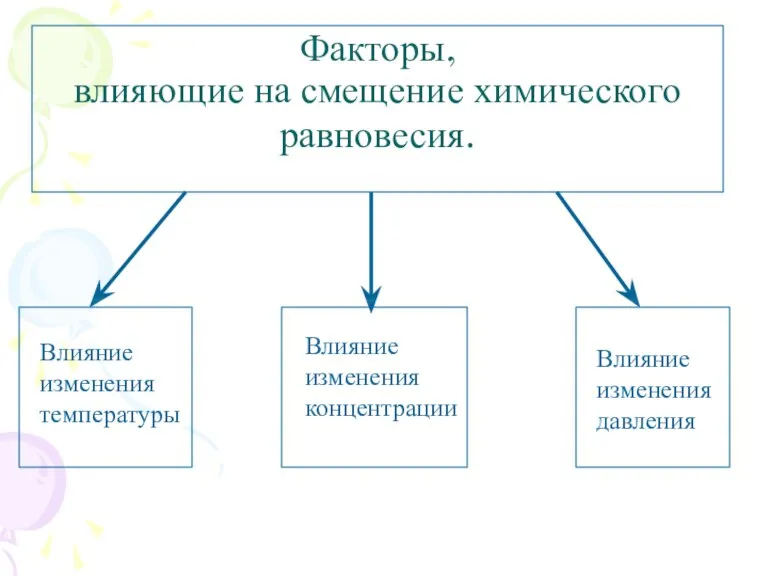
- 6. Факторы, влияющие на смещение химического равновесия.
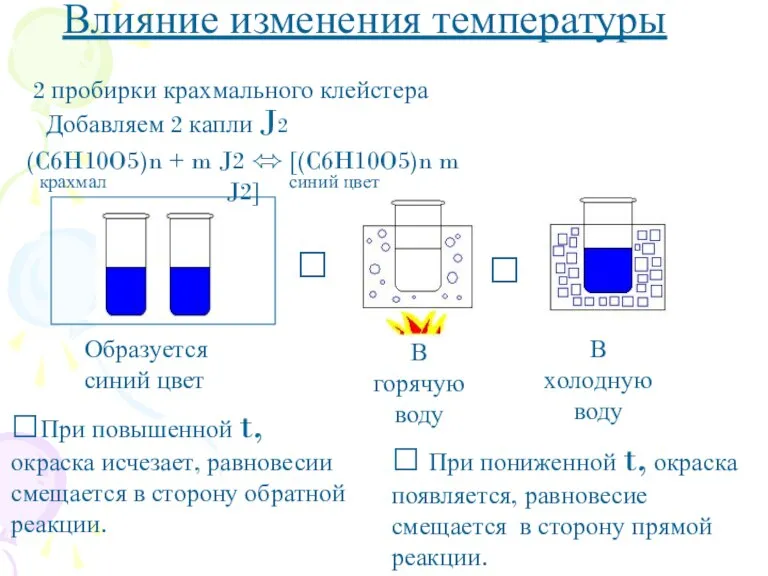
- 7. ? ? Влияние изменения температуры 2 пробирки крахмального клейстера Добавляем 2 капли J2 ?При повышенной t,
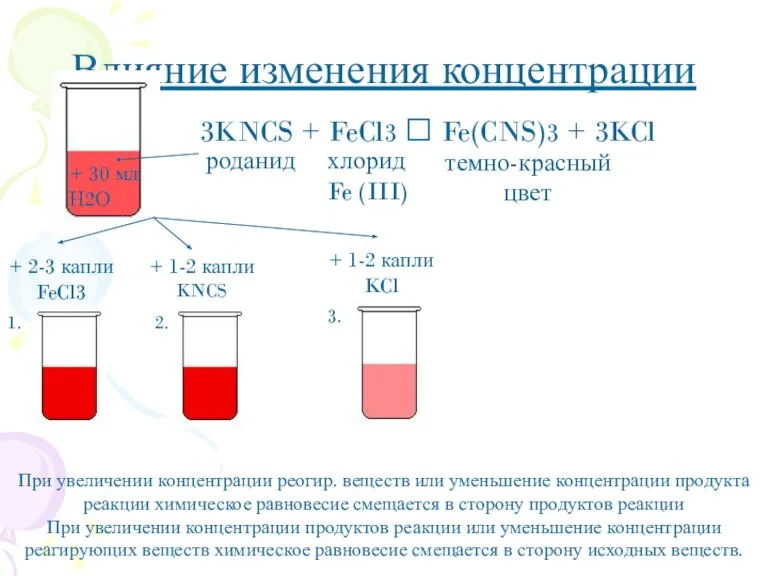
- 8. Влияние изменения концентрации + 2-3 капли FeCl3 + 1-2 капли KNCS + 1-2 капли KCl При
- 9. Влияние изменения давления 2NO2 ⬄ N2O4 + Q При расширении цвет газа стал темно-бурым, а равновесие
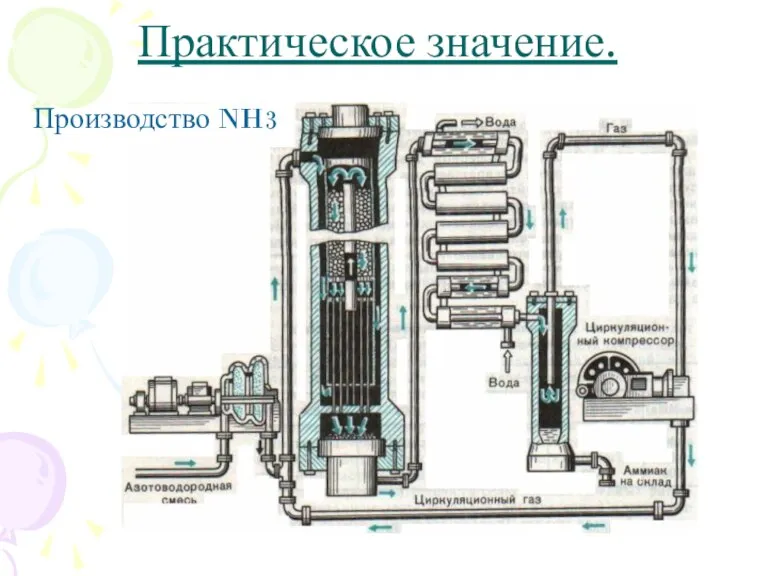
- 10. Практическое значение. Производство NH3
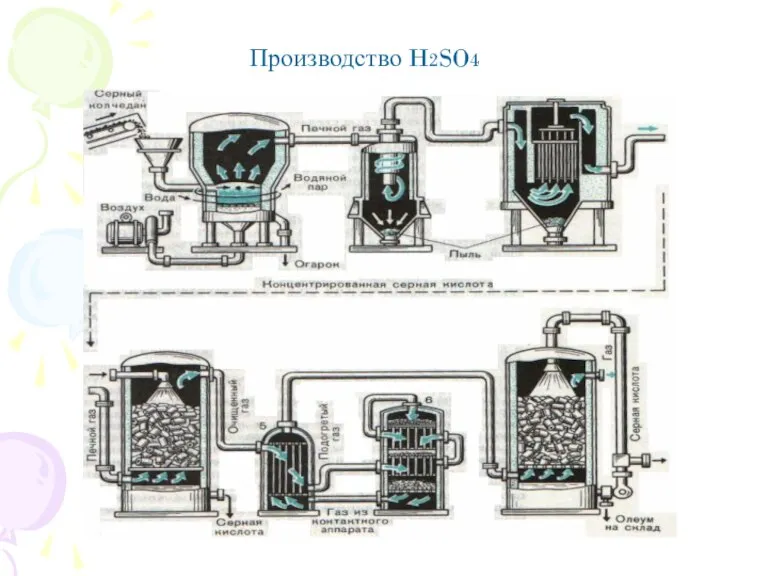
- 11. Производство H2SO4
- 12. Производство HNO3
- 13. 1.Смещение химического равновесия обеспечивает высокий выход желаемого продукта. 2. Открывает путь к управлению химическими реакциями.
- 16. Скачать презентацию





 Famous people of Russia
Famous people of Russia ВЫПУСКНИКУ ШКОЛЫ
ВЫПУСКНИКУ ШКОЛЫ Лёгкая атлетика, гимнастика: общеприкладные упражнения. Баскетбол: односторонняя игра
Лёгкая атлетика, гимнастика: общеприкладные упражнения. Баскетбол: односторонняя игра Поиск информации в Интернет (web)
Поиск информации в Интернет (web) Большакова В.П.Галустьян С.А.
Большакова В.П.Галустьян С.А. Искусство общения
Искусство общения سنگ مزار
سنگ مزار Команда Bell Integrator. Нeограниченные возможности карьерного роста
Команда Bell Integrator. Нeограниченные возможности карьерного роста Страхование торговых кредитов.
Страхование торговых кредитов. Тренинги
Тренинги Жизнь и творчество Александра Солженицына
Жизнь и творчество Александра Солженицына Особенности реализации туристского продукта туроператором/турагентом
Особенности реализации туристского продукта туроператором/турагентом Распределение базы данных
Распределение базы данных Презентация на тему Охрана труда и техника безопасности Инструкция ИОТ-014-2004
Презентация на тему Охрана труда и техника безопасности Инструкция ИОТ-014-2004  Диалог по телефону
Диалог по телефону riding a horse
riding a horse Воля и пути её формирования у учащихся
Воля и пути её формирования у учащихся Уклады жизни образовательной организации
Уклады жизни образовательной организации Презентация на тему Страницы истории Страницы истории XIX века
Презентация на тему Страницы истории Страницы истории XIX века  Звуки [й], [о], обозначение их буквой ё
Звуки [й], [о], обозначение их буквой ё Повторяем Западно-Сибирский экономический район
Повторяем Западно-Сибирский экономический район People power for a harmonious and long-lasting family
People power for a harmonious and long-lasting family Услуги сети ISDN
Услуги сети ISDN Циркуляр о кухаркинных детях
Циркуляр о кухаркинных детях Презентация на тему Вулканологи
Презентация на тему Вулканологи Культура в СССР в 20— 30 -е гг
Культура в СССР в 20— 30 -е гг Основы религиозных культур и светской этики
Основы религиозных культур и светской этики Солдаты России
Солдаты России