Содержание
- 2. Внутренняя энергия Сумма кинетических энергий хаотического движения всех частиц тела относительно центра масс тела (молекул, атомов)
- 3. Внутренняя энергия одноатомного идеального газа Для идеального газа: U=U(T), т.к. взаимодействием на расстоянии пренебрегаем или Внутренняя
- 4. Способы изменения внутренней энергии Совершение работы А над телом ( U увелич.) самим телом (U уменьш.)
- 5. Работа в термодинамике По третьему закону Ньютона: Работа внешних сил над газом: Работа газа:
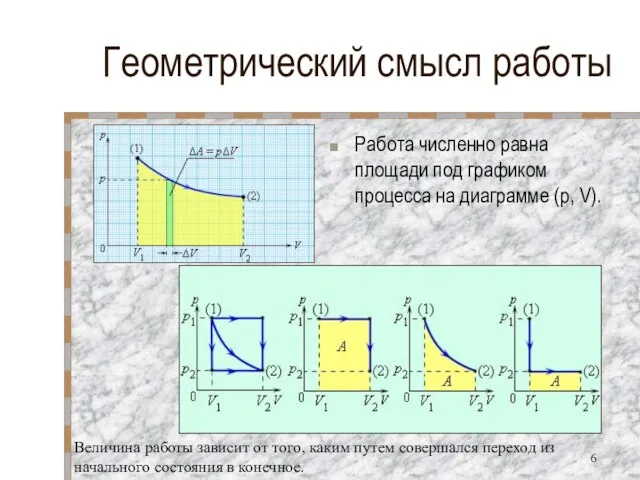
- 6. Геометрический смысл работы Работа численно равна площади под графиком процесса на диаграмме (p, V). Величина работы
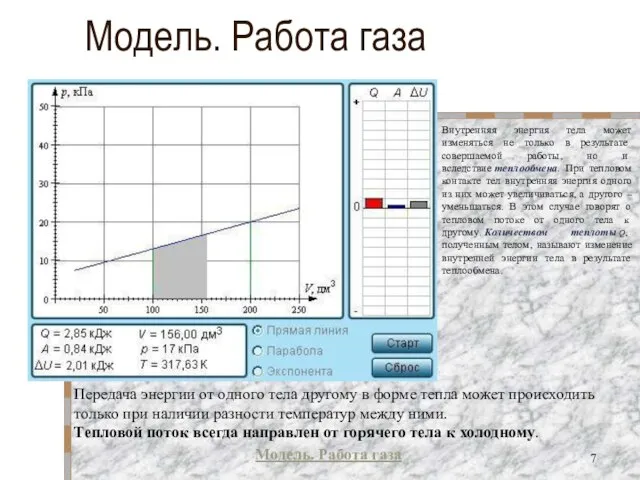
- 7. Модель. Работа газа Модель. Работа газа Внутренняя энергия тела может изменяться не только в результате совершаемой
- 8. Количество теплоты Q = cm(t02-t01) – нагревание (охлаждение) Q=±λm - плавление (отвердевание) Q = ±Lm -
- 9. Первый закон термодинамики Обмен энергией между термодинамической системой и окружающими телами в результате теплообмена и совершаемой
- 10. Первый закон термодинамики Изменение внутренней энергии системы при переходе ее из одного состояния в другое равно
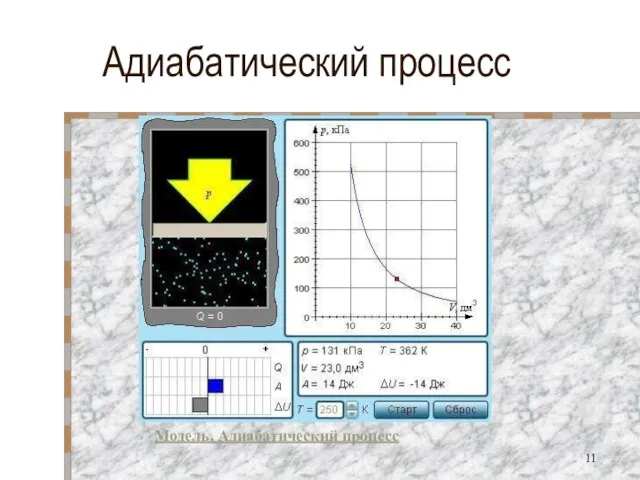
- 11. Адиабатический процесс Модель. Адиабатический процесс
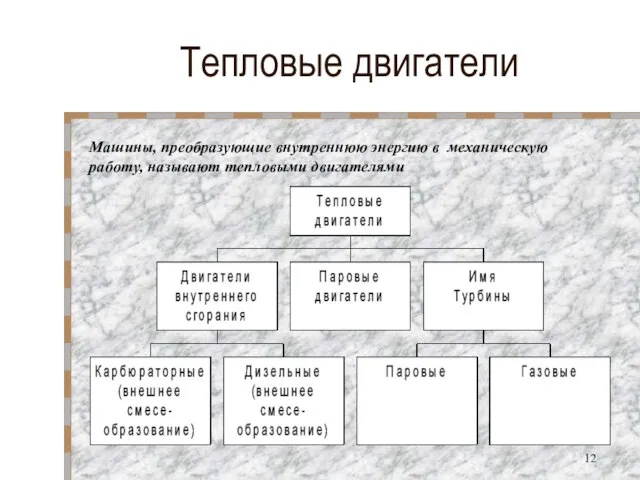
- 12. Тепловые двигатели Машины, преобразующие внутреннюю энергию в механическую работу, называют тепловыми двигателями
- 13. Термодинамический цикл Круговой процесс на диаграмме (p, V). Реально существующие тепловые двигатели (паровые машины, двигатели внутреннего
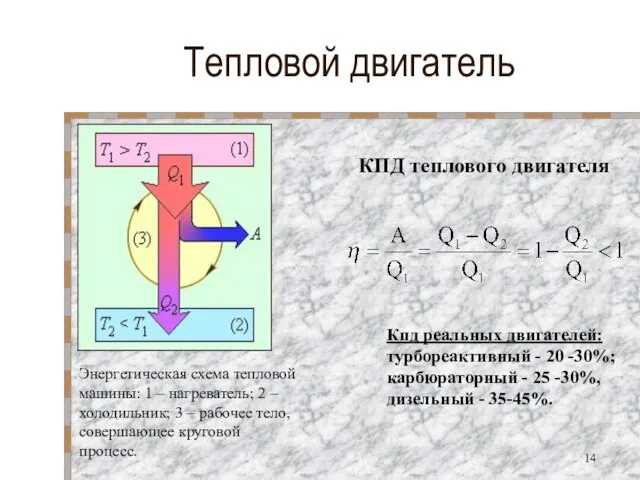
- 14. Тепловой двигатель КПД теплового двигателя Кпд реальных двигателей: турбореактивный - 20 -30%; карбюраторный - 25 -30%,
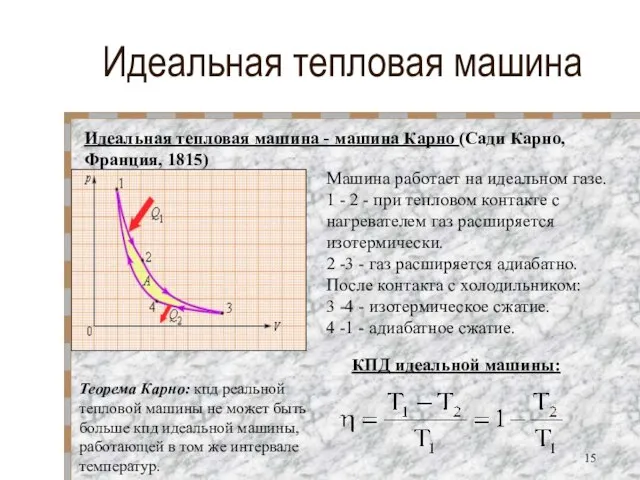
- 15. Идеальная тепловая машина Идеальная тепловая машина - машина Карно (Сади Карно, Франция, 1815) Машина работает на
- 16. Второй закон термодинамики Второй з-н термодинамики указывает направление возможных энергетических превращений и тем самым выражает необратимость
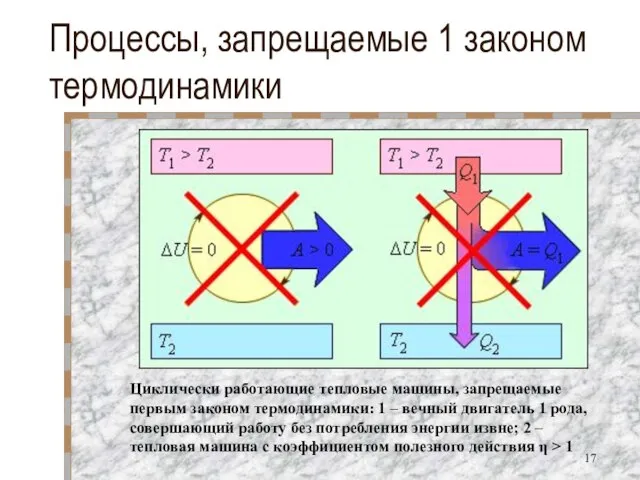
- 17. Процессы, запрещаемые 1 законом термодинамики Циклически работающие тепловые машины, запрещаемые первым законом термодинамики: 1 – вечный
- 19. Скачать презентацию









 Презентация на тему Километр (3 класс)
Презентация на тему Километр (3 класс) Известные имена. Софья Ковалевская
Известные имена. Софья Ковалевская Особенности кризиса 2008-2ХХХгг.
Особенности кризиса 2008-2ХХХгг. Графика
Графика Общие вопросы антибактериальной терапии
Общие вопросы антибактериальной терапии Составное глагольное сказуемое
Составное глагольное сказуемое Ch1 - Lecture2
Ch1 - Lecture2 Увеличительные приборы
Увеличительные приборы Болат өндірісінің теориясы мен технологиясы
Болат өндірісінің теориясы мен технологиясы Международные транспортные коридоры
Международные транспортные коридоры Гравюра
Гравюра Природно-климатические условия среды обитания и здоровье человека. Акклиматизация и ее гигиеническое значение. Солнечная радиаци
Природно-климатические условия среды обитания и здоровье человека. Акклиматизация и ее гигиеническое значение. Солнечная радиаци Кайнозойская эра
Кайнозойская эра Греция сегодня
Греция сегодня Алгоритм с ветвлением в среде программирования Turbo Pascal
Алгоритм с ветвлением в среде программирования Turbo Pascal ИСКУССТВО ОРИГАМИ
ИСКУССТВО ОРИГАМИ Параметры областного бюджета Тверской области на 2008-2010 годы
Параметры областного бюджета Тверской области на 2008-2010 годы 90 лет ГТО
90 лет ГТО Декоративные народные промыслы
Декоративные народные промыслы Возникновение и развитие логистики
Возникновение и развитие логистики PO
PO Композиция (от лат. compositio)
Композиция (от лат. compositio) Библиотека – как информационная база. Структура библиотеки ВГУЭС
Библиотека – как информационная база. Структура библиотеки ВГУЭС Психологические особенности младших школьников с общим недоразвитием речи
Психологические особенности младших школьников с общим недоразвитием речи Презентация на тему Эра космонавтики
Презентация на тему Эра космонавтики  Чернышов Вадим Геннадьевич. Сертификат участника
Чернышов Вадим Геннадьевич. Сертификат участника САПР ТП ВЕРТИКАЛЬ
САПР ТП ВЕРТИКАЛЬ История развития психопатологии в России
История развития психопатологии в России