Слайд 2Цели и задачи урока:
Выяснить источник кислорода в природе; познакомиться с лабораторными и

промышленными способами получения кислорода
Познакомиться с понятием о катализаторе
Познакомиться с важнейшими химическими свойствами кислорода
Научиться давать названия оксидам
Слайд 3*
Способы получения кислорода
1) В природе кислород образуется в процессе фотосинтеза
2) В

промышленности его получают перегонкой сжиженного воздуха при t = - 1830 С
Слайд 4 3) В лаборатории кислород получают реакциями разложения:
а) воды под действием электрического

тока (электролиз):
2H2O → 2H2 + O2
б) пероксида водорода под действием MnO2:
MnO2
2Н2О2 → 2Н2О + О2
Слайд 5Разложение перекиси водорода в присутствии оксида марганца (IV)

Слайд 6! Катализатор – вещество, которое изменяет скорость реакции, но само при этом

не расходуется
Слайд 7*
в) перманганата калия при нагревании:
2KMnO4 → K2MnO4 + MnO2 + O2

Разложение этой соли идёт при нагревании её
выше 2000 С
Слайд 8Как проверить, собрался ли кислород в сосуде?
Подумайте …

Слайд 9*
Проверка собравшегося кислорода

Слайд 10*
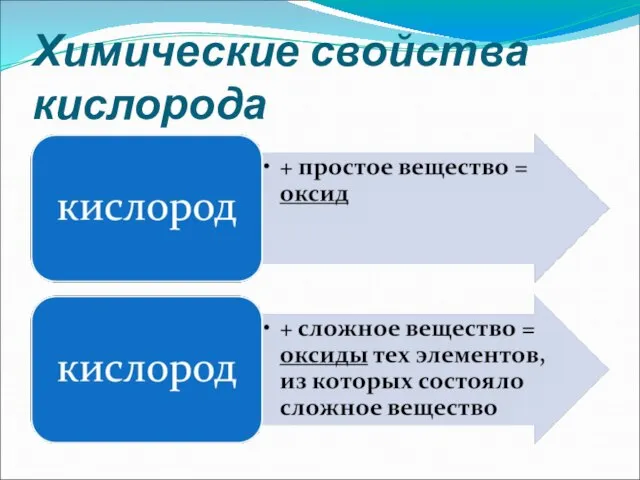
Химические свойства кислорода
Допишите уравнения реакций:
Ca + O2 →
Na + O2 →
Al

+ O2 →
S + O2 →
H2S + O2 →
CH4 + O2→
Слайд 12Оксиды – это сложные вещества, состоящие из двух элементов, одним из которых

является кислород
Слайд 13Названия оксидов
Слово «оксид»
+ название элемента в родительном падеже
+ валентность элемента

в данном оксиде (если она переменная)
Слайд 14Реакции с участием кислорода
Реакции взаимодействия веществ с кислородом относятся к реакциям окисления
Реакции

взаимодействия веществ с кислородом, протекающие с выделением большого количества тепла и света, называются реакциями горения












 Федерализм
Федерализм Молоко
Молоко Производная и её геометрический смысл
Производная и её геометрический смысл Инвестиционно-финансовая группа
Инвестиционно-финансовая группа Беспроводная передача электричества
Беспроводная передача электричества Презентация на тему Кодирование графической информации
Презентация на тему Кодирование графической информации Использование деятельного подхода в ОД при формировании ОБЖ
Использование деятельного подхода в ОД при формировании ОБЖ Он-лайн система управленческого учета
Он-лайн система управленческого учета Типы реакций
Типы реакций Энергия солнца в Вашем Доме!
Энергия солнца в Вашем Доме! Московские лабораторииэкономики и технологии знанийпредставляют
Московские лабораторииэкономики и технологии знанийпредставляют Электроёмкость. Конденсаторы
Электроёмкость. Конденсаторы Измерение высоты здания разными способами
Измерение высоты здания разными способами Словообразования
Словообразования Восточная Европа
Восточная Европа Презентация на тему Инвестиции
Презентация на тему Инвестиции Получение наличных средств в сети круглосуточных банкоматов Сбербанка России и других банков по всему миру Безналичная оплата то
Получение наличных средств в сети круглосуточных банкоматов Сбербанка России и других банков по всему миру Безналичная оплата то Предпосылки петровских преобрахований
Предпосылки петровских преобрахований Люблю я Кавказ
Люблю я Кавказ Принцип построения сети ОКС №7. Режимы сигнализации
Принцип построения сети ОКС №7. Режимы сигнализации Программы обучения онлайн 2020
Программы обучения онлайн 2020 Дорогие ребята! Мы шагаем в проект «Среди миров»
Дорогие ребята! Мы шагаем в проект «Среди миров» Кашира
Кашира International Corporate Match Race 10-11 September 2011 Yacht Club of Greece
International Corporate Match Race 10-11 September 2011 Yacht Club of Greece Уголовный процесс Чешской республики
Уголовный процесс Чешской республики Парад студенчества 2018
Парад студенчества 2018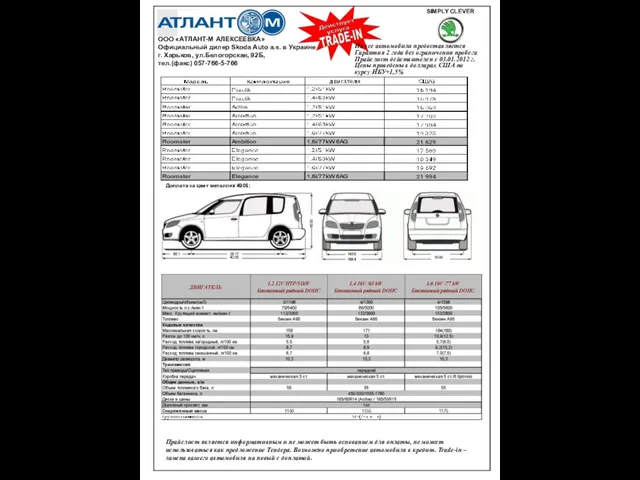 На все автомобили предоставляется Гарантия 2 года без ограничения пробега Прайслист действителен с 03.01.2012 г. Цены приведены в долла
На все автомобили предоставляется Гарантия 2 года без ограничения пробега Прайслист действителен с 03.01.2012 г. Цены приведены в долла О создании Восточно-Сибирского научно образовательного инновационного комплекса в Республике Бурятия
О создании Восточно-Сибирского научно образовательного инновационного комплекса в Республике Бурятия