Содержание
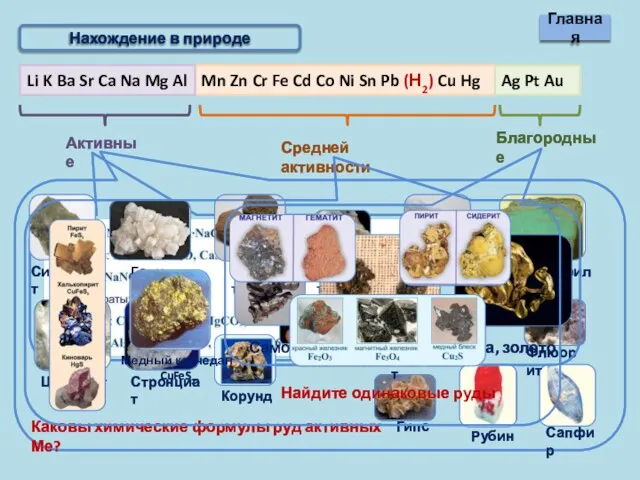
- 2. Металлы Нахождение в природе Внешний вид и условия хранения Получение металлов Химические свойства металлов Соединения металлов
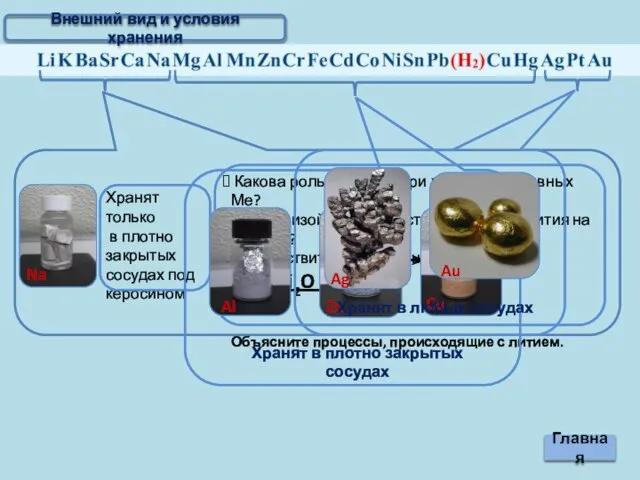
- 3. Внешний вид и условия хранения
- 4. Внешний вид и условия хранения Главная
- 5. Mn Zn Cr Fe Cd Co Ni Sn Pb (Н2) Cu Hg Li K Ba Sr
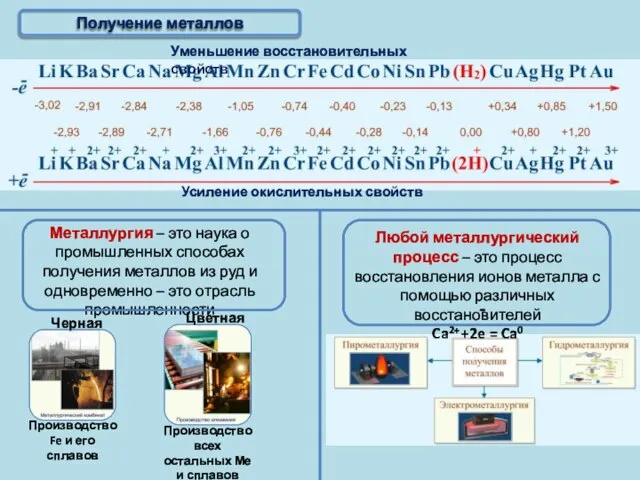
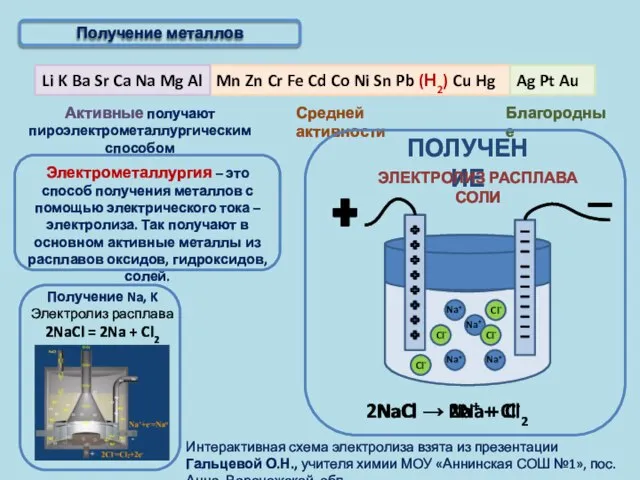
- 6. Получение металлов
- 7. Активные получают пироэлектрометаллургическим способом Благородные Получение металлов Электрометаллургия – это способ получения металлов с помощью электрического
- 8. Активные получают пироэлектрометаллургическим способом Благородные Получение металлов T 950°C, Al2O3 в расплаве криолита (Na3AlF6); на катоде:
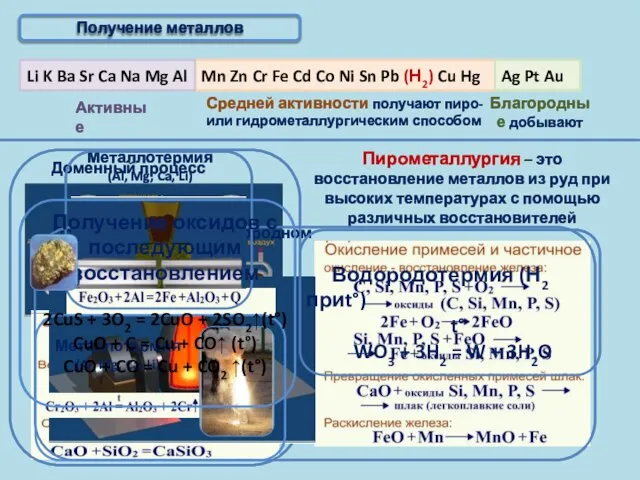
- 9. Получение металлов Пирометаллургия – это восстановление металлов из руд при высоких температурах с помощью различных восстановителей
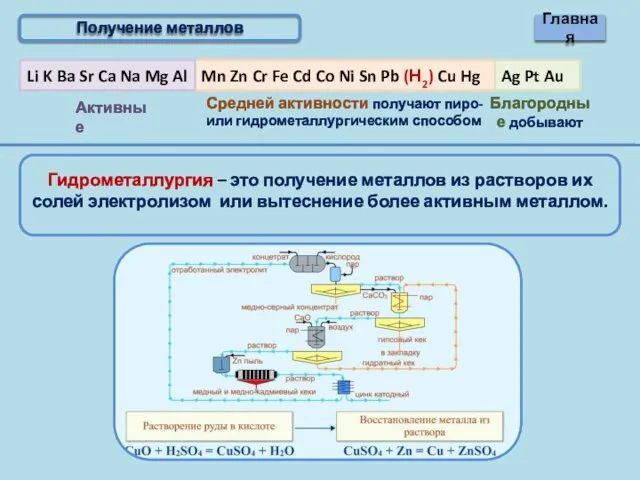
- 10. Получение металлов Главная
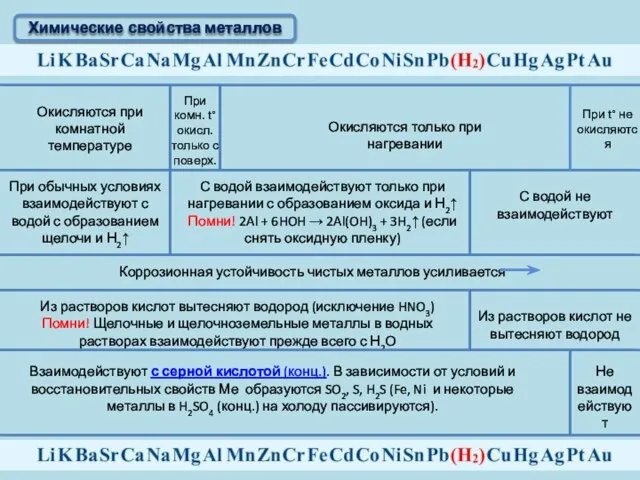
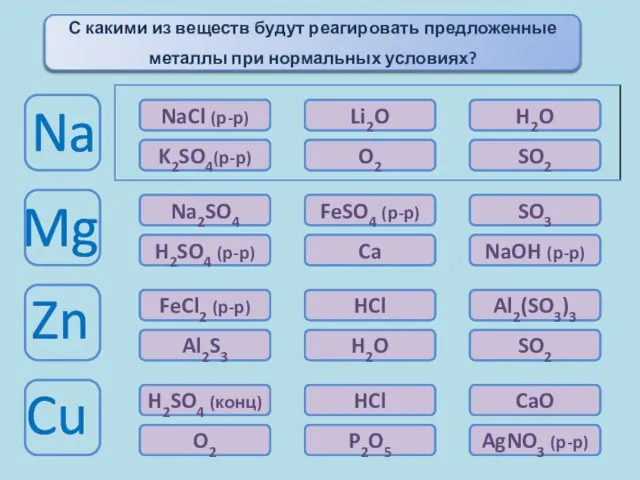
- 11. Химические свойства металлов Окисляются при комнатной температуре При комн. t°окисл. только с поверх. Окисляются только при
- 12. Химические свойства металлов Взаимодействуют с разбавленной и концентрированной азотной кислотой и в зависимости от условий, восстановительных
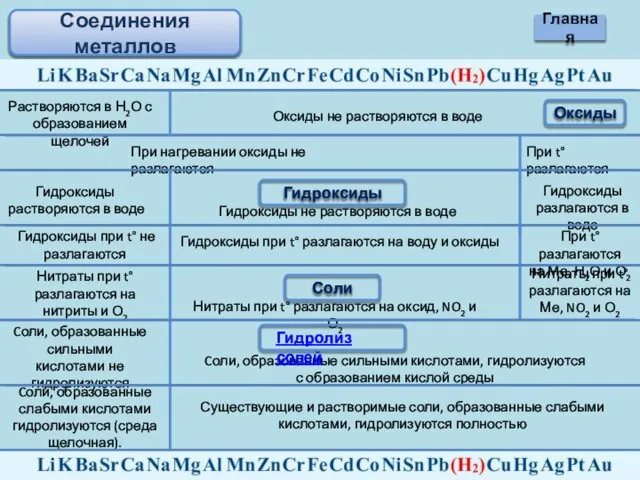
- 13. Соединения металлов Оксиды Растворяются в Н2О с образованием щелочей Оксиды не растворяются в воде При нагревании
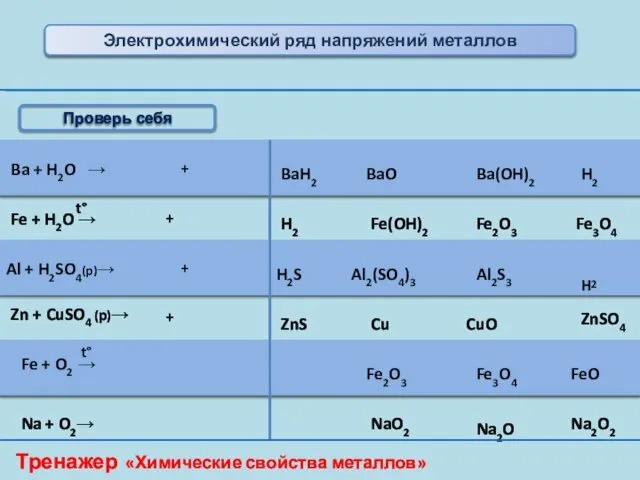
- 14. Ba + H2O → BaH2 BaO Ba(OH)2 H2 Fe + H2O → H2 Fe(OH)2 Fe2O3 Fe3O4
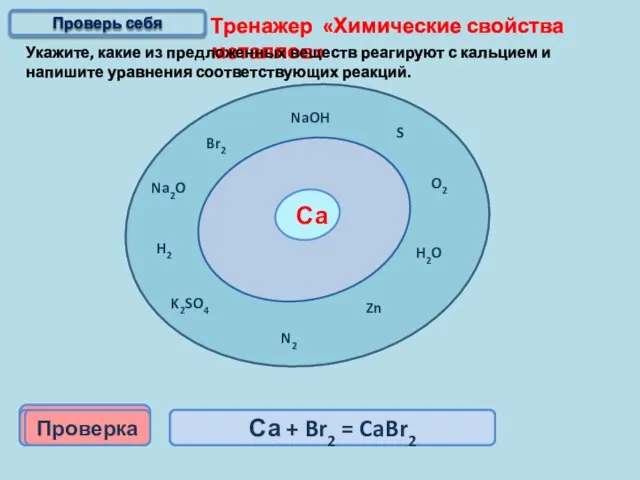
- 15. Тренажер «Химические свойства металлов» Укажите, какие из предложенных веществ реагируют с кальцием и напишите уравнения соответствующих
- 16. Коэффициент перед формулой восстановителя в реакции, схема которой Ca + HNO3 (конц.) → Ca(NO3)2 + N2↑+
- 17. ошибка ошибка ошибка молодец молодец ошибка ошибка молодец молодец ошибка ошибка ошибка молодец ошибка молодец ошибка
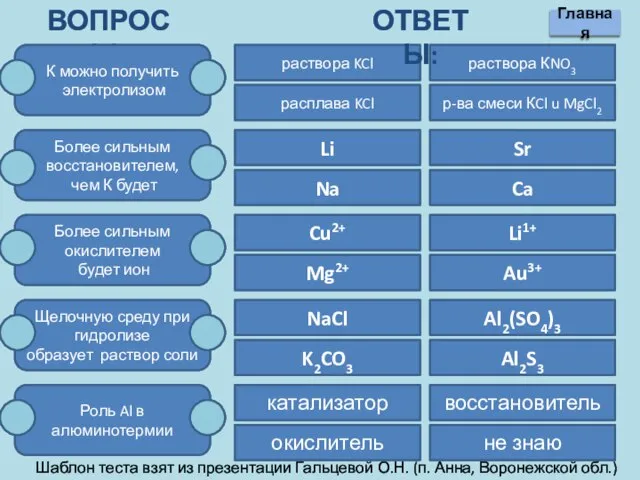
- 18. Вопросы: К можно получить электролизом Более сильным восстановителем, чем К будет Более сильным окислителем будет ион
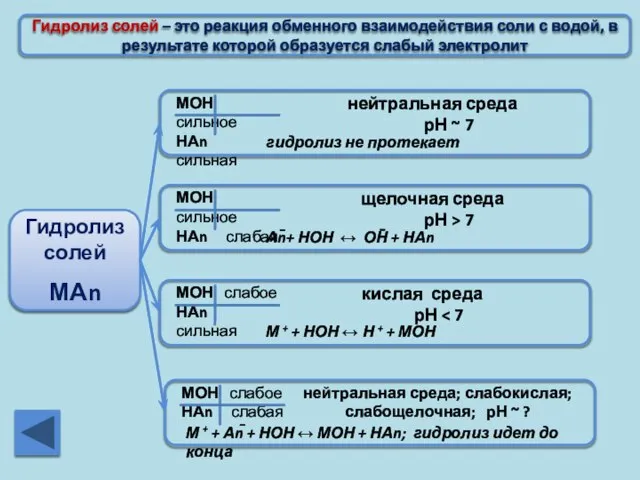
- 19. Гидролиз солей – это реакция обменного взаимодействия соли с водой, в результате которой образуется слабый электролит
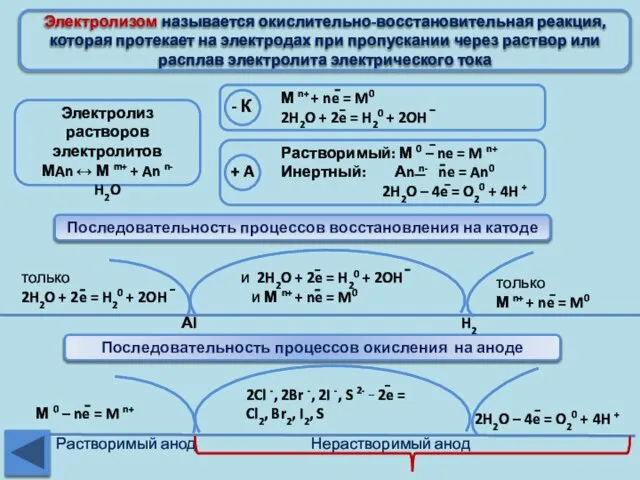
- 20. Электролизом называется окислительно-восстановительная реакция, которая протекает на электродах при пропускании через раствор или расплав электролита электрического
- 21. Электрохимический ряд напряжений металлов Уменьшение восстановительных свойств Усиление окислительных свойств Факторы, определяющие положение металла в электрохимическом
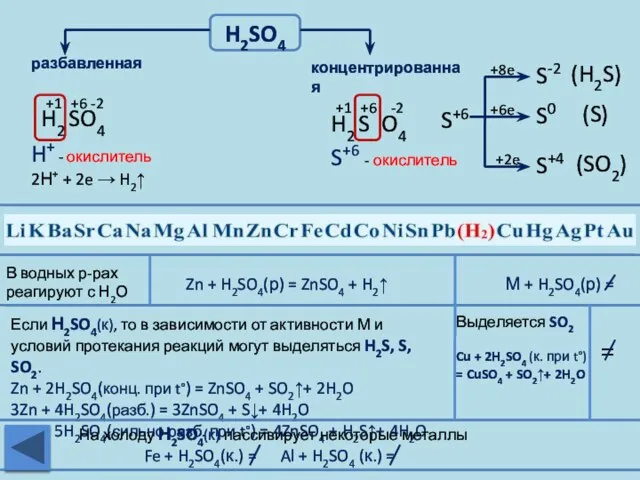
- 22. H2SO4 разбавленная концентрированная Zn + H2SO4(р) = ZnSO4 + H2↑ М + H2SO4(р) = В водных
- 24. Скачать презентацию





 Игровая зависимость
Игровая зависимость Групповой психоанализ
Групповой психоанализ О РАБОТЕ СЕКЦИИ ПРОМЫШЛЕННОЙ ЭКОЛОГИИ И РАЦИОНАЛЬНОГО ПРИРОДОПОЛЬЗОВАНИЯ ПО ВОПРОСАМ ВОДОПОЛЬЗОВАНИЯ В ОРЕНБУРГСКОЙ ОБЛАСТИ
О РАБОТЕ СЕКЦИИ ПРОМЫШЛЕННОЙ ЭКОЛОГИИ И РАЦИОНАЛЬНОГО ПРИРОДОПОЛЬЗОВАНИЯ ПО ВОПРОСАМ ВОДОПОЛЬЗОВАНИЯ В ОРЕНБУРГСКОЙ ОБЛАСТИ Animals in the ABC
Animals in the ABC План реализации проекта
План реализации проекта Константин Симонов
Константин Симонов Презентация на тему Малые тела солнечной системы
Презентация на тему Малые тела солнечной системы Заповеди любви
Заповеди любви Вальдорфская школа
Вальдорфская школа Во что верят люди? Религия. Тема №2
Во что верят люди? Религия. Тема №2 Тициан. Жизнь и творчество.. Жизнь Тициана: Жизнь Тициана:ТИЦИАН (1476/77 –1576), венецианский живописец эпохи Возрождения. Родился в гор
Тициан. Жизнь и творчество.. Жизнь Тициана: Жизнь Тициана:ТИЦИАН (1476/77 –1576), венецианский живописец эпохи Возрождения. Родился в гор Йо-йо
Йо-йо Привет, Весна!
Привет, Весна! Совместная маркетинговая программа «Сервис Плюс» для партнеров
Совместная маркетинговая программа «Сервис Плюс» для партнеров Кровотечения. Первая медицинская помощь
Кровотечения. Первая медицинская помощь Предпрофильная подготовка
Предпрофильная подготовка Проект: Юный проповедник 2017
Проект: Юный проповедник 2017 Металлургический комплекс России
Металлургический комплекс России Право + Защита прав людей, живущих с ВИЧ
Право + Защита прав людей, живущих с ВИЧ Грин стар
Грин стар Грамматика со смешариками
Грамматика со смешариками Эпоха ХХ века - эра великих людей и изобретений
Эпоха ХХ века - эра великих людей и изобретений Презентация на тему Исторический обзор садово-паркового искусства
Презентация на тему Исторический обзор садово-паркового искусства Авиация Советского Союза
Авиация Советского Союза Элетронная таблица Excel
Элетронная таблица Excel Гороскоп первоклассника
Гороскоп первоклассника Модели смертности
Модели смертности «Государственно-частное партнерство: региональный аспект»
«Государственно-частное партнерство: региональный аспект»