Содержание
- 2. превращение одних веществ в другие. Вещества, полученные в результате реакции, отличаются от исходных веществ составом, строением
- 3. Признаки химических реакций Появление запаха Выделение газа Изменение окраски Выпадение осадка Растворение осадка Образование воды Выделение
- 4. Классификация по тепловому эффекту Эндотермические – с поглощением тепла + Q Экзотермические – с выделением тепла
- 5. Классификация по числу и составу исходных и образующихся веществ Реакции соединения: А + В = АВ
- 6. Тестовое задание. 1. Соотнесите: Тип реакции Схема реакции 1. замещения; а) 2ΗgO → 2Ηg+O2 ; 2.
- 7. 3. Реакции, в результате которых из одного сложного вещества образуется несколько более простого состава относятся к:
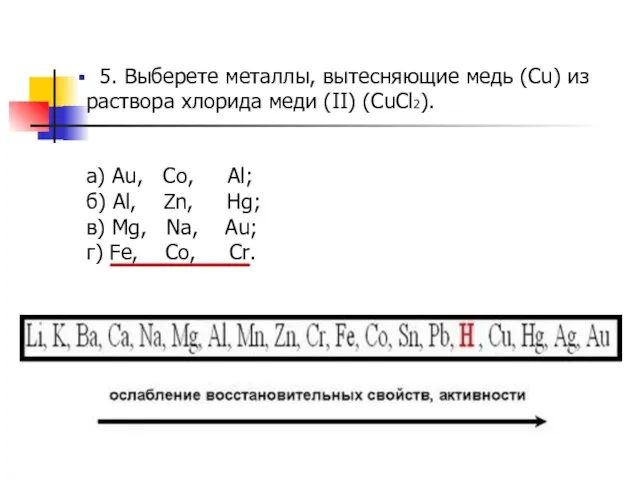
- 8. 5. Выберете металлы, вытесняющие медь (Cu) из раствора хлорида меди (II) (CuCl2). а) Au, Co, Al;
- 9. 6. По данным схемам реакций, запишите уравнения реакций. 1. Гидроксид меди (II) = оксид меди (II)
- 10. 6. Составьте уравнения последовательных реакций, используя подходящие реактивы: а) Ba → BaO → Ba(OH)2 → BaSO4
- 11. Домашнее задание Осуществите цепочку переходов S → SO2 → H2SO3 → Na2SO3 → SO2
- 13. Скачать презентацию









 чудеса Microsoft Office PowerPoint
чудеса Microsoft Office PowerPoint Преддипломная практика (стажировка)
Преддипломная практика (стажировка) Лев Николаевич Толстой. Жизнь и литература
Лев Николаевич Толстой. Жизнь и литература Как выбрать идеальный авточехол
Как выбрать идеальный авточехол Химическая промышленность
Химическая промышленность Тема проекта:Единый государственный экзамен (ЕГЭ)Творческое название:«Что уж ЕГЭ грядущий нам готовит?»
Тема проекта:Единый государственный экзамен (ЕГЭ)Творческое название:«Что уж ЕГЭ грядущий нам готовит?» Р. 3. Доходность и риск
Р. 3. Доходность и риск Русская живопись в I половине XIX века
Русская живопись в I половине XIX века Счастье
Счастье Презентация на тему Правописание суффиксов причастий (7 класс)
Презентация на тему Правописание суффиксов причастий (7 класс) Презентация на тему Мастерство учителя
Презентация на тему Мастерство учителя Кухни зарубежных стран
Кухни зарубежных стран ОП 35-36 (27-09-2016) ОТТС (3)
ОП 35-36 (27-09-2016) ОТТС (3) Сергей Савченко
Сергей Савченко Презентация на тему Billionaire without billion
Презентация на тему Billionaire without billion  The obligation
The obligation  Статистический анализ показателей национального богатства Российской Федерации
Статистический анализ показателей национального богатства Российской Федерации Презентация на тему Древнееврейское царство. Мудрость царя Соломона
Презентация на тему Древнееврейское царство. Мудрость царя Соломона Подросток как гражданин
Подросток как гражданин ОРГАНИЗАЦИЯ РАБОТЫ УЧАЩИХСЯ НАД ИССЛЕДОВАТЕЛЬСКИМИ ПРОЕКТАМИ: ПОДГОТОВКА К ЖИЗНИ ИЛИ ЖИЗНЬ?
ОРГАНИЗАЦИЯ РАБОТЫ УЧАЩИХСЯ НАД ИССЛЕДОВАТЕЛЬСКИМИ ПРОЕКТАМИ: ПОДГОТОВКА К ЖИЗНИ ИЛИ ЖИЗНЬ? Modlitwa o Cud. Madre Di Tutti Le Genti wyk. Jan Paweł II
Modlitwa o Cud. Madre Di Tutti Le Genti wyk. Jan Paweł II Горох
Горох Научно-практическая конференция школьников Люберецкого муниципального района«Ломоносов среди нас»
Научно-практическая конференция школьников Люберецкого муниципального района«Ломоносов среди нас» Проектная деятельность
Проектная деятельность Искусство в моей жизни
Искусство в моей жизни Вебинар «Особенности активного привлечения клиентов в ИТ-отрасли» При поддержке http://smartsourcing.ru/http://smartsourcing.ru/ - презентация
Вебинар «Особенности активного привлечения клиентов в ИТ-отрасли» При поддержке http://smartsourcing.ru/http://smartsourcing.ru/ - презентация Е.Н.Ковтунд.ф.н., профессор, заместитель Председателя Совета по филологии УМО по классическому университетскому образованию (МГУ
Е.Н.Ковтунд.ф.н., профессор, заместитель Председателя Совета по филологии УМО по классическому университетскому образованию (МГУ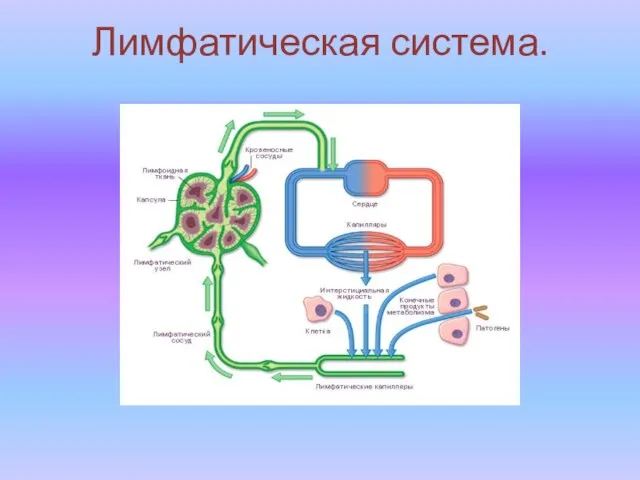 Лимфатическая система
Лимфатическая система