Проект «ТАЙНЫ ВОДЫ» Авторы: учащиеся 8в класса МОУ «СОШ №2 г.Калининска» Руководитель: Шустикова М.В.
Содержание
- 2. Тип проекта: Информационно-исследовательский; Межпредметный; Групповой; Среднесрочный. Место в учебном процессе: Тема «Практическая работа. Анализ воды.» 8
- 3. Цель проекта : Изучить свойства воды, её значение в природе и жизни человека. Познакомиться с основными
- 4. Задачи: Изучить литературные источники о свойствах воды, её значение в природе и жизни человека. Практически познакомиться
- 5. Теоретическая часть учебного проекта. План. Что мы знаем о воде? Физические свойства воды. Роль воды и
- 6. Что мы знаем о воде? Капля. Качественный состав – состоит из водорода и кислорода, Тип вещества
- 7. Дождевая вода чище природной. Природная вода не бывает совершенно чистой. Наиболее чистой является дождевая вода, но
- 8. Очищенная вода намного полезнее. Чтобы освободить природную воду от взвешенных в ней частиц, ее фильтруют сквозь
- 9. Жёсткая и мягкая воды. Количество примесей в пресных водах обычно лежит в пределах от 0,01 до
- 10. Запасы воды на Земле. Вода — весьма распространенное на Земле вещество. Почти 3/4 поверхности земного шара
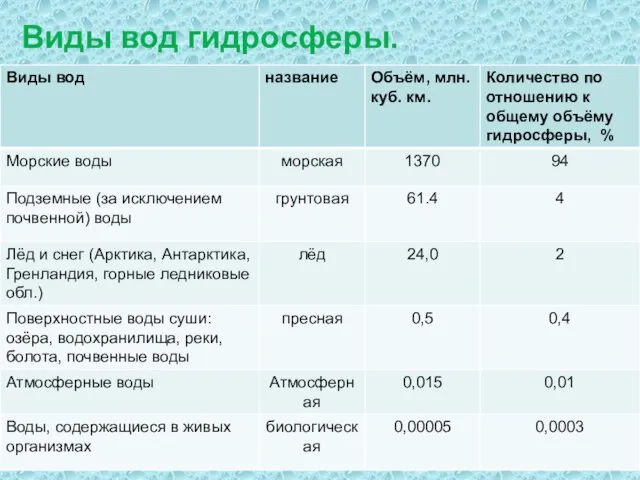
- 11. Виды вод гидросферы.
- 12. Трудно найти в природе другое вещество, физические свойства которого были бы так необычны, разнообразны, аномальны.
- 13. Агрегатные состояния воды В природе вода встречается в трёх агрегатных состояниях: в жидком, твёрдом и газообразном
- 14. Температура кипения воды 100 0С, плавления – 0 0С. Эти аномально высокие значения учёные объясняют тем,
- 15. Плотность воды Плотность воды при переходе из твёрдого состояния в жидкое не уменьшается, как почти у
- 16. Плотность воды Но наибольшей плотности вода достигает при 4 оС. При этой температуре заканчивается перемещение слоёв,
- 17. Теплоёмкость воды Вода обладает аномально высокой теплоёмкостью – 4,18 Дж/(г∙К). Ни одно вещество не требует таких
- 18. Высокая полярность воды вызывает: Диэлектрическую проницаемость Способность воды растворять другие полярные соединения Способность воды вызывать электролитическую
- 19. Поверхностное натяжение Вода обладает большим поверхностным натяжением По утверждению К.С.Лосева, у абсолютно чистой воды эта величина
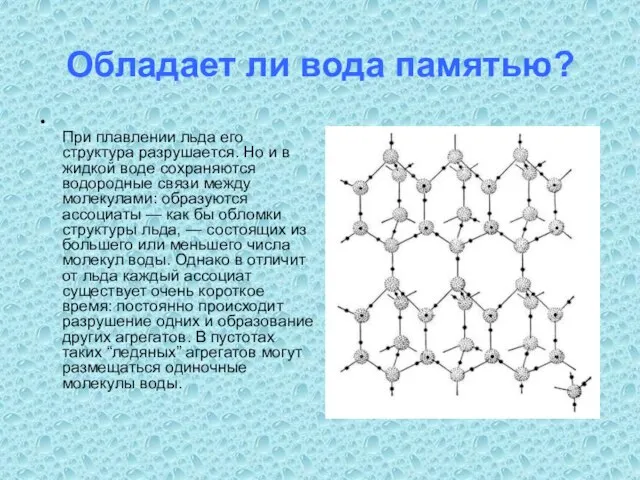
- 20. Обладает ли вода памятью? При плавлении льда его структура разрушается. Но и в жидкой воде сохраняются
- 21. Строение воды. Молекула воды имеет угловое строение; входящие в ее состав ядра образуют равнобедренный треугольник, в
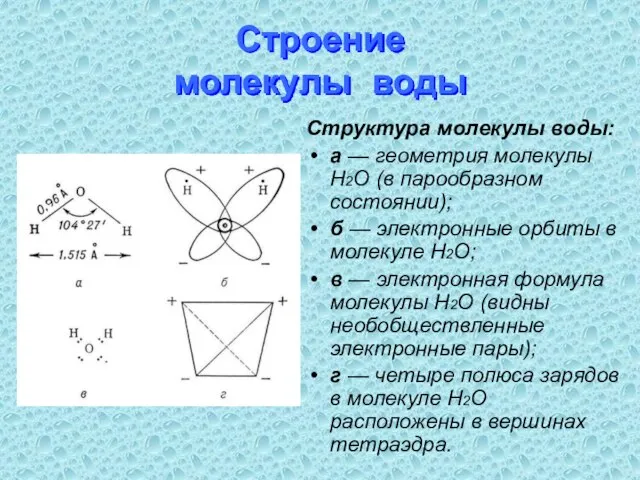
- 22. Строение молекулы воды Структура молекулы воды: а — геометрия молекулы H2O (в парообразном состоянии); б —
- 23. «Подобное растворяется в подобном» Вещества с ионным типом химической связи лучше растворяются в полярных растворителях, неполярные
- 24. Роль воды и растворов. происхождение жизни связывается с морем. вода представляет собой среду, в которой протекают
- 25. Вода в живом организме. Мозг человека-81%; В 5 л крови- 4л воды; Кости-30%; Хрящи-60%; Печень-70%; Мышцы-50-75%;
- 26. Потребность воды у живых организмов. Подсолнух -1л/день, Тридцатилетняя берёза – 60л/день, Высокий хмель – 300л/день, Быстрорастущие
- 27. Плазмолиз – это уменьшение тургора, высасывание воды из клетки, что приводит к увяданию растения. Если почва
- 28. Листья > корни > почва Концентрация растворов в листьях больше всего! Следовательно, происходит засасывание воды из
- 29. Проникая в клетки, вода создает в клетках избыточное давление, которое слегка растягивает оболочки клеток и поддерживает
- 30. Профессии воды. Вода… -колыбель жизни на Земле. -основа жизни на Земле. -преобразователь природы, землекоп. -среда обитания
- 31. «Живая» и «мёртвая» вода
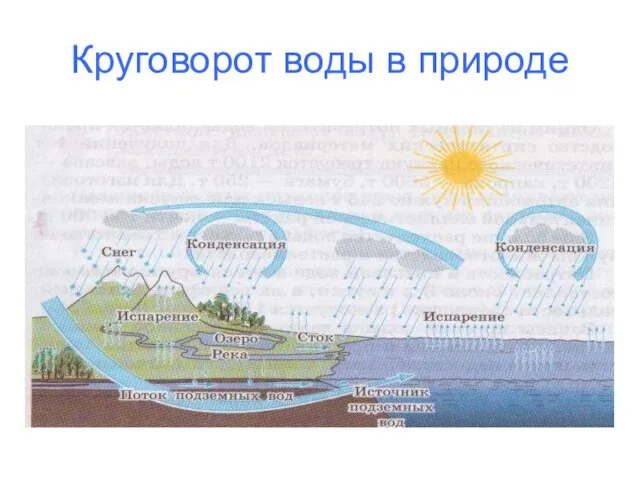
- 32. Круговорот воды в природе
- 33. Экологическое состояние воды. На качество воды и биологическую продуктивность Мирового океана влияют: Бесхозяйственная деятельность людей Увеличение
- 34. Потребление воды в быту.
- 35. ВОДОЁМЫ Калининского района. Калининский МР расположен в Среднем Поволжье, и все реки, протекающие по его территории,
- 36. Практическая часть проекта. ОПЫТ №1. Определение прозрачности воды. Оборудование и реактивы: стеклянный цилиндр диаметром 2-2.5 см
- 37. Содержание и порядок выполнения опыта. 1.Изучите инструкцию по проведению опыта. Установите стеклянный цилиндр диаметром 2-2.5 см
- 38. Оформите отчёт, заполнив таблицу:
- 39. ОПЫТ № 2. Определение интенсивности запаха воды. Оборудование и реактивы: коническая колба со стеклянной пробкой, образцы
- 40. Содержание и порядок выполнения опыта. 1.Изучите инструкцию по проведению опыта. В коническую колбу налейте исследуемую воду
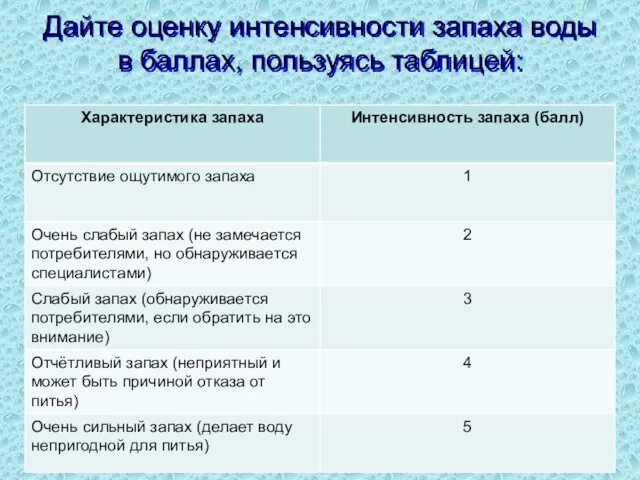
- 41. Дайте оценку интенсивности запаха воды в баллах, пользуясь таблицей:
- 42. Оформите отчёт, заполнив таблицу:
- 43. Капля. Сделайте вывод о свойствах исследуемой пробы воды.
- 45. Скачать презентацию





































 Мои права. Имею право…
Мои права. Имею право…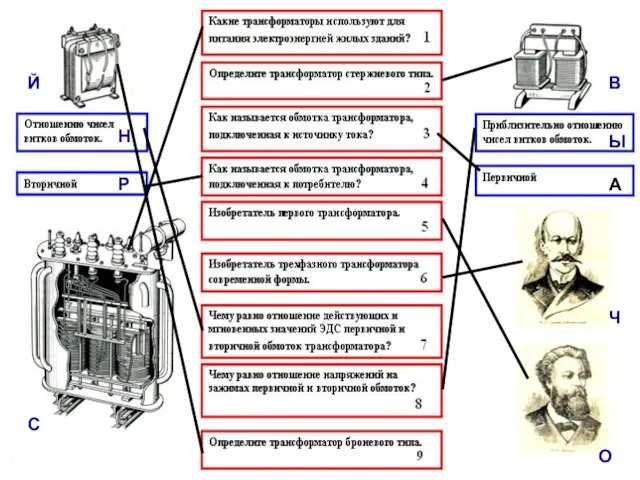 С В АР О Ч Н Ы Й. Сварочный трансформатор Цель: повторить устройство трансформатора; выяснить в чем особенность сварочного трансфор
С В АР О Ч Н Ы Й. Сварочный трансформатор Цель: повторить устройство трансформатора; выяснить в чем особенность сварочного трансфор ЭМОЦИИ И ЗДОРОВЬЕ
ЭМОЦИИ И ЗДОРОВЬЕ Java Enterprise обучение, работа, перспективы
Java Enterprise обучение, работа, перспективы Временное жилище летом
Временное жилище летом Немного о себе
Немного о себе 1 июня - День защиты детей
1 июня - День защиты детей Procrastination and intellectual level
Procrastination and intellectual level Социальное партнерство в сфере воспитания
Социальное партнерство в сфере воспитания Законы и другие нормативно-правовые акты по организации безопасности в условиях ЧС
Законы и другие нормативно-правовые акты по организации безопасности в условиях ЧС Квартирная проводка
Квартирная проводка Информационная политика Правительства Кировской области февраль 2010
Информационная политика Правительства Кировской области февраль 2010 Устройство и содержание бесстыкового пути ОАО РЖД
Устройство и содержание бесстыкового пути ОАО РЖД OOO «Пандора Аутленд» – ваш проводник в мире техники
OOO «Пандора Аутленд» – ваш проводник в мире техники Уникальный летний культурно-исторический лагерь Ұлы дала жастары
Уникальный летний культурно-исторический лагерь Ұлы дала жастары Профессиональная компетентность педагога
Профессиональная компетентность педагога Предложение на комплексную поставку оборудования и выполнение работ (EPC) по проекту строительства обогатительной фабрики
Предложение на комплексную поставку оборудования и выполнение работ (EPC) по проекту строительства обогатительной фабрики ЦО №1748 «Вертикаль»
ЦО №1748 «Вертикаль» Методические рекомендациипо использованию метода проектовдля изучения темы«Виды рекламной фотосъемки»
Методические рекомендациипо использованию метода проектовдля изучения темы«Виды рекламной фотосъемки» О
О J’aime et je n’aime pas...
J’aime et je n’aime pas... Николай Васильеви ч Гоголь (1809 — 1852)
Николай Васильеви ч Гоголь (1809 — 1852)  Вкусные украшения для праздника
Вкусные украшения для праздника Вознесенская райгосадминистрация
Вознесенская райгосадминистрация Светодиодные светильники
Светодиодные светильники Стратегия развития современных технологий мобильной связи на Дальнем Востоке и в Восточной Сибири
Стратегия развития современных технологий мобильной связи на Дальнем Востоке и в Восточной Сибири Презентация на тему Степень с целым показателем 8 класс
Презентация на тему Степень с целым показателем 8 класс  Путь к моей мечте
Путь к моей мечте