Слайд 2Химическое равновесие
Реакции, которые одновременно протекают в прямом и обратном направлении, называются обратимыми
Состояние

химического обратимого процесса, при котором скорость прямой реакции равна скорости обратной реакции, называется химическим равновесием
Слайд 3Смещение химического равновесия осуществляется в соответствии с принципом Ле Шателье
Если на систему,

находящуюся в состоянии химического равновесия, оказать внешнее воздействие (изменить концентрацию, температуру, давление), то равновесие смещается в сторону той реакции, которая ослабляет это воздействие
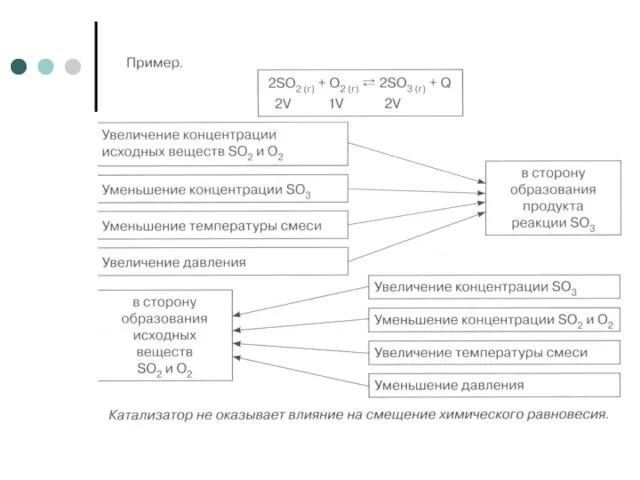
Слайд 5Процессы, протекающие при обратимых реакциях

Слайд 6Процессы, протекающие при обратимых реакциях
прямая реакция
αА + βВ γС +

δD
обратная реакция
υ ═ k1 · [A]α · [B]β
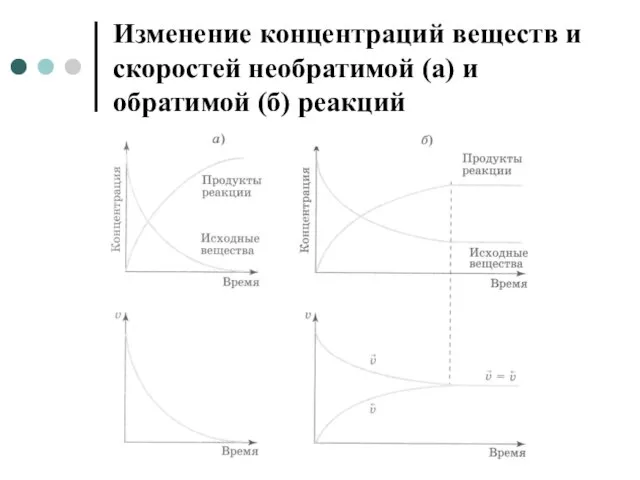
Слайд 7Изменение концентраций веществ и скоростей необратимой (а) и обратимой (б) реакций






 Коллекция дидактических игр для устного счёта 1 класс
Коллекция дидактических игр для устного счёта 1 класс Театральные этюды
Театральные этюды Работа с одарёнными детьми
Работа с одарёнными детьми Презентация на тему Графика
Презентация на тему Графика Электродинамика
Электродинамика Теплолюксmirror. Обогреватель зеркал
Теплолюксmirror. Обогреватель зеркал Устный
Устный Кто будет начальником
Кто будет начальником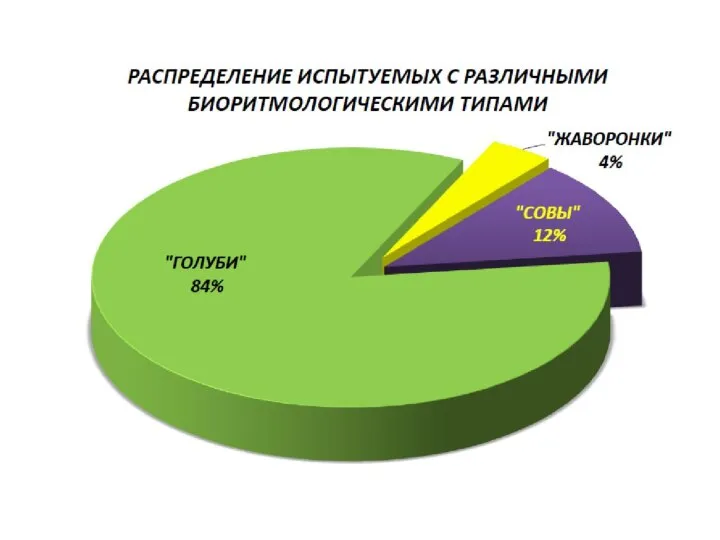 Уровень психологической напряженности у лиц с различными биоритмологическими типами
Уровень психологической напряженности у лиц с различными биоритмологическими типами Виды применяемых систем автоблокировки
Виды применяемых систем автоблокировки Илья Павлов
Илья Павлов Презентация по проектной деятельности 2 группа
Презентация по проектной деятельности 2 группа Блюдо из птицы
Блюдо из птицы Святые места Воронежа
Святые места Воронежа Технология планирования карьеры
Технология планирования карьеры Общероссийское голосование
Общероссийское голосование Валютная система
Валютная система  от
от Конкурс проектов lingua latina per se illustrata. Гуманитарный факультет
Конкурс проектов lingua latina per se illustrata. Гуманитарный факультет Механизм государственного регулирования внешнеторговой деятельности
Механизм государственного регулирования внешнеторговой деятельности Берегите тепло в доме
Берегите тепло в доме Проектный конкурс. Деревня WorldSkills 2019
Проектный конкурс. Деревня WorldSkills 2019 Муниципальное бюджетное общеобразовательное учреждение средняя общеобразовательная школа № 10 ст. Павловской
Муниципальное бюджетное общеобразовательное учреждение средняя общеобразовательная школа № 10 ст. Павловской Escape from North Korea
Escape from North Korea Презентация на тему Решение задач
Презентация на тему Решение задач  Презентация на тему Вышивка крестиком
Презентация на тему Вышивка крестиком  Тарифы без скидки
Тарифы без скидки Правописание союзов
Правописание союзов