Содержание
- 2. Гидролизом соли называется взаимодействие ионов соли с водой, в результате которого изменяется рН среды. В процессе
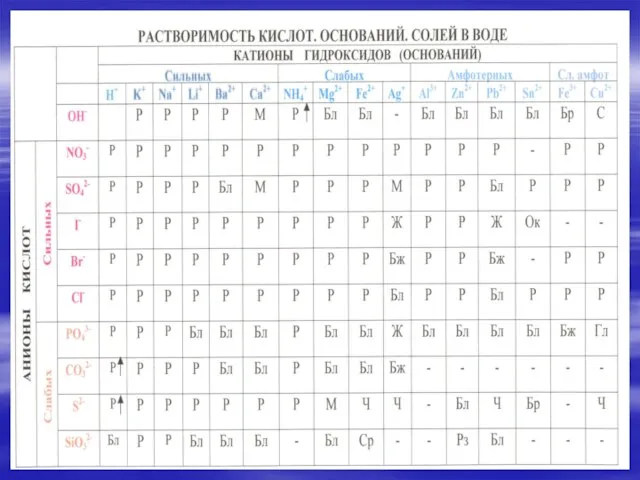
- 4. ОКРАСКА ЛАКМУСОВОЙ БУМАГИ В РАЗЛИЧНЫХ СРЕДАХ
- 5. В зависимости от силы исходной кислоты и исходного основания, образовавших соль, выделяют 4 типа солей. Соли,
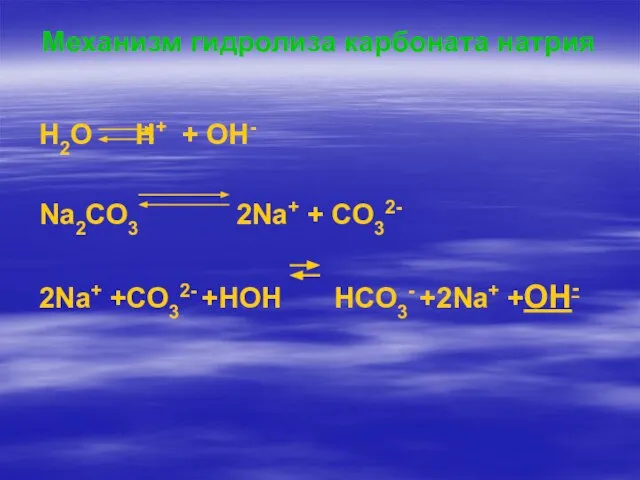
- 6. Механизм гидролиза карбоната натрия H2O H+ + OH- Na2CO3 2Na+ + CO32- 2Na+ +CO32- +HOH HCO3-
- 7. CO32- +HOH HCO3- +OH- Na2CO3 +H2O NaHCO3 +NaOH Одним из продуктов данной обменной реакции является кислая
- 8. Схема гидролиза карбоната натрия Na2CO3 NaOH H2CO3 сильное основание слабая кислота [OH]- > [H]+ (что сильней
- 9. FeCl2 ↔ Fe2+ + 2Cl- Fe2+ + H2O ↔ (FeOH)+ + H+ FeCl2 + H2O ↔
- 10. Механизм гидролиза хлорида алюминия H2O H+ + OH- AlCl3 Al3+ + 3Cl- Al3+ +3Cl- +HOH Al
- 11. Al3+ + HOH AlOH2+ + H+ AlCl3 + H2O AlOHCl2 + HCl Одним из продуктов данной
- 12. Схема гидролиза хлорида алюминия AlCl3 Al(OH)3 HCl слабое основание сильная кислота [OH]- (что сильней того и
- 13. 4. Соли, образованные катионом сильного основания и анионом сильной кислоты не подвергаются гидролизу. К таким солям
- 14. Механизм гидролиза хлорида натрия H2O H+ + OH- NaСl Na+ + Cl- Na+ +Cl- +HOH Cl-
- 15. NaCl + Н2О = Сформулируем вывод: Раствор соли, образованной__________________, имеет________________________реакцию, так как в растворе__________________________________.
- 16. Схема гидролиза карбоната натрия NaCl NaOH HCl сильное основание сильная кислота [OH]- = [H]+ Н е
- 17. Самостоятельно заполните таблицу
- 18. Самостоятельно заполните таблицу
- 19. Количественной характеристикой гидролиза является степень гидролиза α (которую выражают в процентах). где n - число моль
- 21. Скачать презентацию




![Схема гидролиза карбоната натрия Na2CO3 NaOH H2CO3 сильное основание слабая кислота [OH]-](/_ipx/f_webp&q_80&fit_contain&s_1440x1080/imagesDir/jpg/372827/slide-7.jpg)



![Схема гидролиза хлорида алюминия AlCl3 Al(OH)3 HCl слабое основание сильная кислота [OH]-](/_ipx/f_webp&q_80&fit_contain&s_1440x1080/imagesDir/jpg/372827/slide-11.jpg)



![Схема гидролиза карбоната натрия NaCl NaOH HCl сильное основание сильная кислота [OH]-](/_ipx/f_webp&q_80&fit_contain&s_1440x1080/imagesDir/jpg/372827/slide-15.jpg)



 Устройство компьютера
Устройство компьютера Презентация рекламного агентства Миксарт Инновация advertising, btl, marketing, events, mobile marketing 2010 год
Презентация рекламного агентства Миксарт Инновация advertising, btl, marketing, events, mobile marketing 2010 год Обработка информации 10-11класс
Обработка информации 10-11класс Обмерный план
Обмерный план Организация питания и питьевого режима в период подготовки и в дни проведения ЕГЭ
Организация питания и питьевого режима в период подготовки и в дни проведения ЕГЭ Обмануть свои глаза
Обмануть свои глаза Н.В.Гоголь Ревизор
Н.В.Гоголь Ревизор Дискриминаторы сигналов
Дискриминаторы сигналов Презентация на тему Виды вирусных заболеваний человека, животных и растений
Презентация на тему Виды вирусных заболеваний человека, животных и растений  Voľba študijného odboru
Voľba študijného odboru C'est mon meilleur ami
C'est mon meilleur ami Библейский сюжет “Поклонение волхвов”
Библейский сюжет “Поклонение волхвов” Микеланджело Буанорроти (1475-1564)
Микеланджело Буанорроти (1475-1564) Коммуникационные технологии
Коммуникационные технологии Русская икона. Иконография
Русская икона. Иконография Выбор дверей
Выбор дверей Презентация Ангарского филиала ООО «Уралприбор»
Презентация Ангарского филиала ООО «Уралприбор» Военная биография моего прадеда Нестерова Михаила Нестеровича
Военная биография моего прадеда Нестерова Михаила Нестеровича Изделия в технике «изонить»
Изделия в технике «изонить» А Вы хотите быть счастливой
А Вы хотите быть счастливой Предпосылки открытия Периодического закона Д. И. Менделеевым
Предпосылки открытия Периодического закона Д. И. Менделеевым «Язык программирования Pascal»
«Язык программирования Pascal» Техническое регулирование в Российской Федерации и Таможенном союзе ЭЛЕКТРООБОРУДОВАНИЕАнализ, новости и тенденциив 2012 годуДр
Техническое регулирование в Российской Федерации и Таможенном союзе ЭЛЕКТРООБОРУДОВАНИЕАнализ, новости и тенденциив 2012 годуДр Идентификация клиента, представителя клиента, выгодоприобретателя, бенефициарного владельца
Идентификация клиента, представителя клиента, выгодоприобретателя, бенефициарного владельца Human-computer interaction
Human-computer interaction Оборотный капитал корпорации
Оборотный капитал корпорации  Литературный фантик конфет Птичье молоко
Литературный фантик конфет Птичье молоко Угрозы и вызовы XXI века
Угрозы и вызовы XXI века