Содержание
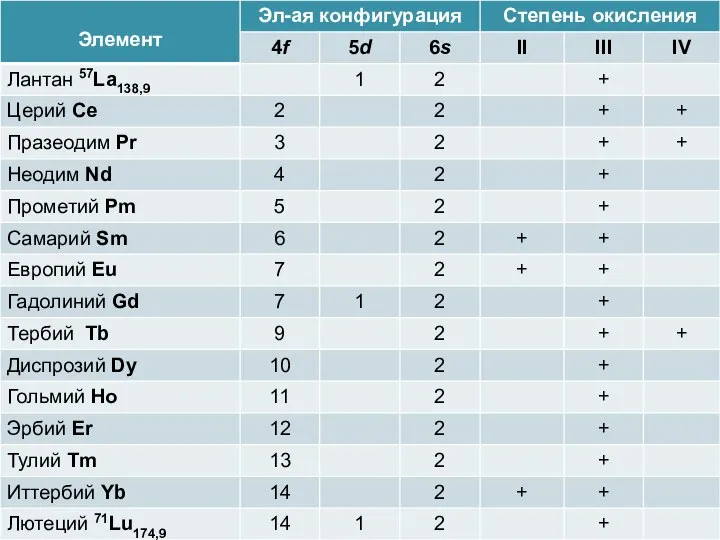
- 2. РЕДКОЗЕМЕЛЬНЫЕ ЭЛЕМЕНТЫ Термин "редкоземельные металлы" объединяет 17 химических элементов, включая лантаноиды, располагаются в таблице Менделеева под
- 3. РЗМ В ИСТОРИИ Название «редкоземельные элементы» исторически сложилось в конце XVIII, когда ошибочно считали, что минералы,
- 4. РЗМ В ИСТОРИИ 1794г. – И.Я. Гадолин из нового минерала, названного иттербитом, выделил окись нового элемента,
- 5. РАСПРОСТРАНЁННОСТЬ РЗЭ И ИХ МИНЕРАЛЫ Монацит (Се, La...) РО4 50 - 68% Ln2О3 , 22 -
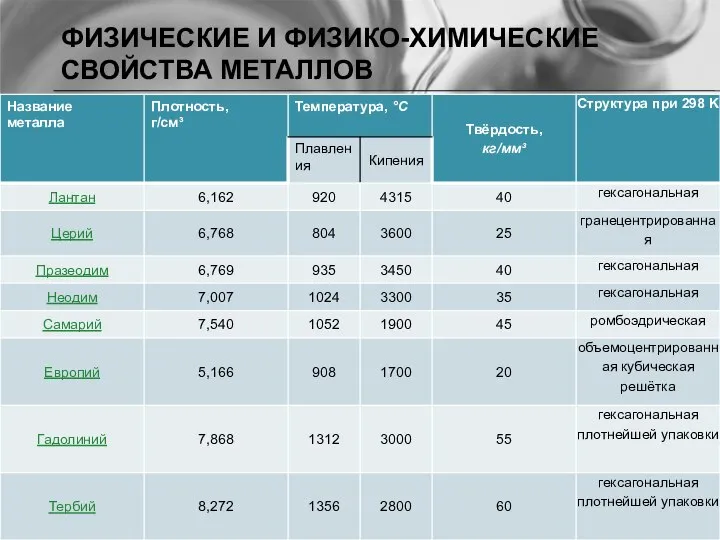
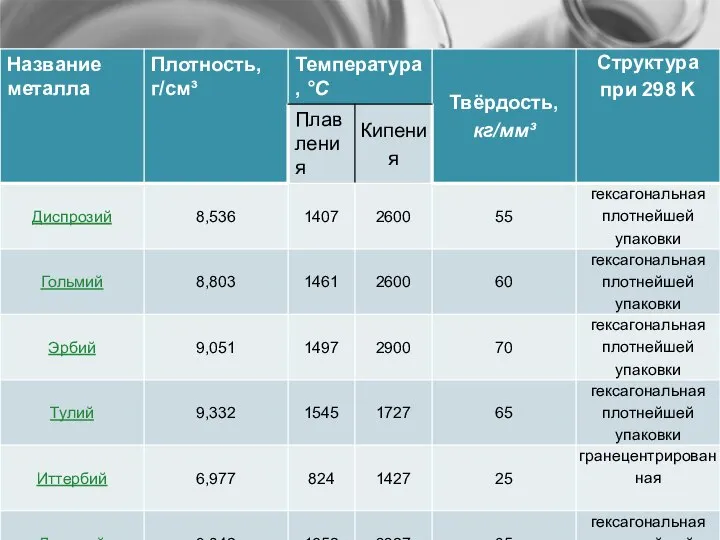
- 7. ФИЗИЧЕСКИЕ И ФИЗИКО-ХИМИЧЕСКИЕ СВОЙСТВА МЕТАЛЛОВ
- 9. СОЕДИНЕНИЯ РЕДКОЗЕМЕЛЬНЫХ ЭЛЕМЕНТОВ Оксиды Высшие оксиды: Полуторные: Низшие:
- 10. СОЕДИНЕНИЯ РЕДКОЗЕМЕЛЬНЫХ ЭЛЕМЕНТОВ Гидроксиды Металлические свойства РЗЭ возрастают в следующем порядке Lu, Yb, Tu, Er, Ho,
- 11. СОЕДИНЕНИЯ РЕДКОЗЕМЕЛЬНЫХ ЭЛЕМЕНТОВ Сульфаты Ln2O3 + 6H2SO4 → 2Ln(HSO4)3 + ЗН2О 2Ln(HSO4)3 → Ln2(SO4)3 + 3S03
- 12. СОЕДИНЕНИЯ РЕДКОЗЕМЕЛЬНЫХ ЭЛЕМЕНТОВ Тиосульфаты В воде, подкисленной соляной кислотой, разлагаются: Ln2(S2O3)3 = Ln2(SO3)3 + 3S Двойные
- 13. СОЕДИНЕНИЯ РЕДКОЗЕМЕЛЬНЫХ ЭЛЕМЕНТОВ Селенаты Селенаты иттрия и лантаноидов и цериселенат Ln2(SeО4)3∙nH2O; Y2(SeO4)3∙nH2O; Ce(SeO4)2 Ln2O3 + 3H2SeO4
- 14. СОЕДИНЕНИЯ РЕДКОЗЕМЕЛЬНЫХ ЭЛЕМЕНТОВ Селениты Ln2(SeО3)3∙nH2О получают, действуя на растворы солей рзэ селенитом натрия или селенистой кислотой.
- 15. СОЕДИНЕНИЯ РЕДКОЗЕМЕЛЬНЫХ ЭЛЕМЕНТОВ Нитраты Ln2О3 + 6N2О4 → 2Ln(NO3)3 + 3N2O3. Ln2О3 + 6HNO3 → 2Ln(NO3)3
- 16. СОЕДИНЕНИЯ РЕДКОЗЕМЕЛЬНЫХ ЭЛЕМЕНТОВ Нитриты Ln(NО2)3 образуются в виде кристаллических осадков при прибавлении к нитрату или хлориду
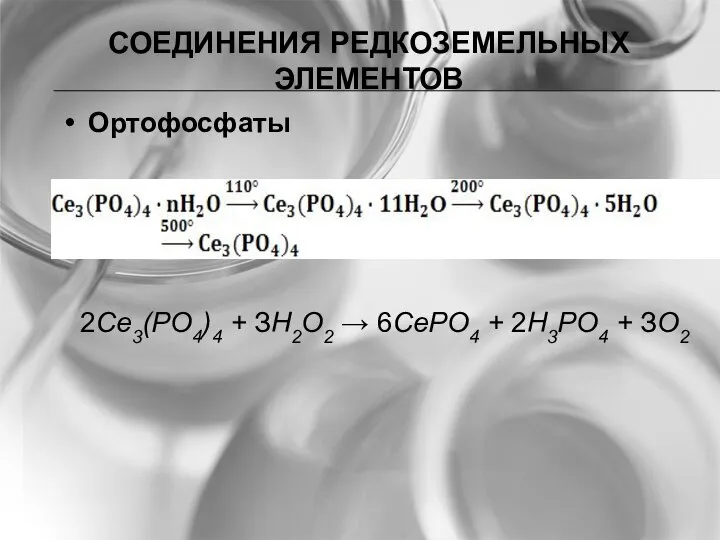
- 17. СОЕДИНЕНИЯ РЕДКОЗЕМЕЛЬНЫХ ЭЛЕМЕНТОВ Ортофосфаты 2Се3(РO4)4 + ЗН2O2 → 6СеРO4 + 2Н3РO4 + ЗО2
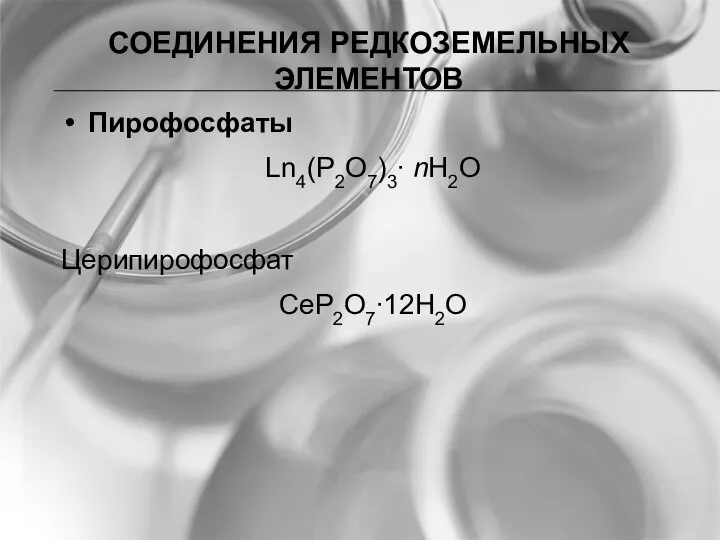
- 18. СОЕДИНЕНИЯ РЕДКОЗЕМЕЛЬНЫХ ЭЛЕМЕНТОВ Пирофосфаты Ln4(Р2O7)3∙ nН2O Церипирофосфат СеР2О7∙12Н2О
- 19. СОЕДИНЕНИЯ РЕДКОЗЕМЕЛЬНЫХ ЭЛЕМЕНТОВ Карбонаты Ln2(CО3)3 + 2Н2О → 2Ln(OH)CO3 + Н2СО3.
- 20. СОЕДИНЕНИЯ РЕДКОЗЕМЕЛЬНЫХ ЭЛЕМЕНТОВ Оксалаты Ln2(SО4)3 + ЗН2С2О4 = Ln2(C2О4)3 + 3H2SО4. Редкоземельные элементы с оксалатами щелочных
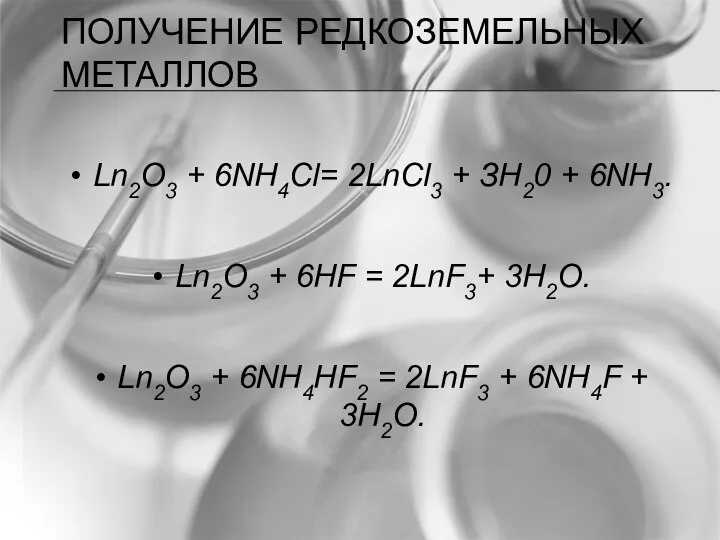
- 21. СОЕДИНЕНИЯ РЕДКОЗЕМЕЛЬНЫХ ЭЛЕМЕНТОВ Фториды Ln2О3 + 6HF = 2LnF3 + 3H2О Ln2О3 + 6NH4HF2 = 2LnF3
- 22. СОЕДИНЕНИЯ РЕДКОЗЕМЕЛЬНЫХ ЭЛЕМЕНТОВ Гидриды Максимальное содержание водорода в гидридах соответствует формуле LnH3. LnH3 + 3НС1 =
- 23. СОЕДИНЕНИЯ РЕДКОЗЕМЕЛЬНЫХ ЭЛЕМЕНТОВ Комплексные соединения 1. ЭДТА – этилендиаминтетрауксусная кислота С14H16O8N2: 2. Кислые алкилфосфаты:
- 24. СОЕДИНЕНИЯ РЕДКОЗЕМЕЛЬНЫХ ЭЛЕМЕНТОВ Комплексные соединения 3. Нейтральные экстрагенты: Состав комплексов зависит от рН раствора и изменяется
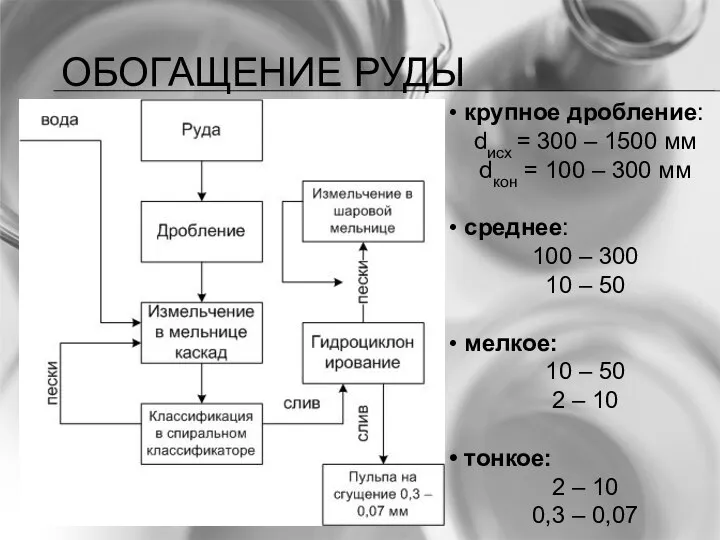
- 25. ОБОГАЩЕНИЕ РУДЫ крупное дробление: dисх = 300 – 1500 мм dкон = 100 – 300 мм
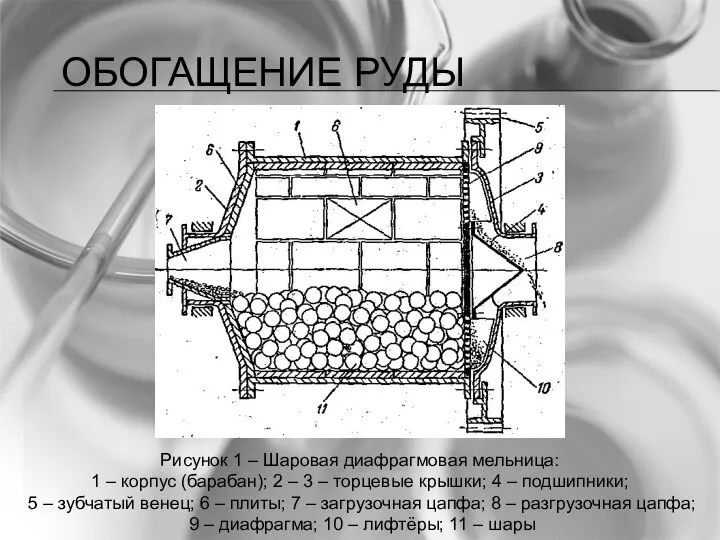
- 26. ОБОГАЩЕНИЕ РУДЫ Рисунок 1 – Шаровая диафрагмовая мельница: 1 – корпус (барабан); 2 – 3 –
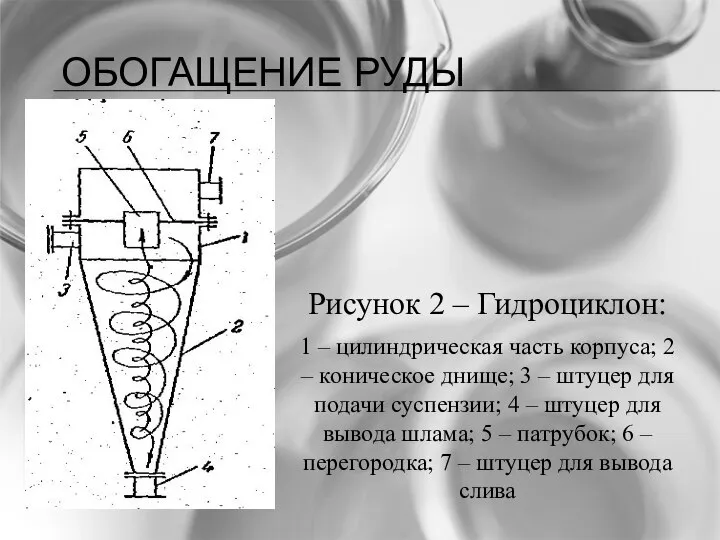
- 27. ОБОГАЩЕНИЕ РУДЫ Рисунок 2 – Гидроциклон: 1 – цилиндрическая часть корпуса; 2 – коническое днище; 3
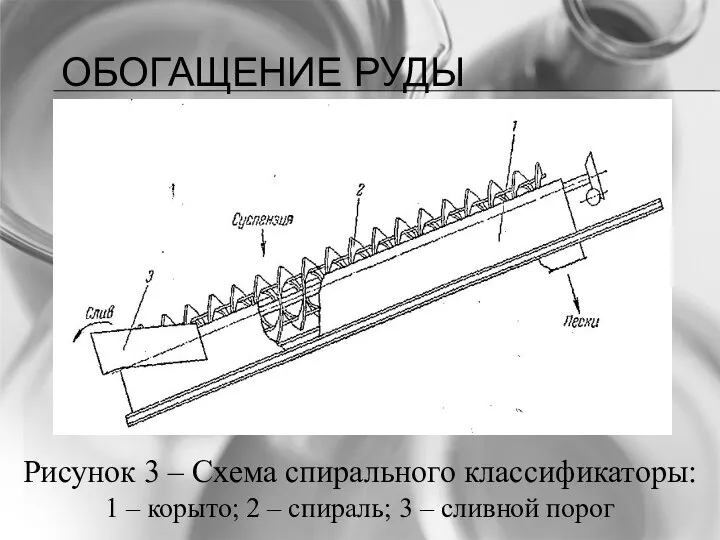
- 28. ОБОГАЩЕНИЕ РУДЫ Рисунок 3 – Схема спирального классификаторы: 1 – корыто; 2 – спираль; 3 –
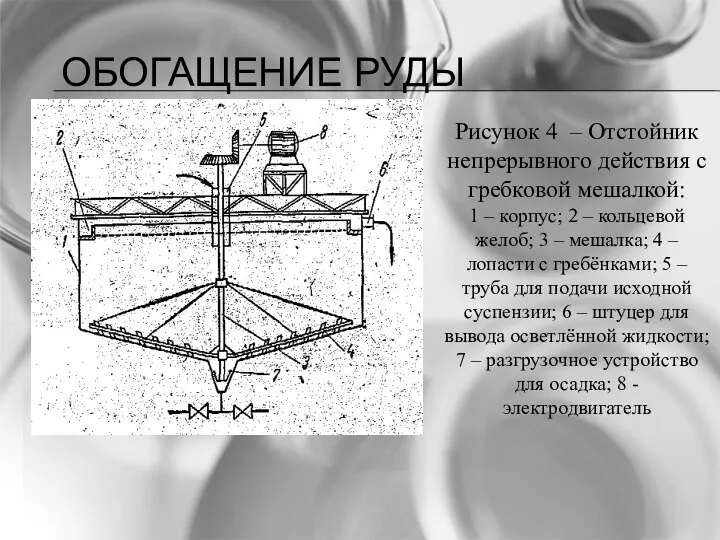
- 29. ОБОГАЩЕНИЕ РУДЫ Рисунок 4 – Отстойник непрерывного действия с гребковой мешалкой: 1 – корпус; 2 –
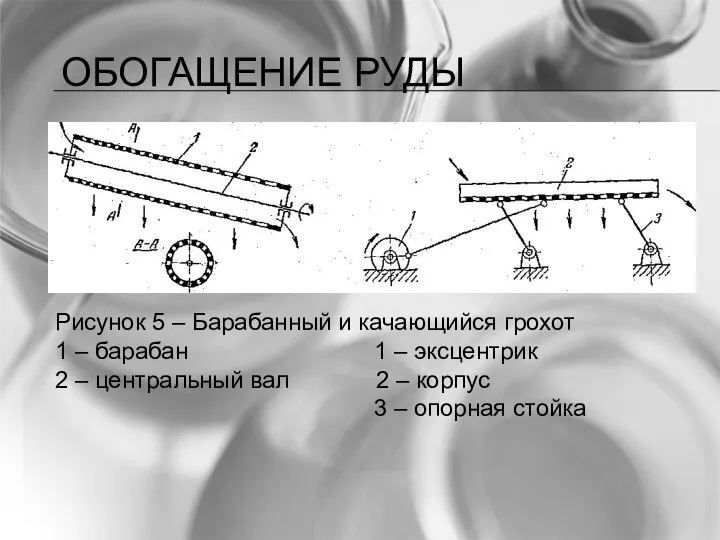
- 30. ОБОГАЩЕНИЕ РУДЫ Рисунок 5 – Барабанный и качающийся грохот 1 – барабан 1 – эксцентрик 2
- 31. МЕТОДЫ РАЗДЕЛЕНИЯ РЗЭ Для разделения рзэ применимы следующие методы: 1) дробная кристаллизация и дробное осаждение; 2)
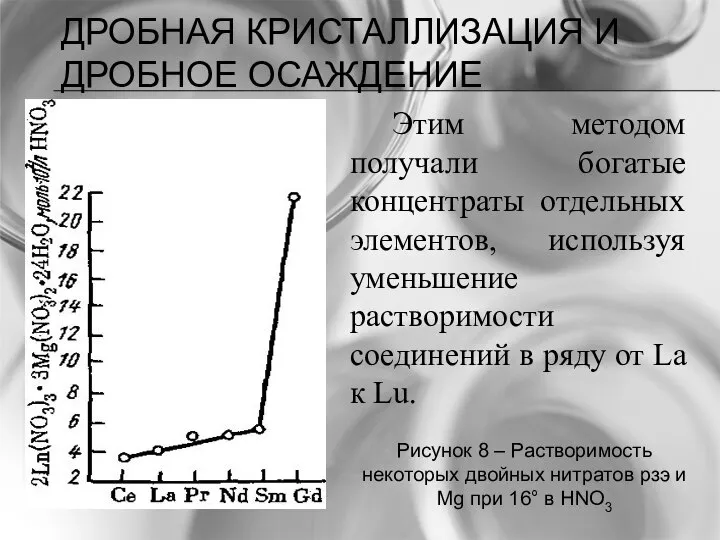
- 32. ДРОБНАЯ КРИСТАЛЛИЗАЦИЯ И ДРОБНОЕ ОСАЖДЕНИЕ Рисунок 8 – Растворимость некоторых двойных нитратов рзэ и Mg при
- 33. ОСАЖДЕНИЕ ОКСАЛАТОВ рН выделения оксалатов некоторых РЗЭ в присутствии трилона А: La— 6,0, Рг —5,5, Nd
- 34. ИЗБИРАТЕЛЬНОЕ ОКИСЛЕНИЕ — ВОССТАНОВЛЕНИЕ Электродные потенциалы РЗЭ с изменением степени окисления следующие: Ce3+→Ce4+ 1,74; Pr3+→ Pr4+
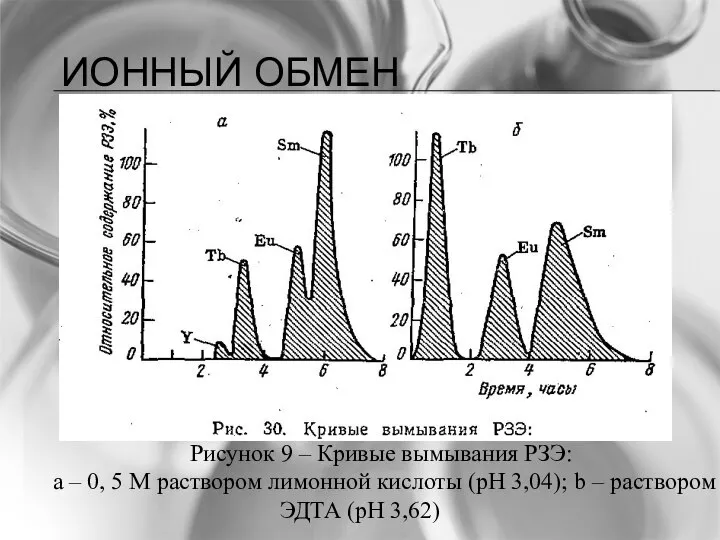
- 35. ИОННЫЙ ОБМЕН Рисунок 9 – Кривые вымывания РЗЭ: а – 0, 5 М раствором лимонной кислоты
- 36. ЭКСТРАКЦИЯ «+»: получение высококачественных соединений большая производительность процесса В качестве экстракторов для разделения РЗЭ чаще всего
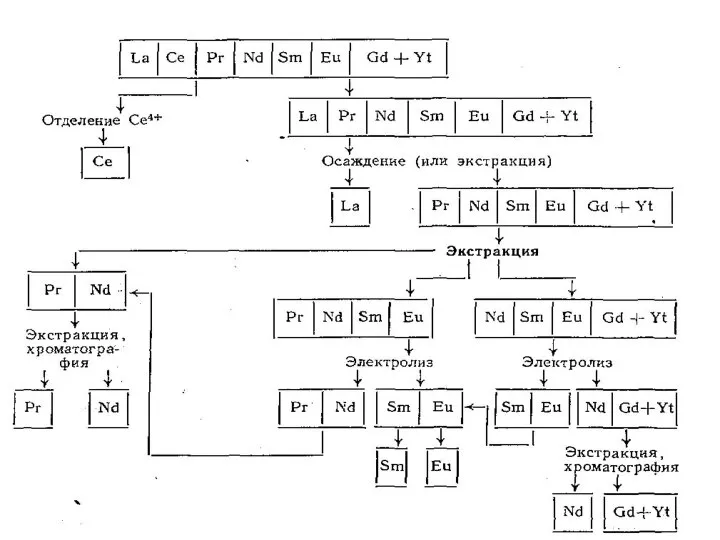
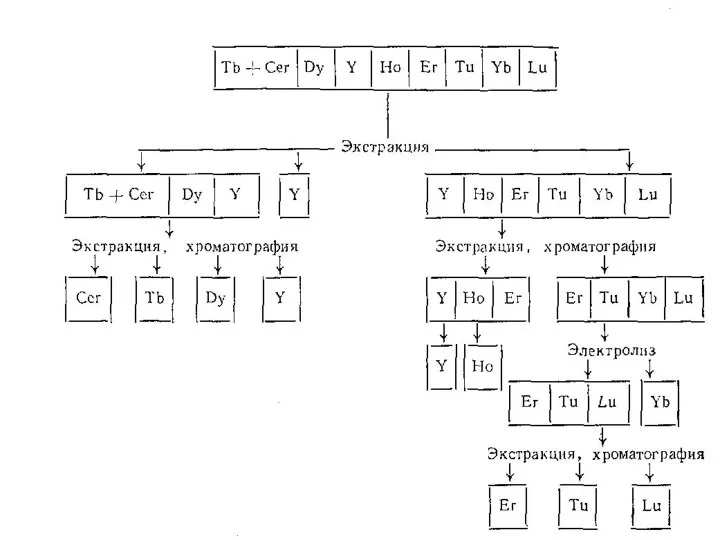
- 37. ПРИНЦИПИАЛЬНАЯ СХЕМА РАЗДЕЛЕНИЯ РЗЭ
- 38. ПРИНЦИПИАЛЬНАЯ СХЕМА РАЗДЕЛЕНИЯ РЗЭ
- 39. ПОЛУЧЕНИЕ РЕДКОЗЕМЕЛЬНЫХ МЕТАЛЛОВ Ln2О3 + 6NH4Cl= 2LnCl3 + ЗН20 + 6NH3. Ln2О3 + 6HF = 2LnF3+
- 40. МЕТАЛОТЕРМИЧЕСКИЙ СПОСОБ I группа: La, Ce, Pr, Nd, мишметалл с tплав. ~ 1100ºС. У хлоридов повышенная
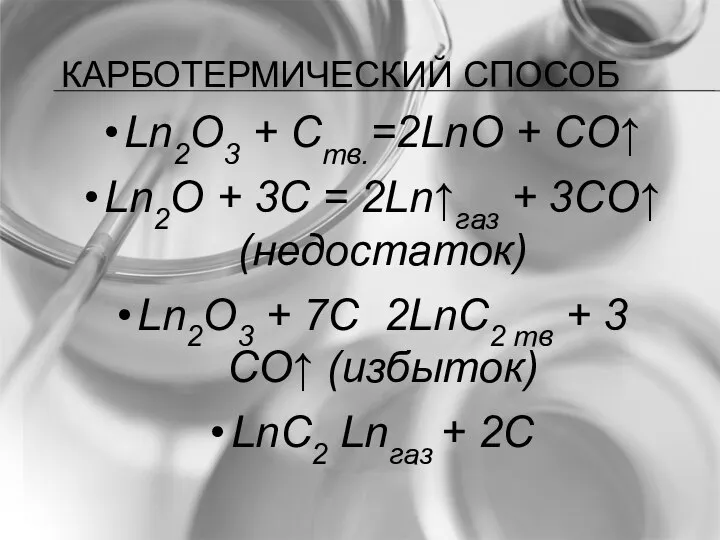
- 41. КАРБОТЕРМИЧЕСКИЙ СПОСОБ Ln2O3 + Cтв.=2LnO + CO↑ Ln2O + 3C = 2Ln↑газ + 3CO↑ (недостаток) Ln2O3
- 42. АЛЮМОТЕРМИЧЕСКИЙ СПОСОБ Термодинамика: Ln2O3 + Al = 2Ln + Al2O3 + G, если в шихту ввести
- 43. ПОЛУЧЕНИЕ РЗМ ЛИТИЙ ТЕРМИЧЕСКИМ ВОССТАНОВЛЕНИЕМ ИЗ ХЛОРИДА Выход металла в слиток при использовании Na и K
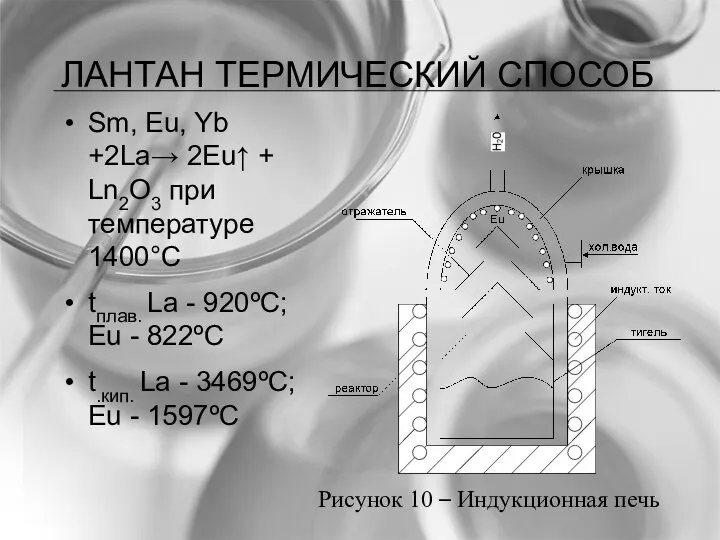
- 44. ЛАНТАН ТЕРМИЧЕСКИЙ СПОСОБ Sm, Eu, Yb +2La→ 2Eu↑ + Ln2O3 при температуре 1400°С tплав. La -
- 45. КАЛЬЦИЙТЕРМИЧЕЙСКИЙ СПОСОБ 2LnF3 тв. + 3Caтв. = 2Lnж + 3CaF2 ж - ∆G T = 1700-1800ºC
- 46. ПРИМЕНЕНИЕ Скандий – высокопрочные AlSc сплавы, элетроннолучевые трубки; Иттрий – люминофоры, стекло, сенсоры, радары, лазеры, сверхпроводники;
- 47. ПРИМЕНЕНИЕ Самарий – постоянные магниты, микроволновые фильтры, ядерная промышленность; Европий – люминофоры; Тербий – люминофоры; Диспрозий
- 49. Скачать презентацию




























 ГЛАВА №7
ГЛАВА №7 Классный час
Классный час Представление методической темы: Общие методические рекомендации к решению задач по генетике.
Представление методической темы: Общие методические рекомендации к решению задач по генетике. Токарные работы
Токарные работы Скандинавская ходьба
Скандинавская ходьба Презентация на тему Планета Венера
Презентация на тему Планета Венера Неосторожная преступность
Неосторожная преступность Технические средства мультимедиа.Компьютерные презентации
Технические средства мультимедиа.Компьютерные презентации РАЗРЯДЫ ПРИЛАГАТЕЛЬНЫХ
РАЗРЯДЫ ПРИЛАГАТЕЛЬНЫХ Ассоциация ОИРОМ (объединение исследователей рынка и общественного мнения)
Ассоциация ОИРОМ (объединение исследователей рынка и общественного мнения) Урок презентация Кровеносная система человека 4 класс
Урок презентация Кровеносная система человека 4 класс  Презентация на тему: Выборочное изложение по тексту Е.В. Мурашовой
Презентация на тему: Выборочное изложение по тексту Е.В. Мурашовой Наука и образование
Наука и образование ЕГИПЕТСКИЙ ТРЕУГОЛЬНИК
ЕГИПЕТСКИЙ ТРЕУГОЛЬНИК Методы автоматической обработки тем сообщений в потоках новостных сообщений
Методы автоматической обработки тем сообщений в потоках новостных сообщений Мы готовим детей к неизвестным профессиям будущего
Мы готовим детей к неизвестным профессиям будущего Вклад Ломоносова в формирование и развитие русского литературного языка
Вклад Ломоносова в формирование и развитие русского литературного языка Проектирование корпоративных информационных систем
Проектирование корпоративных информационных систем Арт-терапия в начальной школе
Арт-терапия в начальной школе Половое воспитание ребенка
Половое воспитание ребенка Учитель физики высшей категории
Учитель физики высшей категории Алгоритм решения задач по химии
Алгоритм решения задач по химии Презентация на тему Число 3
Презентация на тему Число 3 Презентация на тему: Основные причины возникновения пожара в быту
Презентация на тему: Основные причины возникновения пожара в быту Услуги персонального менеджера
Услуги персонального менеджера Вредным привычкам скажем: «Нет!»
Вредным привычкам скажем: «Нет!» Моделирование и формализация
Моделирование и формализация Что такое родина (1 класс)
Что такое родина (1 класс)