Содержание
- 2. Сухий залишок організму людини – 5 кг Організм людини на 65-90% складається з води, її частка
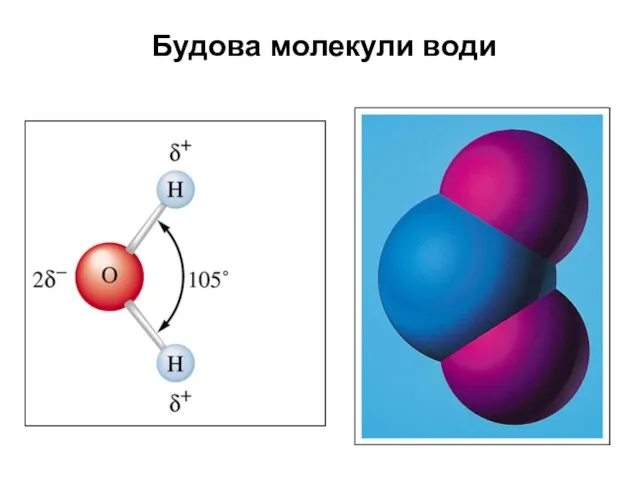
- 3. Будова молекули води
- 4. властивості води: високий поверхневий натяг, низька в’язкість, високі температури плавлення; високі температури кипіння; більш висока густина
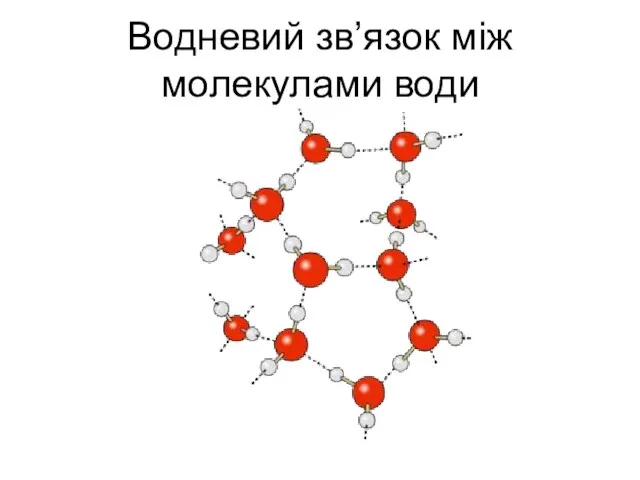
- 5. Водневий зв’язок між молекулами води
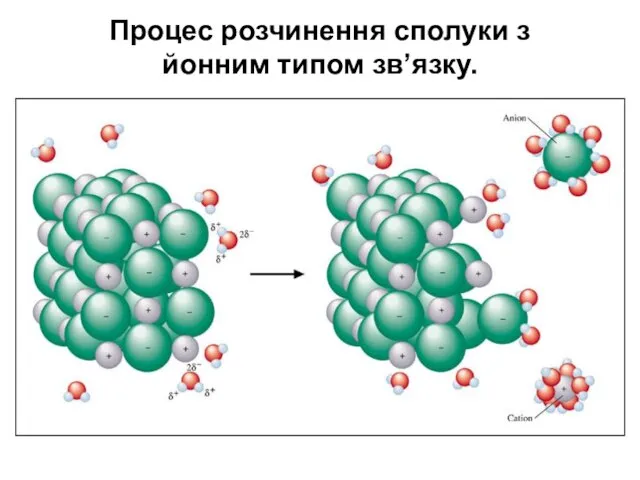
- 6. Процес розчинення сполуки з йонним типом зв’язку.
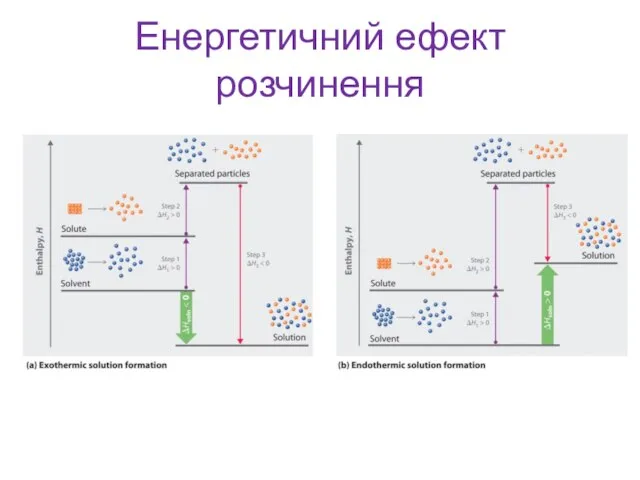
- 7. Енергетичний ефект розчинення При розчиненні руйнується зв'язок між молекулами в речовині, що розчиняється і розчиннику, що
- 8. Енергетичний ефект розчинення
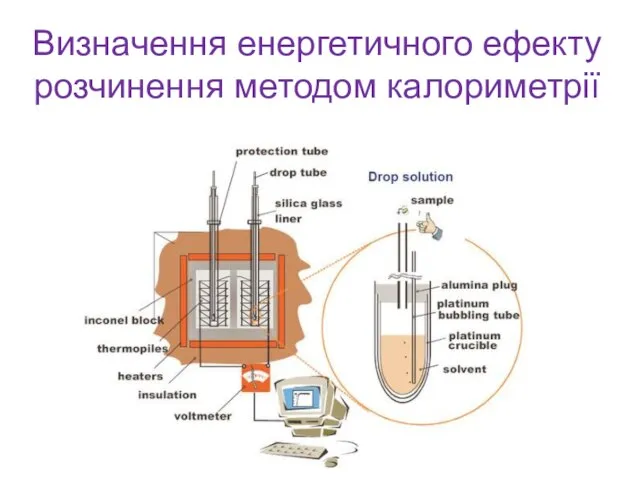
- 9. Визначення енергетичного ефекту розчинення методом калориметрії
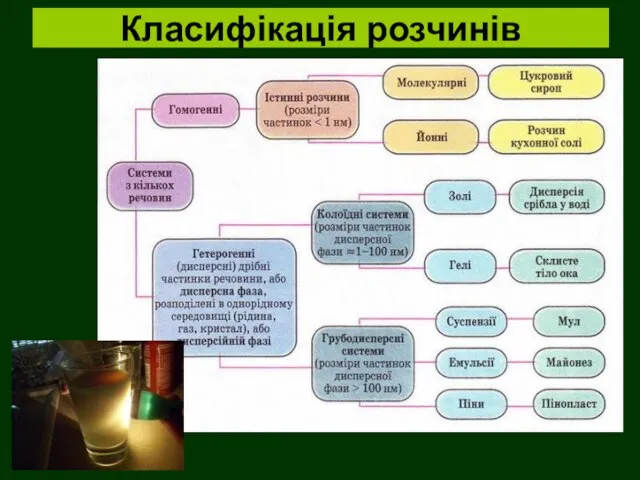
- 10. Класифікація розчинів
- 11. Розчин (за агрегатним станом) Твердий Рідкий Газоподібний
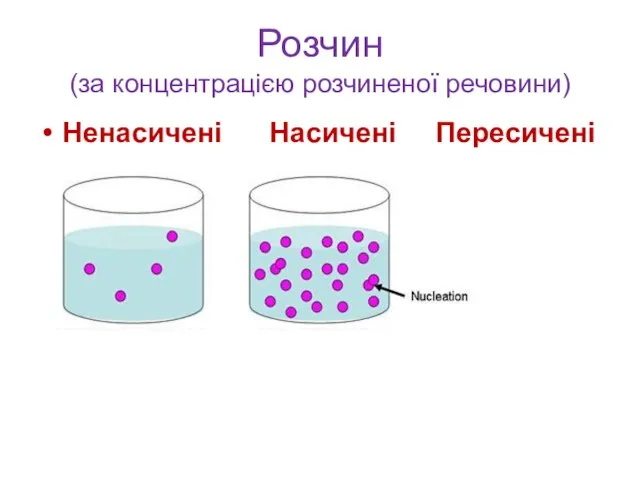
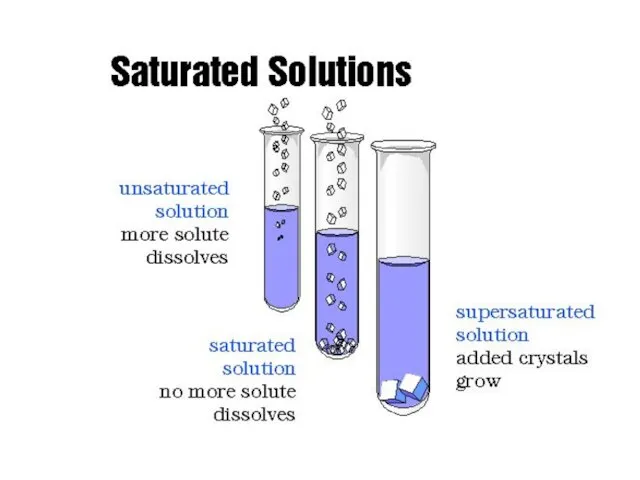
- 12. Розчин (за концентрацією розчиненої речовини) Ненасичені Насичені Пересичені
- 14. Вирощення кристалів натрій ацетату
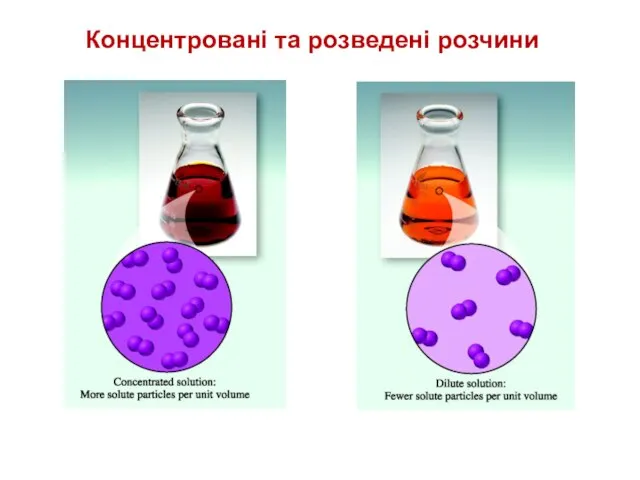
- 15. Концентровані та розведені розчини
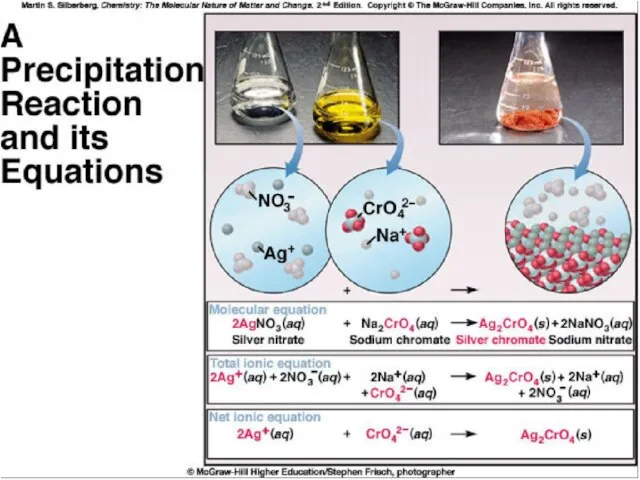
- 16. Розчини електролітів та неелектролітів
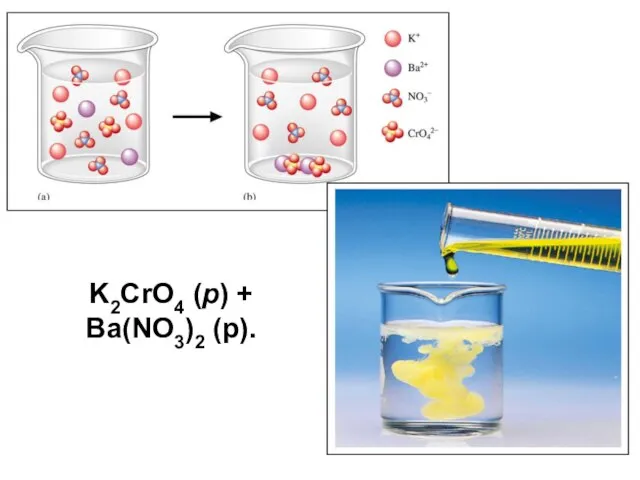
- 18. K2CrO4 (р) + Ba(NO3)2 (р).
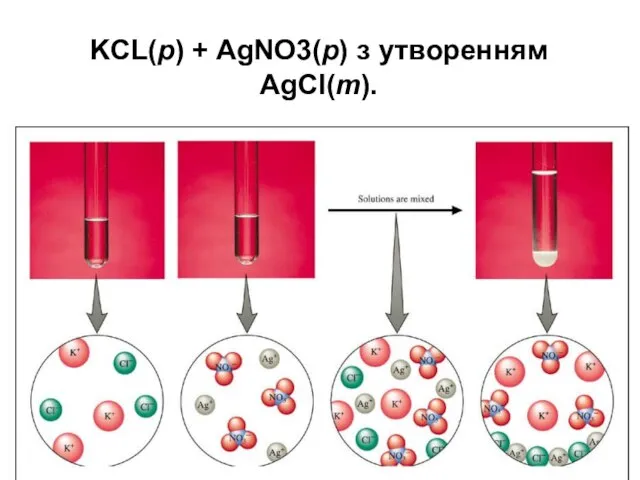
- 19. KCL(р) + AgNO3(р) з утворенням AgCl(т).
- 21. Розчинність Розчинність – це максимальна маса речовини, яка може за даних умов (температури, тиску) розчинитись у
- 22. Добуток розчинності
- 23. Масова частка – це відношення маси розчиненої речовини до маси розчину. W = m(розч.реч-ни) / m(р-ну)
- 24. Закон Генрі: маса m газу, розчиненого в рідині даного об'єму, при сталій температурі пропорційна парціальному тиску
- 25. На великих глибинах, де зовнішній тиск збільшується, збільшується розчинність газів в крові. При швидкому підйомі з
- 26. Колігативні властивості розчинів зменшення тиску насиченої пари; зменшення температури плавлення; підвищення температури кипіння; поява осмотичного тиску
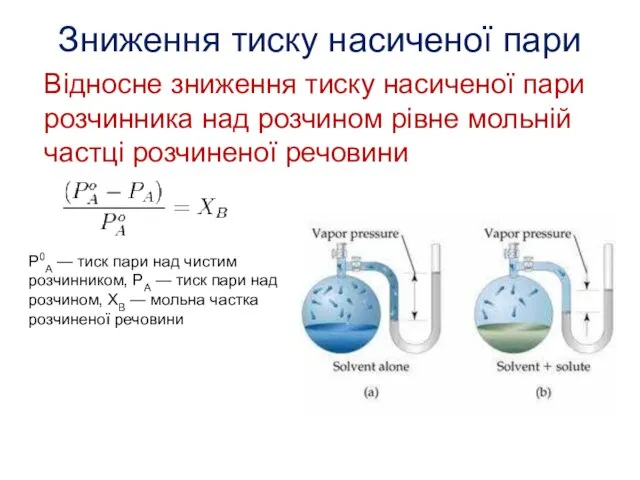
- 27. Зниження тиску насиченої пари Відносне зниження тиску насиченої пари розчинника над розчином рівне мольній частці розчиненої
- 28. Змішали 1 моль бензолу та 1 моль толуолу. При температурі 79,6 ˚С тиск насиченої пари бензену
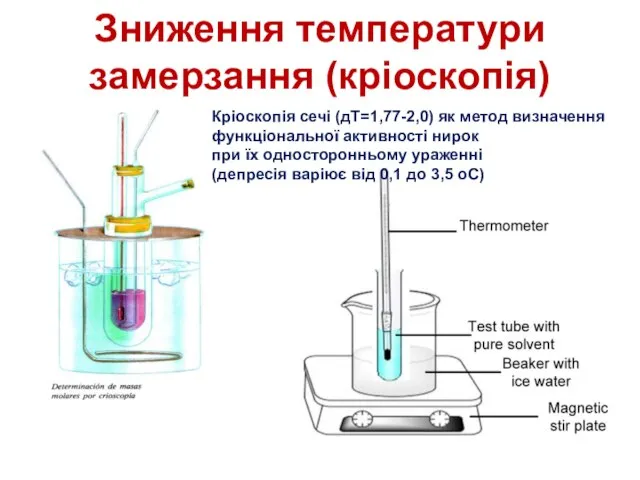
- 29. Зниження температури замерзання (кріоскопія) При затвердінні розчину спочатку випадають кристали чистого розчинника, в результаті чого розчин
- 30. Зниження температури замерзання (кріоскопія) Кріоскопія сечі (дТ=1,77-2,0) як метод визначення функціональної активності нирок при їх односторонньому
- 31. Зниження температури замерзання ΔTf = - kf m Визначте точку замерзання 2.00л морської води (kf =
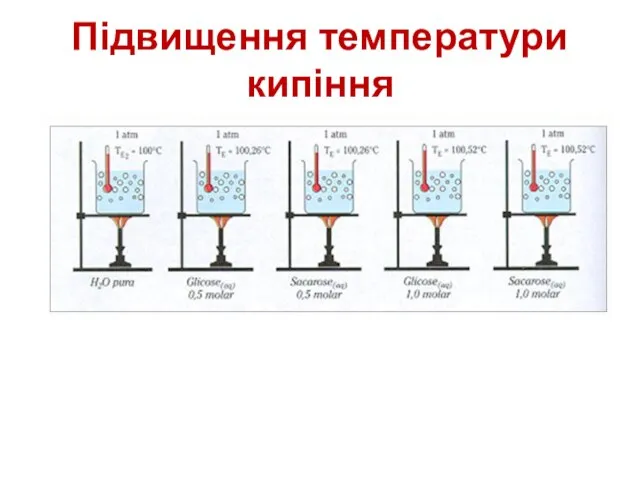
- 32. Підвищення температури кипіння
- 33. Підвищення температури кипіння (ебуліоскопія) Підвищення температури кипіння розчину прямопропорційне молярній концентрації розчиненої речовини. ΔTb = kb
- 34. Підвищення температури кипіння ΔTb = kb m Температура кипіння розчину, що містить 40 г невідомої речовини,
- 35. Осмос Процес односторонньої дифузії молекул через напівпроникну мембрану називається осмосом
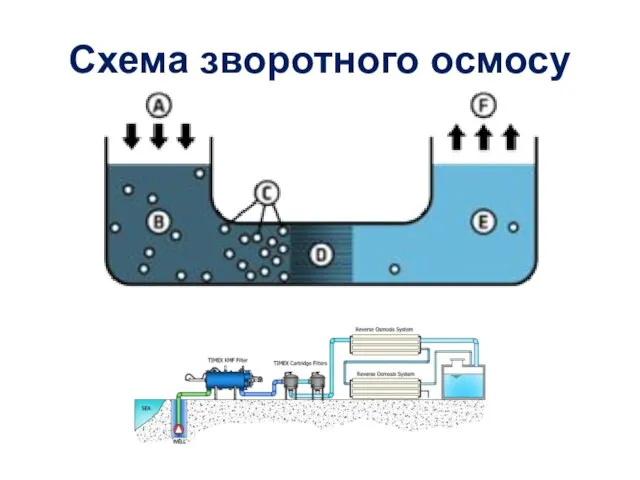
- 36. Схема зворотного осмосу
- 37. Осмос і вимірювання осмотичного тиску
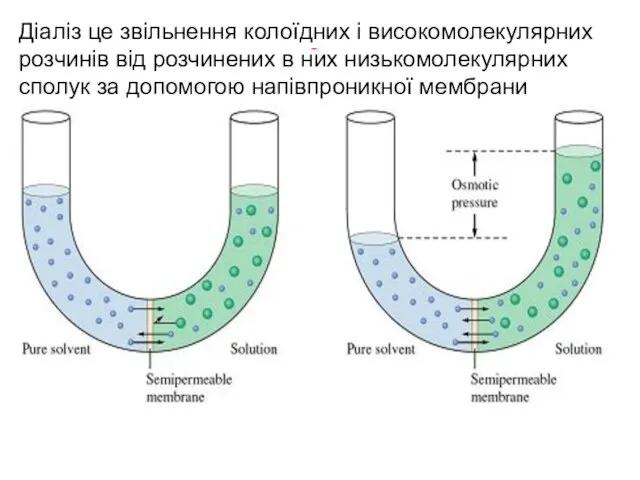
- 39. Діаліз це звільнення колоїдних і високомолекулярних розчинів від розчинених в них низькомолекулярних сполук за допомогою напівпроникної
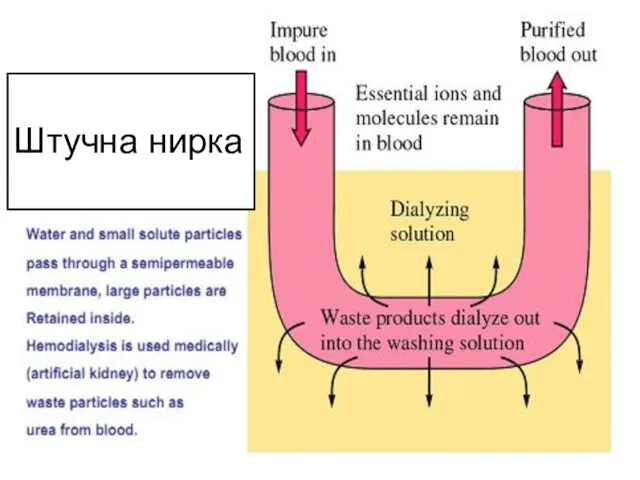
- 40. Штучна нирка
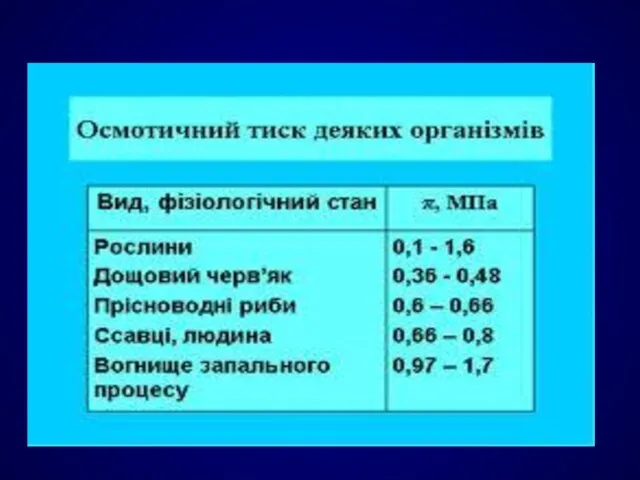
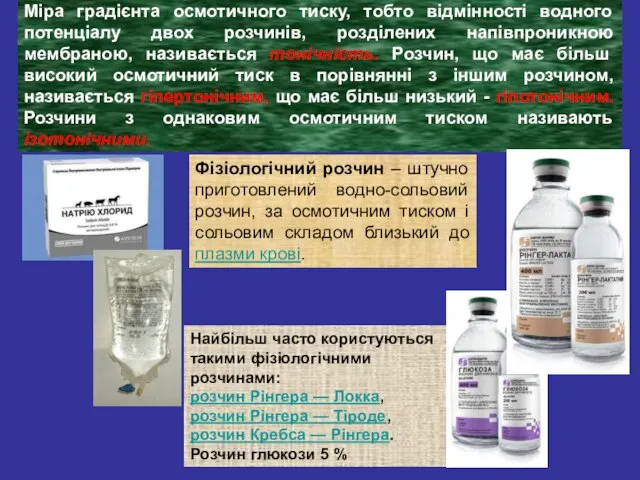
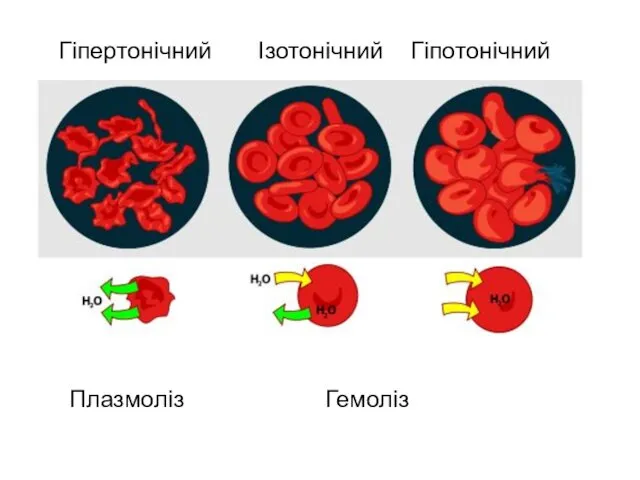
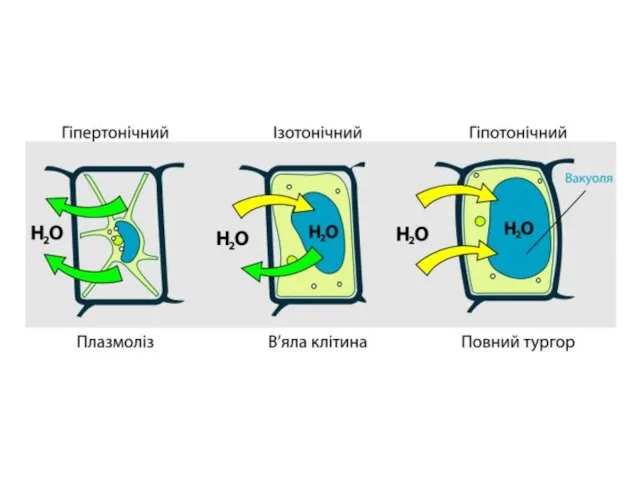
- 41. Міра градієнта осмотичного тиску, тобто відмінності водного потенціалу двох розчинів, розділених напівпроникною мембраною, називається тонічність. Розчин,
- 42. Плазмоліз Гемоліз Гіпертонічний Ізотонічний Гіпотонічний
- 45. Скачать презентацию




















 Подсудность гражданских дел
Подсудность гражданских дел Основы военной службы
Основы военной службы Профилактика и коррекция плоскостопия у детей дошкольного возраста
Профилактика и коррекция плоскостопия у детей дошкольного возраста Передача информации по техническим каналам связи
Передача информации по техническим каналам связи Постижение самого себя
Постижение самого себя  Китайский язык
Китайский язык Введение в экономику (Л7).Примеры
Введение в экономику (Л7).Примеры Главные русские меры
Главные русские меры «ТАЙНАЯ ВЕЧЕРЯ» Презентацию подготовила Ученица 9 «А» класса МБОУ «№ГИМНАЗИЯ № 38» Атишева Юлия
«ТАЙНАЯ ВЕЧЕРЯ» Презентацию подготовила Ученица 9 «А» класса МБОУ «№ГИМНАЗИЯ № 38» Атишева Юлия Buklet (2)
Buklet (2) Третий этап развития психологии
Третий этап развития психологии Тема 6_Менеджмент_юристы
Тема 6_Менеджмент_юристы «Облачные технологии в современном бизнесе» Андрей Купченко, ActiveCloud. - презентация
«Облачные технологии в современном бизнесе» Андрей Купченко, ActiveCloud. - презентация Мебель по вашим размерам и вкусовым пристрастиям Лесков&К
Мебель по вашим размерам и вкусовым пристрастиям Лесков&К Школа дошколят «Перспектива»
Школа дошколят «Перспектива» Презентация на тему Редкие животные, занесенные в Красную книгу (3 класс)
Презентация на тему Редкие животные, занесенные в Красную книгу (3 класс) Механизация приготовления концентрированных кормов в УНИЦ Агротехнопарк ФГБОУ ВО РГАТУ Рязанского района Рязанской области
Механизация приготовления концентрированных кормов в УНИЦ Агротехнопарк ФГБОУ ВО РГАТУ Рязанского района Рязанской области Информационная безопасность России
Информационная безопасность России  Бабочки
Бабочки Учитель и современный урок Взгляд на будущее нашего образования…
Учитель и современный урок Взгляд на будущее нашего образования… Реализм как художественный стиль эпохи
Реализм как художественный стиль эпохи Презентация на тему Согласование времен английского языка
Презентация на тему Согласование времен английского языка  Калла из фоамирана
Калла из фоамирана Решение заданий с модулем и параметром
Решение заданий с модулем и параметром Презентация на тему Мир профессий
Презентация на тему Мир профессий  Королевские ворота
Королевские ворота Презентация на тему Искусство первобытного человека
Презентация на тему Искусство первобытного человека 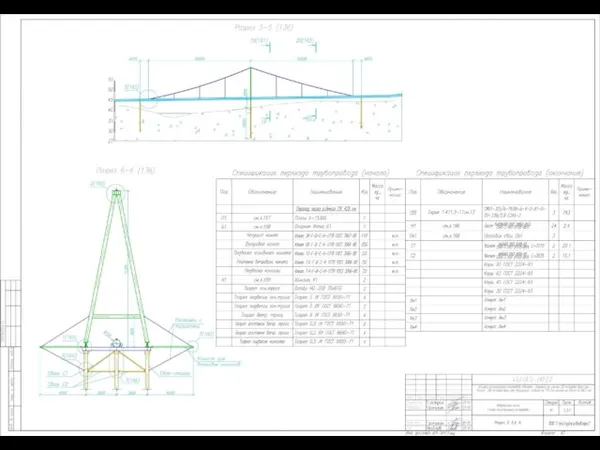 Проектное решение сваи СМОТ газопровод
Проектное решение сваи СМОТ газопровод