Содержание
- 2. План лекції 1. Теорії, що пояснюють процес само-спалахування 2. Температура самоспалахування речовин. Фактори, що впливають на
- 3. 1. ТЕОРІЇ, ЩО ПОЯСНЮЮТЬ ПРОЦЕС САМОСПАЛАХУВАННЯ Самоспалахування – виникнення горіння внаслідок різкого збільшення швидкості екзотермічних реакцій
- 4. 1.1. Теплова теорія самоспалахування За тепловою теорією умовою виникнення горіння є досягнення критичної температури в системі,
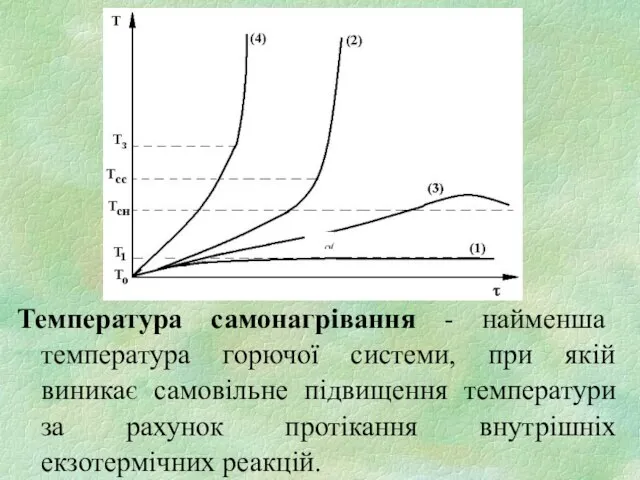
- 5. Температура самонагрівання - найменша температура горючої системи, при якій виникає самовільне підвищення температури за рахунок протікання
- 6. Інтенсивність тепловиділення: Графік зміни швидкості тепловиділення q(+) з температурою відображається експоненційною кривою. Інтенсивність тепловіддачі: q(-) =
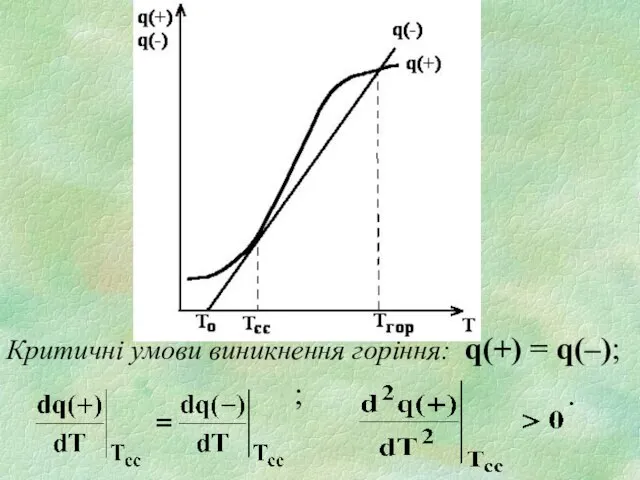
- 7. Критичні умови виникнення горіння: q(+) = q(–); ; .
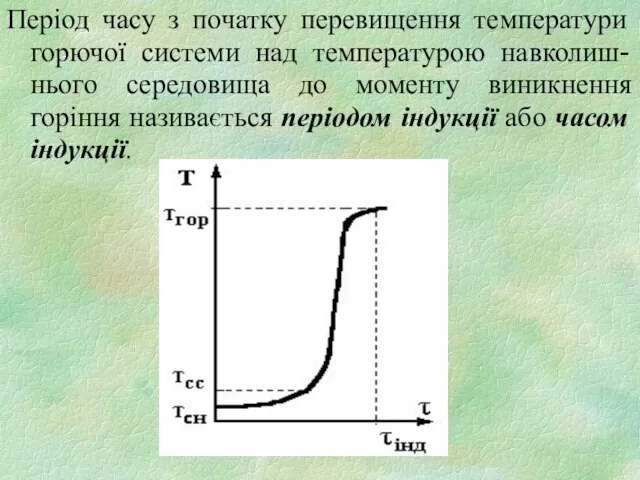
- 8. Період часу з початку перевищення температури горючої системи над температурою навколиш-нього середовища до моменту виникнення горіння
- 9. 1.2. Ланцюгова теорія самоспалахування За ланцюговою теорією виникнення горіння (тобто різке збільшення швидкості реакції окислення) є
- 10. ТИПИ ЛАНЦЮГОВИХ РЕАКЦІЙ Зародження (ініціювання) ланцюгів - стадія ланцюгової реакції, в якій утворюються вільні радикали з
- 11. Розгалуження ланцюгів - стадія ланцюгового процесу, у якій перетворення активних проміжних продуктів реакції призводить до збільшення
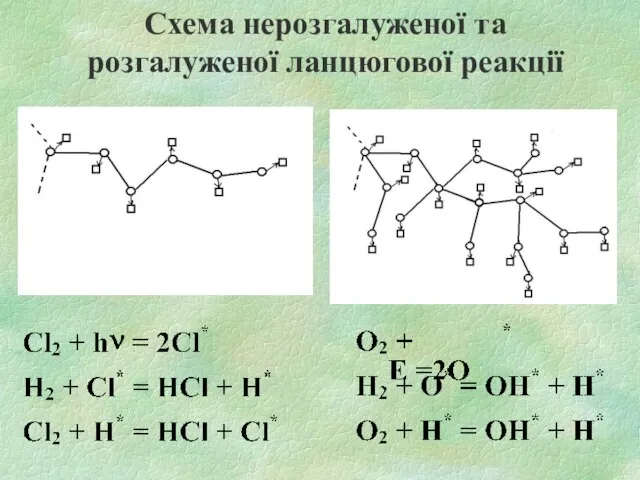
- 12. Схема нерозгалуженої та розгалуженої ланцюгової реакції
- 13. Швидкість ланцюгової реакції: де n – концентрація активних центрів, ωо - швидкість початкового ініціювання (утворення) АЦ,
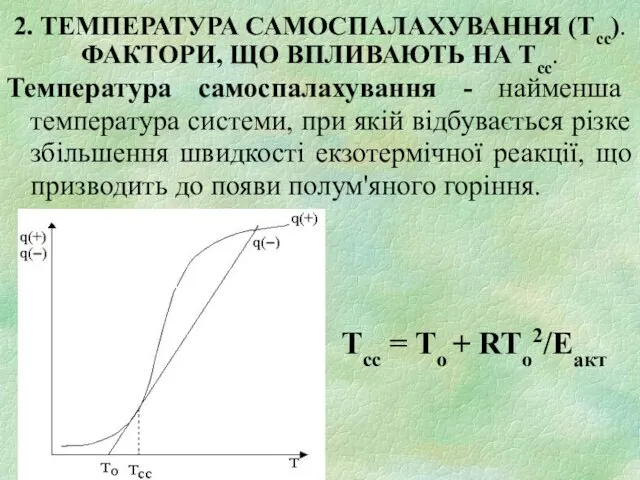
- 14. 2. ТЕМПЕРАТУРА САМОСПАЛАХУВАННЯ (Тсс). ФАКТОРИ, ЩО ВПЛИВАЮТЬ НА Тсс. Температура самоспалахування - найменша температура системи, при
- 15. На Tсс речовин впливають три групи факторів: 1) вид горючої речовини середня довжина вуглецевого ланцюга lсер;
- 16. 2.1. Хімічна будова горючої речовини При збільшенні енергії розриву зв'язку реакція окислення, а отже й процес
- 18. 2.2. Склад горючої суміші Концентрація горючої речовини q(+)=QнVгсwхр Найбільша швидкість хімічної реакції, а отже і тепловиділення
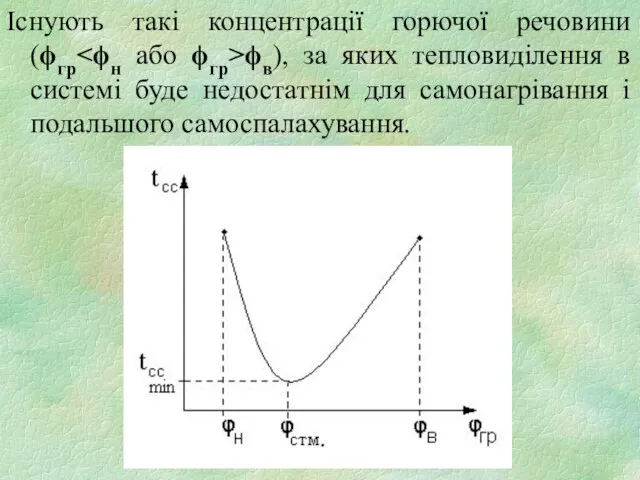
- 19. Існують такі концентрації горючої речовини (ϕгр ϕв), за яких тепловиділення в системі буде недостатнім для самонагрівання
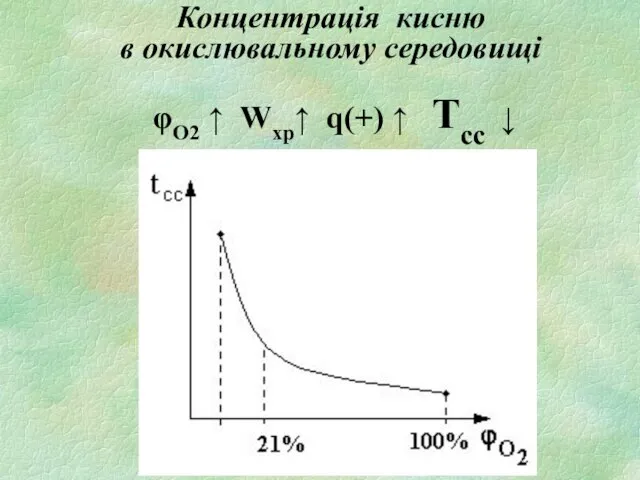
- 20. Концентрація кисню в окислювальному середовищі φО2 ↑ Wхр↑ q(+) ↑ Tсс ↓
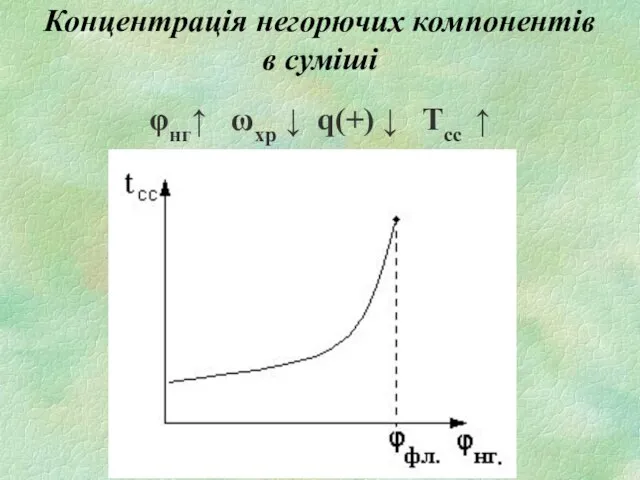
- 21. Концентрація негорючих компонентів в суміші φнг↑ ωхр ↓ q(+) ↓ Tсс ↑
- 22. 2.3. Умови, в яких знаходиться система Об'єм і діаметр посудини. q(+) = QнVгсwхр q(-) = α
- 23. 3. ВИЗНАЧЕННЯ Тсс Експериментальні методи 1) метод впускання заздалегідь готової холодної суміші у вакуумовану нагріту посудину;
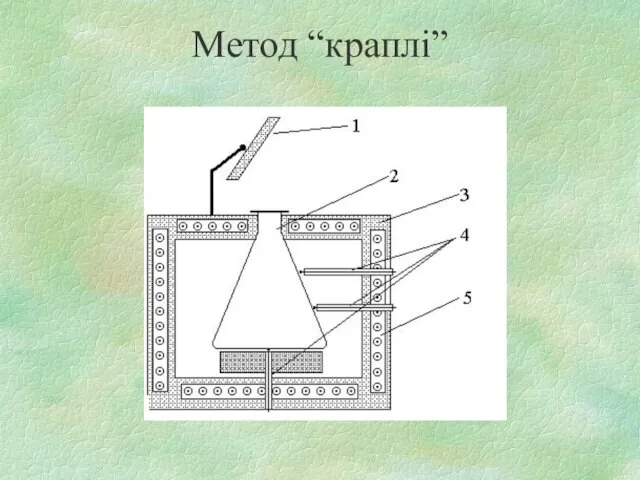
- 24. Метод “краплі”
- 25. Розрахункове визначення Tсс при lcеp ≤ 5 при lcеp ≥ 5 Ланцюг - безперервна послідовність пов'язаних
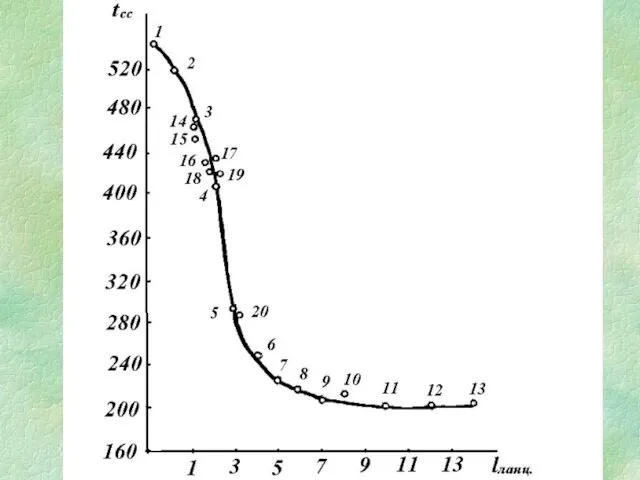
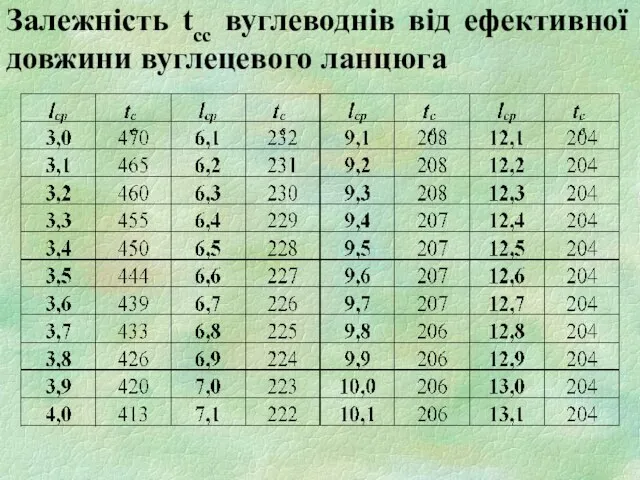
- 26. Залежність tсс вуглеводнів від ефективної довжини вуглецевого ланцюга
- 27. Температуру самоспалахування інших класів органічних сполук можна розрахувати за формулою: tсс = а⋅tссалк + b де
- 28. 4. Практичне значення температури самоспалахування Тсс використовують для оцінки пожежної небезпеки речовин Чим нижче температура самоспалахування
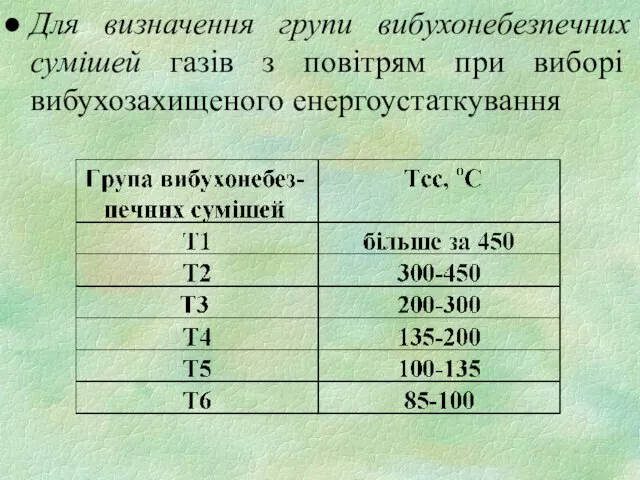
- 29. Для визначення групи вибухонебезпечних сумішей газів з повітрям при виборі вибухозахищеного енергоустаткування
- 31. Скачать презентацию
















 Синтаксические свойства инфинитива
Синтаксические свойства инфинитива Презентация 1
Презентация 1 Die BRD (1949 -1990)
Die BRD (1949 -1990) Родными тропами
Родными тропами SPb_GBOU_SPO_Akusherskiy_kolledzh_Yana_Skolova_402 (1)
SPb_GBOU_SPO_Akusherskiy_kolledzh_Yana_Skolova_402 (1) Реставрация картины Г. Угрюмова Испытание силы Яна Усмаря
Реставрация картины Г. Угрюмова Испытание силы Яна Усмаря «Пётр Великий русской литературы» (В.Г.Белинский)
«Пётр Великий русской литературы» (В.Г.Белинский) История и перспективы производства видеопродукции нового формата в России и за рубежом
История и перспективы производства видеопродукции нового формата в России и за рубежом Создание единого китайского государства
Создание единого китайского государства Экологические проблемы мира
Экологические проблемы мира Национальная посуда народов мира
Национальная посуда народов мира Персидская империя.
Персидская империя. Программное обеспечение для поддержки информационной бизнес-аналитики
Программное обеспечение для поддержки информационной бизнес-аналитики Презентация на тему Классификация профессий Профессия и специальность Способы классификации
Презентация на тему Классификация профессий Профессия и специальность Способы классификации Сжатие информации. Алгоритм Хаффмана
Сжатие информации. Алгоритм Хаффмана LIEBHERR LTM 1160-5.1Самоходный кран большой грузоподъемности (160 тонн)
LIEBHERR LTM 1160-5.1Самоходный кран большой грузоподъемности (160 тонн) Презентация на тему Кайнозойская эра
Презентация на тему Кайнозойская эра Презентация на тему Трудовая дисциплина и ответственность за её нарушение
Презентация на тему Трудовая дисциплина и ответственность за её нарушение  Poker face
Poker face Волейбол – виды подач
Волейбол – виды подач Эволюция интернет-трейдинга
Эволюция интернет-трейдинга ГЕНЕРАТОРЫ ИМПУЛЬСНЫХ НАПРЯЖЕНИЙ СУБНАНОСЕКУНДНОЙ ДЛИТЕЛЬНОСТИразработки ЗАО «НПАО ФИД-технология»
ГЕНЕРАТОРЫ ИМПУЛЬСНЫХ НАПРЯЖЕНИЙ СУБНАНОСЕКУНДНОЙ ДЛИТЕЛЬНОСТИразработки ЗАО «НПАО ФИД-технология» Название проекта
Название проекта Новый Год
Новый Год Немеркнущая красота России или Сквозь эпохи и поколения
Немеркнущая красота России или Сквозь эпохи и поколения Основные понятия «Теории вероятностей»
Основные понятия «Теории вероятностей» Овощи и их вредители
Овощи и их вредители География сельского хозяйства мира
География сельского хозяйства мира