Содержание
- 2. Цель урока: познакомиться с историей открытия и распространением щелочных металлов в природе и живых организмах; изучить
- 3. Металлы Сu, Au, Ag не взаимодействуют с водой даже при нагревании. Металлы обладают электропроводностью и теплопроводностью.
- 7. История открытия Нахождение в природе Нахождение в живых объектах природы Физические свойства, особенности строения атомов Химические
- 8. В ЧЁМ УНИКАЛЬНОСТЬ ЩЕЛОЧНЫХ МЕТАЛЛОВ?
- 9. ИСТОРИКИ
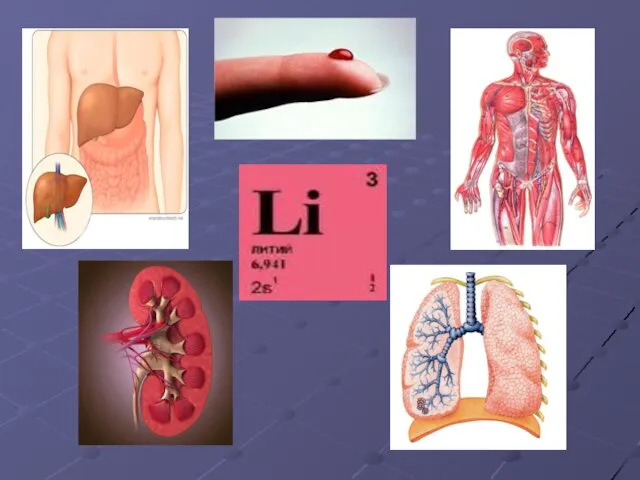
- 10. ЛИТИЙ (Lithium) 3Li Литий – самый лёгкий серебристо – белый металл. Открыт в 1817 году шведским
- 11. Вскоре Арфведсон обнаружил литий в сподумене LiAl[Si2O6], позже ставшем важнейшим минералом элемента № 3. В 1818
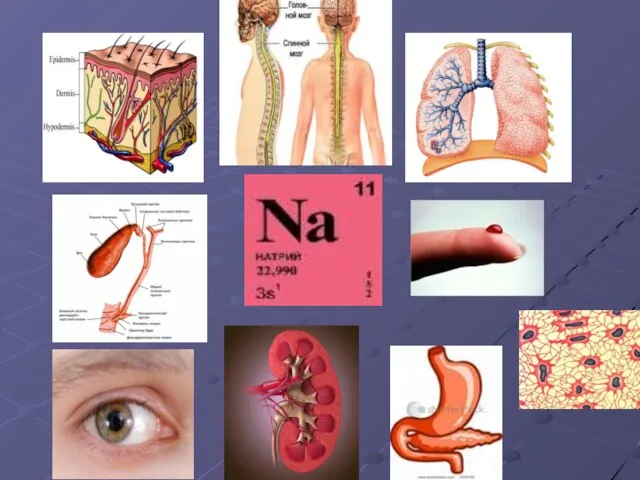
- 12. НАТРИЙ (Natrium)11Na Натрий – мягкий, серебристо – белый металл. В чистом виде получен при электролизе едкого
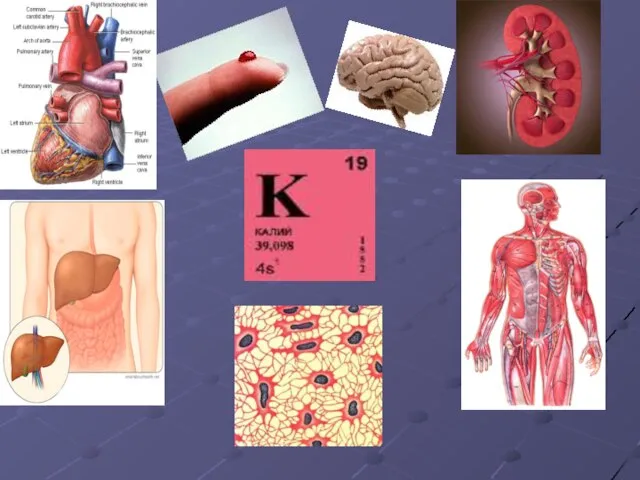
- 13. КАЛИЙ (Kalium) 19K Калий – серебристо-белый, очень мягкий и легкоплавкий металл. Получен при электролизе едкого кали
- 14. РУБИДИЙ (Rubidium) 37Rb Рубидий – лёгкий и очень мягкий (как воск),серебристо-белый металл. Открыт в 1861 году
- 15. ЦЕЗИЙ (Caesium) 55Cs Блестящая поверхность цезия имеет бледно-золотистый цвет. В 1860 году немецкие учёные Р. Бунзен
- 16. Цезий, как известно, был первым элементом, открытым с помощью спектрального анализа, разработанного в 1859 году немецкими
- 17. Франций (Franium) 87Fr Возможность существования и основные свойства элемента №87 были предсказаны Д.И.Менделеевым. В 1871 году
- 18. Первое сообщение об открытии 87-элемента как продукта радиоактивного распада актиния-228 сделал в 1913 году английский химик
- 19. ГЕОЛОГИ
- 20. Нахождение в природе Натрий и калий широко распространены в природе в виде солей Соединения других щелочных
- 21. БИОЛОГИ
- 25. Среднее содержание в организме человека 608мг. Суточная потребность 1.5-6мг.
- 26. Суточная потребность 0,004-0,03мг
- 27. В организме человека не содержится.
- 28. ФИЗИКИ
- 29. ХИМИКИ
- 30. ТЕХНОЛОГИ - ПРАКТИКИ
- 31. LI
- 32. Na
- 33. K
- 34. Rb
- 35. Cs
- 36. Франций . Последний член семейства щелочных металлов франций настолько радиоактивен, что его нет в земной коре
- 37. Правильные ответы Б В Г В А
- 38. Согласны синий Не согласны красный
- 39. ИТОГОВАЯ ОЦЕНКА 10 – 12 баллов 5 8 – 10 баллов 4 6 – 8 баллов
- 40. ПАРАД МЕТАЛЛОВ, КАК ПАРАД ПЛАНЕТ, НЕТ ГЛАВНЫХ И ВТОРОСТЕПЕННЫХ НЕТ. МЕТАЛЛЫ РАЗНЫЕ ПО-СВОЕМУ ВАЖНЫ И В
- 42. Скачать презентацию







![Вскоре Арфведсон обнаружил литий в сподумене LiAl[Si2O6], позже ставшем важнейшим минералом элемента](/_ipx/f_webp&q_80&fit_contain&s_1440x1080/imagesDir/jpg/276433/slide-10.jpg)


























 Speaking shopping
Speaking shopping Наложение повязок
Наложение повязок BRITISH POETS
BRITISH POETS Урок 2. Практическая работа Обозначение материков
Урок 2. Практическая работа Обозначение материков Основные идеи«Демократического выбора»в области экономической политики
Основные идеи«Демократического выбора»в области экономической политики Команда – главный компонент эффективности
Команда – главный компонент эффективности Информационный дефицит
Информационный дефицит Очистка, дезинфекция, хранение небулайзера при использовании одним пациентом
Очистка, дезинфекция, хранение небулайзера при использовании одним пациентом Приготовление пончиков
Приготовление пончиков Культура России во второй половине XIX- начала XX века
Культура России во второй половине XIX- начала XX века Фармакокинетический мониторинг
Фармакокинетический мониторинг Однородные члены, связанные сочинительными союзами, и пунктуация при них
Однородные члены, связанные сочинительными союзами, и пунктуация при них Виды моделей данных
Виды моделей данных Лекция 0Основы компьютерной графики
Лекция 0Основы компьютерной графики Всероссийская олимпиада по искусству
Всероссийская олимпиада по искусству Математика может стать понятней…
Математика может стать понятней… Big ben
Big ben Конспект организованной образовательной деятельности в подготовительной группе
Конспект организованной образовательной деятельности в подготовительной группе Find 1 word for 3 pictures
Find 1 word for 3 pictures Контур. Бухгалтерия: о возможностях сервиса
Контур. Бухгалтерия: о возможностях сервиса Информация о неиспользуемом объекте Характеристика объекта Капитальное строение (изолированное (встроенное) помещение), г.Кричев,
Информация о неиспользуемом объекте Характеристика объекта Капитальное строение (изолированное (встроенное) помещение), г.Кричев, Кафедра маркетингового менеджмента, город Донецк. Команда Новаторы
Кафедра маркетингового менеджмента, город Донецк. Команда Новаторы EXPERT и PROF
EXPERT и PROF Спортивные товары бренда Kelme
Спортивные товары бренда Kelme Формы, методы и технологии продвижения школьной медиации
Формы, методы и технологии продвижения школьной медиации Зрительные диктанты И.Т. Федоренко
Зрительные диктанты И.Т. Федоренко А19.Слитное, дефисное, раздельное написание.
А19.Слитное, дефисное, раздельное написание. Tsiolkovskiy
Tsiolkovskiy