Содержание
- 2. Реформа системы регулирования фармацевтического рынка В т.г. намечается реформа системы регулирования фармацевтического рынка готовится новое законодательство
- 3. Глобальное видение проблемы При этом крайне желательно посмотреть как решается эта проблема в других странах (глобальное
- 4. Видение проблемы на глобальном уровне Из материалов международного совещания по фармацевтическому качеству, Голландия, ноябрь 2003 г.
- 5. Система регулирования фармацевтического рынка Недостатки нашего видения: в 2002 г. почти никто не возражал против включения
- 6. Система регулирования (продолжение) Терминология: - фармпродукт, - качество фармпродуктов, - обеспечение качества, - GMP – новое
- 7. Система регулирования (продолжение 2) Еще о недостатках видения
- 8. Система регулирования (продолжение 3) Причины недостатков видения
- 9. Правила GMP развиваются самоинспекция, валидация, Уполномоченное Лицо, аудит поставщиков, параметрический выпуск, приложения (порядка 20 приложений) За
- 10. Нововведения за 2003 г. Директива 2003/94/ЕС от 8.10.2003 г., изменившая трактовку понятия «качество лекарств» пересмотр двух
- 11. Что впереди? GMP+ Статистические методы контроля Управление рисками Непрерывный аналитический контроль процессов В перспективе - единая
- 12. «Комплексная система обеспечения качества, охватывающая все факторы разработки, производства и снабжения, влияющие, порознь или совместно, на
- 13. Статистические методы контроля качества Анализ тенденций 6 сигма процесс Приемочный контроль Управление процессами Соответствие процесса и
- 14. Управление рисками пригодность для применения – верховенство потребителя приостановить ужесточение спецификаций, но более устойчивые свойства продукции
- 15. Единая система фармацевтического качества Разработку (качество через дизайн), Экспертизу регистрационных материалов, GMP, Инспектирование Пострегистрационные изменения ОБЪЕДИНЯЕТ
- 16. Единая система для всех стран Предполагается, что единая система будет принята во всех странах и на
- 17. Важнейшие элементы системы обеспечения качества лекарств на национальном уровне
- 18. Лаборатории Фармакопеи Инспекции GMP ОТД CTD-Q Контуры системы обеспечения фармацевтического качества 21 века КАЧЕСТВО
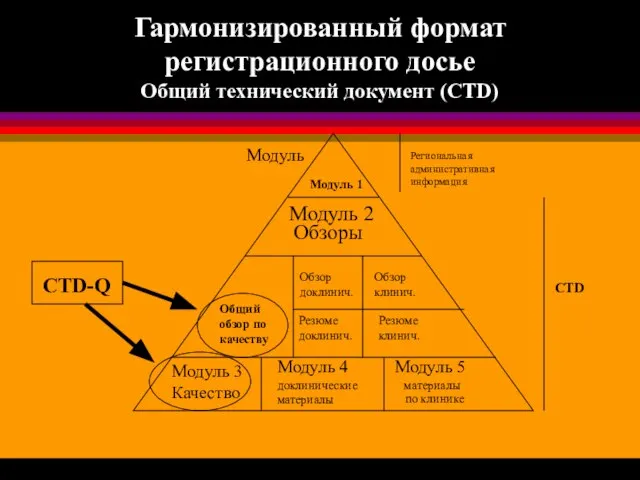
- 19. Гармонизированный формат регистрационного досье Общий технический документ (CTD) Модуль 1 Модуль 2 Обзор доклинич. Обзор клинич.
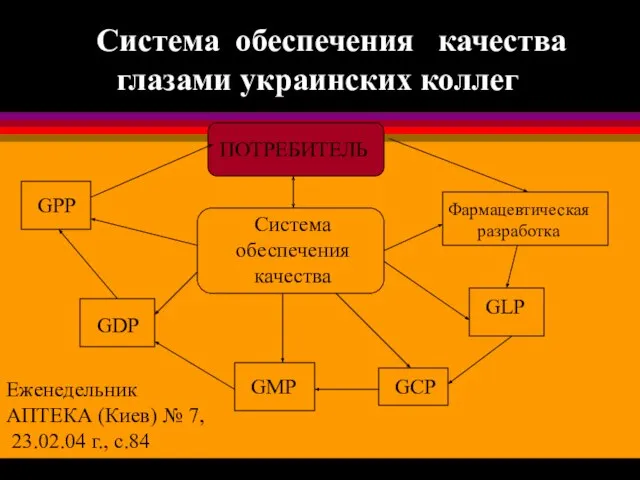
- 20. Система обеспечения качества глазами украинских коллег ПОТРЕБИТЕЛЬ Система обеспечения качества Фармацевтическая разработка GLP GCP GMP GDP
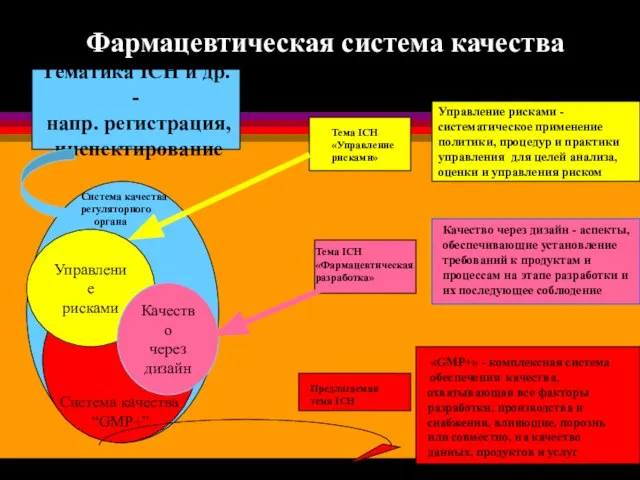
- 21. Управление рисками Качество через дизайн Управление рисками - систематическое применение политики, процедур и практики управления для
- 23. Скачать презентацию

















 Merci professeur!
Merci professeur! Обучение персонала. Тема 7
Обучение персонала. Тема 7 Правописание падежных окончаний имен существительных единственного числа
Правописание падежных окончаний имен существительных единственного числа Презентация на тему Рельеф Южной Америки (7 класс)
Презентация на тему Рельеф Южной Америки (7 класс) Популяции
Популяции Частые и популярные вопросы, а также помощь новичку.
Частые и популярные вопросы, а также помощь новичку. Урок рисования
Урок рисования Почему мы часто слышим слово «экология»? (1 класс)
Почему мы часто слышим слово «экология»? (1 класс) Сгибание и разгибание рук в упоре лежа на полу
Сгибание и разгибание рук в упоре лежа на полу Лекція 2 Принципи та методи психологічних досліджень (1)
Лекція 2 Принципи та методи психологічних досліджень (1) 5096c16a06984dc6b0c01fd05158c787
5096c16a06984dc6b0c01fd05158c787 Правила техники безопасности при работе с тканью
Правила техники безопасности при работе с тканью Влияние компьютера на здоровье человека
Влияние компьютера на здоровье человека Первое сентября
Первое сентября Прямые паруса и их бегучий такелаж шлюпа Мирный
Прямые паруса и их бегучий такелаж шлюпа Мирный Плоскостопие
Плоскостопие Правительство Пермского края Об итогах социально-экономического развития Октябрьского муниципального района Пермского края за
Правительство Пермского края Об итогах социально-экономического развития Октябрьского муниципального района Пермского края за  Когда в сердце разгорается любовь
Когда в сердце разгорается любовь Есть или не есть –вот в чем вопрос?
Есть или не есть –вот в чем вопрос? Скарбнiца народнай мудрасцi
Скарбнiца народнай мудрасцi Как образуются кристаллы?
Как образуются кристаллы? ТАТАРО-МОНГОЛЬСКОЕ НАШЕСТВИЕ НА РУСЬ
ТАТАРО-МОНГОЛЬСКОЕ НАШЕСТВИЕ НА РУСЬ  Научные базы данных EBSCO - основной электронный ресурс для академических библиотек
Научные базы данных EBSCO - основной электронный ресурс для академических библиотек Порядок и хаос 5 класс
Порядок и хаос 5 класс Взаимоотношения между организмами
Взаимоотношения между организмами Память и внимание
Память и внимание Биологические системы самоорганизации
Биологические системы самоорганизации Работа: «Дух русского народа крепче всякого оружия»
Работа: «Дух русского народа крепче всякого оружия»