Содержание
- 2. П Р О Ц Е С С Ы П Е Р Е Х О Д А
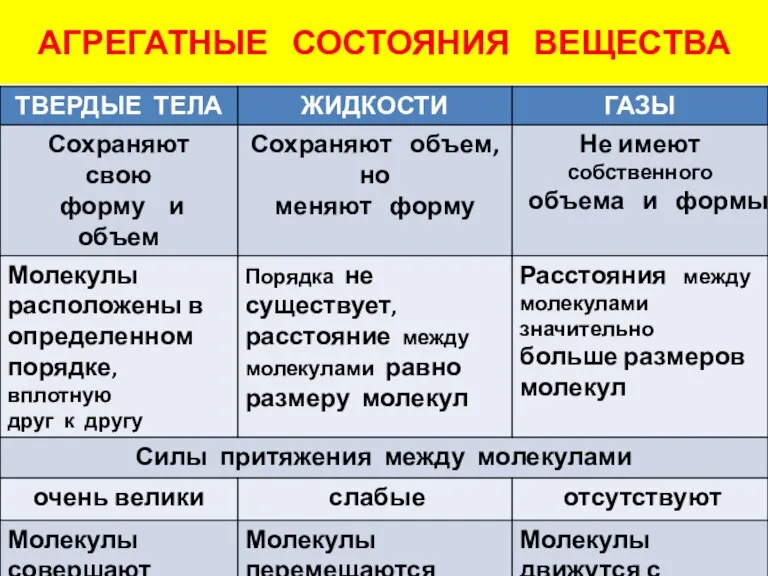
- 3. АГРЕГАТНЫЕ СОСТОЯНИЯ ВЕЩЕСТВА
- 4. ИСПАРЕНИЕ Испарением называется переход из жидкого состояния в газообразное. С точки зрения молекулярно-кинетической теории, испарение –
- 5. ОСОБЕННОСТИ ИСПАРЕНИЯ Испарение происходит при любой температуре Только со свободной поверхности При испарении температура жидкости понижается
- 6. СКОРОСТЬ ИСПАРЕНИЯ ЗАВИСИТ От температуры (с ростом Т увелич. ЕК ) От площади свободной поверхности (большее
- 7. К О Н Д Е Н С А Ц И Я – это переход вещества из
- 8. ПРИМЕРЫ КОНДЕНСАЦИИ Образование росы или тумана по утрам (температура понижается и водяной пар становится перенасыщенным) Образование
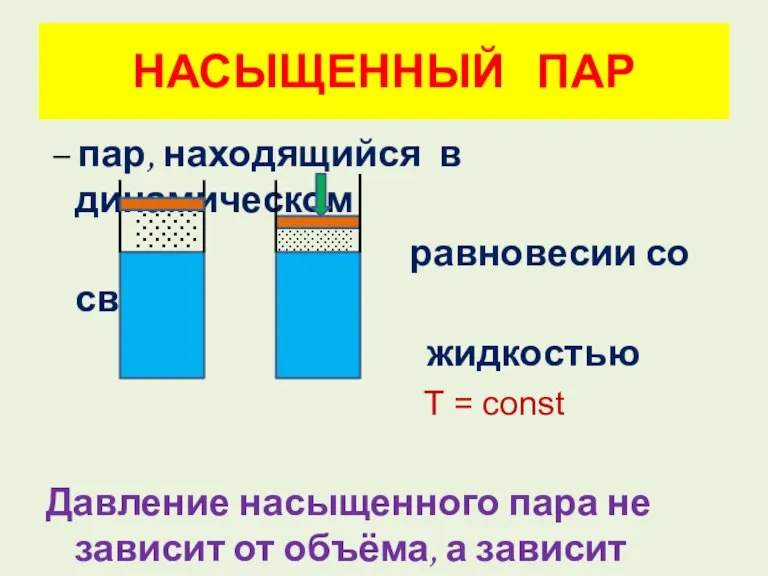
- 9. НАСЫЩЕННЫЙ ПАР – пар, находящийся в динамическом равновесии со своей жидкостью T = const Давление насыщенного
- 10. НАСЫЩЕННЫЙ ПАР и НЕНАСЫЩЕННЫЙ ПАР
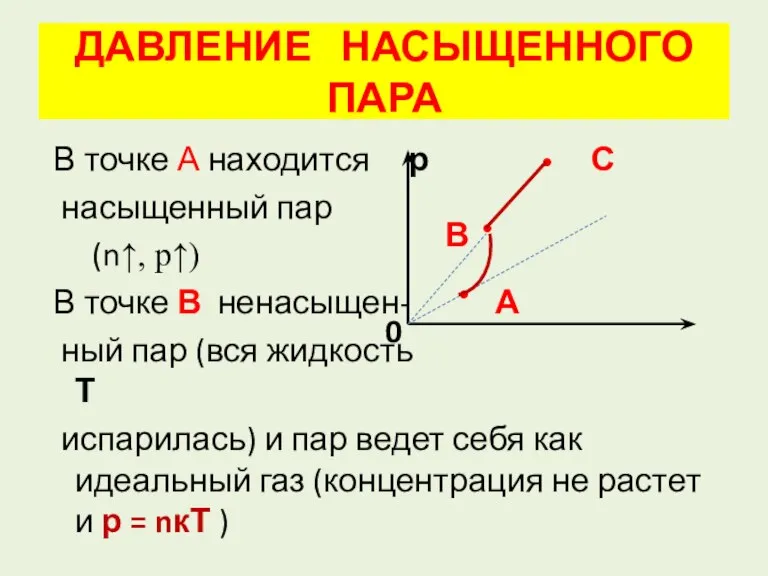
- 11. ДАВЛЕНИЕ НАСЫЩЕННОГО ПАРА В точке А находится р С насыщенный пар (n↑, р↑) В точке В
- 12. КИПЕНИЕ Кипение - это процесс бурного парообразования по всему объему жидкости, происходящий внутрь многочисленных пузырей пара.
- 13. МЕХАНИЗМ КИПЕНИЯ В жидкости всегда присутствуют растворенные газы, которые выделяются на дне и стенках сосуда. Пары
- 14. ИТОГ УРОКА 1. В чем состоит разница между кипением и испарением? 2. Назвать особенности испарения? 3.
- 15. 6. Как меняется давление насыщенного пара с ростом температуры? 7. Пар и газ – это одно
- 16. ДОМАШНЕЕ ЗАДАНИЕ § 70, 71 Знать механизмы кипения и испарения Уметь объяснять график
- 18. Скачать презентацию











 Презентация на тему Аттестация и квалификационный экзамен гражданского служащего таможенных органов
Презентация на тему Аттестация и квалификационный экзамен гражданского служащего таможенных органов Схемы на переключаемых емкостях
Схемы на переключаемых емкостях Основы организационно-управленческой диагностики
Основы организационно-управленческой диагностики Практика- Инфекции 1- (общие положения. Туберкулез и сепсис)
Практика- Инфекции 1- (общие положения. Туберкулез и сепсис) Мониторинг в образовании
Мониторинг в образовании Электротехника и электроника
Электротехника и электроника МультиБанк - инструмент увеличения продаж
МультиБанк - инструмент увеличения продаж Факторы производства, производительность труда
Факторы производства, производительность труда МОУ СОШ № 4 . г. Всеволожск Ленинградская область Тема. Дисциплина Ученица 7 класса «Б» Матвейчук Антонина Учитель Потапова О.Н.
МОУ СОШ № 4 . г. Всеволожск Ленинградская область Тема. Дисциплина Ученица 7 класса «Б» Матвейчук Антонина Учитель Потапова О.Н. Презентация1
Презентация1 Структура СРНС (лекция 4-1)
Структура СРНС (лекция 4-1) Стихотворения для детей Николай Алексеевич Некрасов
Стихотворения для детей Николай Алексеевич Некрасов Системный анализ в профессиональной деятельности 1 раздел
Системный анализ в профессиональной деятельности 1 раздел Что нас окружает ?
Что нас окружает ? Санитарно-техническое оборудование. Условные обозначения и сокращения
Санитарно-техническое оборудование. Условные обозначения и сокращения Марийская эстрадная песня и ее исполнители
Марийская эстрадная песня и ее исполнители PPT Organisms
PPT Organisms Методическое пособие для школьных психологов«Психологическая подготовка учащихся к ЕГЭ»
Методическое пособие для школьных психологов«Психологическая подготовка учащихся к ЕГЭ» Население Эстонии в процентах
Население Эстонии в процентах Направления и тарифы сборных перевозок
Направления и тарифы сборных перевозок Учение о лицах в Древнем Риме
Учение о лицах в Древнем Риме Гальванопластика
Гальванопластика Библиотека Родина в три века Стара Загора, 29 септ. 2010 150 години. - презентация
Библиотека Родина в три века Стара Загора, 29 септ. 2010 150 години. - презентация МБУДО Дом детства и юношества Ритм
МБУДО Дом детства и юношества Ритм ПОНЯТИЕ ДОГОВОРА
ПОНЯТИЕ ДОГОВОРА Методы регистрации магнитных полей человека
Методы регистрации магнитных полей человека Тургенев И.С.
Тургенев И.С. Сельское хозяйство. Растениеводство
Сельское хозяйство. Растениеводство