Содержание
- 2. «Жизнь есть способ существования белковых тел» (Фридрих Энгельс)
- 3. План 1. Белки. 2. Аминокислоты. 3. Структуры белков. 4. Свойства белков. 5. Классификация белков. 6. Специфичность
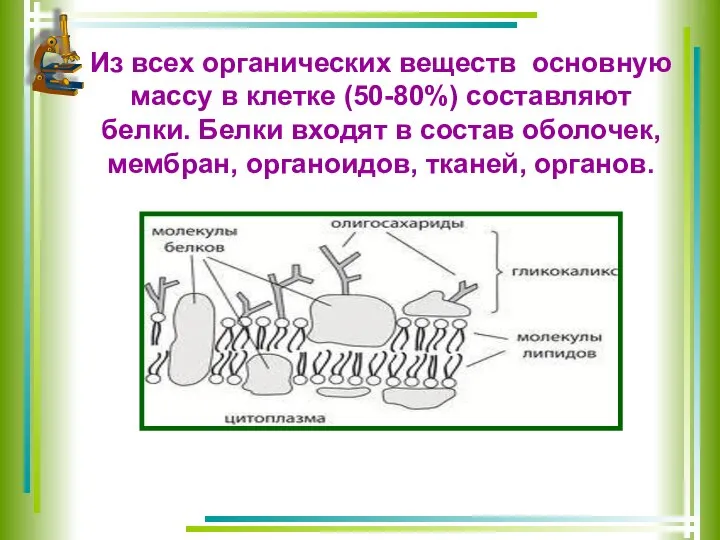
- 4. Из всех органических веществ основную массу в клетке (50-80%) составляют белки. Белки входят в состав оболочек,
- 5. Химический состав В состав белков входят такие химические элементы как: кислород, углерод (С), водород (Н), азот
- 6. БЕЛКИ - это сложные органические вещества клетки, выполняющие разнообразные функции. Они представляют собой гигантские полимерные молекулы
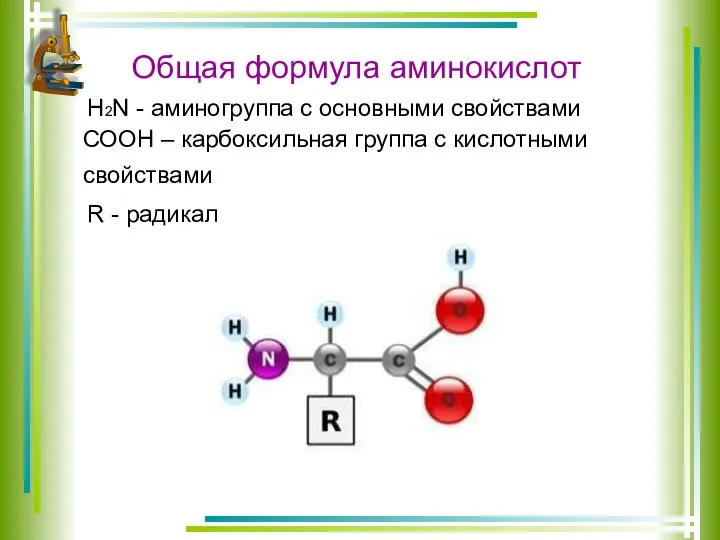
- 7. Общая формула аминокислот Н2N - аминогруппа с основными свойствами СООН – карбоксильная группа с кислотными свойствами
- 8. Аминокислоты Аминокислоты – это азотсодержащие органические соединения, в составе которых присутствуют две функциональные группы: аминогруппа, придающая
- 9. В тканях и клетках встречается 170 различных аминокислот, в составе белков обнаруживается лишь 26 из них,
- 10. В этих продуктах содержаться незаменимые для человека аминокислоты
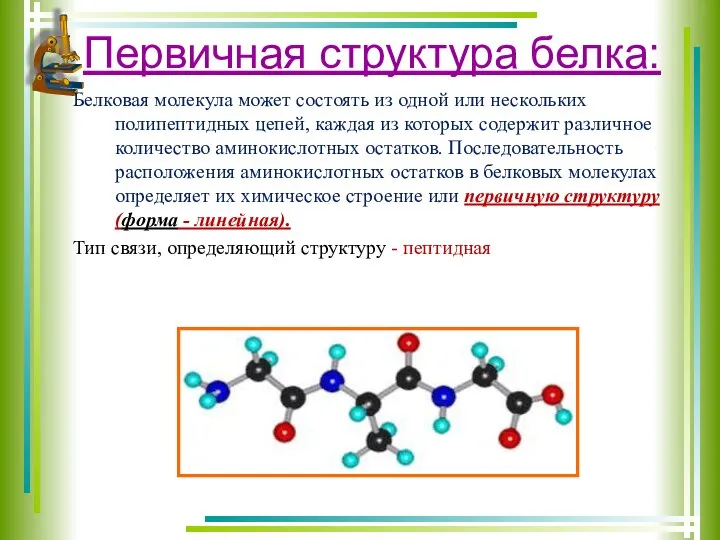
- 11. Первичная структура белка: Белковая молекула может состоять из одной или нескольких полипептидных цепей, каждая из которых
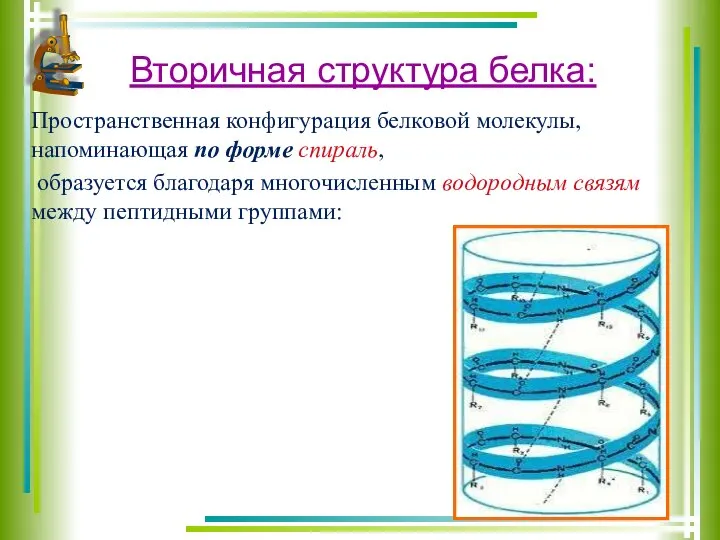
- 12. Вторичная структура белка: Пространственная конфигурация белковой молекулы, напоминающая по форме спираль, образуется благодаря многочисленным водородным связям
- 13. Третичная структура белка: трёхмерная пространственная «упаковка» вторичной спирали в глобулу (по форме напоминает клубок) Типы связей
- 14. Четвертичная структура белка Некоторые белковые макромолекулы могут соединяться друг с другом и образовывать крупные агрегаты (комплекс
- 15. Свойства белков Денатурация - нарушение естественной структуры белка. Причина: высокая температура. воздействие радиации, химических веществ и
- 16. Классификация белков Простые - состоят только из аминокислот. Сложные - могут состоять из белков и других
- 17. Видовая специфичность белков Специфичность определяется набором аминокислот, их количеством и последовательностью расположения в полипептидной цепи. У
- 19. Скачать презентацию












 Автор: учитель биологии Константинова Елена Анатольевна
Автор: учитель биологии Константинова Елена Анатольевна Значение и охрана насекомых
Значение и охрана насекомых Понятие о систематике растений
Понятие о систематике растений Пока дышу – живу. Модедь Дондерса
Пока дышу – живу. Модедь Дондерса Учение о клетке
Учение о клетке Мышцы, их строение и функции
Мышцы, их строение и функции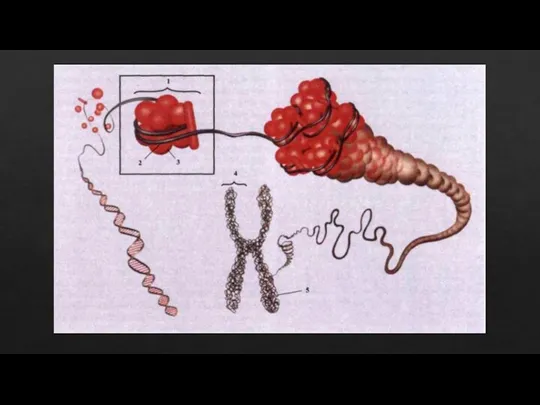 Хромосоми. Правила хромосом
Хромосоми. Правила хромосом Презентация на тему "Обмен веществ и энергии - основа процессов жизнедеятельности организма" - презентации по Биологии
Презентация на тему "Обмен веществ и энергии - основа процессов жизнедеятельности организма" - презентации по Биологии Гипофиз, hypophysis
Гипофиз, hypophysis Презентация на тему Влияние солнечной активности на социальные процессы
Презентация на тему Влияние солнечной активности на социальные процессы  Закаливание
Закаливание Класс ферментов оксидоредуктазы
Класс ферментов оксидоредуктазы Топырақта тіршілік ететін организмдер
Топырақта тіршілік ететін организмдер Класс моллюски
Класс моллюски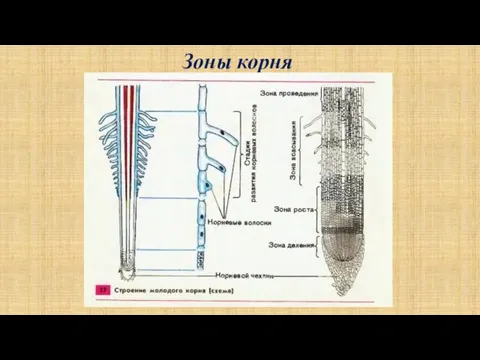 Дыхательные корни. Отростки боковых корней, выступающие над поверхностью почвы
Дыхательные корни. Отростки боковых корней, выступающие над поверхностью почвы Жучки
Жучки Биосоциальная сущность человека. Тема 1.1
Биосоциальная сущность человека. Тема 1.1 Приспособляемость живых организмов к суровым условиям Антарктиды
Приспособляемость живых организмов к суровым условиям Антарктиды Простые механизмы в живой природе
Простые механизмы в живой природе Опасные растения и грибы
Опасные растения и грибы Хвойный лес
Хвойный лес Кобчик – птица 2021 года
Кобчик – птица 2021 года Вода в жизни живых организмов
Вода в жизни живых организмов Род дикобразы (hystrix)
Род дикобразы (hystrix) Как звери и птицы готовятся к холодам
Как звери и птицы готовятся к холодам Тип Плоские черви. Класс Ресничные черви
Тип Плоские черви. Класс Ресничные черви Значение насекомых в природе и жизни человека
Значение насекомых в природе и жизни человека Восстановление зрения
Восстановление зрения