д. заносятся в лабораторный журнал.
Лабораторный журнал – официальный документ, имеющий юридическую силу, в котором в последовательном хронологическом порядке указываются условия проведения экспериментов и результаты измерений. Аккуратное ведение лабораторного журнала позволяет исследователю создать адекватный и поддающийся проверке отчет, защитить свой приоритет относительно сделанных им анализов.
Лабораторный журнал представляет собой тетрадь (журнал) с пронумерованными страницами, прошитыми страницами толстой ниткой, концы которой скреплены на последней странице сургучом с оттиском официальной печати учреждения. Данные следует вписывать ручкой, но не карандашом. Если в процессе занесения в журнал результатов эксперимента были позже обнаружены опечатки или фактические ошибки, они исправляются ручкой другого (красного) цвета, ставится дата и фамилия исправляющего.
Лабораторный журнал
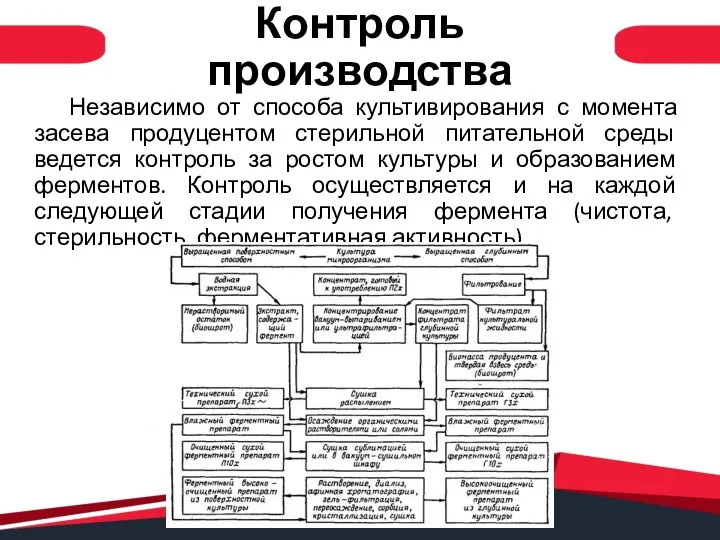








 Экоцарство - природное государство. Экологическая мозаика
Экоцарство - природное государство. Экологическая мозаика Змеи
Змеи Современное состояние ихтиофауны Удомельского водохранилища
Современное состояние ихтиофауны Удомельского водохранилища Пузыреплодник калинолистный /Рэд Барон пурпурный/
Пузыреплодник калинолистный /Рэд Барон пурпурный/ Критические факторы, влияющие на развитие плода
Критические факторы, влияющие на развитие плода Незаменимые на земле
Незаменимые на земле Прокариотическая клетка
Прокариотическая клетка Цепи питания
Цепи питания Сердечно-сосудистая система
Сердечно-сосудистая система Движение в живой природе
Движение в живой природе Строение клетки
Строение клетки Плоские и круглые черви
Плоские и круглые черви Земноводные, или амфибии
Земноводные, или амфибии Детёныши животных
Детёныши животных Презентация на тему Цитоплазма
Презентация на тему Цитоплазма  Сухая биохимия: применение биоинформатики для протеомики
Сухая биохимия: применение биоинформатики для протеомики Глоссарий
Глоссарий Влияние различных условий (температура, pH) на структуру белков. Лабораторная работа 1
Влияние различных условий (температура, pH) на структуру белков. Лабораторная работа 1 Презентация на тему "Общие законы действия факторов среды на организм" - презентации по Биологии
Презентация на тему "Общие законы действия факторов среды на организм" - презентации по Биологии Типы мышц человека. Строение мышц
Типы мышц человека. Строение мышц Галерея цветов
Галерея цветов Водне середовище існування
Водне середовище існування Витамины
Витамины Анатомия. Эндокринная система. Пищеварительная система. Дыхательная система
Анатомия. Эндокринная система. Пищеварительная система. Дыхательная система Кровеносная система. Кровь
Кровеносная система. Кровь Фракталы в природе
Фракталы в природе Взаимодействия в макромолекулах
Взаимодействия в макромолекулах Биология. Занятие 1
Биология. Занятие 1