Содержание
- 2. Широко простирает химия руки свои в дела человеческие. ( Михаил Васильевич Ломоносов)
- 3. Тема «Азотосодержащие вещества» Позволяет не только давать характеристику аминокислотам и белкам (их строение, свойства, применение, пищевая
- 4. Пенообразование Белки в качестве пенообразователей широко используют при производстве кондитерских изделий (тесто бисквитное), взбивании сливок, сметаны,
- 5. Денатурация белка.
- 6. Денатурация белков. Тепловая обработка мяса Основное назначение тепловой обработки — размягчение продуктов для улучшения усвоения их
- 7. Омлет (гидратация белков) Гидратация белков. Гидратацией называется способность белков прочно связывать значительное количество влаги.
- 8. Дегидратация белков. Дегидратацией называется потеря белками связанной воды при сушке, замораживании и размораживании мяса и рыбы,
- 9. Гидролиз белка. Основа студней и заливных блюд — крепкий бульон, в который после длительной варки перешли
- 11. Состав жиров Жиры – это сложные эфиры , образованные трехатомным спиртом – глицерином и одноосновными карбоновыми
- 12. Жиры растительного и животного происхождения
- 13. «Свойства жиров» В состав жидких растительных масел входят непредельные карбоновые кислоты , способны к реакциям присоединения
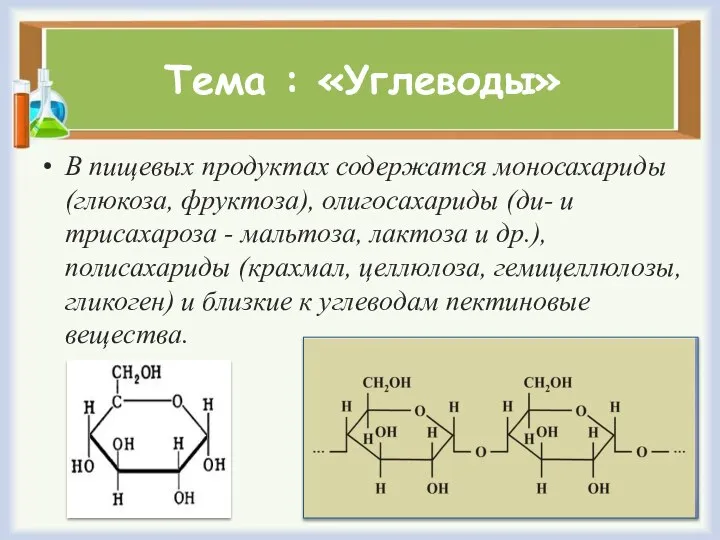
- 14. Тема : «Углеводы» В пищевых продуктах содержатся моносахариды (глюкоза, фруктоза), олигосахариды (ди- и трисахароза - мальтоза,
- 15. Свойства углеводов Брожение Глубокому распаду подвергаются сахара при брожении дрожжевого теста. Под действием ферментов дрожжей сахара
- 16. Крахмал. Процессы происходящие при выпечке. Биохимические процессы связаны с изменением состояния крахмала и белков, и при
- 17. Химические свойства крахмала Крахмал легко подвергается гидролизу: Ступенчатый ферментативный гидролиз крахмала. Крахмал → декстрины → мальтоза
- 18. Варка овощей. Когда овощи помещают в кипяток, их структура изменяется из хрустящей и жесткой, в мягкую
- 19. Зависимость свойств от среды. изменение окраски пигментов в зависимости от PH среды. Хороший повар знает: чтобы
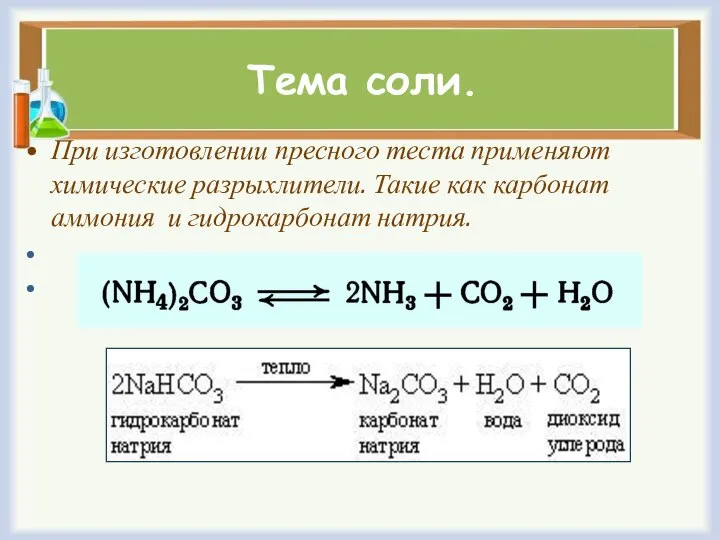
- 20. Тема соли. При изготовлении пресного теста применяют химические разрыхлители. Такие как карбонат аммония и гидрокарбонат натрия.
- 21. Хлорид натрия NaCl NaCl применяют как вкусовую добавку и для консервирования пищевых продуктов. Такой хлорид натрия
- 22. Приготовление рассолов, маринадов и сиропов.
- 23. Вычисления массовой доли. m(раствора)=m(вещества)+m(воды) Используем формулу массовой доли для приготовления рассолов и маринадов заданной процентной концентрации.
- 24. Выводы: Таким образом формирование химических знаний в процессе обучения оказывает влияние на качество профессиональной подготовки студентов,
- 26. Скачать презентацию





















 Подключичная артерия
Подключичная артерия Декоративные крысы
Декоративные крысы Альтернативные источники энергии
Альтернативные источники энергии Лабораторная работа Исследование признаков классов однодольных и двудольных растений (8 класс)
Лабораторная работа Исследование признаков классов однодольных и двудольных растений (8 класс) Класс Жгутиконосцы, тип Инфузории. Урок № 6
Класс Жгутиконосцы, тип Инфузории. Урок № 6 Торф. Виды торфа
Торф. Виды торфа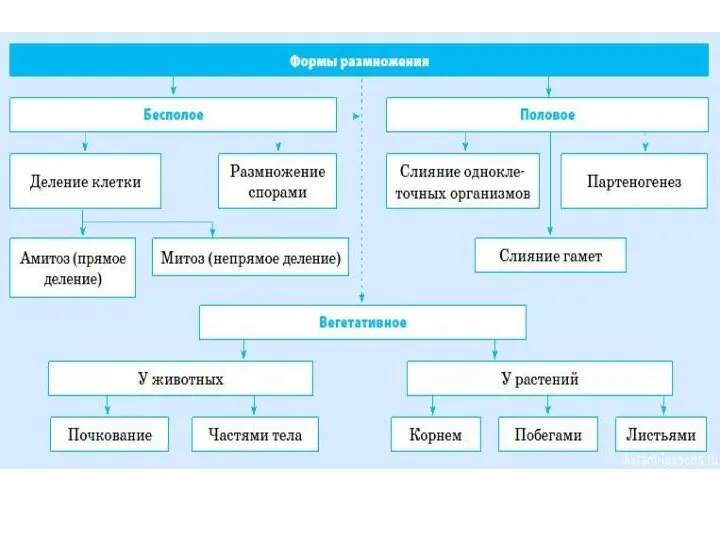 Половое и бесполое размножение
Половое и бесполое размножение Лесное сообщество. Животный и растительный мир
Лесное сообщество. Животный и растительный мир Кастрация самцов
Кастрация самцов Плоды, их строение, значение, распространение в природе
Плоды, их строение, значение, распространение в природе Презентация на тему Развитие жизни на Земле 2
Презентация на тему Развитие жизни на Земле 2  Опорно-двигательная система человека
Опорно-двигательная система человека Презентация на тему Вегетативное размножение покрытосеменных растений
Презентация на тему Вегетативное размножение покрытосеменных растений  Ткани (1)
Ткани (1) Биокатализаторы
Биокатализаторы 832648_№3-realizaciya-nasledstvennoi-informacii
832648_№3-realizaciya-nasledstvennoi-informacii Большая подборка по второй части. 22 задание
Большая подборка по второй части. 22 задание Не губите первоцветы, весны первые приметы
Не губите первоцветы, весны первые приметы Теплица. Выращивание овощей
Теплица. Выращивание овощей Вирусы. История открытия вирусов
Вирусы. История открытия вирусов Анатомические и функциональные цепи
Анатомические и функциональные цепи Роль живых организмов в природе
Роль живых организмов в природе list_vneshnee_i_vnutrennee_stroenie
list_vneshnee_i_vnutrennee_stroenie Типы питания. Типы питания. Автотрофы и гетеротрофы
Типы питания. Типы питания. Автотрофы и гетеротрофы Презентация на тему Семейство Злаковые
Презентация на тему Семейство Злаковые  Прокариоты, эукариоты. Принцип классификации микроорганизмов
Прокариоты, эукариоты. Принцип классификации микроорганизмов Ладожская орнитологическая станция. Приглашение к участию в ее работе
Ладожская орнитологическая станция. Приглашение к участию в ее работе Простейшие. Инфузории. Вопросы
Простейшие. Инфузории. Вопросы