Содержание
- 2. ЛЕКЦИИ 3-4 ЗАГРЯЗНЕНИЕ ОКРУЖАЮЩЕЙ СРЕДЫ. БИОИНДИКАЦИЯ И БИОТЕСТИРОВАНИЕ. Типы загрязнения окружающей среды Ксенобиотики. Биодоступность ксенобиотиков. Биодеградация
- 3. ЗАГРЯЗНЕНИЕ ОКРУЖАЮЩЕЙ СРЕДЫ – процесс привнесения в окружающую среду или возникновения в ней новых, обычно не
- 4. ОСНОВНЫЕ ИСТОЧНИКИ АНТРОПОГЕННОГО ЗАГРЯЗНЕНИЯ химические и фармацевтические предприятия; предприятия целлюлозно-бумажной и печатной индустрии – основные потребители
- 5. ХИМИЧЕСКОЕ ЗАГРЯЗНЕНИЕ . – изменение естественных химических свойств среды в результате выбросов промышленными предприятиями, транспортом, сельским
- 6. ПРИОРИТЕТЫЕ ХИМИЧЕСКИЕ ЗАГРЯЗНИТЕЛИ . соединения тяжелых металлов; пестициды; полициклические ароматические углеводородов; хлорорганические соединения; нефтепродукты, фенолы; детергенты;
- 7. ФИЗИЧЕСКОЕ ЗАГРЯЗНЕНИЕ воздействие, вызывающее отклонение от нормы физических параметров окружающей среды Радиоактивное загрязнение – поступление в
- 8. ФИЗИЧЕСКОЕ ЗАГРЯЗНЕНИЕ Шумовое загрязнение - характеризуется превышением естественного уровня шумового фона. Характерно для городов, окрестностей аэродромов,
- 9. БИОЛОГИЧЕСКОЕ ЗАГРЯЗНЕНИЕ выражается преимущественно в бактериальном загрязнении – привнесении в окружающую среду патогенных микроорганизмов. Бактериальному загрязнению
- 10. Ксенобиотики (от греч. ξένος – чуждый и βίος – жизнь) – условная категория для обозначения чужеродных
- 11. БИОДЕГРАДАЦИЯ КСЕНОБИОТИКОВ преобразование сложных веществ с помощью биологической активности - трансформация – незначительное изменение структуры молекулы
- 12. БИОДОСТУПНОСТЬ КСЕНОБИОТИКОВ Биодоступность – способность ксенобиотика подвергаться биотрансформации Зависит от: генетических свойств микроорганизмов, осуществляющих трансформацию; условий
- 13. БИОДОСТУПНОСТЬ КСЕНОБИОТИКОВ Биодоступность ксенобиотиков зависит от химической структуры: чем сложнее структура, тем менее доступен ксенобиотик для
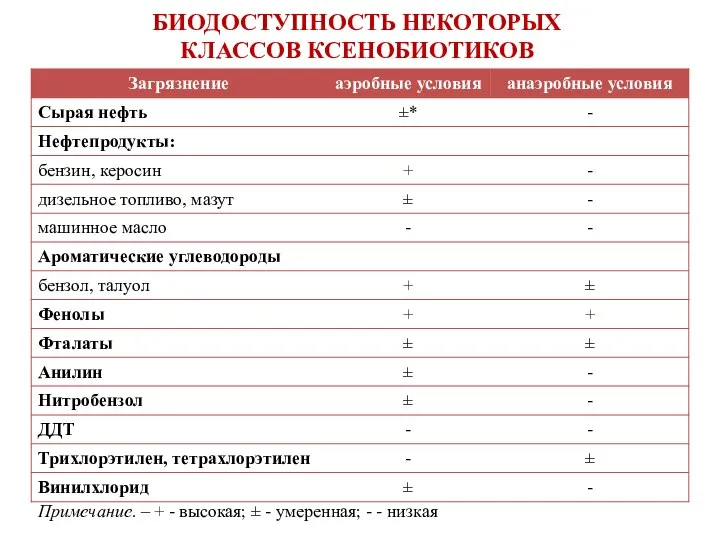
- 14. БИОДОСТУПНОСТЬ НЕКОТОРЫХ КЛАССОВ КСЕНОБИОТИКОВ Примечание. – + - высокая; ± - умеренная; - - низкая
- 15. ФАКТОРЫ ВНЕШНЕЙ СРЕДЫ И БИОДОСТУПНОСТЬ КСЕНОБИОТИКОВ Биодоступность и активность биодеградации ксенобиотиков ограничивают следующие факторы: Неоптимальное значение
- 16. КОНЦЕНТРАЦИЯ КСЕНОБИОТИКА чем выше концентрация ксенобиотика, тем дольше он находится в окружающей среде; если концентрация ксенобиотика
- 17. ФИЗИЧЕСКАЯ НЕДОСТУПНОСТЬ КСЕНОБИОТИКА биодоступность органических соединений обусловлена их сродством к водной, минеральной и газовой фазам окружающей
- 18. НЕДОСТУПНОСТЬ АКЦЕПТОРОВ ЭЛЕКТРОНОВ ИЛИ КОСУБСТРАТОВ Деградация ксенобиотиков микроорганизмами сопряжена с потреблением окислителя (акцептора электронов) или восстановителя
- 19. ТЕМПЕРАТУРА Один из наиболее важных факторов окружающей среды для эффективного протекания процессов биодеструкции: оптимальная температура для
- 20. Для биодеструкции ксенобиотиков в почвенных средах необходима влага. Содержание воды в почве влияет на скорость биодеградации
- 21. ТОКСИЧЕСКОЕ ДЕЙСТВИЕ КСЕНОБИОТИКОВ НА МИКРООРГАНИЗМЫ Зависит от: природы ксенобиотика; концентрации ксенобиотика; продолжительности контакта с микробной клеткой
- 22. МЕХАНИЗМЫ АДАПТАЦИИ МИКРООРГАНИЗМОВ К ТОКСИЧЕСКОМУ ДЕЙСТВИЮ КСЕНОБИОТИКОВ Трансформация ксенобиотика микроорганизмами во многих случаях начинается лишь после
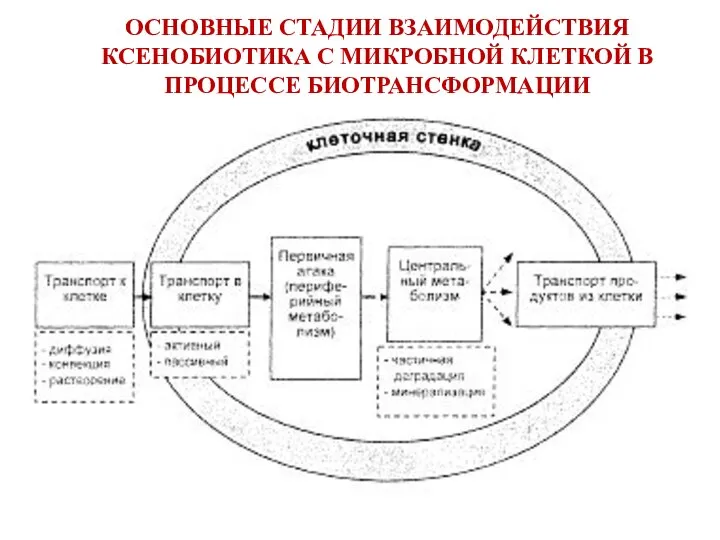
- 23. ОСНОВНЫЕ СТАДИИ ВЗАИМОДЕЙСТВИЯ КСЕНОБИОТИКА С МИКРОБНОЙ КЛЕТКОЙ В ПРОЦЕССЕ БИОТРАНСФОРМАЦИИ
- 24. 2. Транспорт ксенобиотика в клетку транспорт нейтральных и гидрофобных ксенобиотиков через мембрану осуществляется путем диффузии и
- 25. СТАДИИ ВЗАИМОДЕЙСТВИЯ КСЕНОБИОТИКА С МИКРОБНОЙ КЛЕТКОЙ 3. Первичная атака (периферийный метаболизм) - последовательная трансформация органического ксенобиотика
- 26. ПЕРИФЕРИЙНЫЙ МЕТАБОЛИЗМ Включает начальные этапы метаболизма ксенобиотиков Ферменты периферийного метаболизма: имеют широкую субстратную специфичность; являются индуцибельными
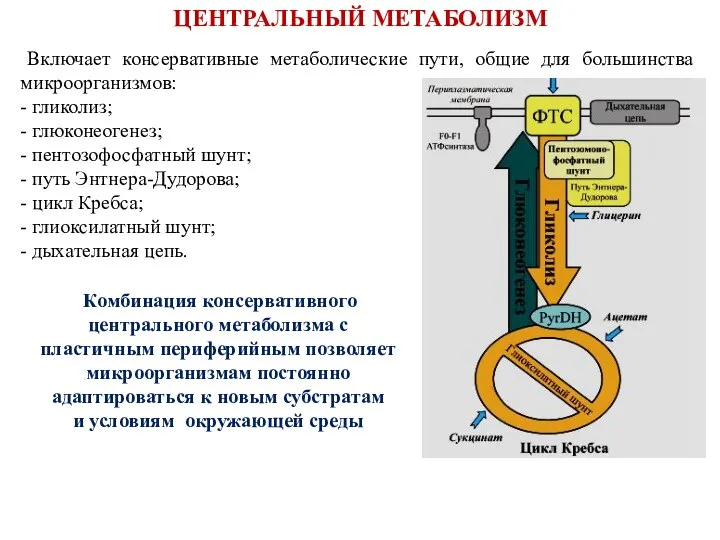
- 27. Включает консервативные метаболические пути, общие для большинства микроорганизмов: - гликолиз; - глюконеогенез; - пентозофосфатный шунт; -
- 28. МЕХАНИЗМЫ ДЕГРАДАЦИИ КСЕНОБИОТИКОВ. Начальные этапы Ксенобиотики могут деградироваться при участии широко спектра реакций подготовительного метаболизма. Аэробные
- 29. МЕХАНИЗМЫ ДЕГРАДАЦИИ КСЕНОБИОТИКОВ Если синтетические ксенобиотики подобны по химическим свойствам природным соединениям, их трансформация проводится по
- 30. МИКРОБИОЛОГИЧЕСКАЯ ДЕСТРУКЦИЯ КСЕНОБИОТИКОВ Наиболее активно участвуют в деградации ксенобиотиков бактерии и грибы, обитающие в почве и
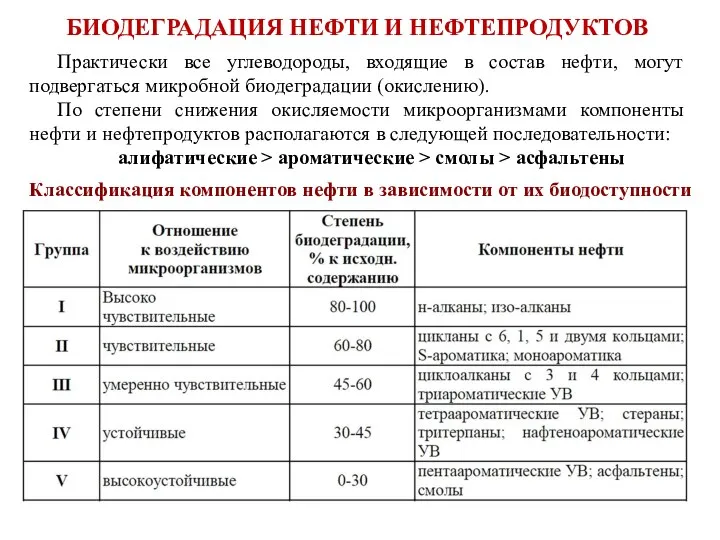
- 31. БИОДЕГРАДАЦИЯ НЕФТИ И НЕФТЕПРОДУКТОВ Нефть - сложная смесь, содержащая более 1000 индивидуальных веществ: жидкие углеводороды (>
- 32. В первые недели после загрязнения почвы нефтью происходят в основном физические процессы миграции и рассеивания углеводородов
- 33. Классификация компонентов нефти в зависимости от их биодоступности Практически все углеводороды, входящие в состав нефти, могут
- 34. Первые сообщения о способности бактерий деградировать нефть – 1946 год. К деградации нефти и нефтепродуктов способны
- 35. в пробах почвы, взятых на территории Кувейта и Саудовской Аравии, в первые недели после загрязнения нефтью
- 36. Наиболее часто бактерии-деструкторы нефти обнаруживаются среди родов Rhodococcus, Pseudomonas, Corynebacterium, Flavobacterium, Micrococcus, Arthrobacter, Mycobacterium, Bacillus. Потенциальными
- 37. У мицелиальных грибов родов Aspergillus, Penicillium, Fusarium, Amorphoteca, Neosartorya, Paecilomyces, Talaromyces, Graphium и дрожжей родов Candida,
- 38. Таксономический состав водных углеводородокисляющих микроорганизмов очень разнообразен: описано 28 родов бактерий и 14 родов мицелиальных и
- 39. Большинство микроорганизмов не утилизируют алканы, содержащие менее 9 атомов углерода, их окислять способны некоторые штаммы родов
- 40. Изоалканы, циклоалканы и ароматические углеводороды более устойчивы к окислению микроорганизмами по сравнению с н-алканами. Многие из
- 41. Максимальное содержание нефти в среде, доступное для биоремедиации, не составляет не более 5-10%. В благоприятных условиях
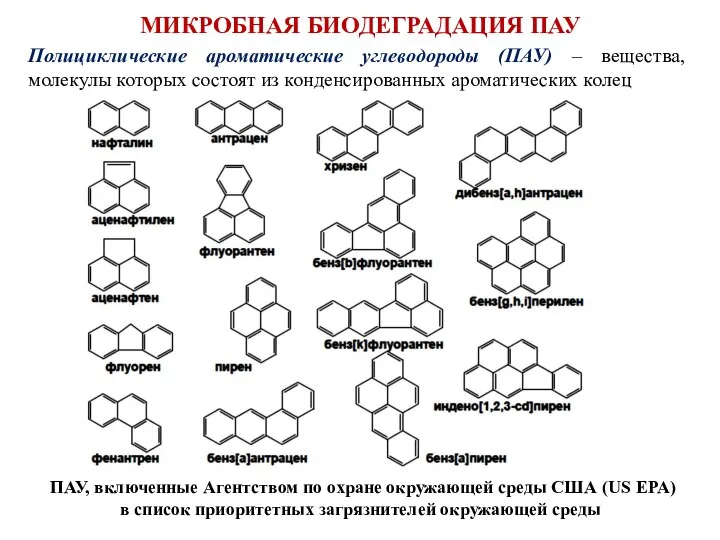
- 42. Полициклические ароматические углеводороды (ПАУ) – вещества, молекулы которых состоят из конденсированных ароматических колец ПАУ, включенные Агентством
- 43. Факторы, влияющие на токсичность и биодоступность ПАУ: растворимость в воде; количество конденсированных ароматических колец в молекулу
- 44. Аэробная деградация ПАУ осуществляется бактериями родов Pseudomonas, Alcaligenes, Bacillus и грибами рода Aspergillus, которые широко распространены
- 45. перенос ПАУ в бактериальную клетку (диффузия; механизмы активного транспорта не известны); гидроксилирование ПАУ (первая необратимая стадия);
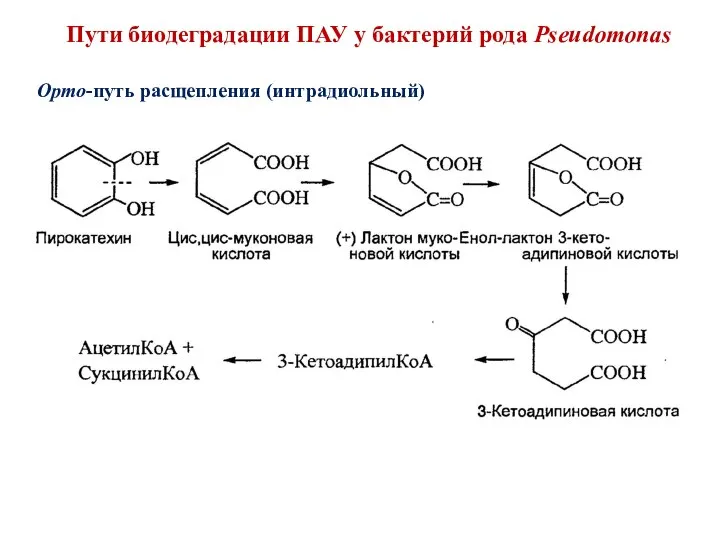
- 46. Пути биодеградации ПАУ у бактерий рода Pseudomonas Орто-путь расщепления (интрадиольный)
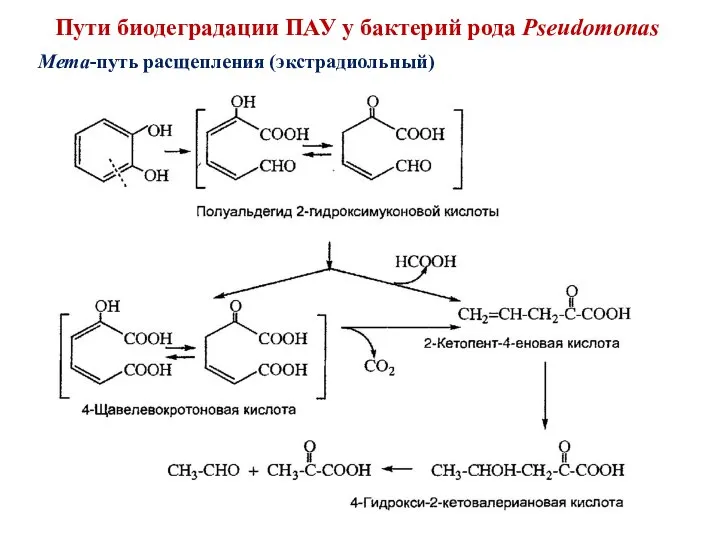
- 47. Мета-путь расщепления (экстрадиольный) Пути биодеградации ПАУ у бактерий рода Pseudomonas
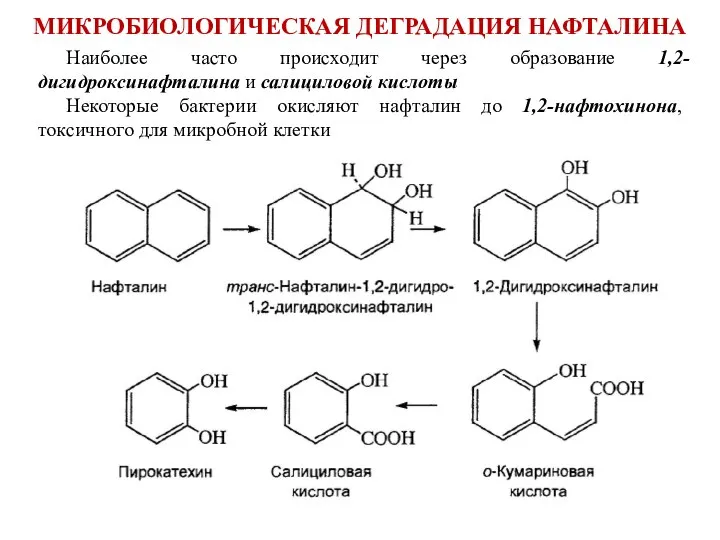
- 48. МИКРОБИОЛОГИЧЕСКАЯ ДЕГРАДАЦИЯ НАФТАЛИНА Наиболее часто происходит через образование 1,2-дигидроксинафталина и салициловой кислоты Некоторые бактерии окисляют нафталин
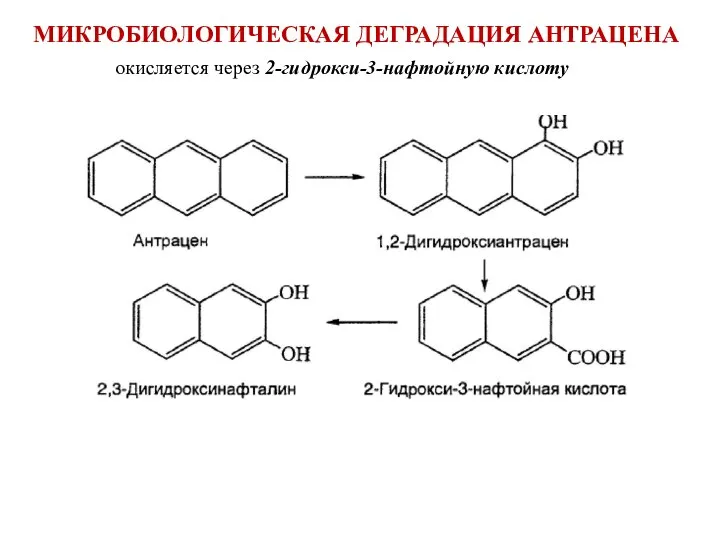
- 49. МИКРОБИОЛОГИЧЕСКАЯ ДЕГРАДАЦИЯ АНТРАЦЕНА окисляется через 2-гидрокси-3-нафтойную кислоту
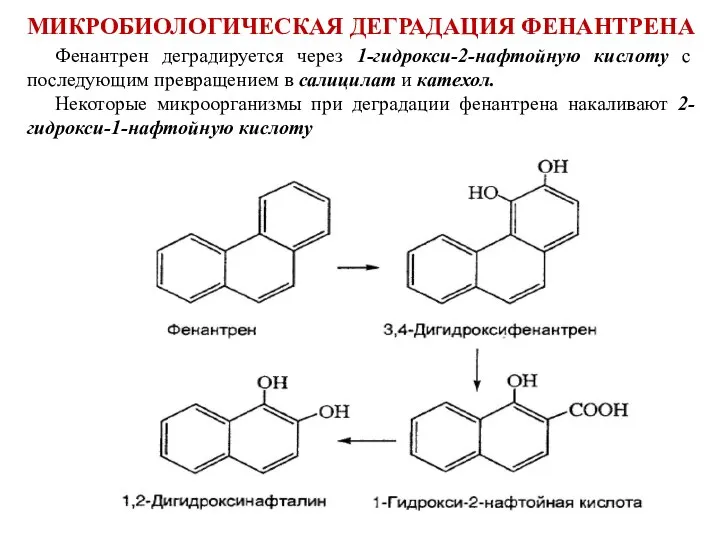
- 50. Фенантрен деградируется через 1-гидрокси-2-нафтойную кислоту с последующим превращением в салицилат и катехол. Некоторые микроорганизмы при деградации
- 51. БИОДЕГРАДАЦИЯ ПОВЕРХНОСТНО- АКТИВНЫХ ВЕЩЕСТВ (ПАВ) Поверхностно-активные вещества (ПАВ) – химические соединения, которые, концентрируясь на поверхности раздела
- 52. ПРИМЕНЕНИЕ ПАВ Моющие средства – наиболее распространены в синтетических моющих средствах алкилбензосульфонат, алкансульфонат (SAS), алкилсульфат (FAS),
- 53. КЛАССИФИКАЦИЯ ПАВ По типу гидрофильных групп (основная): ионные (ионогенные) – диссоциируют в воде на ионы, одни
- 54. БИОДЕГРАДАЦИЯ ПАВ Опасность ПАВ – ингибирование биохимического разложения других ксенобиотиков → в сточных водах содержание ПАВ
- 55. В природных условиях скорость распада ПАВ определяется: уровнем загрязнения и видом загрязняющего вещества; кислотностью и температурой
- 56. Первые работы по изучению деградации ПАВ чистыми культурами бактерий – 50-е годы XX века: - Ризен
- 57. Этапы биодеградации ПАВ Окисление ионогенных ПАВ начинается с конечной метильной группы алкильной цепи (для анионных –
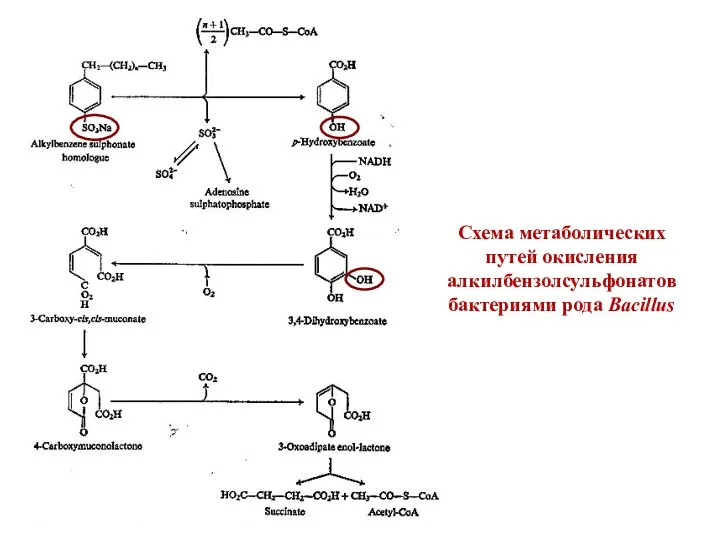
- 58. Схема метаболических путей окисления алкилбензолсульфонатов бактериями рода Bacillus
- 59. Этапы биодеградации ПАВ Деградация неионогенных ПАВ начинается с окисления терминальной метильной группы алкильной цепи до карбоксильного
- 60. МИКРОБИОЛОГИЧЕСКАЯ БИОДЕГРАДАЦИЯ ПЕСТИЦИДОВ Пестициды (сельскохозяйственные ядохимикаты) — химические средства, используемые для борьбы с вредителями и болезнями
- 61. По способу проникновения, характеру и механизму действия : Контактные – непосредственно при соприкосновении; Кишечные – попав
- 62. Альдрин (октален) — 1,2,3,4,10,10-гексахлор-1,4-эндо-5,8-экзодиметилен-1,4,4а, 5,8,8а-гексагидронафталин. Дильдрин (окталокс) — 1,2,3,4,10,10-гексахлор-1,4,5,8-диэндометилен-6,7-эпокси-1,4,4а,5,8,8а-гексагидронафталин. Эндрин (эндрекс) — 1,2,3,4,10,10-гексахлор-6,7-эпокси-1,4,4а,5,6,7,8,8а-октагидро-экзо-1,4- экзо-5,6-диметаннафталин. Хлордан (велзикол,
- 63. По химическим свойствам и биодоступности пестициды – органические ксенобиотики, особенностью которых является наличие различных групп в
- 64. Начальные стадии биодеградации гидролиз (амиды и эфиры) – сравнительно быстро разлагаются в природных условиях; дезалкилирование /
- 65. Возможные результаты биодеградации пестицидов: детоксикация и инактивация пестицида - полная потеря токсических свойств; активация (токсификация) пестицида
- 66. Факторы, определяющие устойчивость пестицидов к биотрансформации отсутствие условий для эффективной микробной трансформации низкая скорость транспорта пестицидов
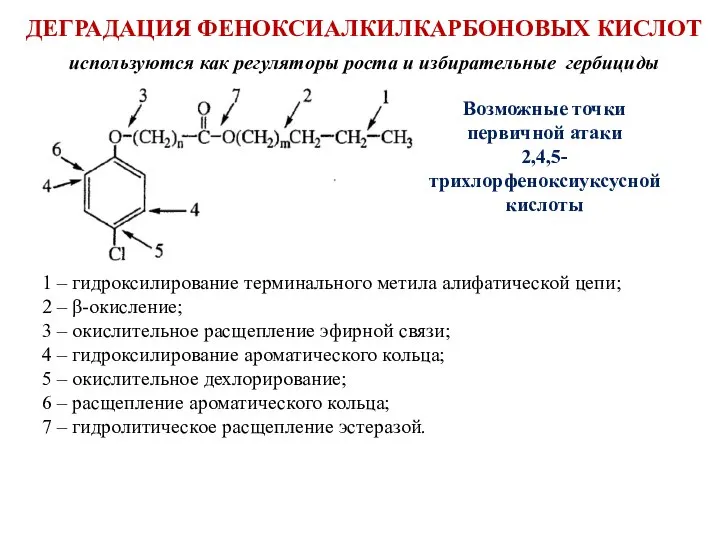
- 67. ДЕГРАДАЦИЯ ФЕНОКСИАЛКИЛКАРБОНОВЫХ КИСЛОТ используются как регуляторы роста и избирательные гербициды Возможные точки первичной атаки 2,4,5- трихлорфеноксиуксусной
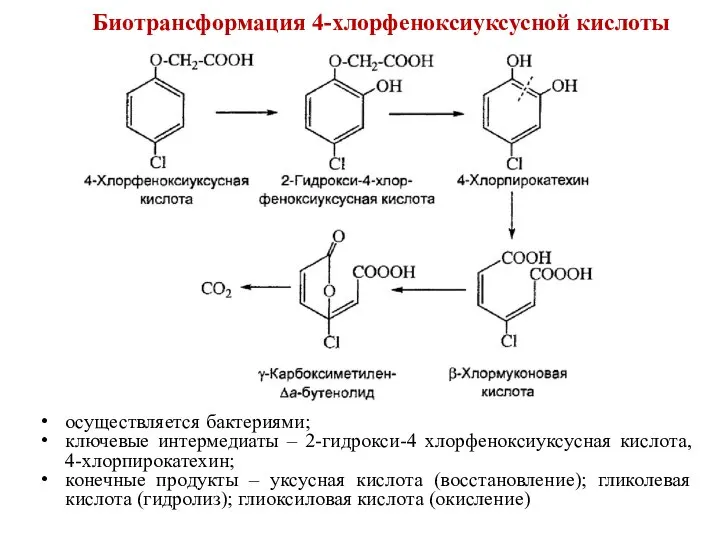
- 68. Биотрансформация 4-хлорфеноксиуксусной кислоты осуществляется бактериями; ключевые интермедиаты – 2-гидрокси-4 хлорфеноксиуксусная кислота, 4-хлорпирокатехин; конечные продукты – уксусная
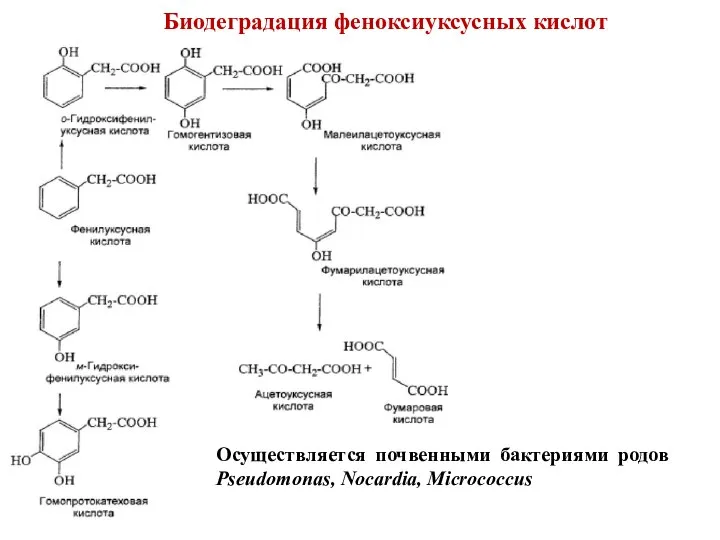
- 69. Биодеградация феноксиуксусных кислот Осуществляется почвенными бактериями родов Pseudomonas, Nocardia, Micrococcus
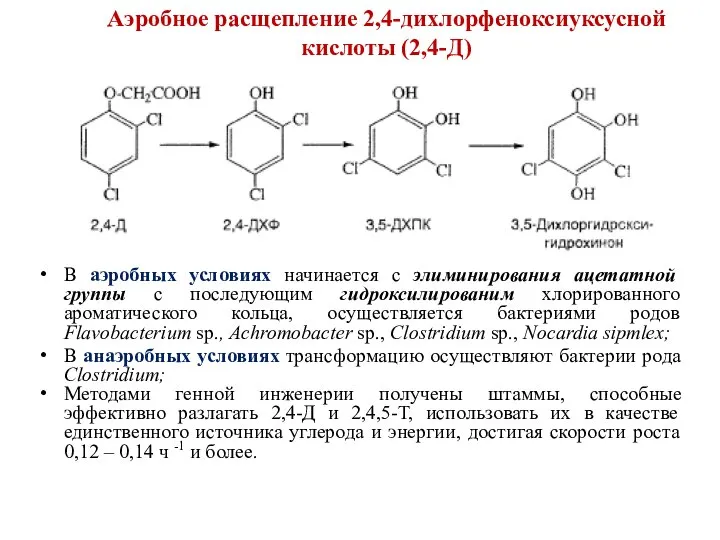
- 70. В аэробных условиях начинается с элиминирования ацетатной группы с последующим гидроксилированим хлорированного ароматического кольца, осуществляется бактериями
- 71. БИОДЕГРАДАЦИЯ ХЛОРИРОВАННЫХ ЖИРНЫХ КИСЛОТ ТХУ, 2,2-дихлорпропионовая кислота, далапон, используются как гербициды Первая реакция – гидролитическое дехлорирование.
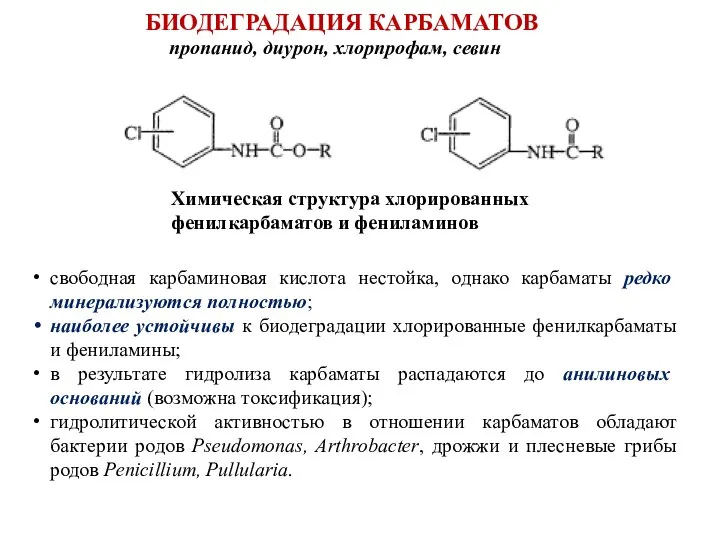
- 72. БИОДЕГРАДАЦИЯ КАРБАМАТОВ пропанид, диурон, хлорпрофам, севин свободная карбаминовая кислота нестойка, однако карбаматы редко минерализуются полностью; наиболее
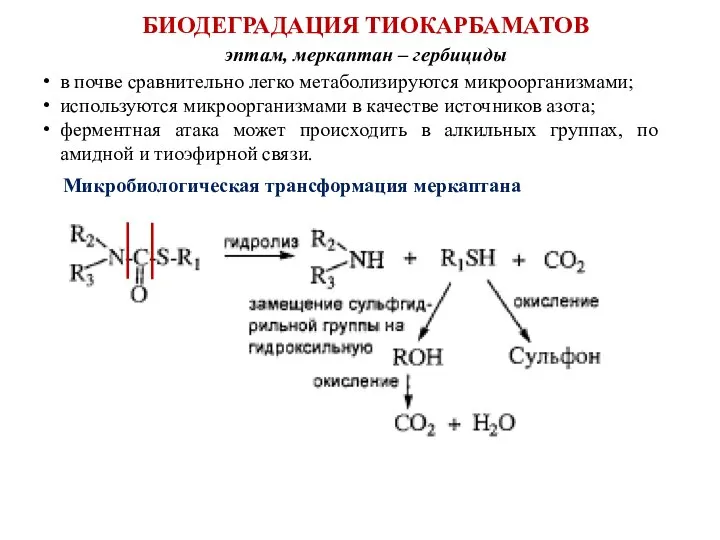
- 73. БИОДЕГРАДАЦИЯ ТИОКАРБАМАТОВ эптам, меркаптан – гербициды в почве сравнительно легко метаболизируются микроорганизмами; используются микроорганизмами в качестве
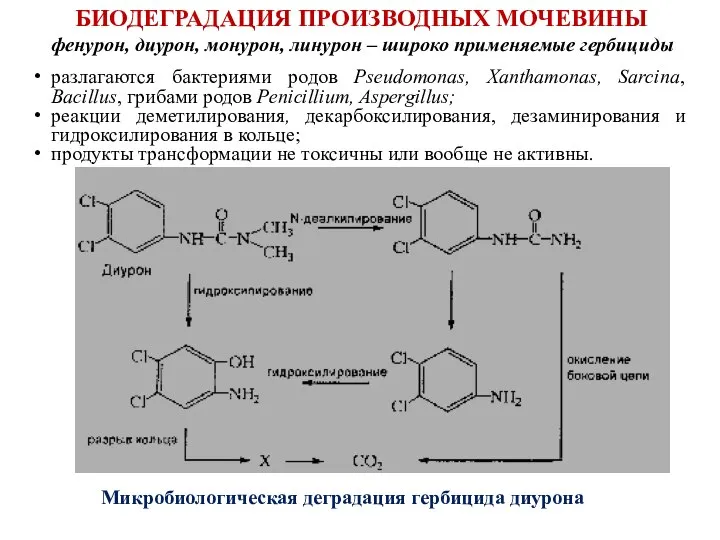
- 74. БИОДЕГРАДАЦИЯ ПРОИЗВОДНЫХ МОЧЕВИНЫ фенурон, диурон, монурон, линурон – широко применяемые гербициды разлагаются бактериями родов Pseudomonas, Xanthamonas,
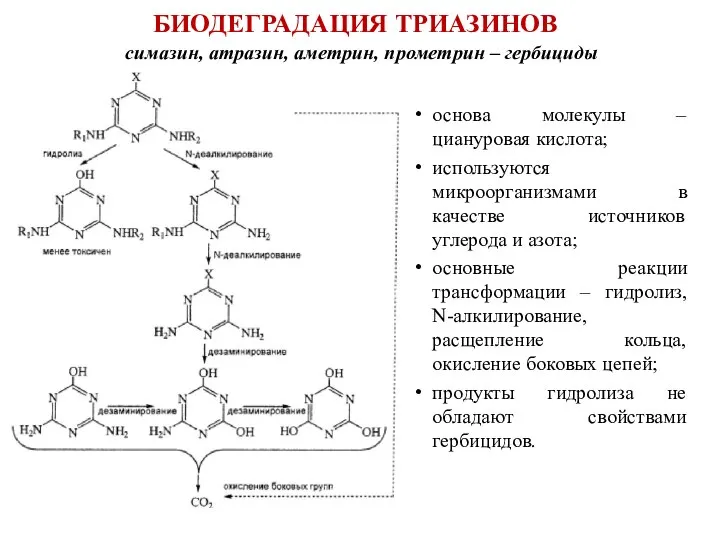
- 75. БИОДЕГРАДАЦИЯ ТРИАЗИНОВ симазин, атразин, аметрин, прометрин – гербициды основа молекулы – циануровая кислота; используются микроорганизмами в
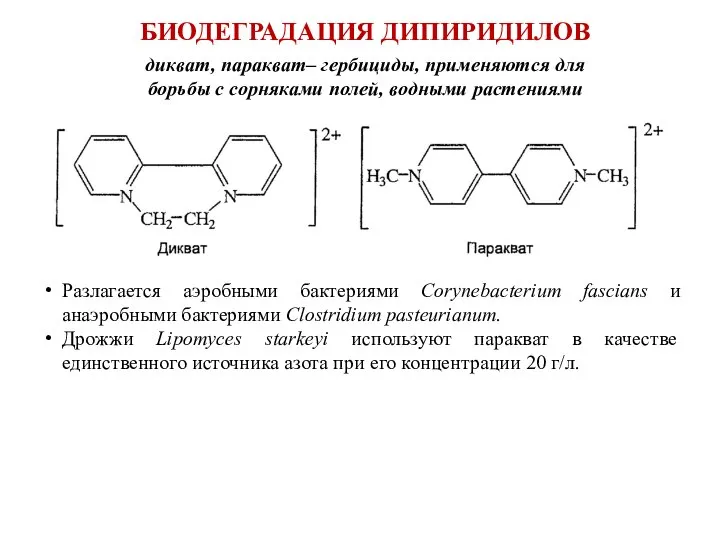
- 76. БИОДЕГРАДАЦИЯ ДИПИРИДИЛОВ дикват, паракват– гербициды, применяются для борьбы с сорняками полей, водными растениями Разлагается аэробными бактериями
- 78. Скачать презентацию























































 Общая характеристика типа Моллюски
Общая характеристика типа Моллюски Сцепленное наследование генов. ЕГЭ по биологии, 28 задача
Сцепленное наследование генов. ЕГЭ по биологии, 28 задача Физиология спорта Повседневная деятельность человека предусматривает два вида активности: психологическую и физическую. Психол
Физиология спорта Повседневная деятельность человека предусматривает два вида активности: психологическую и физическую. Психол Лекарственные растения Донбасса
Лекарственные растения Донбасса Обмен белков. Лекция 1
Обмен белков. Лекция 1 Отдел Моховидные. Класс Печёночники (2)
Отдел Моховидные. Класс Печёночники (2)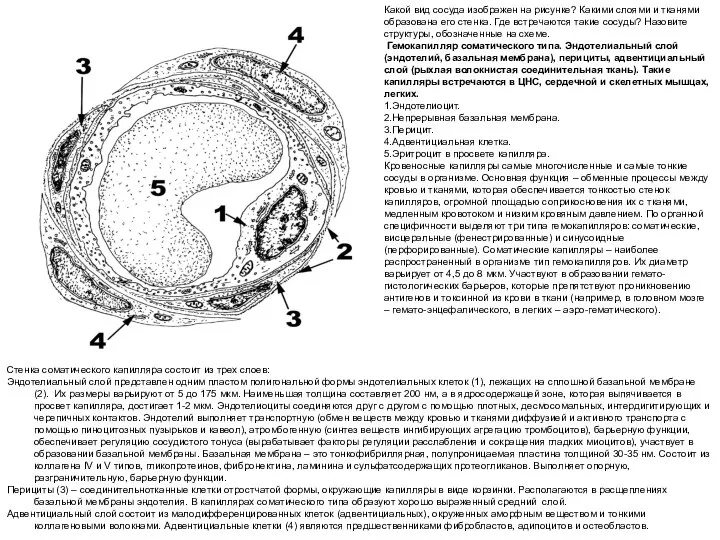 Cердечно Cосудистая Cистема
Cердечно Cосудистая Cистема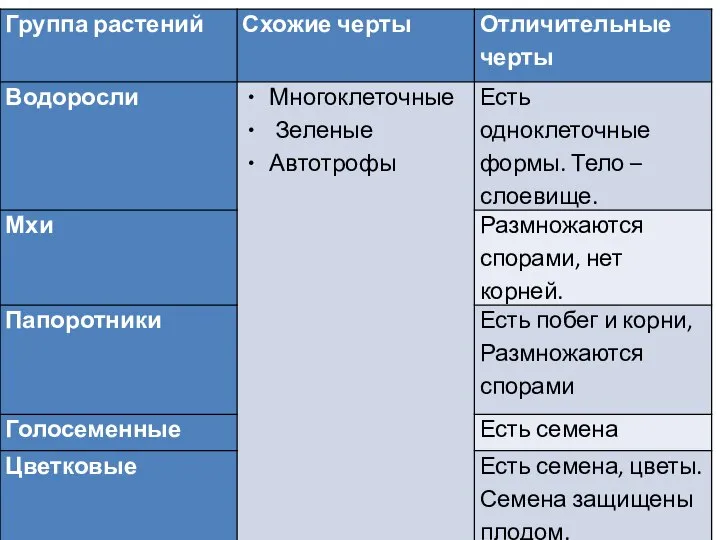 Покрытосеменные растения
Покрытосеменные растения Внезародышевые органы
Внезародышевые органы Биология как наука
Биология как наука Основные принципы классификации микроорганизмов. Различия архебактерий, эубактерий, прокариот и эукариот. Морфологические формы
Основные принципы классификации микроорганизмов. Различия архебактерий, эубактерий, прокариот и эукариот. Морфологические формы Внешнее строение растений. Часть 2
Внешнее строение растений. Часть 2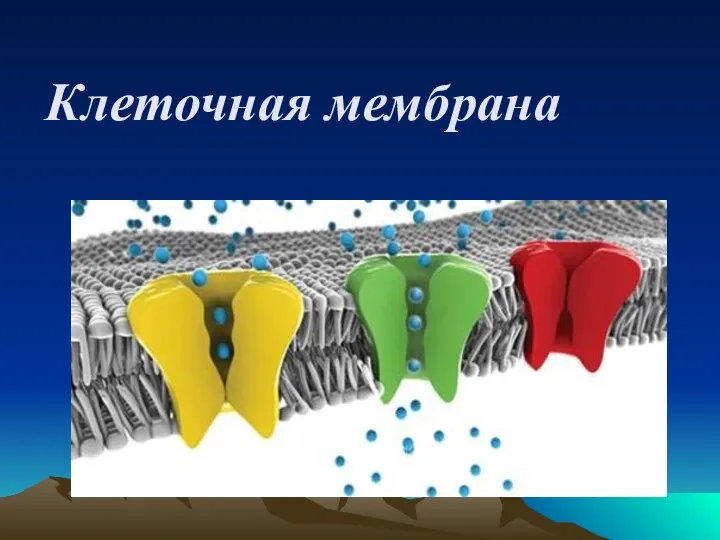 Клеточная мембрана
Клеточная мембрана Растения которые мы употребляем в пищу
Растения которые мы употребляем в пищу Энергетический обмен ( 9 класс)
Энергетический обмен ( 9 класс) Проблемы происхождения человека и первобытная эпоха
Проблемы происхождения человека и первобытная эпоха Овцы, как объект современной физики
Овцы, как объект современной физики Земноводные, или амфибии
Земноводные, или амфибии Механическое движение
Механическое движение Презентация на тему История красной книги
Презентация на тему История красной книги  Презентация на тему Леса России
Презентация на тему Леса России  Николай Семёнович Лесков
Николай Семёнович Лесков День моржа
День моржа Анатомические и функциональные цепи
Анатомические и функциональные цепи Роль животных в природе
Роль животных в природе Обитатели тайги
Обитатели тайги Птица Клёст
Птица Клёст Популяция – единица вида и эволюции
Популяция – единица вида и эволюции