Содержание
- 2. Биологическая химия является наукой, которая изучает химический состав и превращения веществ в организме, а также устанавливает
- 3. -ОН -ОН -ОН -ОН -О- -ОН J J J J J J J J -О- -ОН
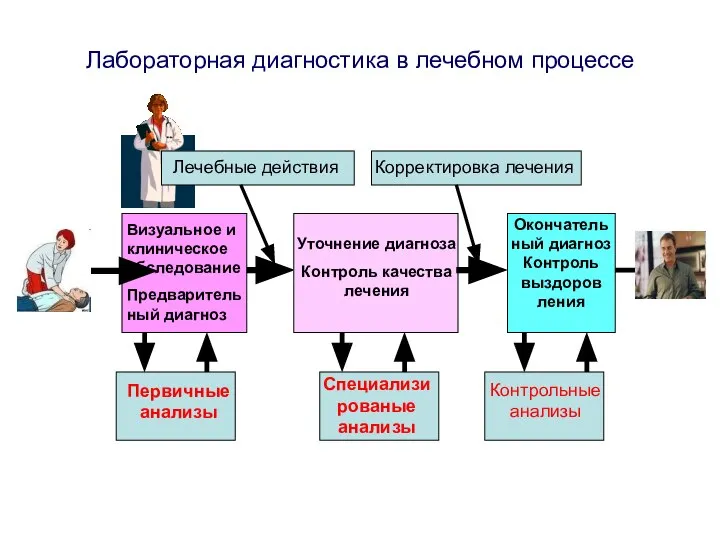
- 4. Визуальное и клиническое обследование Предваритель ный диагноз Уточнение диагноза Контроль качества лечения Окончатель ный диагноз Контроль
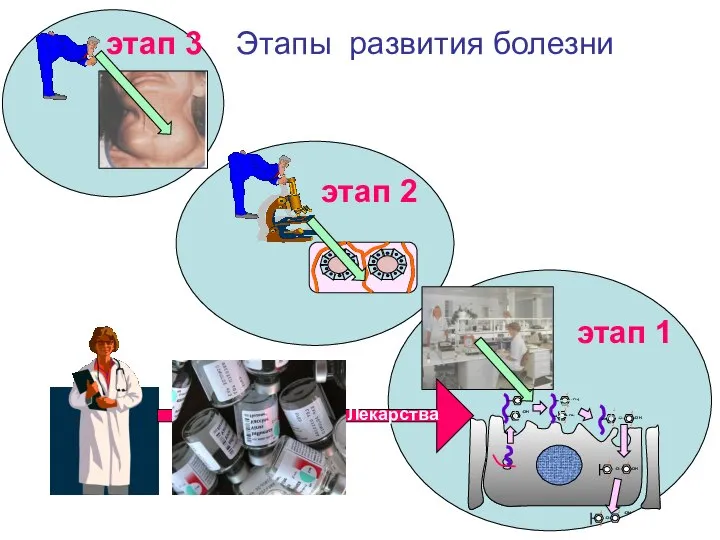
- 5. Роль биохимии в медицине Дает возможность установить причину, вызывающую болезнь; Позволяет понять закономерности, лежащие в основе
- 6. Роль биохимии в медицине С помощью веществ (лекарств) можно устранить нарушения и восстановить нормальное протекание химических
- 7. Разделы биохимии: 1. Статическая биохимия 2. Динамическая биохимия 3. Функциональная биохимия
- 8. Статическая биохимия – изучает химический состав живых организмов; Динамическая биохимия – изучает превращения химических веществ; Функциональная
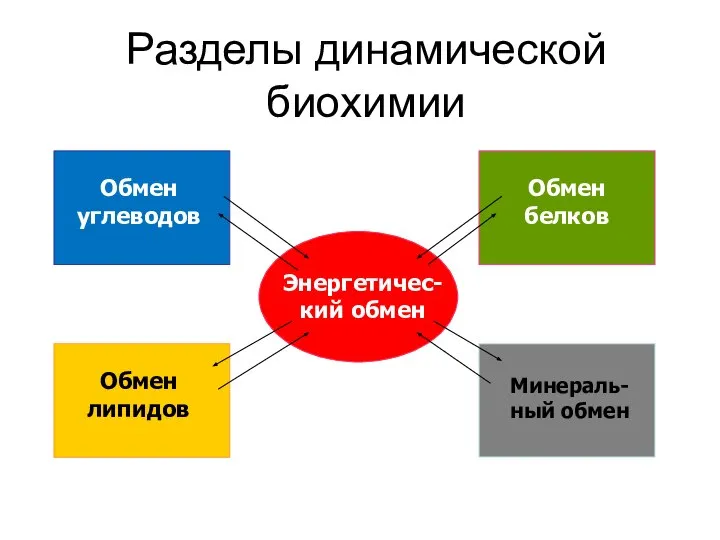
- 9. Разделы динамической биохимии Обмен углеводов Обмен липидов Обмен белков Минераль-ный обмен Энергетичес-кий обмен
- 10. Тема № 1 Строение и свойства белков
- 11. Роль белков в организме Структурная Каталитическая Транспортная Регуляторная Защитная Гомеостатическая Депонирующая Функциональная
- 12. Уровни организации белковой молекулы Первичная структура Вторичная структура Третичная структура Четвертичная структура
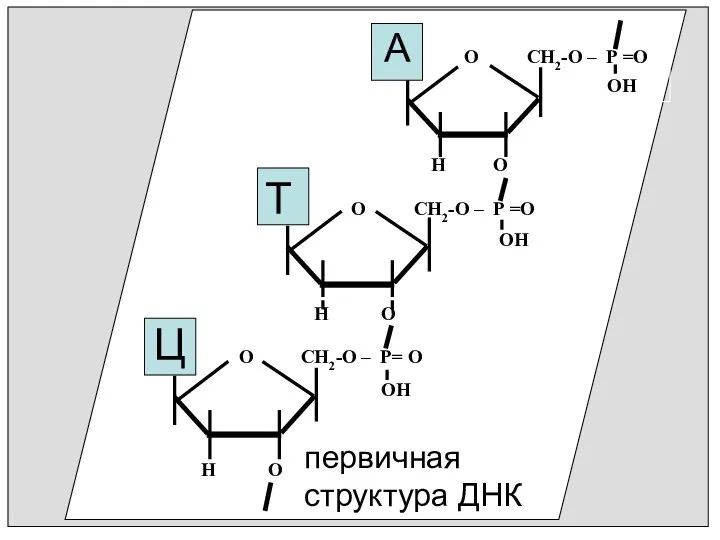
- 13. Под первичной структурой белка понимают порядок соединения аминокислот в полипептидной цепи
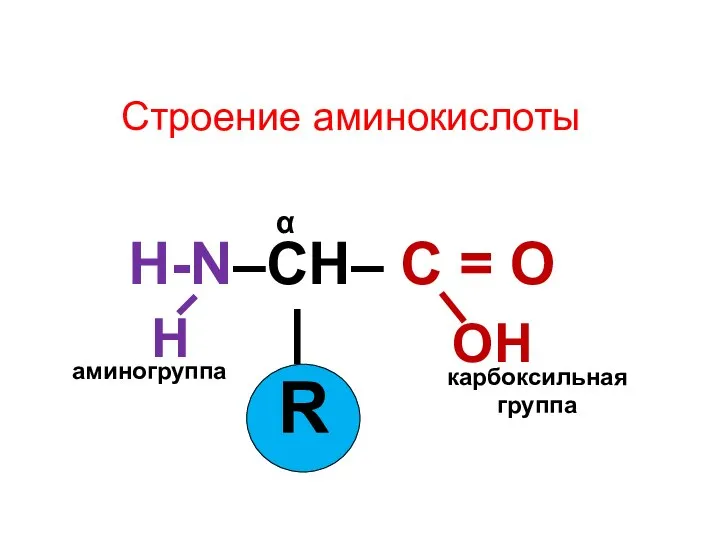
- 14. Строение аминокислоты H-N–CH– C = O | R ОН карбоксильная группа аминогруппа α Н
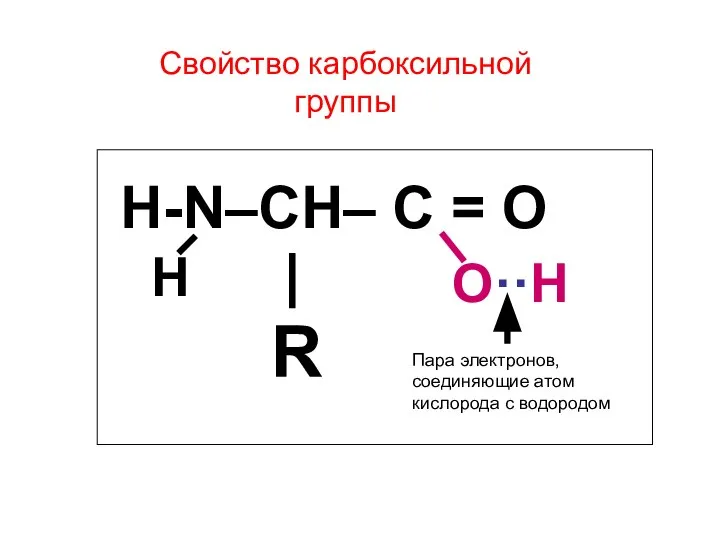
- 15. Свойство карбоксильной группы H-N–CH– C = O | R О··Н Н Пара электронов, соединяющие атом кислорода
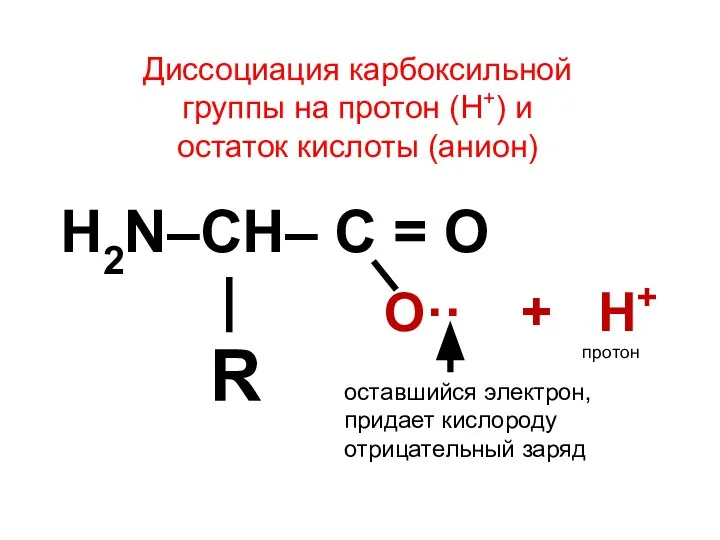
- 16. Диссоциация карбоксильной группы на протон (Н+) и остаток кислоты (анион) H2N–CH– C = O | R
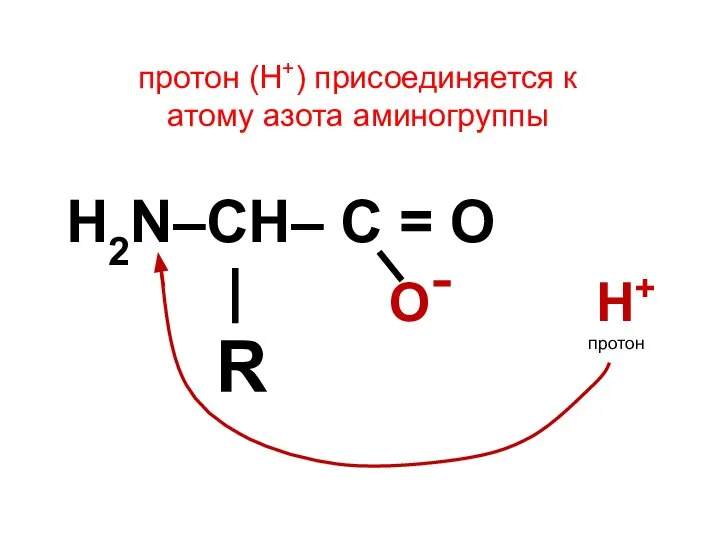
- 17. протон (Н+) присоединяется к атому азота аминогруппы H2N–CH– C = O | R О Н+ протон
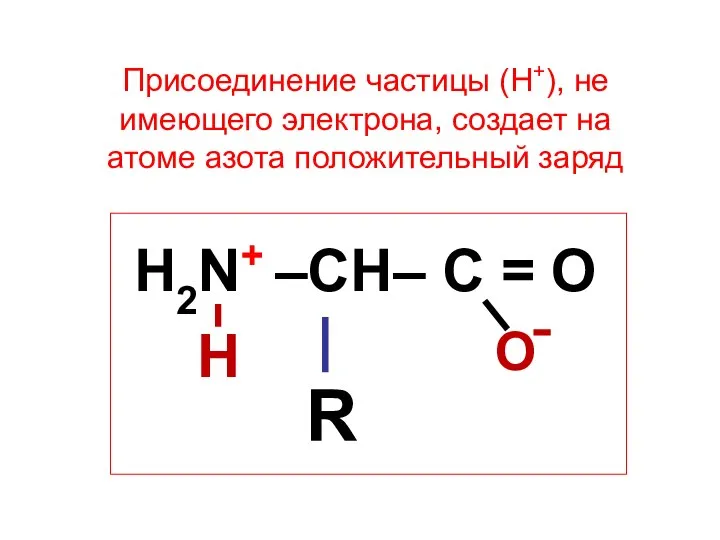
- 18. Присоединение частицы (Н+), не имеющего электрона, создает на атоме азота положительный заряд H2N+ –CH– C =
- 19. H2N–CH– COОН | R В каком состоянии находится аминокислота - в виде сухого порошка или в
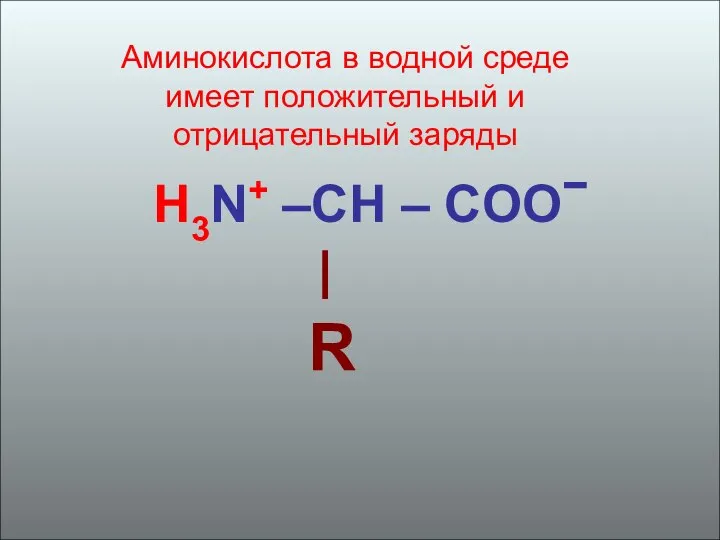
- 20. Аминокислота в водной среде имеет положительный и отрицательный заряды H3N+ –CH – COО | R
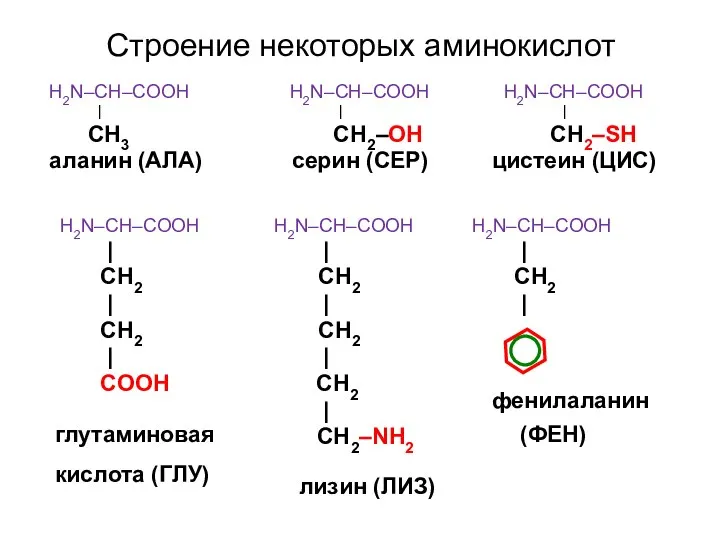
- 21. Строение некоторых аминокислот H2N–CH–COOH H2N–CH–COOH H2N–CH–COOH | | | СН3 СН2–ОН СН2–SН аланин (АЛА) серин (СЕР)
- 22. Классификация аминокислот 1. Моноаминомонокарбоновые 2. Моноаминодикарбоновые 3. Диаминомонокарбоновые 4. Серусодержащие 5. Имеющие спиртовую группу 6. Циклические
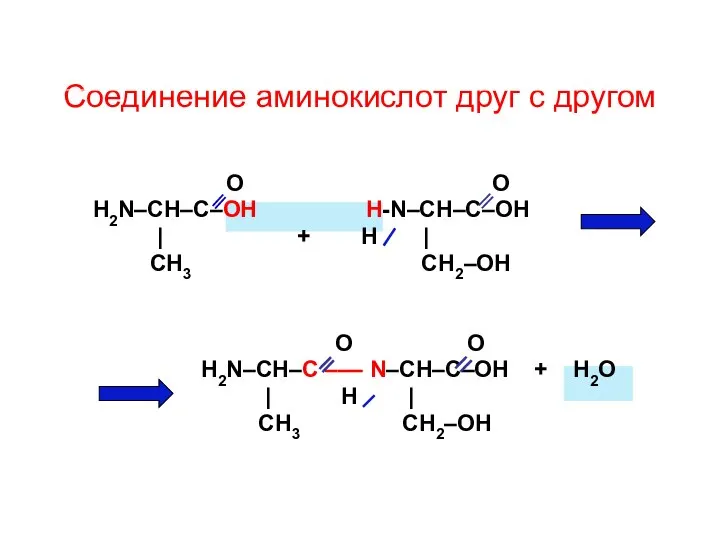
- 23. Соединение аминокислот друг с другом О О H2N–CH–C–OH H-N–CH–C–OH | + H | СН3 СН2–ОН О
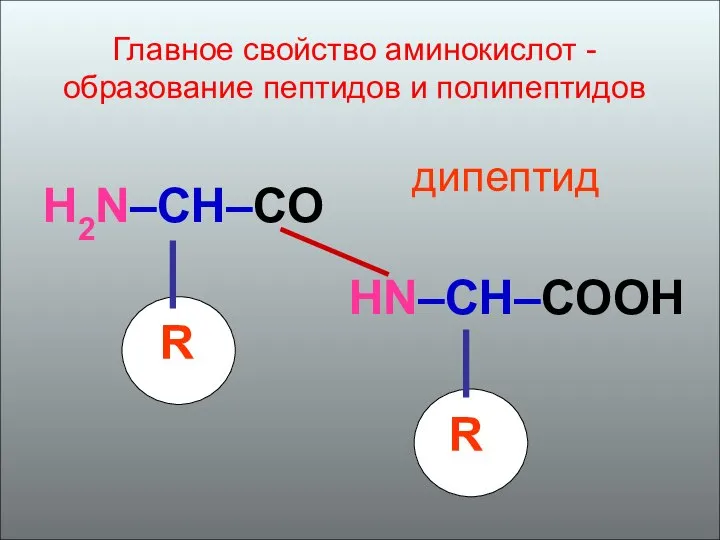
- 24. H2N–CH–CO R HN–CH–COOH R дипептид Главное свойство аминокислот - образование пептидов и полипептидов
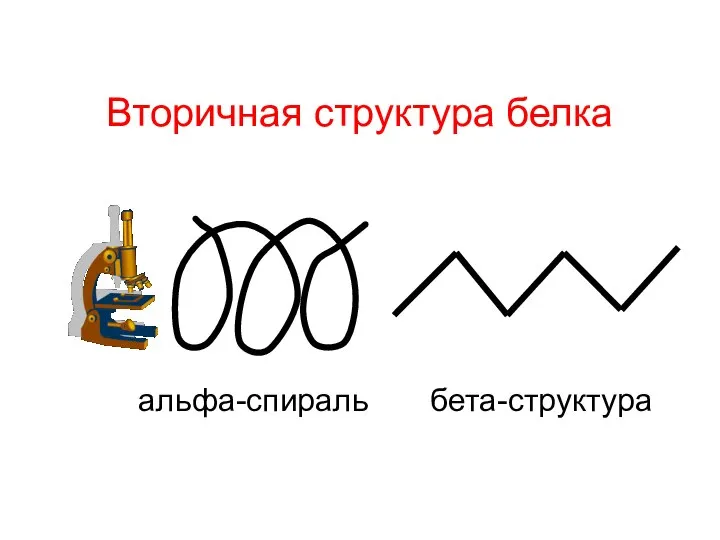
- 25. Вторичная структура белка альфа-спираль бета-структура
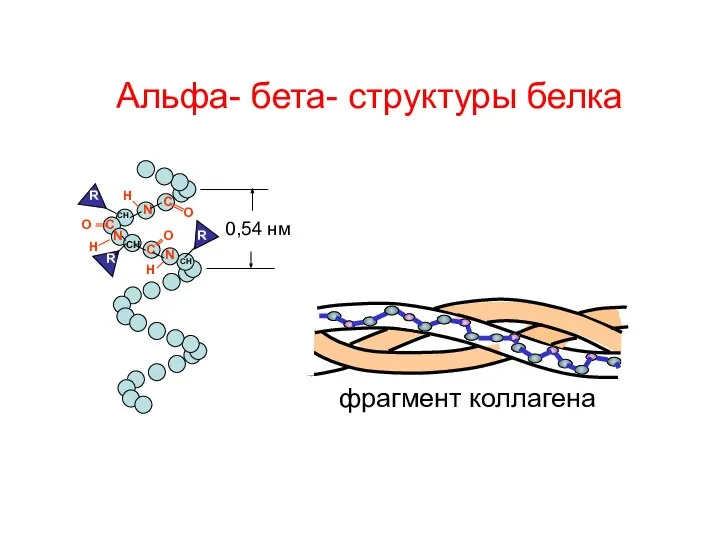
- 26. Альфа- бета- структуры белка 0,54 нм С N CH O C N CH C N CH
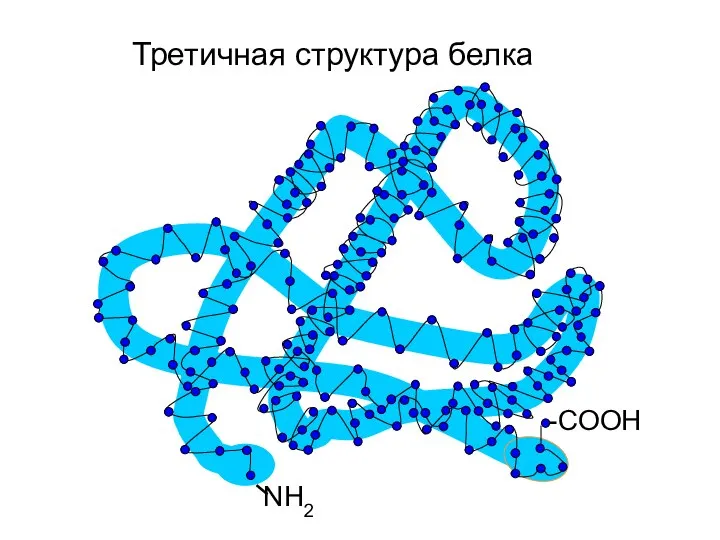
- 27. Третичная структура белка
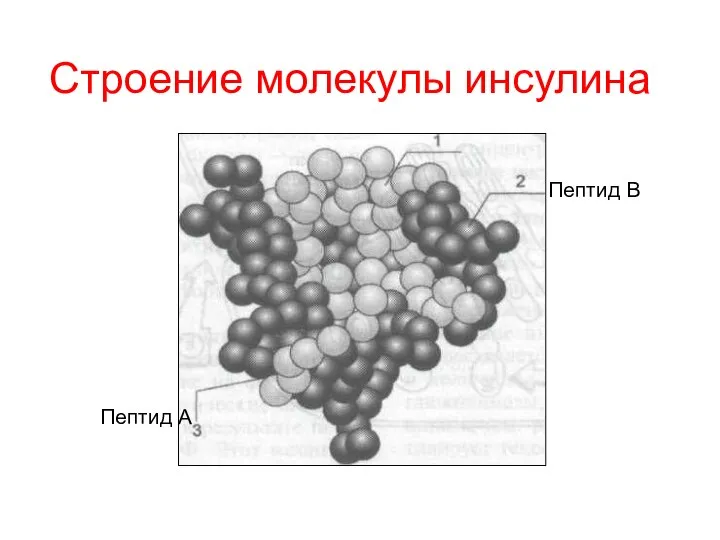
- 28. Строение молекулы инсулина Пептид В Пептид А
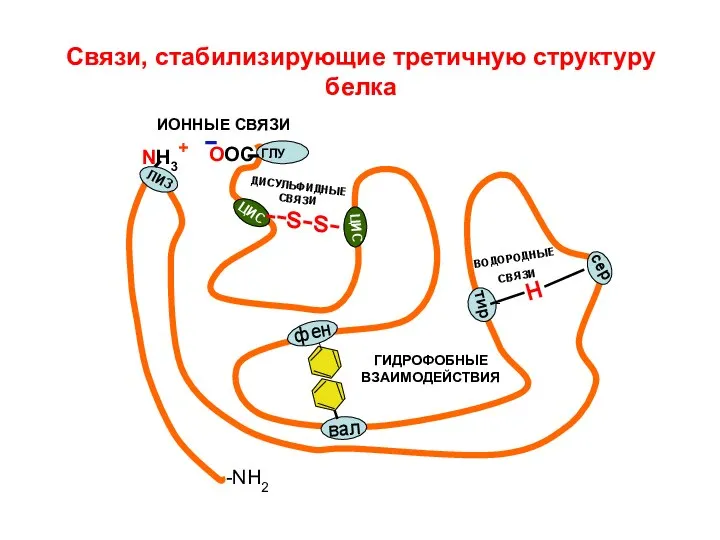
- 29. Связи, стабилизирующие третичную структуру белка фен вал тир сер NH3+ ЛИЗ ГЛУ ЦИС ЦИС --s-s- -NH2
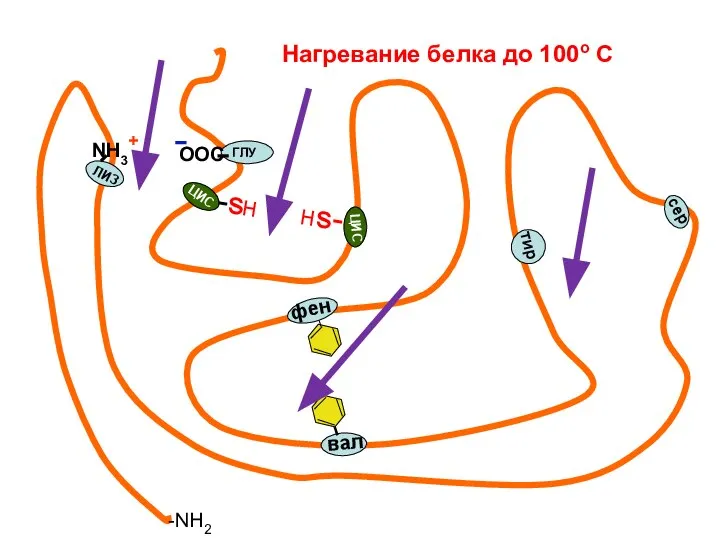
- 30. фен вал тир сер NH3+ ЛИЗ ГЛУ ЦИС ЦИС -sН Нs- -NH2 ООС Нагревание белка до
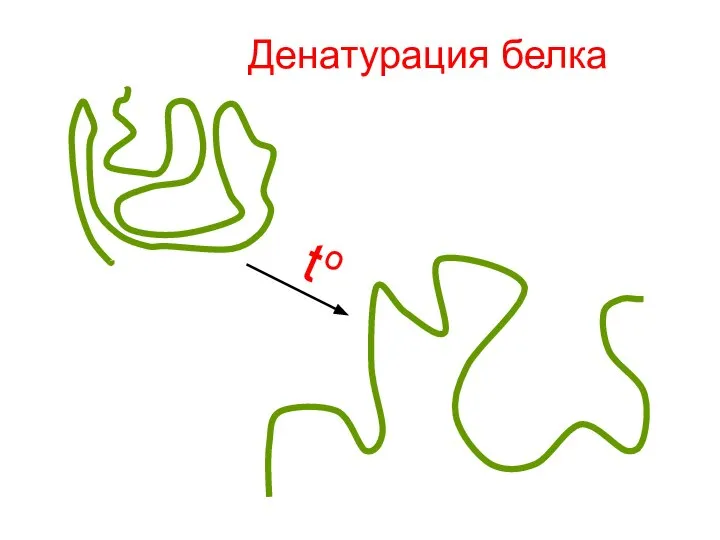
- 31. Денатурация белка tо
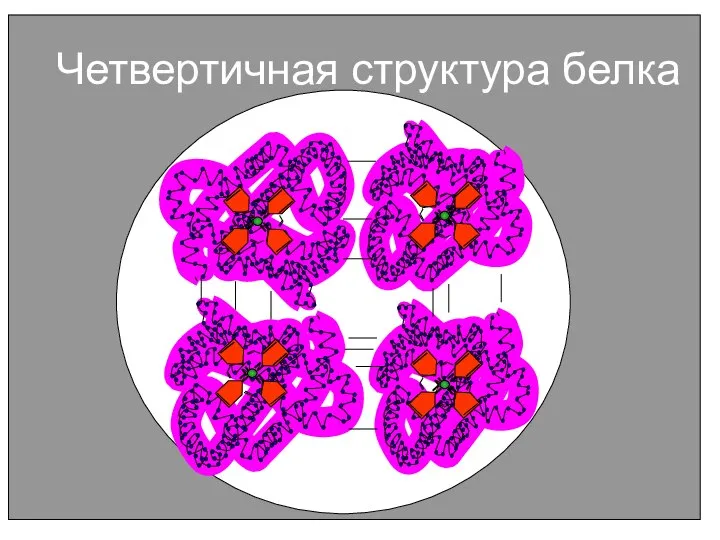
- 32. Четвертичная структура белка N N N N N N N N N N N N N
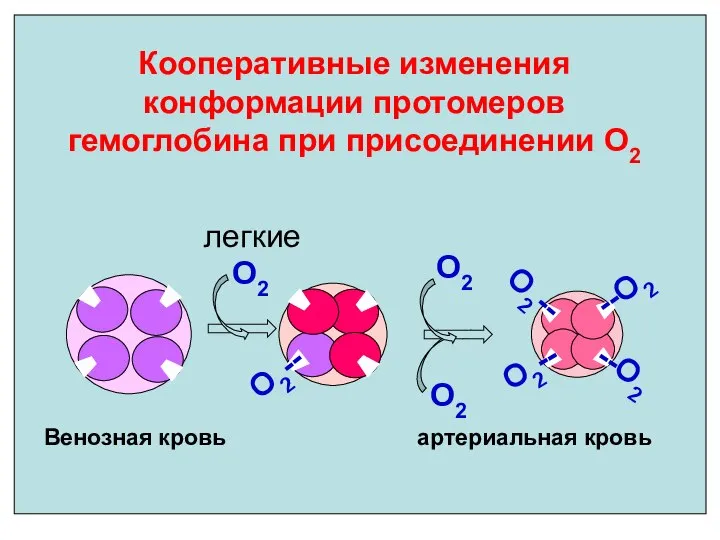
- 33. Кооперативные изменения конформации протомеров гемоглобина при присоединении О2 О2-- --О2 О2-- О2 О2 Венозная кровь артериальная
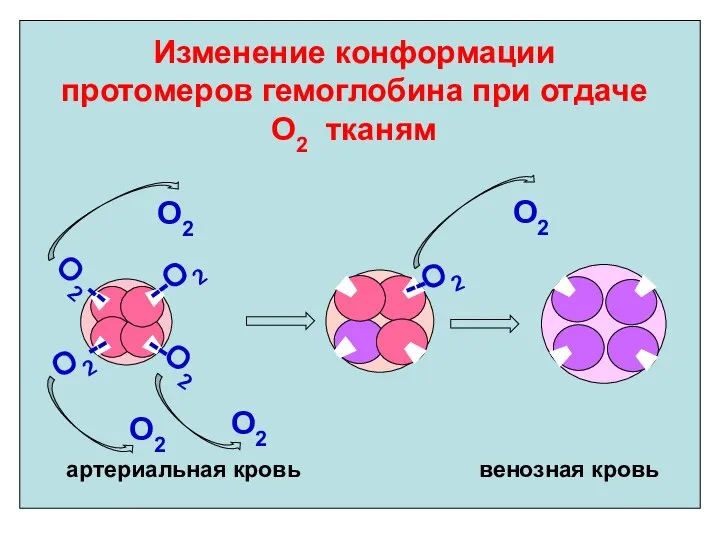
- 34. Изменение конформации протомеров гемоглобина при отдаче О2 тканям О2 О2 артериальная кровь венозная кровь О2 О2
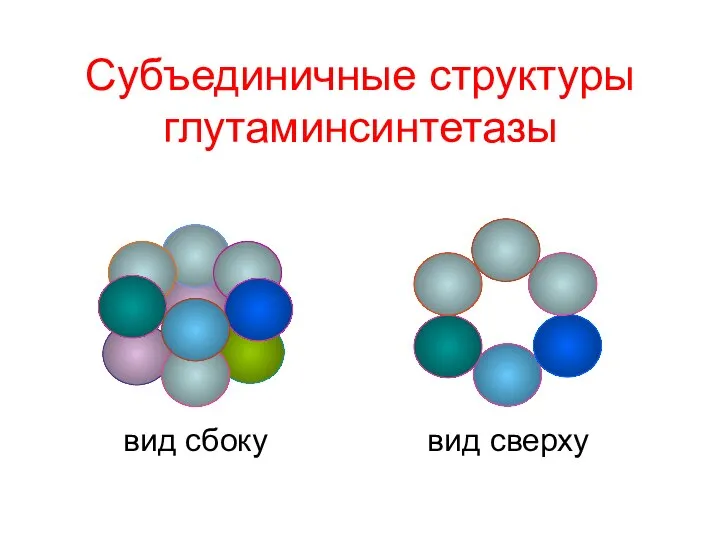
- 35. Субъединичные структуры глутаминсинтетазы вид сбоку вид сверху
- 36. Свойства белков Имеют заряды (положительные и отрицательные) Имеют разную растворимость в воде Способны выпадать в осадок
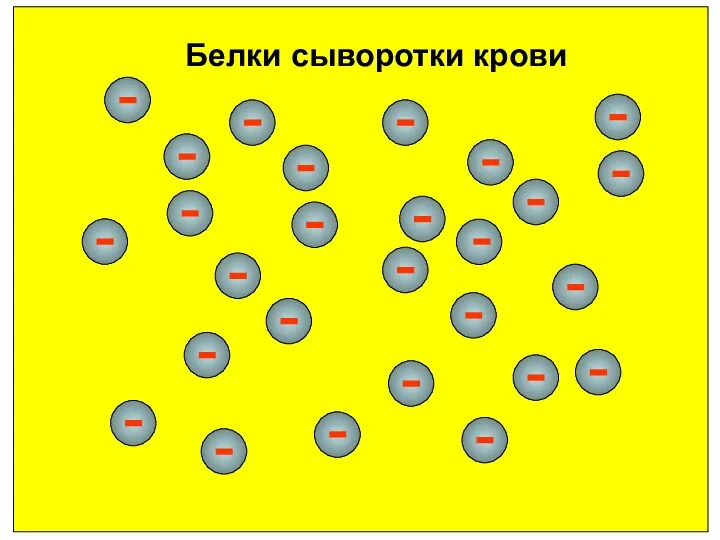
- 37. Белки сыворотки крови
- 38. Отрицательные заряды создают глутаминовая и аспарагиновая кислоты. Положительные заряды создают лизин, аргинин и гистидин. Белки имеют
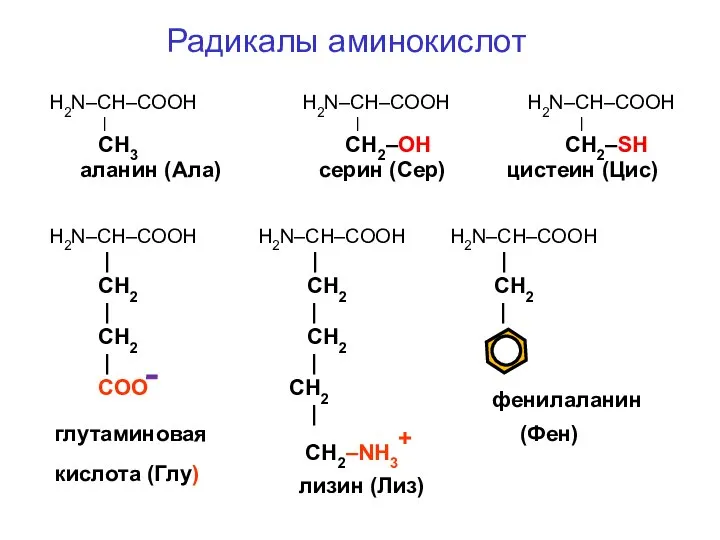
- 39. Радикалы аминокислот H2N–CH–COOH H2N–CH–COOH H2N–CH–COOH | | | СН3 СН2–ОН СН2–SН аланин (Ала) серин (Сер) цистеин
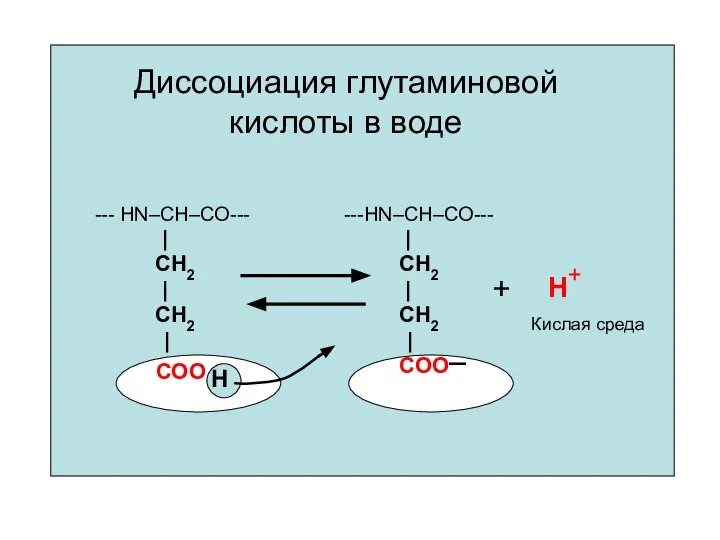
- 40. Диссоциация глутаминовой кислоты в воде ---HN–CH–CO--- | CH2 | CH2 | COO Н+ + Кислая среда
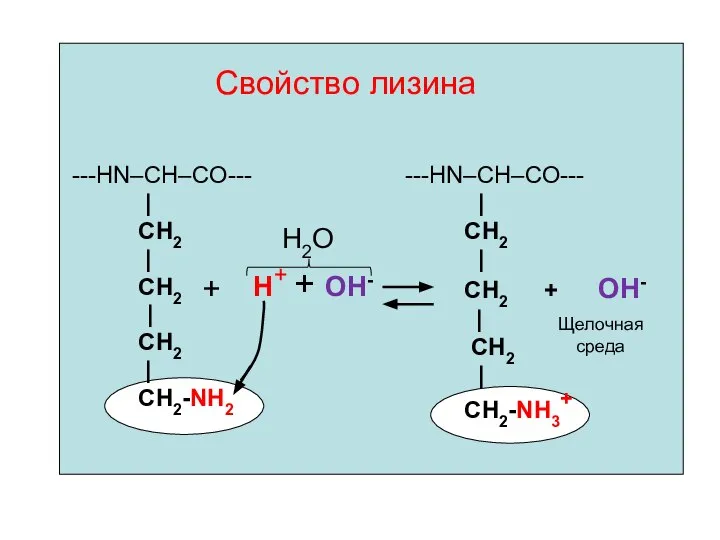
- 41. Свойство лизина ---HN–CH–CO--- | CH2 | CH2 | СН2 | СН2-NН2 Н+ + ОН- + ---HN–CH–CO---
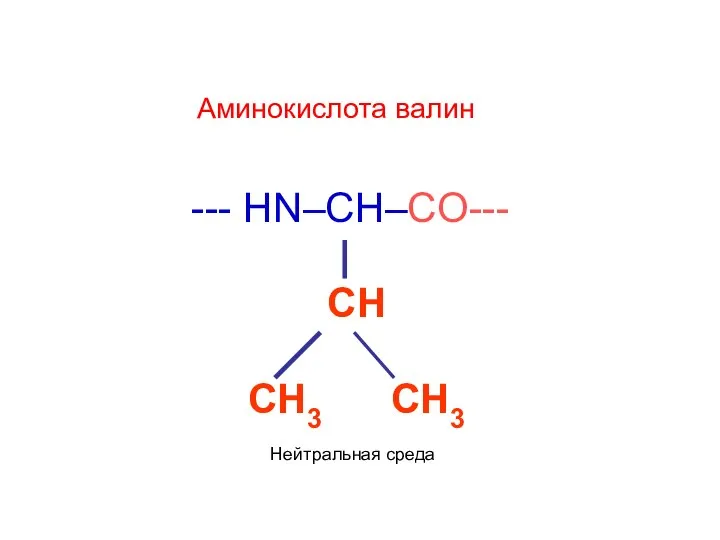
- 42. --- HN–CH–CO--- | CH CH3 CH3 Аминокислота валин Нейтральная среда
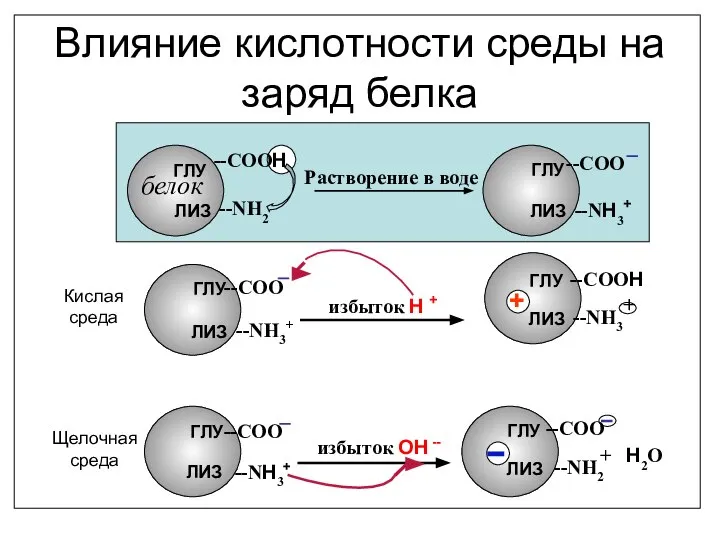
- 43. Влияние кислотности среды на заряд белка белок --СООН --NH2 Растворение в воде --NH3+ --СОО --СОО --NH3+
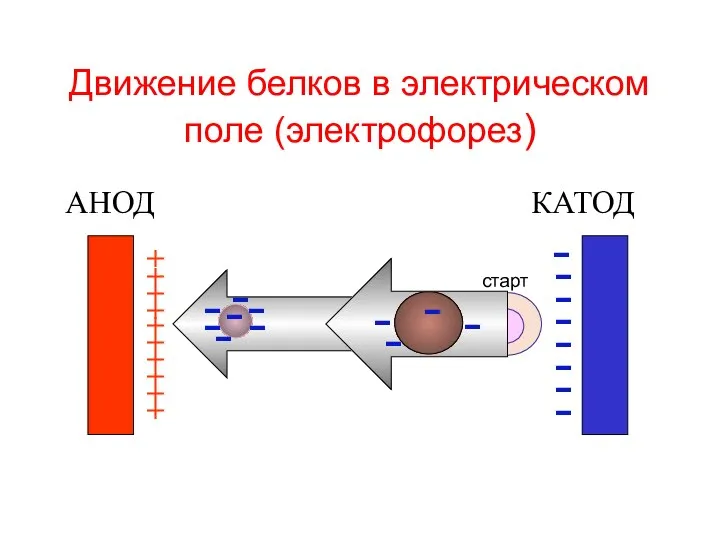
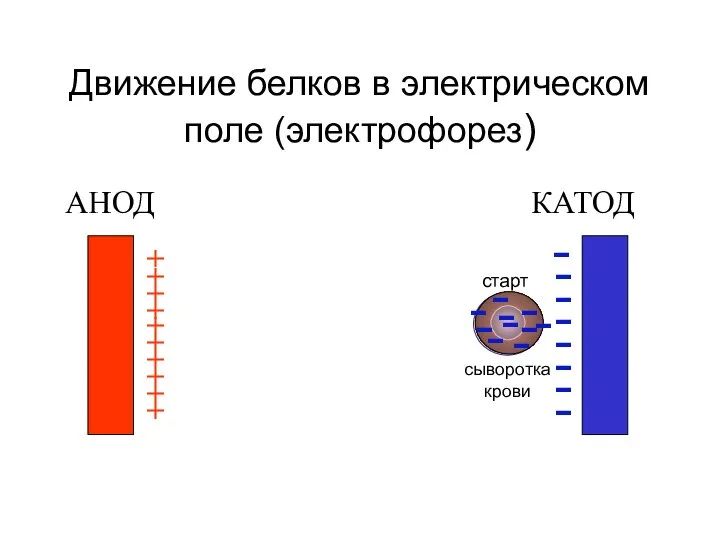
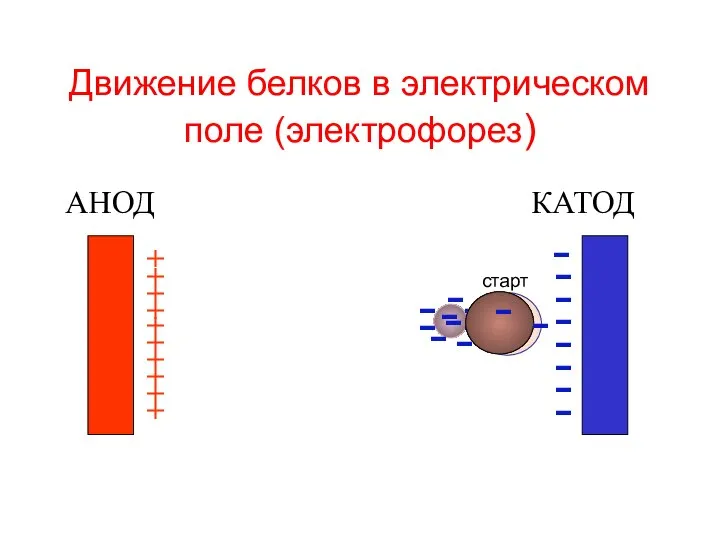
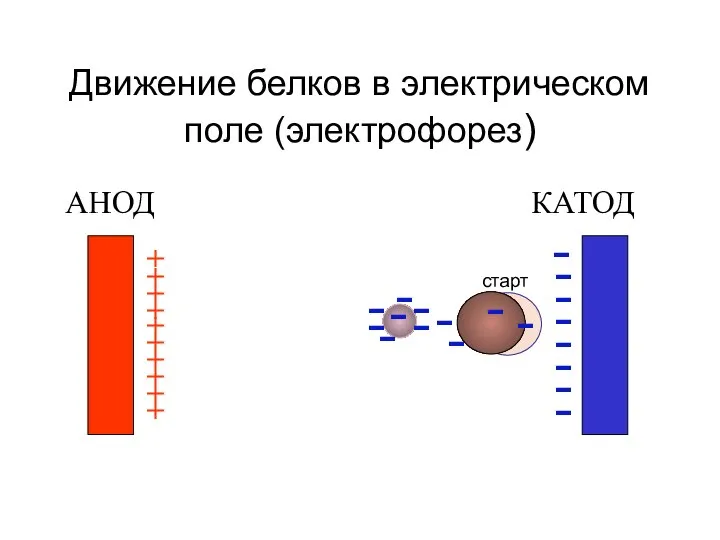
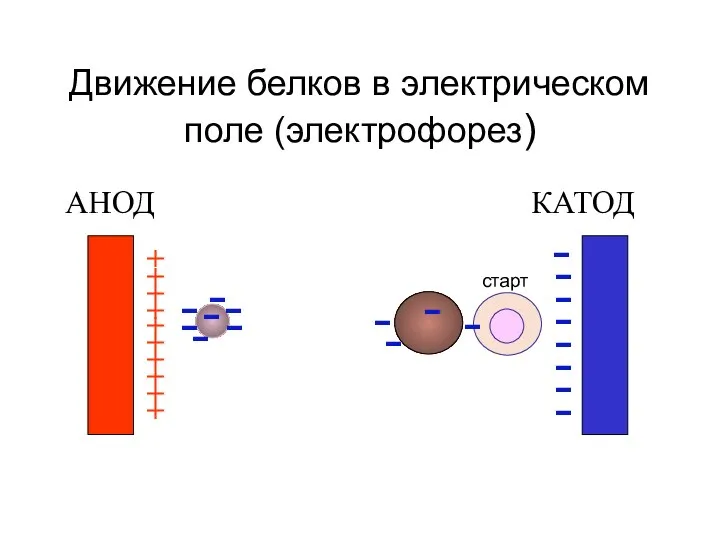
- 44. Движение белков в электрическом поле (электрофорез) АНОД КАТОД + + + + + + + +
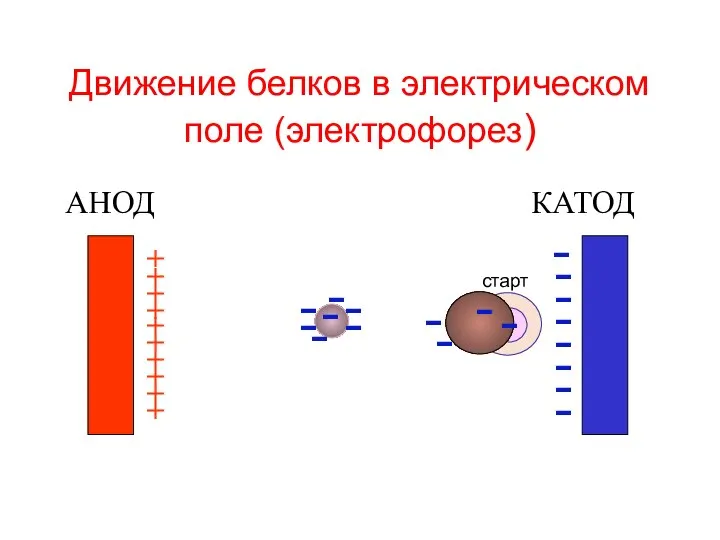
- 45. Движение белков в электрическом поле (электрофорез) АНОД КАТОД + + + + + + + +
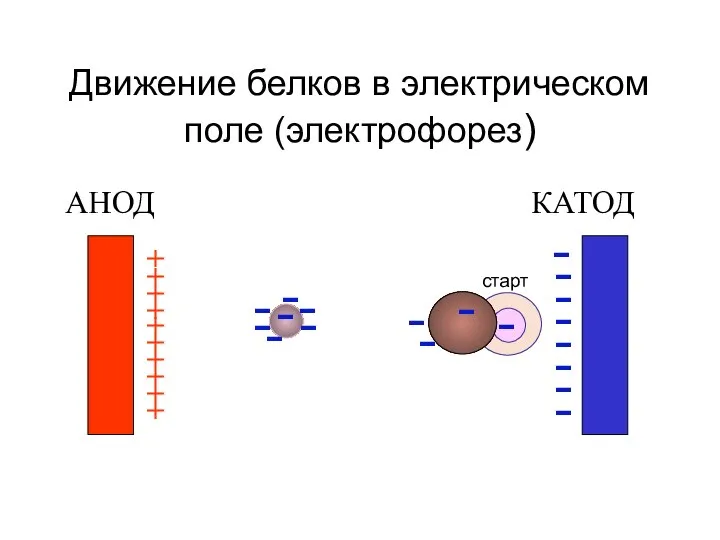
- 46. Движение белков в электрическом поле (электрофорез) АНОД КАТОД + + + + + + + +
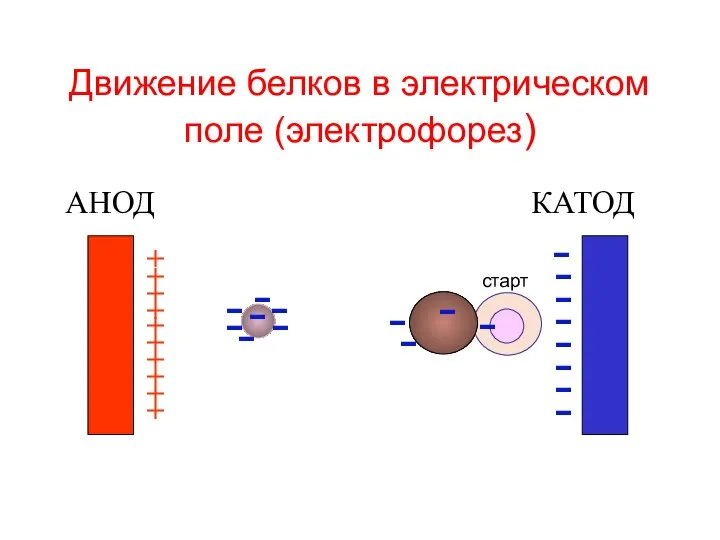
- 47. Движение белков в электрическом поле (электрофорез) АНОД КАТОД + + + + + + + +
- 48. Движение белков в электрическом поле (электрофорез) АНОД КАТОД + + + + + + + +
- 49. Движение белков в электрическом поле (электрофорез) АНОД КАТОД + + + + + + + +
- 50. Движение белков в электрическом поле (электрофорез) АНОД КАТОД + + + + + + + +
- 51. Движение белков в электрическом поле (электрофорез) АНОД КАТОД + + + + + + + +
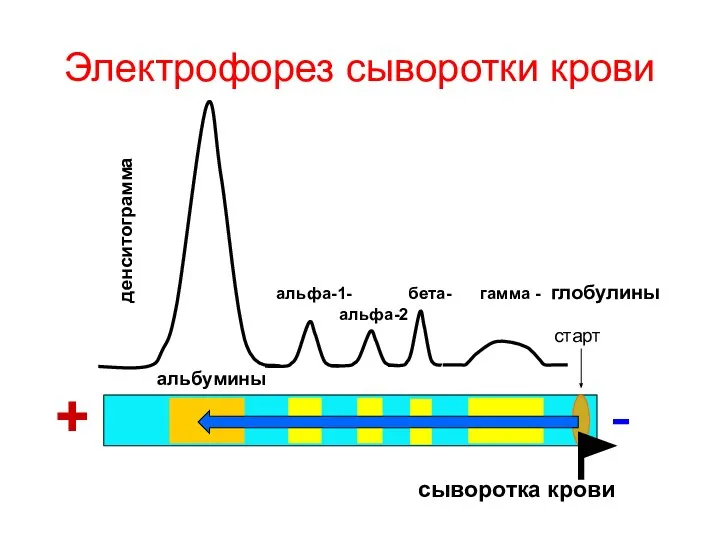
- 52. Электрофорез сыворотки крови + - старт денситограмма альбумины альфа-1- бета- гамма - глобулины альфа-2 сыворотка крови
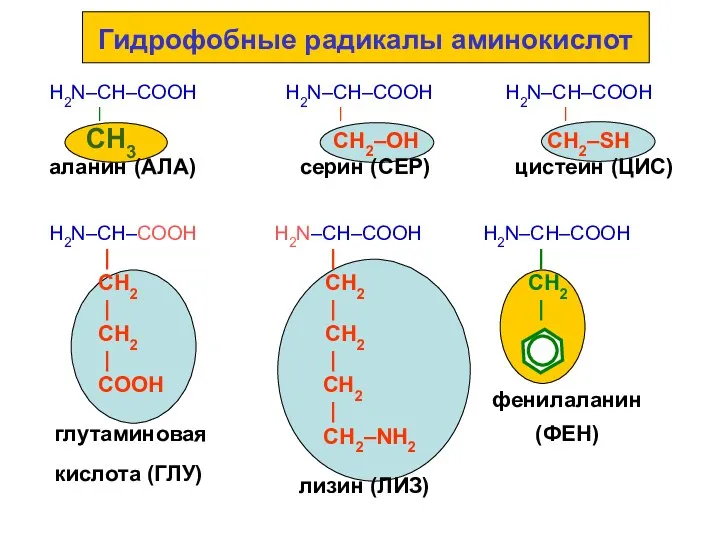
- 53. Роль аминокислот, содержащих гидрофобные радикалы (аланин, валин, лейцин, изолейцин, фенилаланин, тирозин)
- 54. Гидрофобные радикалы аминокислот H2N–CH–COOH H2N–CH–COOH H2N–CH–COOH | | | СН3 СН2–ОН СН2–SН аланин (АЛА) серин (СЕР)
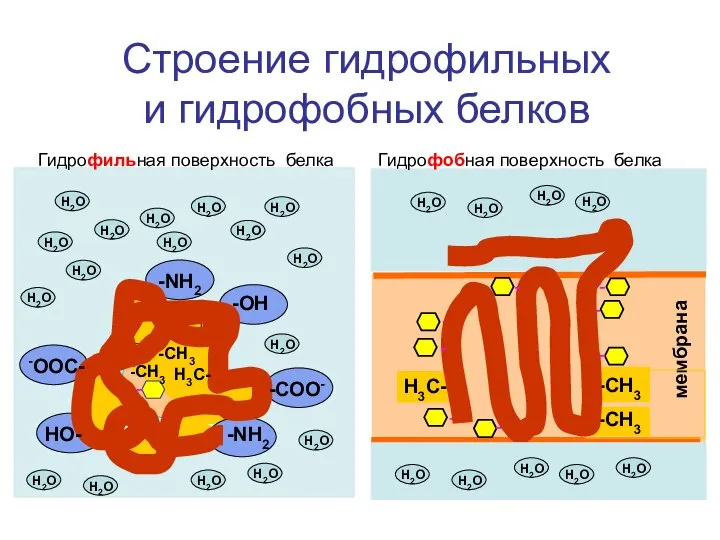
- 55. Строение гидрофильных и гидрофобных белков -ОН -СОО- -NH2 -NH2 -OOC- НО- - -СН3 -СН3 Н3С- -
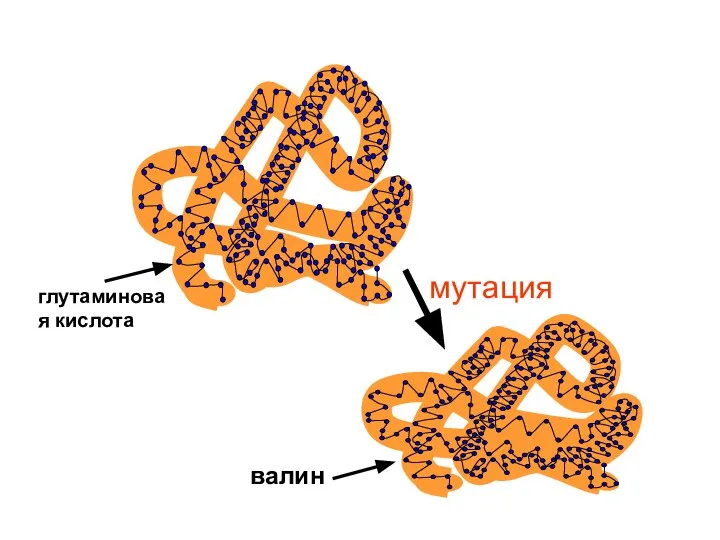
- 57. Протеинопатии Серповидно-клеточная анемия нормальный эритроцит анемия
- 58. глутаминовая кислота валин мутация
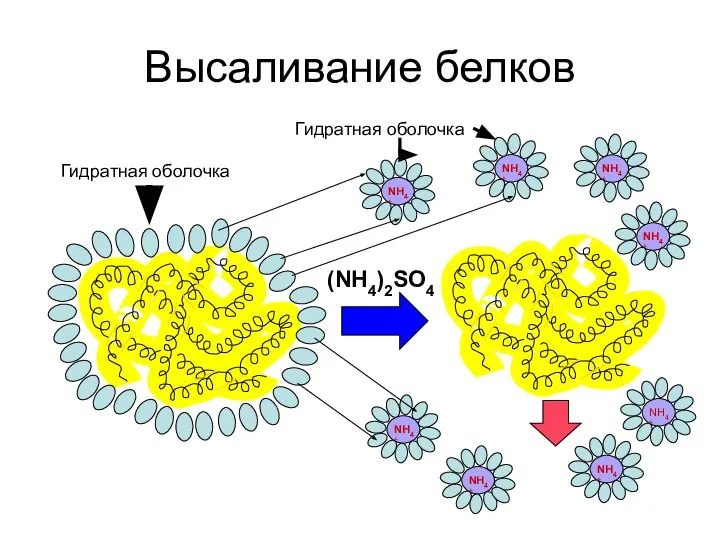
- 59. Высаливание белков (NH4)2SO4 Гидратная оболочка Гидратная оболочка
- 60. Классификация белков Простые белки ( состоят только из аминокислот) Сложные белки (в состав белка входят различные
- 61. Простые и сложные белки ГЕМ альбумин миоглобин
- 62. Простые белки Альбумины Глобулины Протамины Гистоны Глютелины Проламины
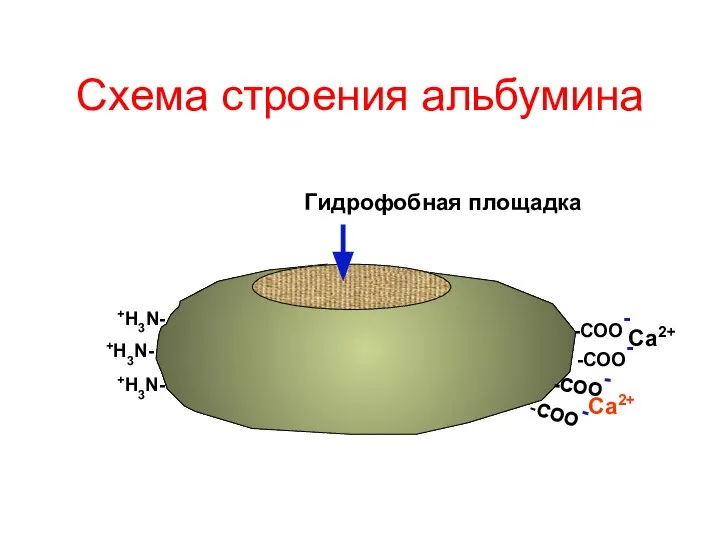
- 63. Схема строения альбумина Гидрофобная площадка -СОО- -СОО- -СОО- -СОО- Са2+ Са2+ +Н3N- +Н3N- +Н3N-
- 64. Роль альбумина Запасной источник аминокислот Компонент буферной системы Осмотически активный белок Переносчик жирных кислот Переносчик жирорастворимых
- 65. глобулины
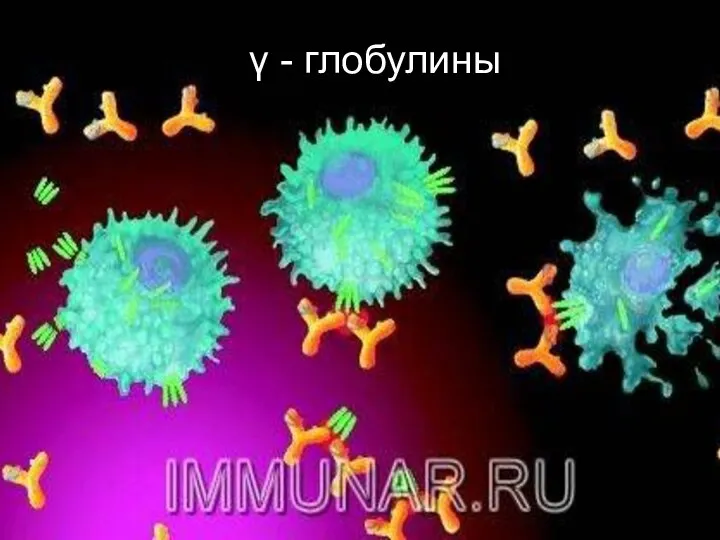
- 66. γ - глобулиновая фракция сыворотки крови Содержит иммунные глобулины (IgA; IgЕ; IgМ; IgD; IgG).
- 67. α1-глобулины α2-глобулины β - глобулины γ - глобулины
- 68. Основной функцией сывороточного IgA является обеспечение местного иммунитета, защита дыхательных, мочеполовых путей и желудочно-кишечного тракта от
- 69. Протамины и гистоны
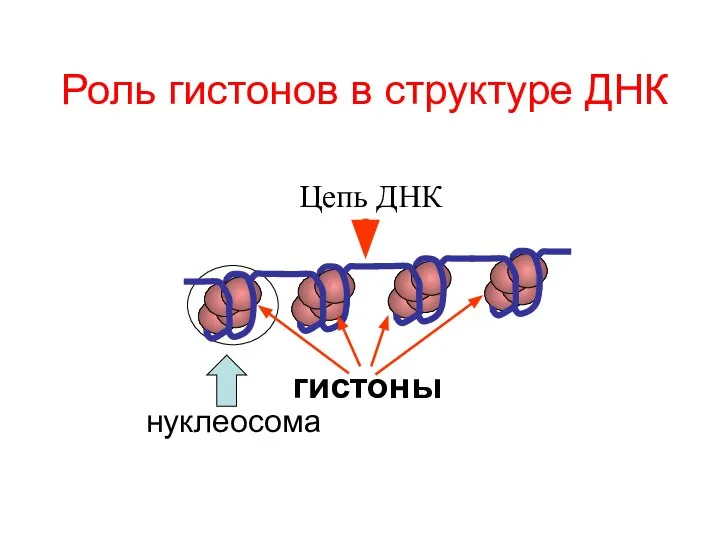
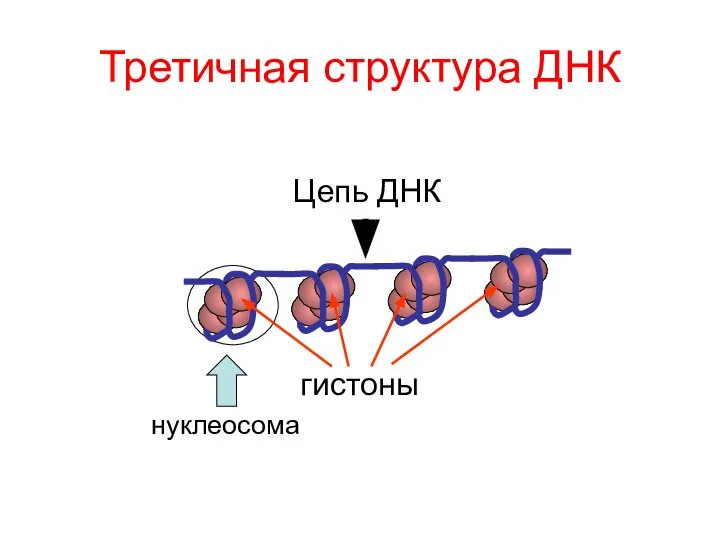
- 70. Роль гистонов в структуре ДНК гистоны Цепь ДНК нуклеосома
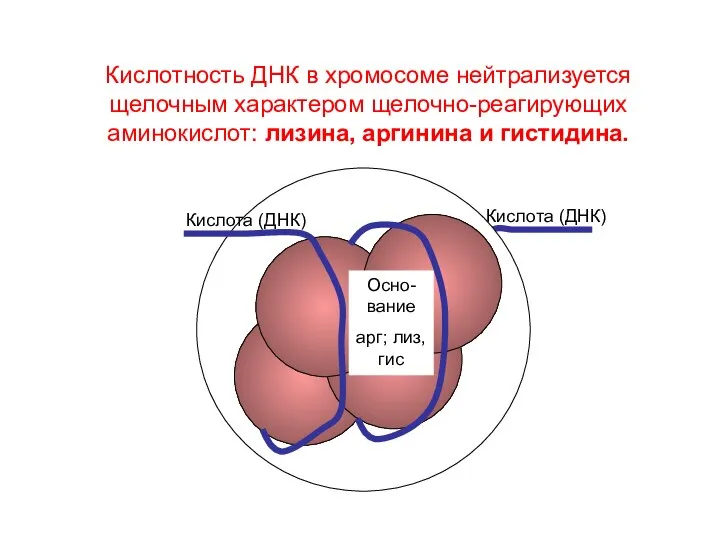
- 71. Кислотность ДНК в хромосоме нейтрализуется щелочным характером щелочно-реагирующих аминокислот: лизина, аргинина и гистидина. Кислота (ДНК) Осно-вание
- 72. Роль протаминов и гистонов Факторы укорочения полинуклеотидной цепи Нейтрализуют кислотность ДНК Являются регуляторами транскрипции (места нуклеосом
- 73. Проламины и глютелины – белки растительного происхождения
- 75. Сложные белки Нуклеопротеины Липопротеины Хромопротеины Фосфопротеины Гликопротеины Белки-ферменты
- 76. Строение нуклеопротеинов
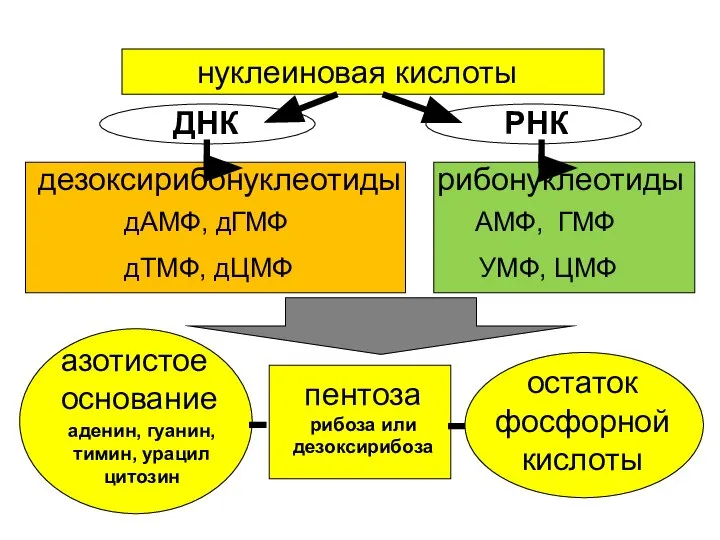
- 77. нуклеиновая кислоты дезоксирибонуклеотиды рибонуклеотиды ДНК РНК дАМФ, дГМФ АМФ, ГМФ дТМФ, дЦМФ УМФ, ЦМФ азотистое основание
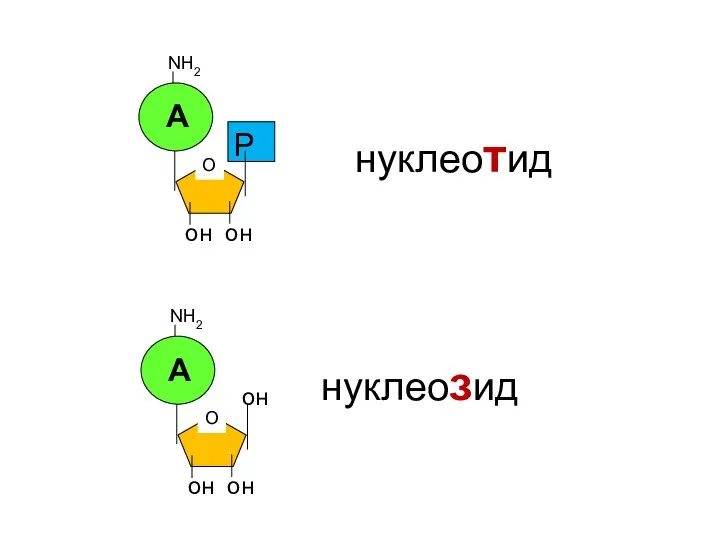
- 78. он он NН2 Р О А он он NН2 О А он нуклеотид нуклеозид
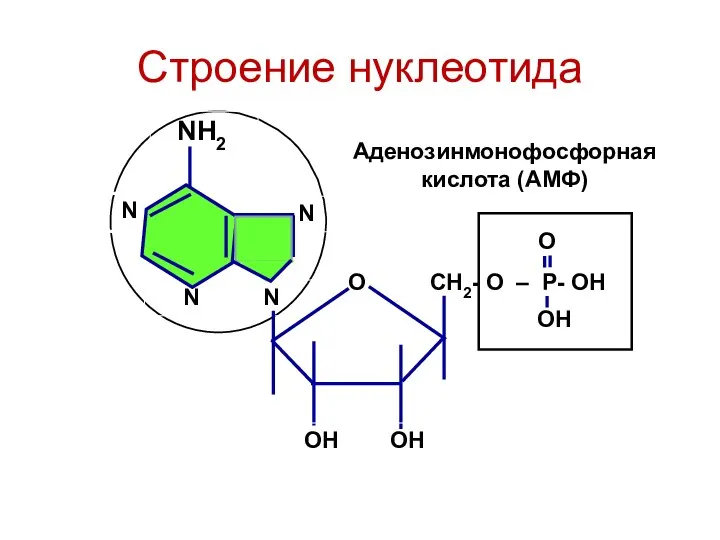
- 79. N N N NH2 N Строение нуклеотида О СН2- О – Р- ОН ОH ОН О
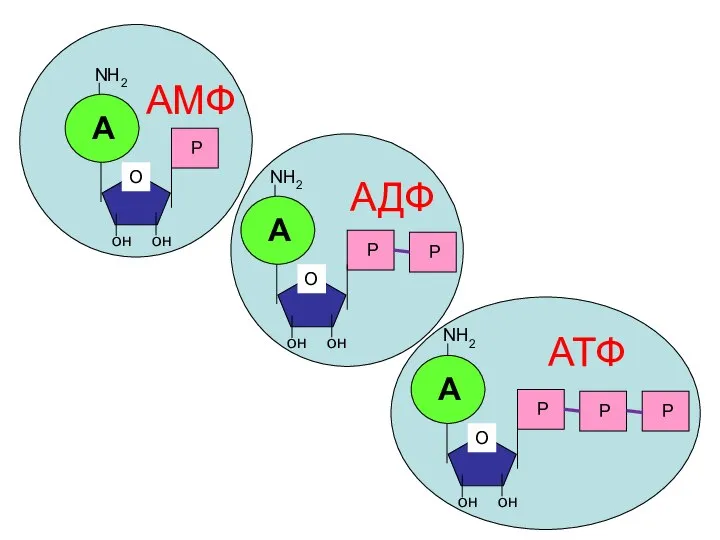
- 80. он он NН2 Р О А он он NН2 Р О А Р он он NН2
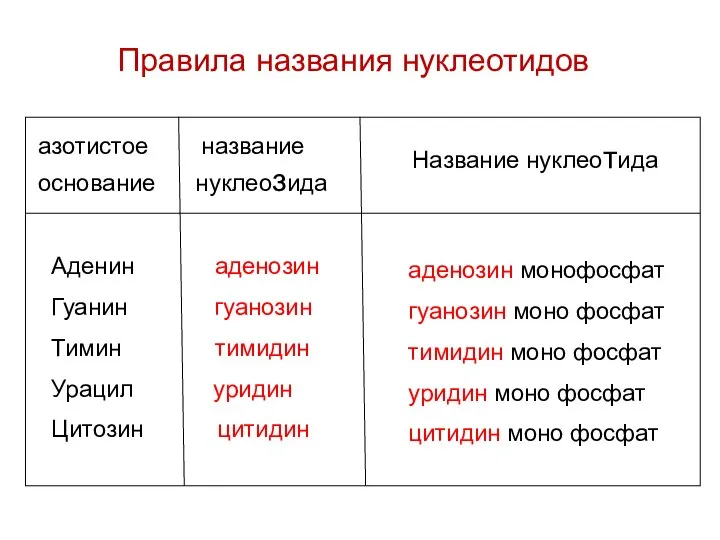
- 81. азотистое название основание нуклеозида Аденин аденозин Гуанин гуанозин Тимин тимидин Урацил уридин Цитозин цитидин аденозин монофосфат
- 82. О СН2-О – Р =О ОН О СН2-О – Р =О Н О ОН О СН2-О
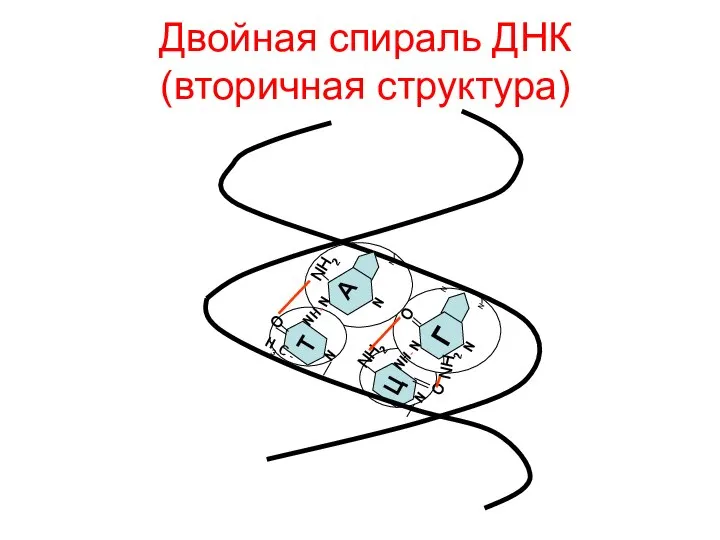
- 83. Двойная спираль ДНК (вторичная структура) O NH2 N N N N NH- N A T H3C
- 84. Третичная структура ДНК гистоны Цепь ДНК нуклеосома
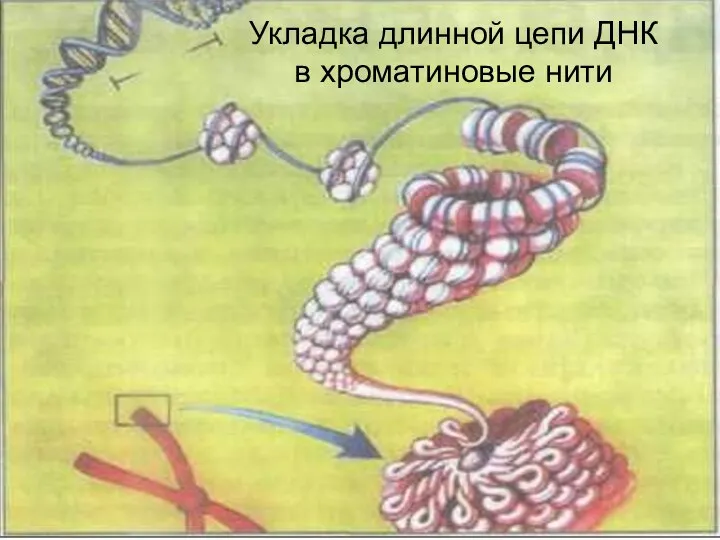
- 85. Укладка длинной цепи ДНК в хроматиновые нити
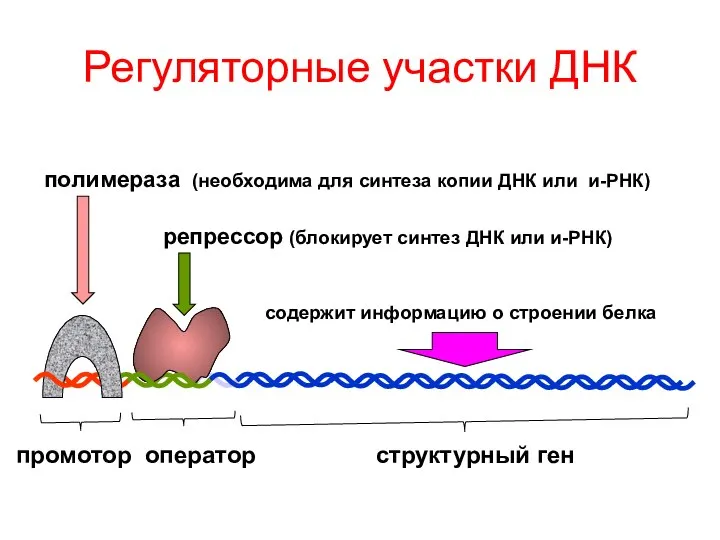
- 86. Регуляторные участки ДНК промотор оператор структурный ген полимераза (необходима для синтеза копии ДНК или и-РНК) репрессор
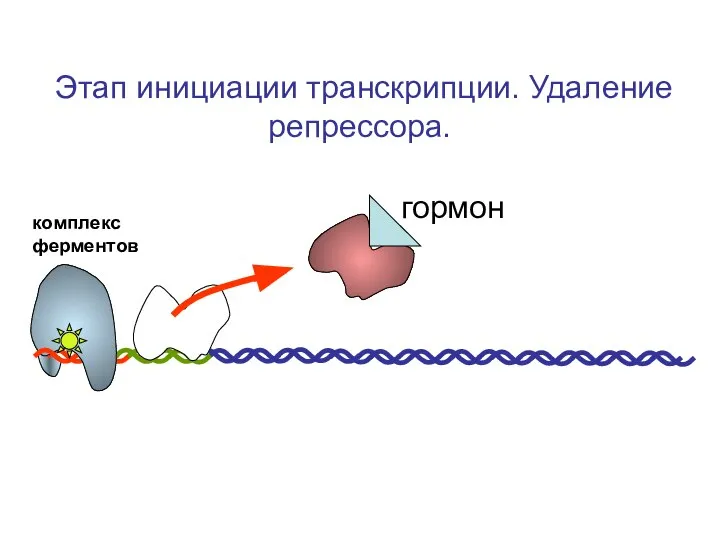
- 87. Этап инициации транскрипции. Удаление репрессора. комплекс ферментов гормон
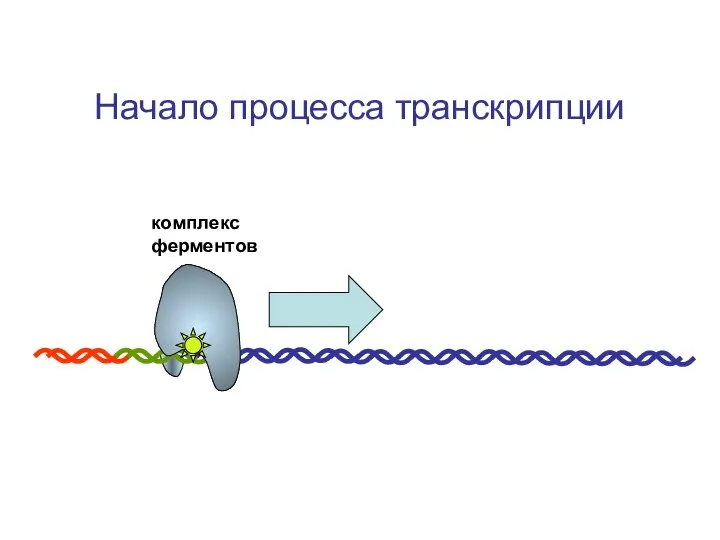
- 88. Начало процесса транскрипции комплекс ферментов
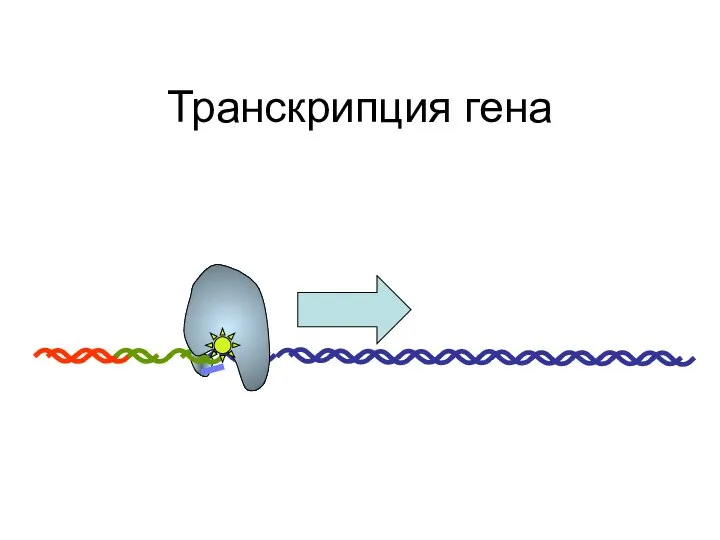
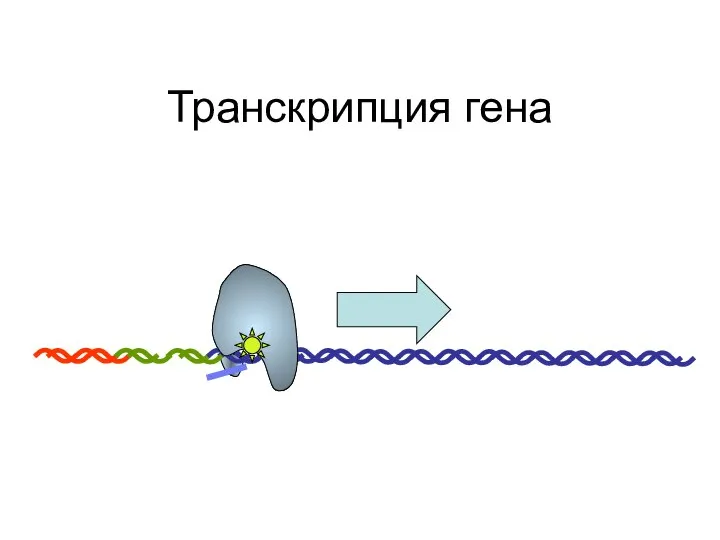
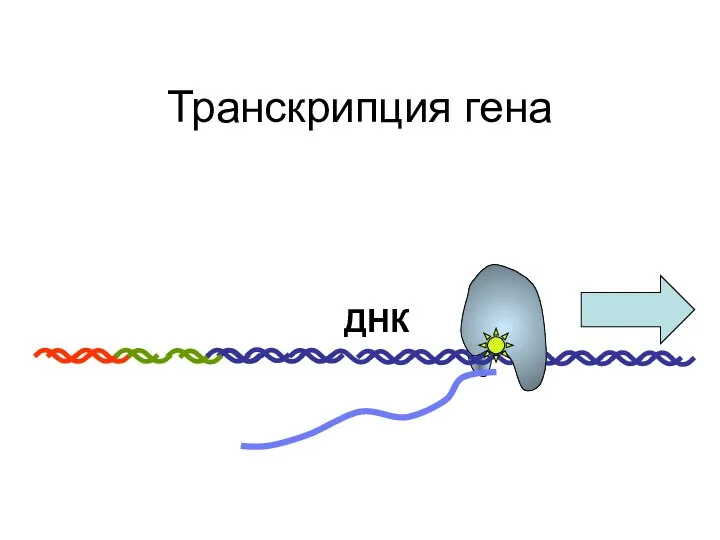
- 89. Транскрипция гена
- 90. Транскрипция гена
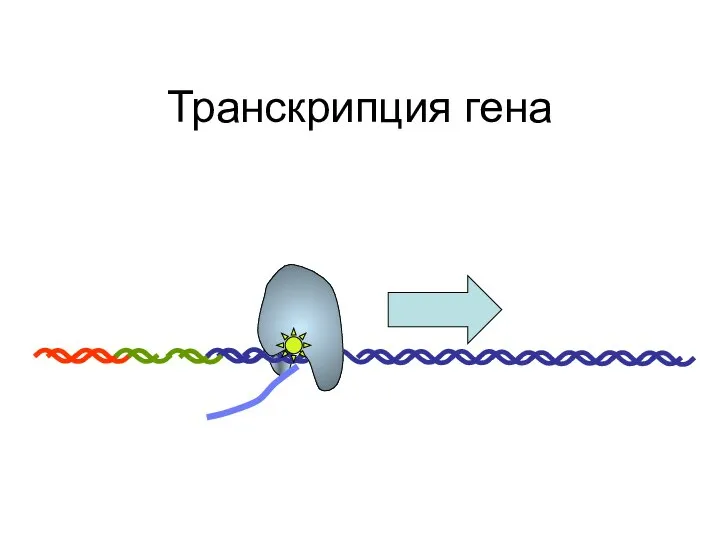
- 91. Транскрипция гена
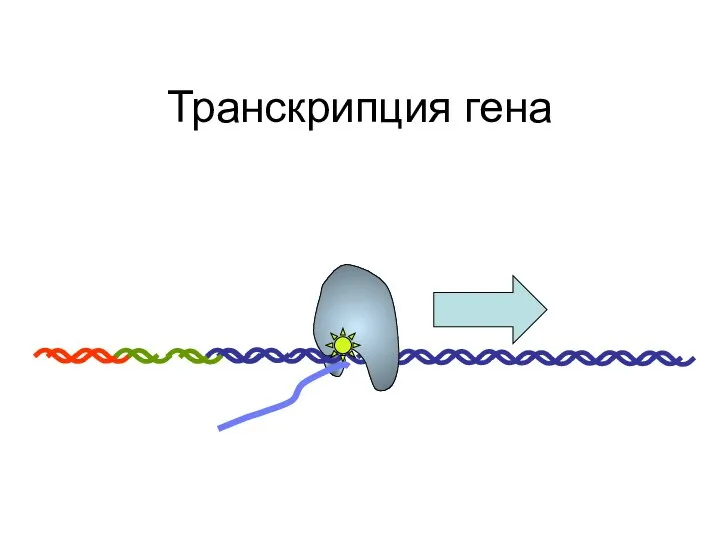
- 92. Транскрипция гена
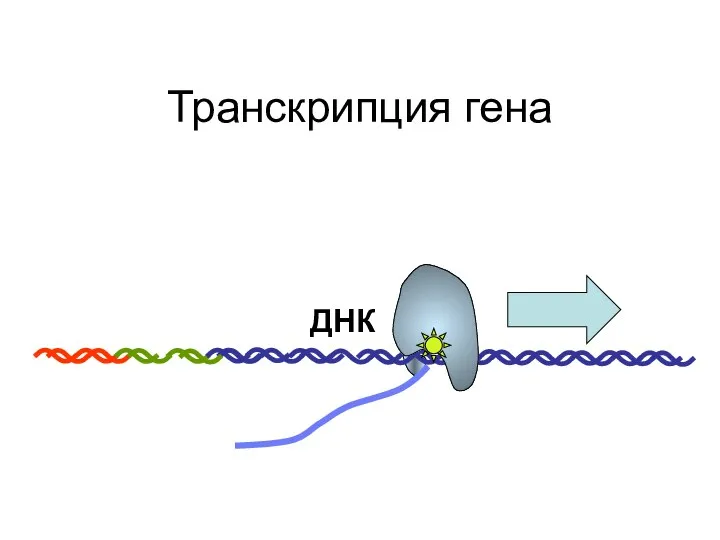
- 93. Транскрипция гена ДНК
- 94. Транскрипция гена ДНК
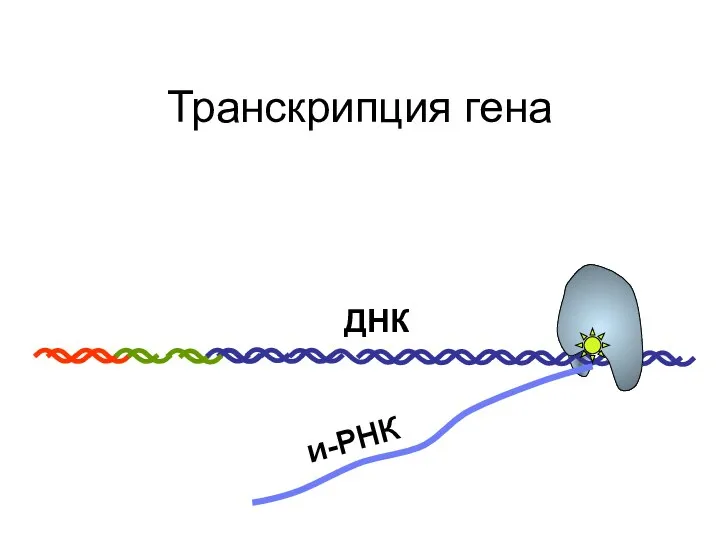
- 95. Транскрипция гена и-РНК ДНК
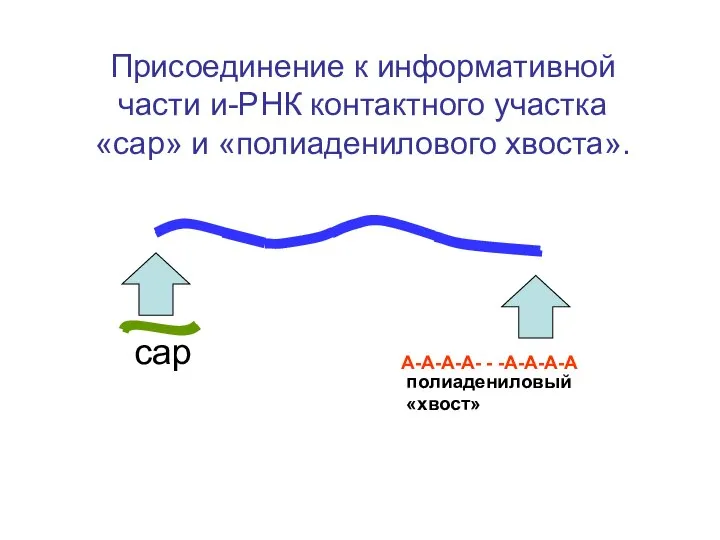
- 96. А-А-А-А- - -А-А-А-А сар полиадениловый «хвост» Присоединение к информативной части и-РНК контактного участка «сар» и «полиаденилового
- 97. А-А-А-А- - -А-А-А-А Завершение синтеза и-РНК сар
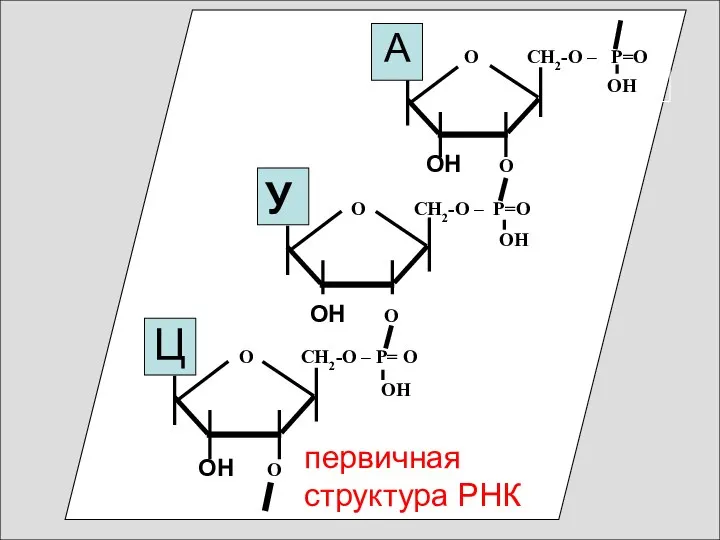
- 98. О СН2-О – Р=О ОН О СН2-О – Р=О ОН О ОН О СН2-О – Р=
- 99. Задача -1 Сколько нуклеотидов содержит информативная часть и-РНК, кодирующая белок, состоящий из 100 аминокислот?
- 100. Задача-2 Кто читает информацию, заключенную в и-РНК?
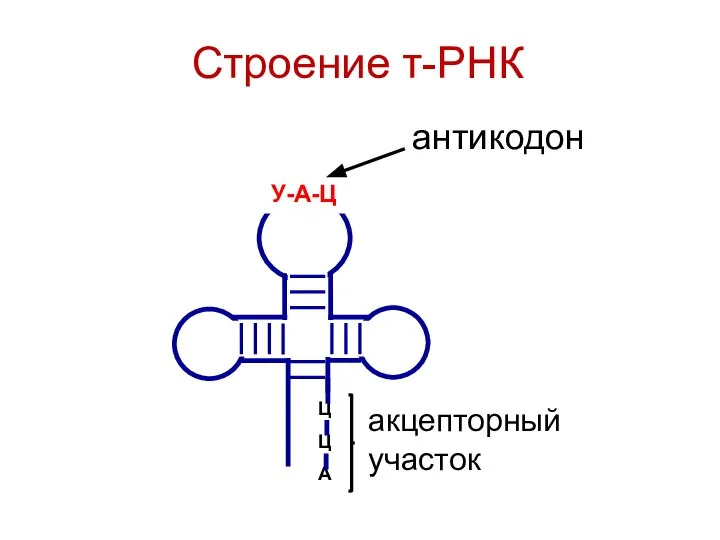
- 101. Строение т-РНК Ц Ц А антикодон акцепторный участок У-А-Ц
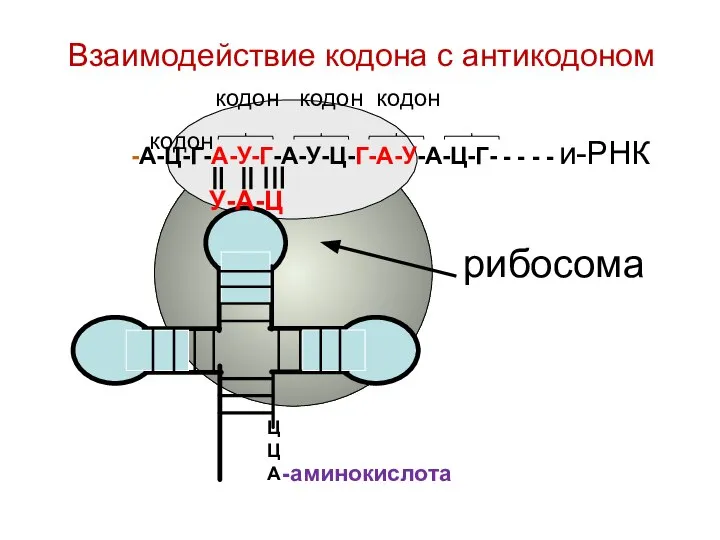
- 102. Взаимодействие кодона с антикодоном кодон кодон кодон кодон -А-Ц-Г-А-У-Г-А-У-Ц-Г-А-У-А-Ц-Г- - - - - и-РНК У-А-Ц ЦЦА
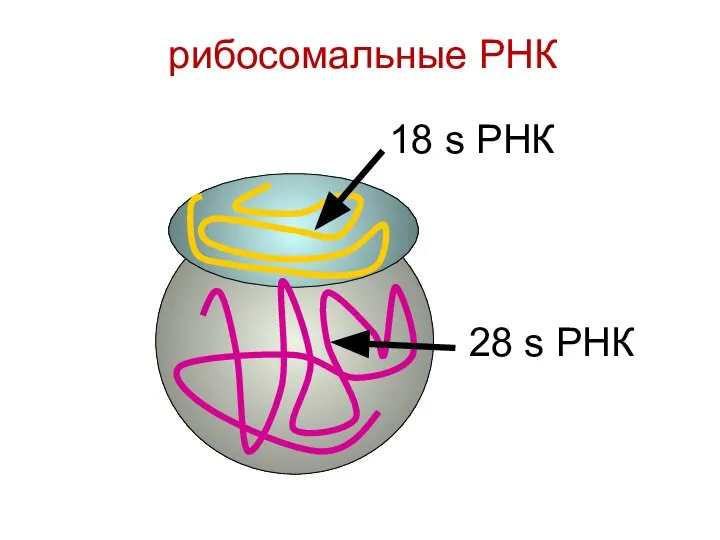
- 103. 18 s РНК 28 s РНК рибосомальные РНК
- 104. Строение липопротеинов
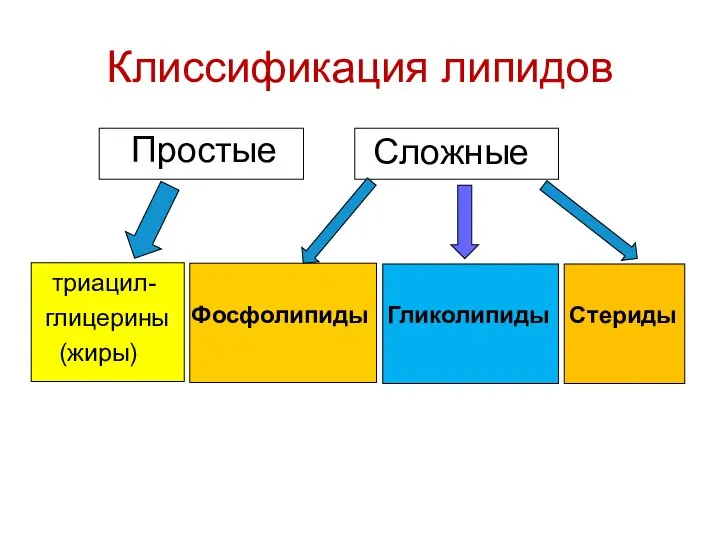
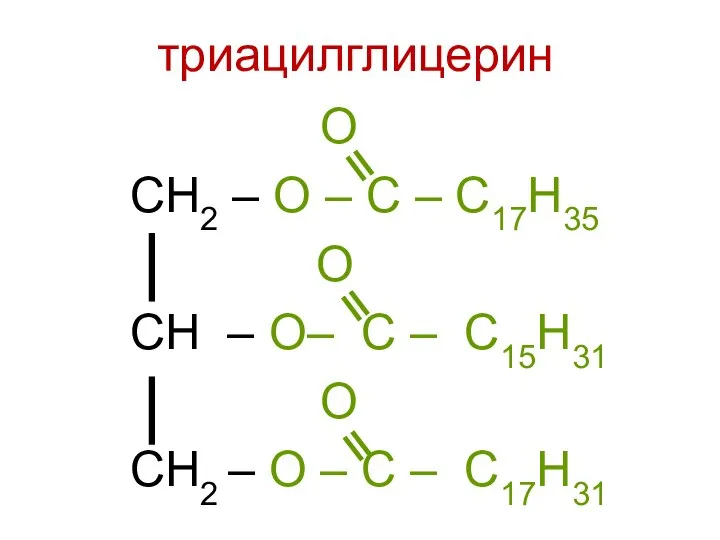
- 105. Клиссификация липидов триацил- глицерины (жиры) Фосфолипиды Гликолипиды Стериды Сложные Простые
- 106. О СН2 – О – С – С17Н35 О СН – О– С – С15Н31 О
- 107. С15Н31 СООН – пальмитиновая кислота С17Н35 СООН – стеариновая кислота С17Н33 СООН – олеиновая кислота С17Н31
- 108. Н3С- СН2-СН2-СН2= СН2-СН2-СН2= СН2-СН2-СН2- СН2-СН2-СН2- СН2-СН2-СООН 16 15 14 13 12 11 10 9 8 7
- 109. Непредельные высшие кислоты не синтезируются в организме человека. Поэтому люди испытывают необходимость ежедневного приема ненасыщенных жирных
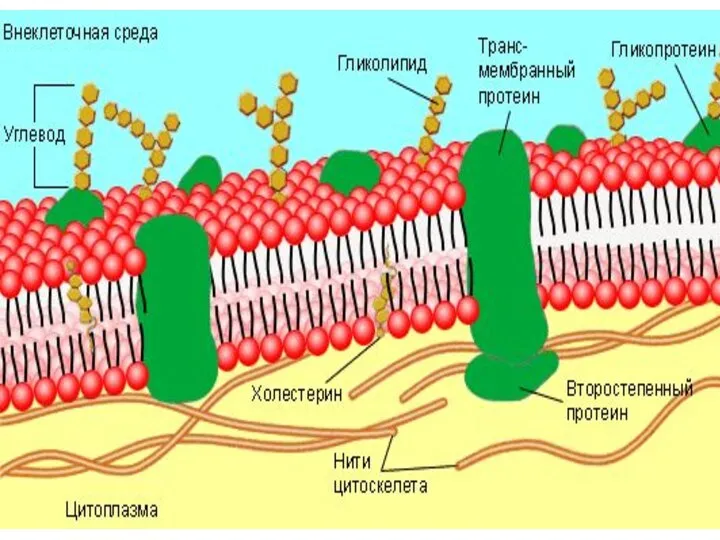
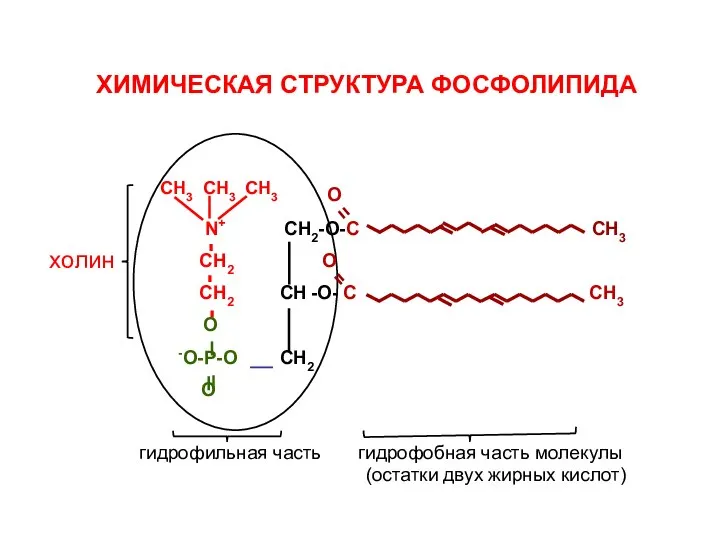
- 110. ХИМИЧЕСКАЯ СТРУКТУРА ФОСФОЛИПИДА гидрофильная часть гидрофобная часть молекулы (остатки двух жирных кислот) О N+ СН2-О-С СН3
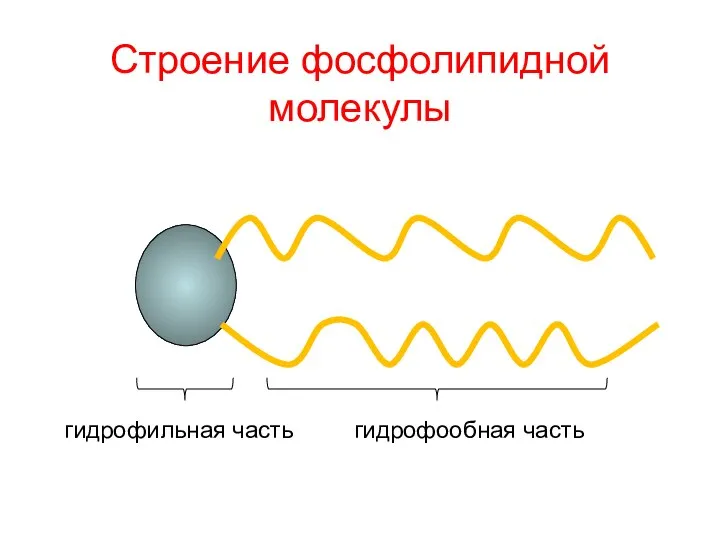
- 111. Строение фосфолипидной молекулы гидрофильная часть гидрофообная часть
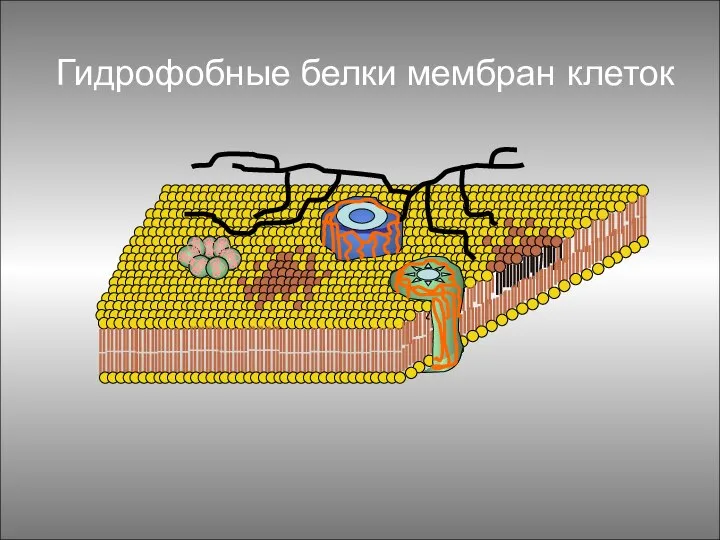
- 112. Гидрофобные белки мембран клеток
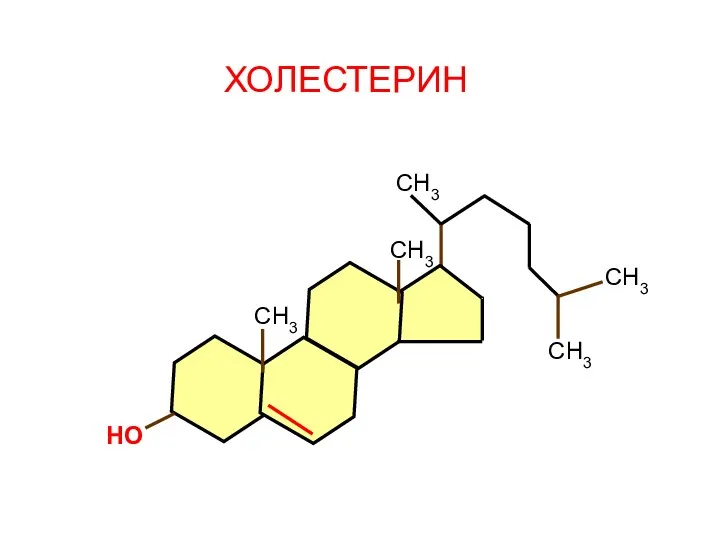
- 113. СН3 СН3 СН3 СН3 СН3 НО ХОЛЕСТЕРИН
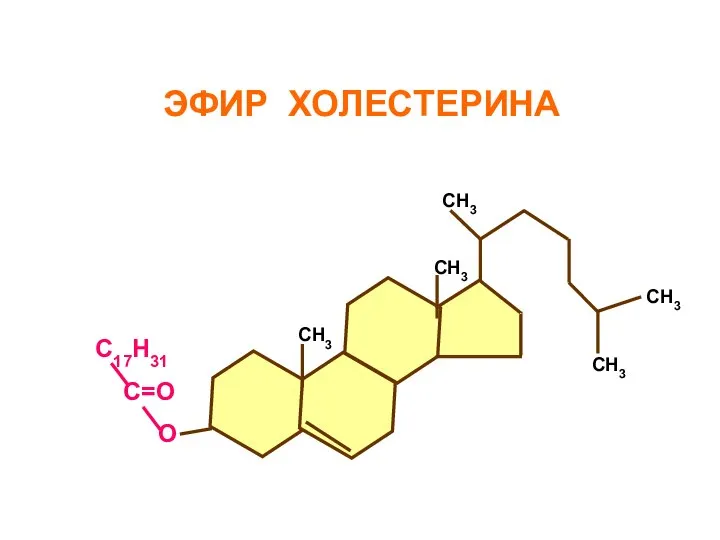
- 114. СН3 СН3 СН3 СН3 СН3 С17Н31 С=О О ЭФИР ХОЛЕСТЕРИНА
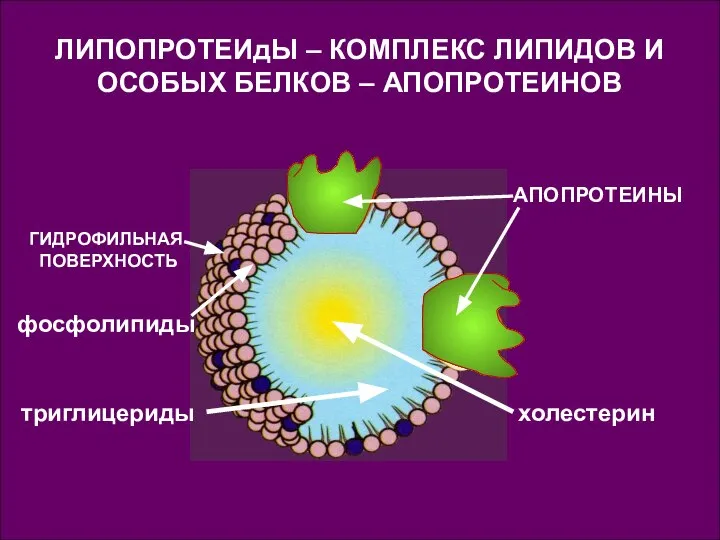
- 115. ЛИПОПРОТЕИдЫ – КОМПЛЕКС ЛИПИДОВ И ОСОБЫХ БЕЛКОВ – АПОПРОТЕИНОВ АПОПРОТЕИНЫ холестерин фосфолипиды ГИДРОФИЛЬНАЯ ПОВЕРХНОСТЬ триглицериды
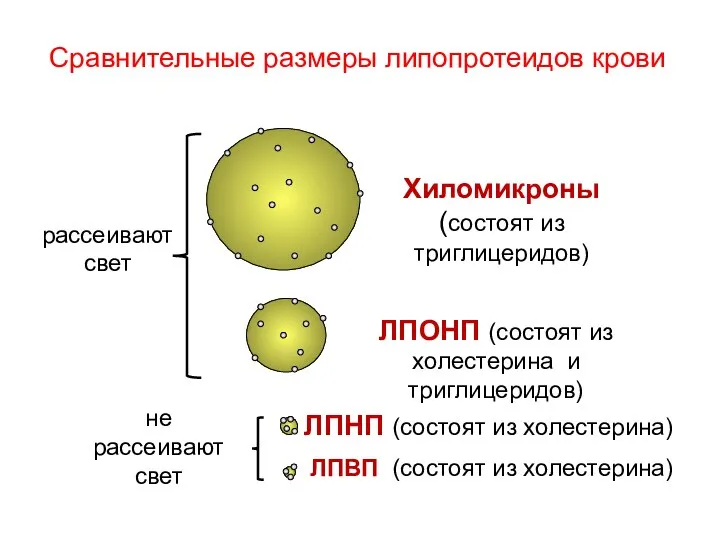
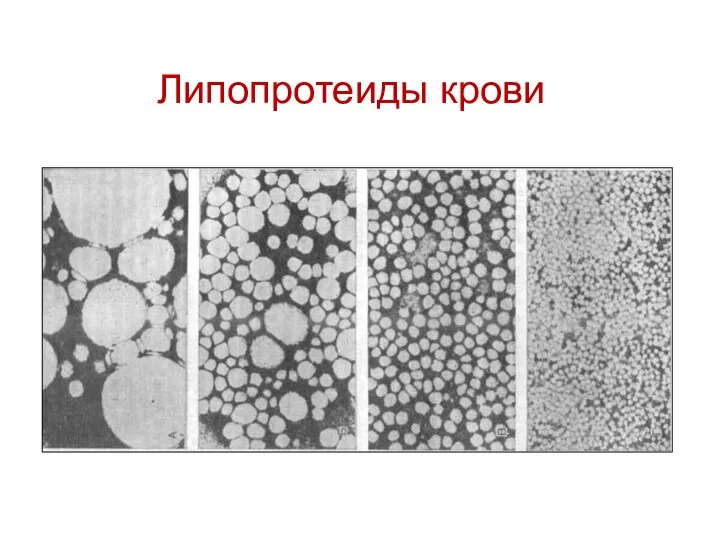
- 116. Сравнительные размеры липопротеидов крови Хиломикроны (состоят из триглицеридов) ЛПОНП (состоят из холестерина и триглицеридов) ЛПНП (состоят
- 117. Липопротеиды крови
- 118. Строение хромопротеинов
- 119. Примеры белков хромопротеинов миоглобин гемоглобин цитохромы
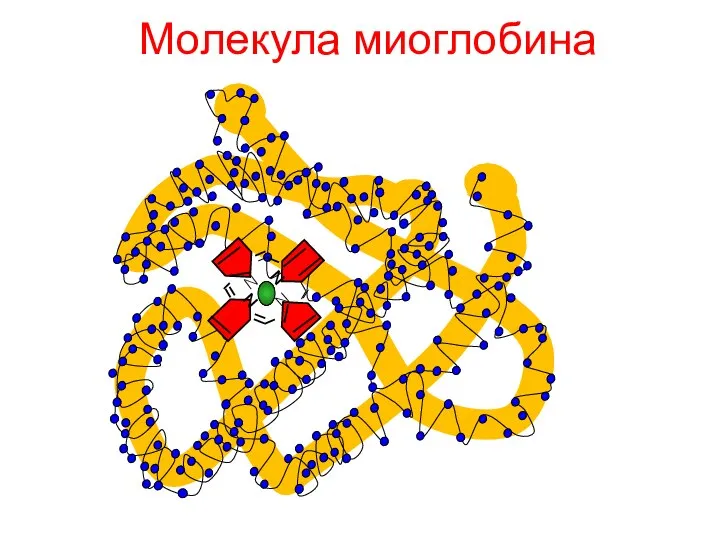
- 120. Молекула миоглобина N N N N
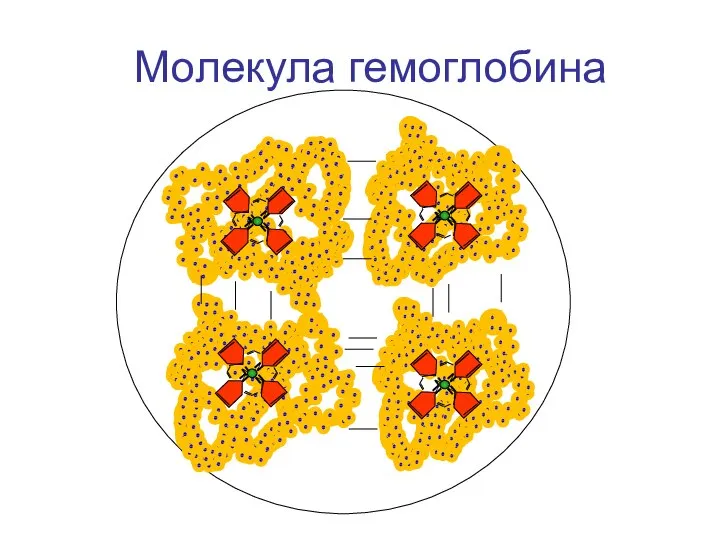
- 121. Молекула гемоглобина N N N N N N N N N N N N N N
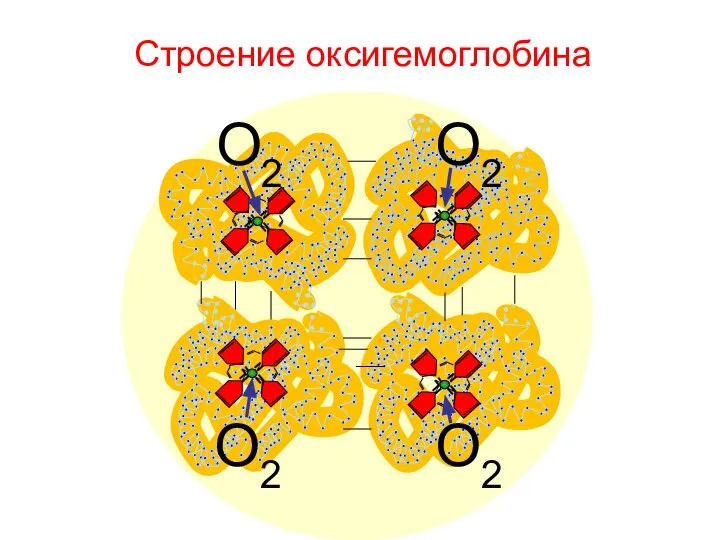
- 122. Строение оксигемоглобина N N N N N N N N N N N N N N
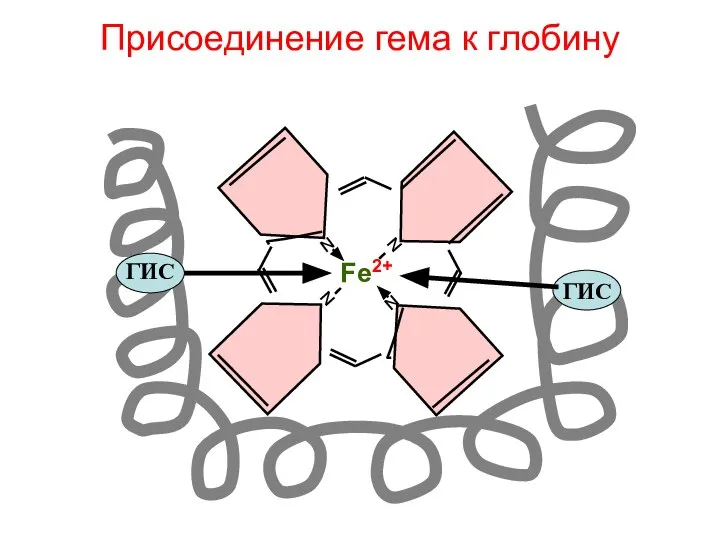
- 123. Присоединение гема к глобину N N N N Fe2+ ГИС ГИС
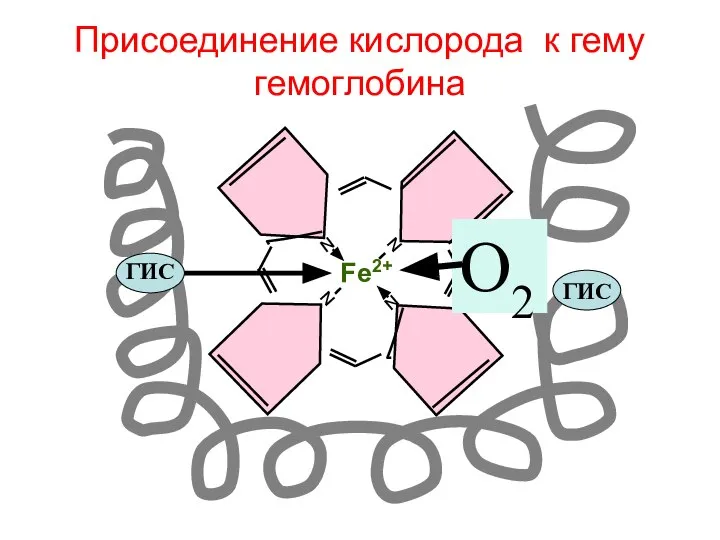
- 124. Присоединение кислорода к гему гемоглобина N N N N Fe2+ ГИС ГИС О2
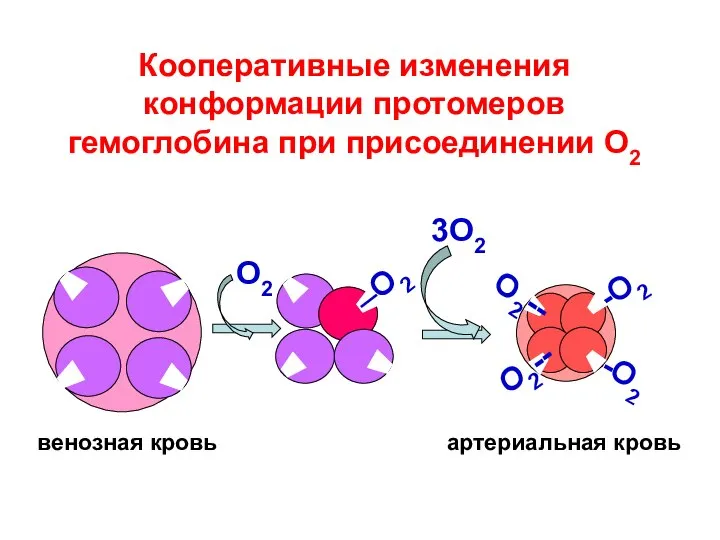
- 125. Кооперативные изменения конформации протомеров гемоглобина при присоединении О2 --О2 --О2 3О2 О2 венозная кровь артериальная кровь
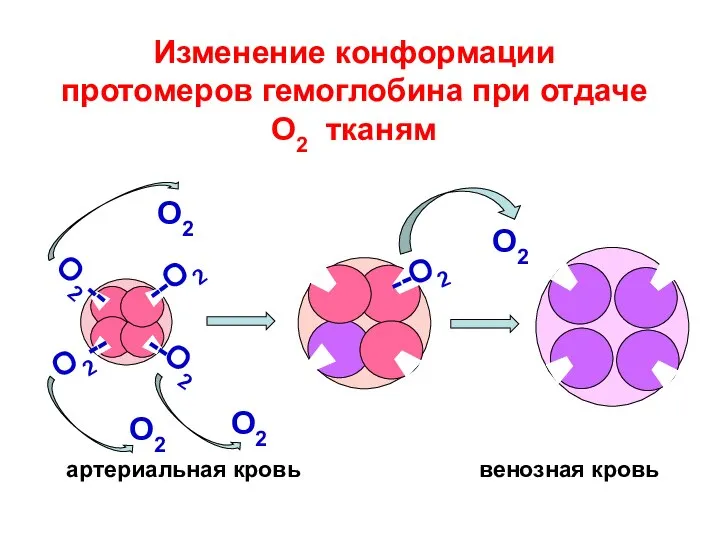
- 126. Изменение конформации протомеров гемоглобина при отдаче О2 тканям О2 О2 артериальная кровь венозная кровь О2 О2
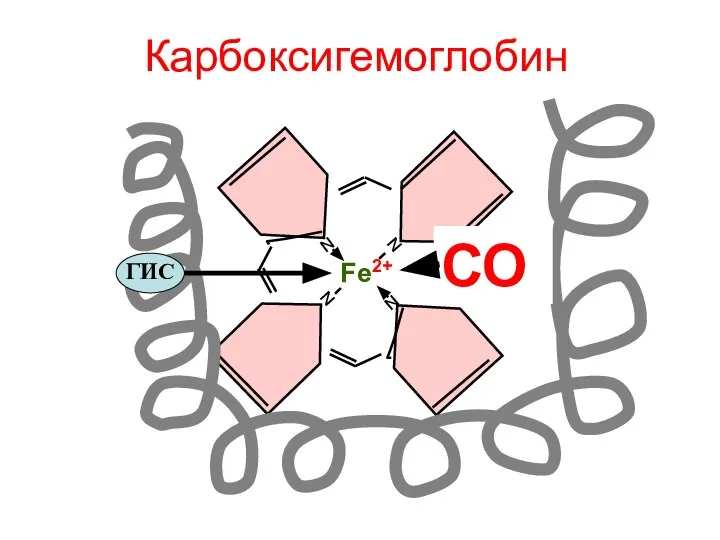
- 127. Карбоксигемоглобин N N N N Fe2+ ГИС СО
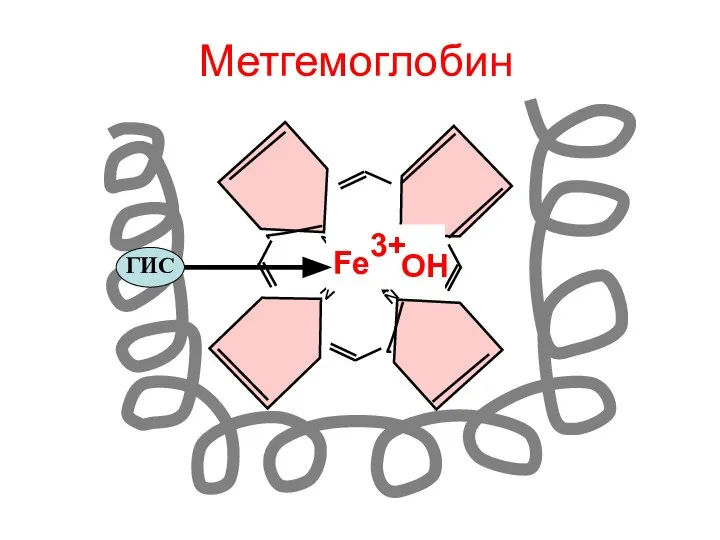
- 128. Метгемоглобин N N N N Fe3+ ГИС ОН
- 129. Гликопротеины (преобладает белковая часть) Протеогликаны (преобладает углеводный компонент)
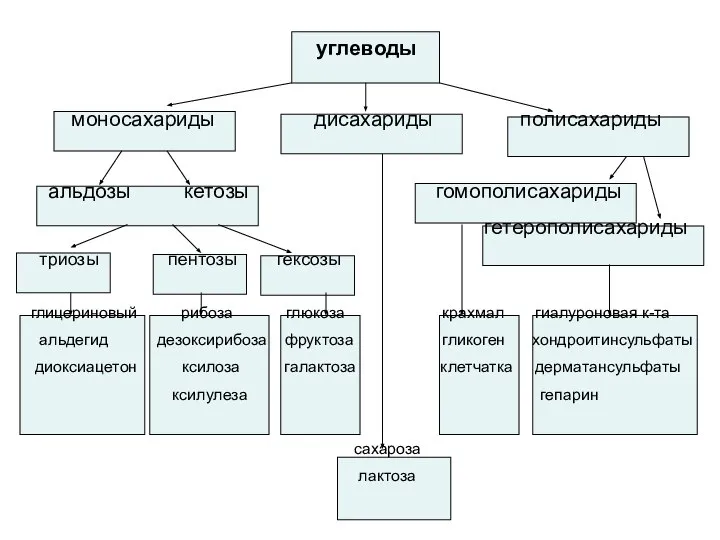
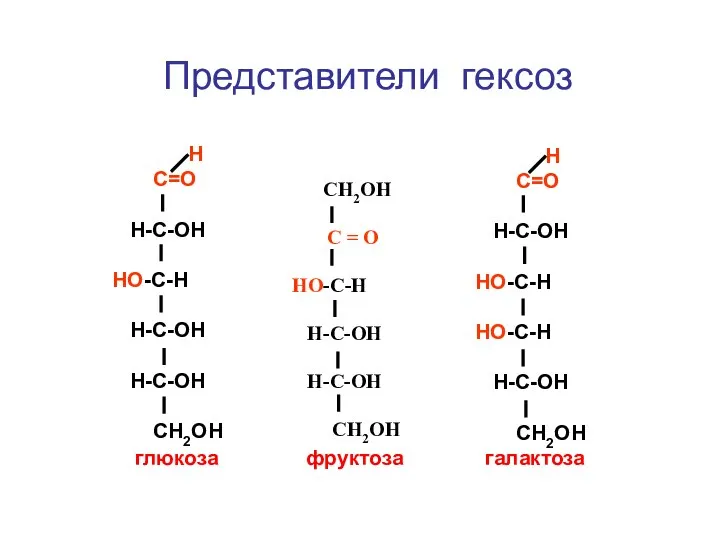
- 130. углеводы моносахариды дисахариды полисахариды альдозы кетозы гомополисахариды гетерополисахариды триозы пентозы гексозы глицериновый рибоза глюкоза крахмал гиалуроновая
- 131. Н С=О Н-С-ОН СН2ОН СН2ОН С=О СН2ОН СН3 С=О СН2ОН Н С=О Н-С-Н СН2ОН Есть ли
- 132. Н С=О Н-С-ОН СН2ОН СН2ОН С=О СН2ОН диоксиацетон глицериновый альдегид формулы триоз
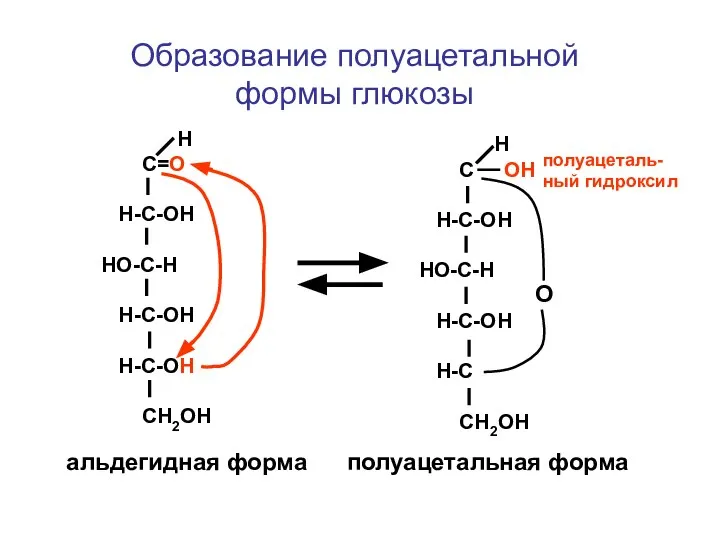
- 133. Н С= О Н- С -ОН НО-С-Н H-C-ОН СН2ОН Н С= О Н-С-ОН Н-С-ОН H-C-ОН СН2ОН
- 134. Н С=О Н-С-ОН HO-С-Н Н-С-ОН H-C-OH СН2ОН СН2ОН С = О НО-С-Н Н-С-ОН Н-С-ОН СН2ОН Н
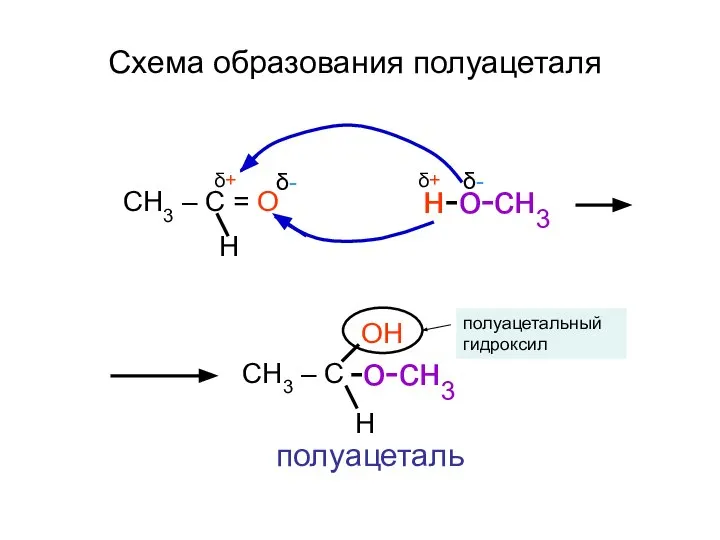
- 135. СН3 – С = О Н н-о-сн3 δ- δ+ δ- δ+ СН3 – С -о-сн3 Н
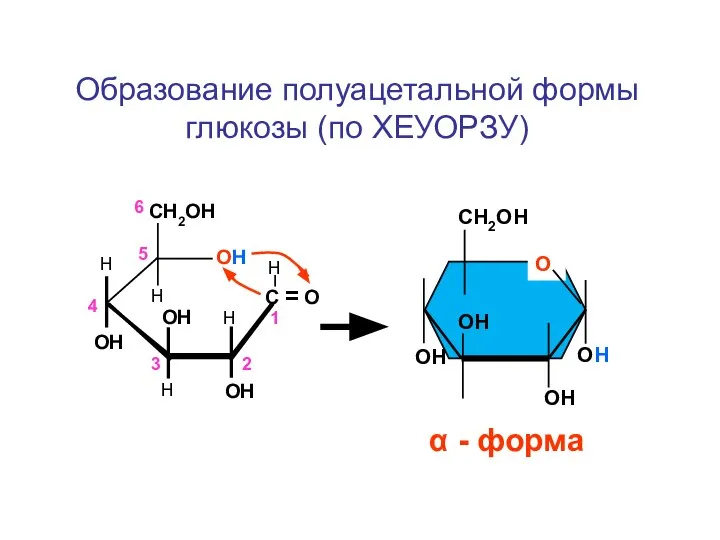
- 136. С = О СН2ОН ОН Н ОН ОН ОН О СН2ОН ОН ОН ОН ОН Н
- 137. Н С=О Н-С-ОН HO-С-Н Н-С-ОН H-C-OH СН2ОН Н С ОН Н-С-ОН HO-С-Н Н-С-ОН H-C СН2ОН О
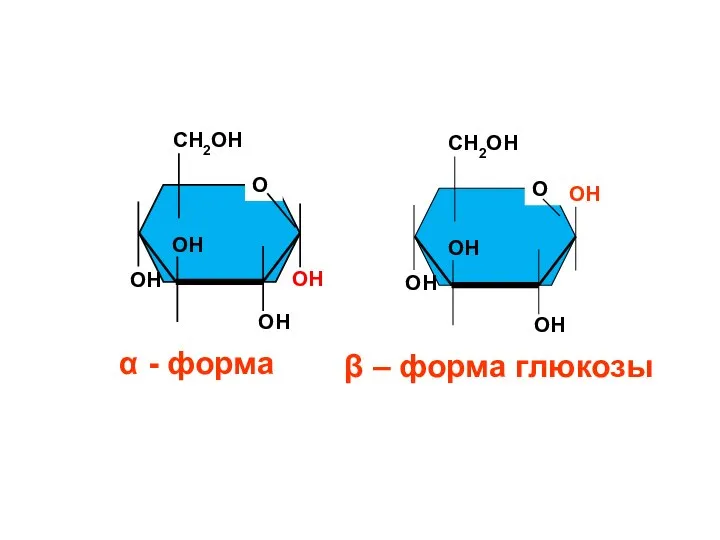
- 138. О СН2ОН ОН ОН ОН ОН β – форма глюкозы О СН2ОН ОН ОН ОН ОН
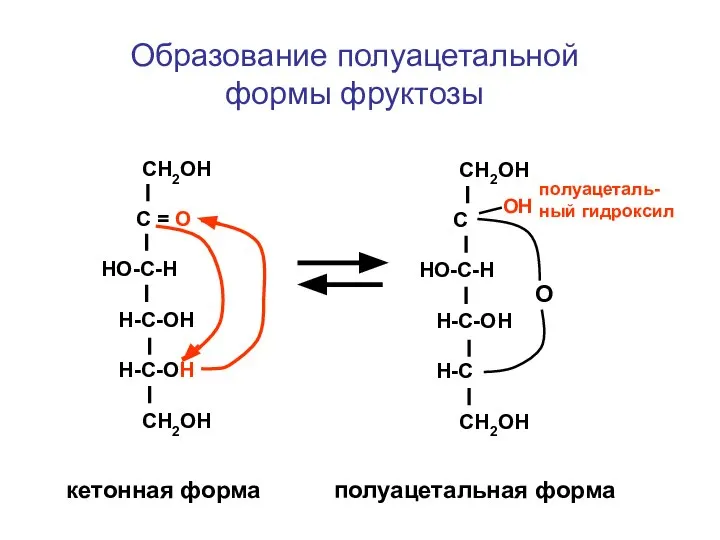
- 139. СН2ОН С = О HO-С-Н Н-С-ОН H-C-OH СН2ОН СН2ОН С HO-С-Н Н-С-ОН H-C СН2ОН О Образование
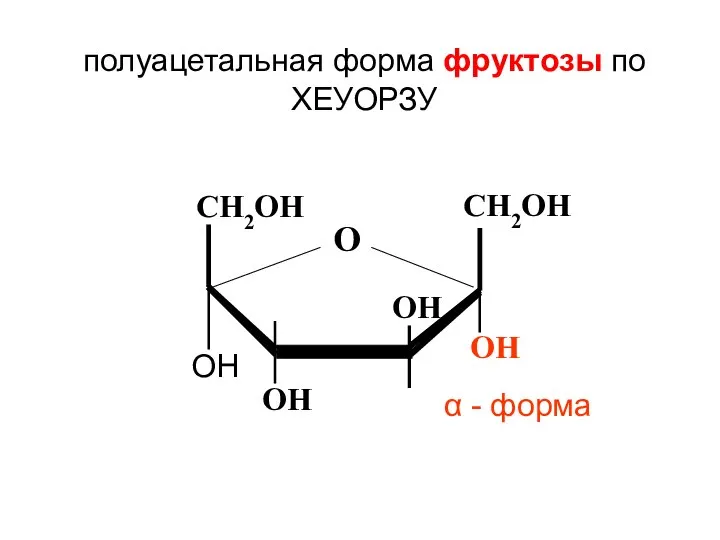
- 140. CH2ОН О CH2ОН ОН ОН ОН ОН полуацетальная форма фруктозы по ХЕУОРЗУ α - форма
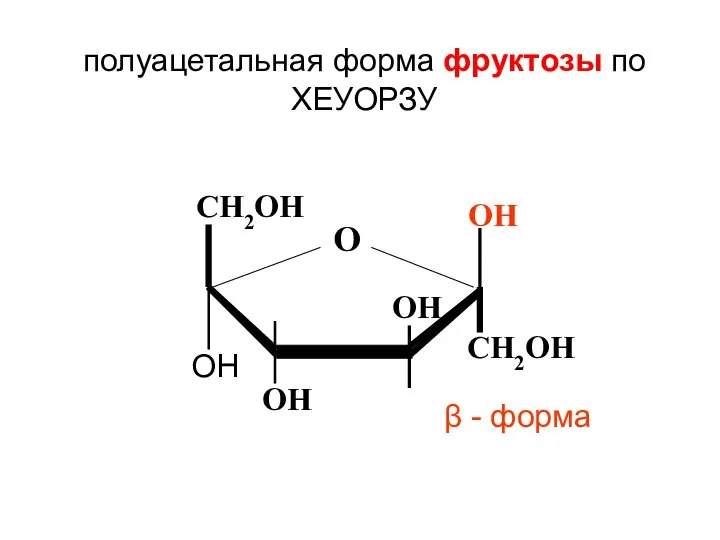
- 141. CH2ОН О CH2ОН ОН ОН ОН ОН полуацетальная форма фруктозы по ХЕУОРЗУ β - форма
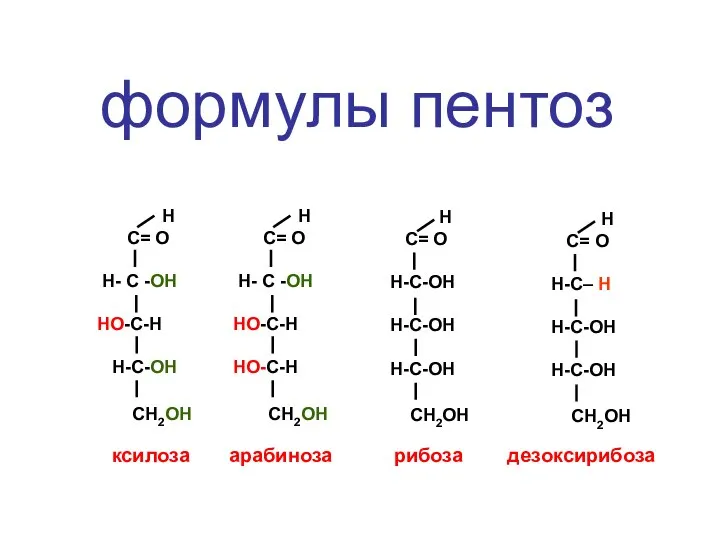
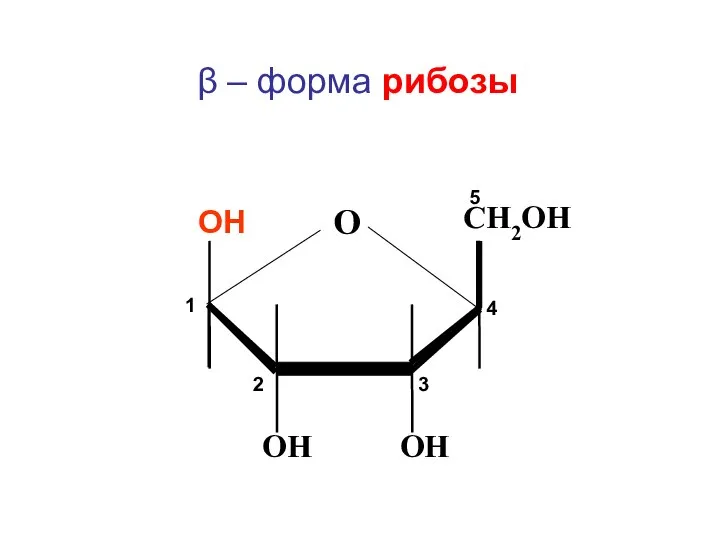
- 142. CH2ОН ОН ОН О ОН β – форма рибозы 1 2 3 4 5
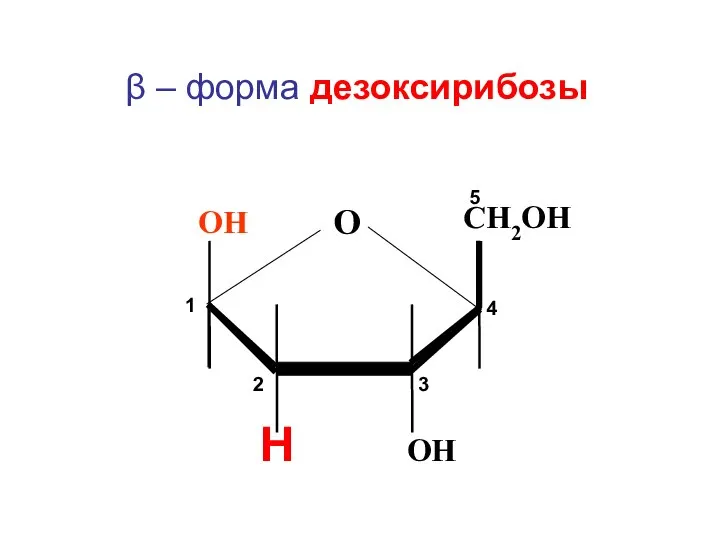
- 143. CH2ОН Н ОН О ОН β – форма дезоксирибозы 1 2 3 4 5
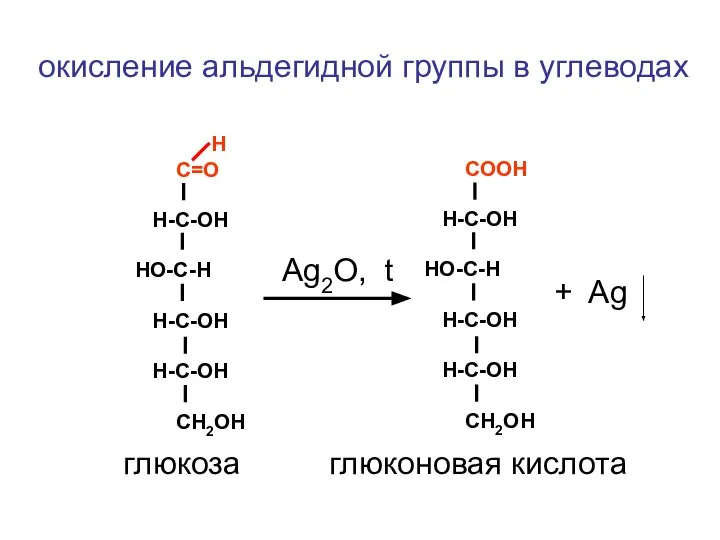
- 144. Н С=О Н-С-ОН HO-С-Н Н-С-ОН H-C-OH СН2ОН СООН Н-С-ОН HO-С-Н Н-С-ОН H-C-OH СН2ОН Аg2O, t +
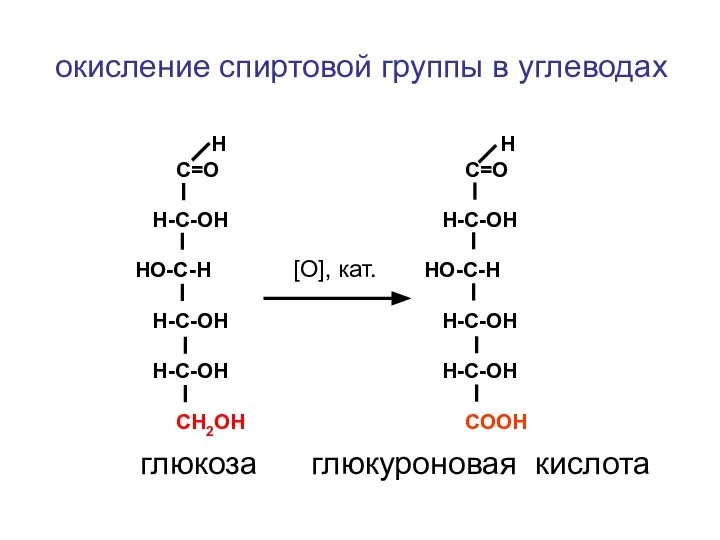
- 145. Н С=О Н-С-ОН HO-С-Н Н-С-ОН H-C-OH СН2ОН глюкоза глюкуроновая кислота окисление спиртовой группы в углеводах Н
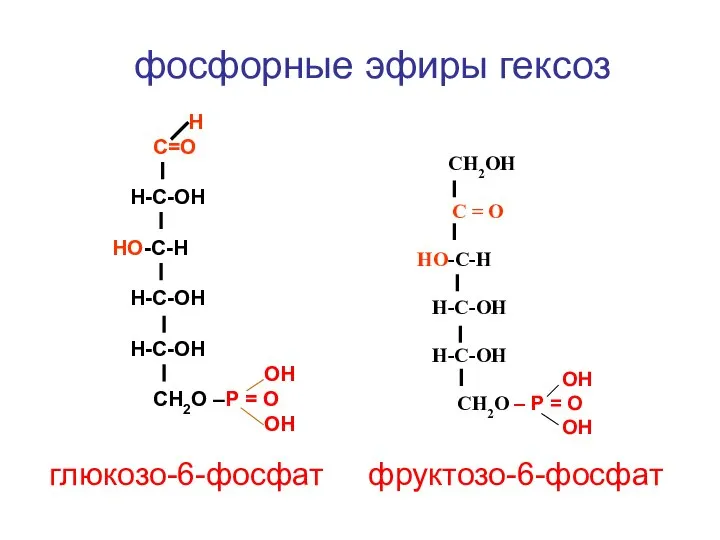
- 146. Н С=О Н-С-ОН HO-С-Н Н-С-ОН H-C-OH ОН СН2О –Р = О ОН СН2ОН С = О
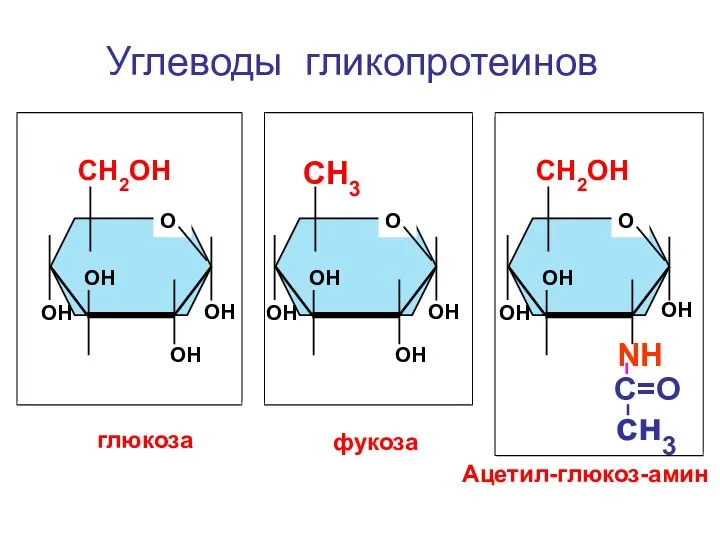
- 147. О СН3 ОН ОН ОН ОН О СН2ОН ОН ОН ОН ОН О СН2ОН ОН ОН
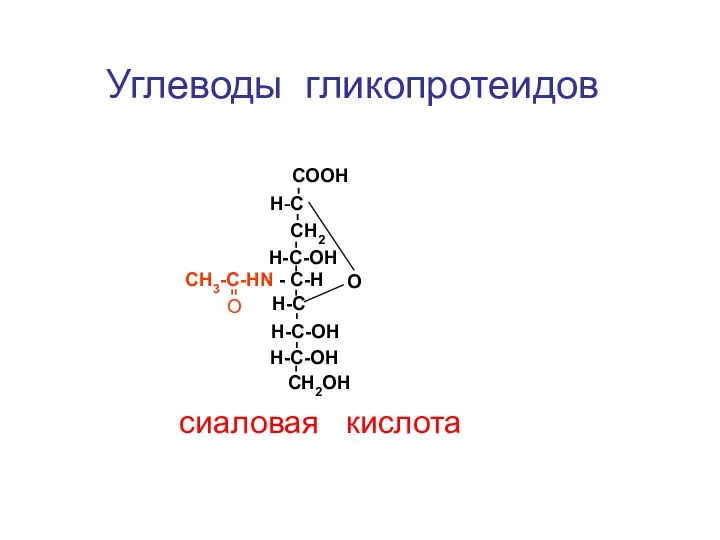
- 148. СООН Н-С СН2 Н-С-ОН СН3-С-НN - С-Н Н-С Н-С-ОН Н-С-ОН СН2ОН О О сиаловая кислота Углеводы
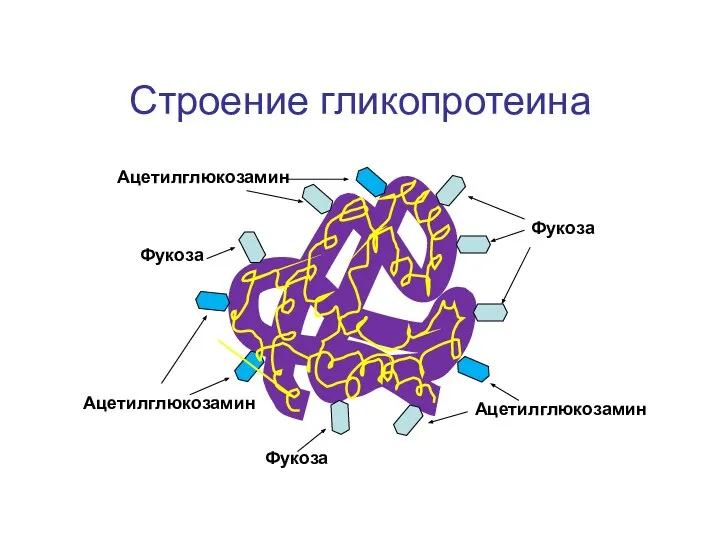
- 149. Строение гликопротеина Фукоза Фукоза Фукоза Ацетилглюкозамин Ацетилглюкозамин Ацетилглюкозамин
- 150. Роль углеводного компонента в гликопротеинах Стабилизирует молекулу белка; Защищает белок от протеолиза (расщепления ферментами);
- 151. Протеогликаны Преобладает углеводный компонент Состоит из белка и гетерополисахарида
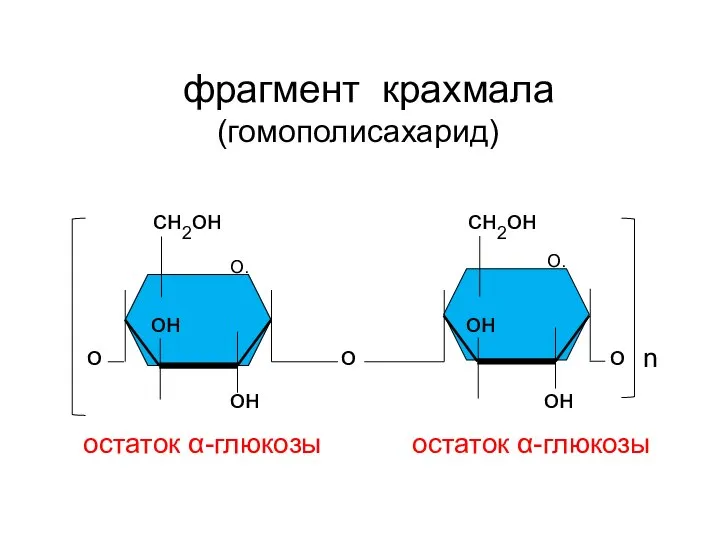
- 152. сн2он сн2он он он о о о он он n фрагмент крахмала (гомополисахарид) остаток α-глюкозы остаток
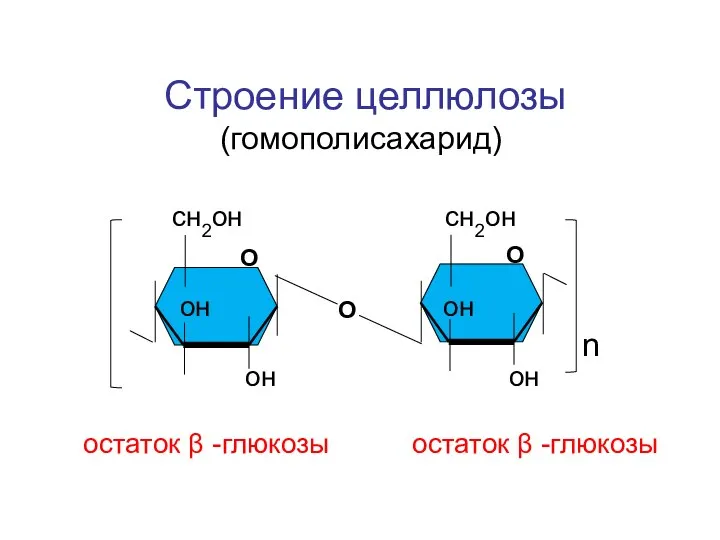
- 153. сн2он сн2он он он он он n Строение целлюлозы (гомополисахарид) О О О остаток β -глюкозы
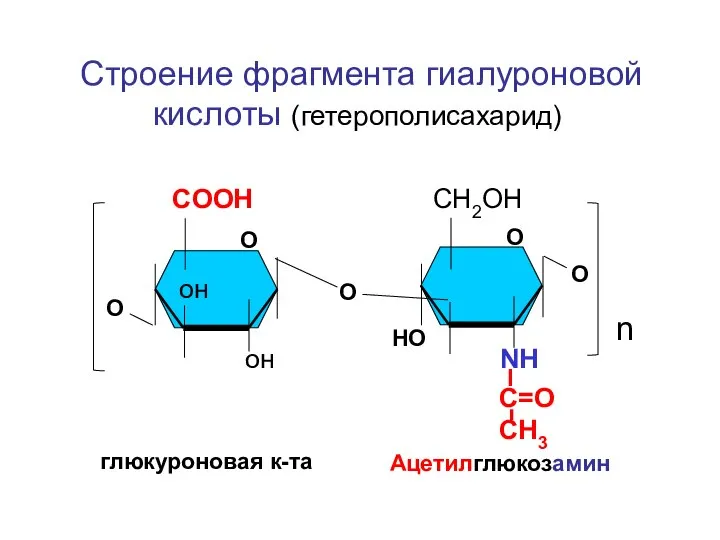
- 154. COOH СН2ОН он он NH n Строение фрагмента гиалуроновой кислоты (гетерополисахарид) О О О C=OCH3 глюкуроновая
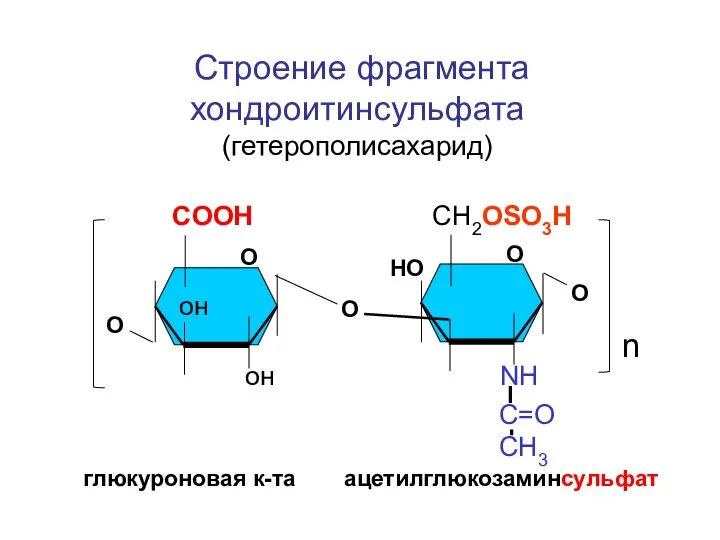
- 155. COOH СН2OSO3H он он NH n Строение фрагмента хондроитинсульфата (гетерополисахарид) О О О C=OCH3 глюкуроновая к-та
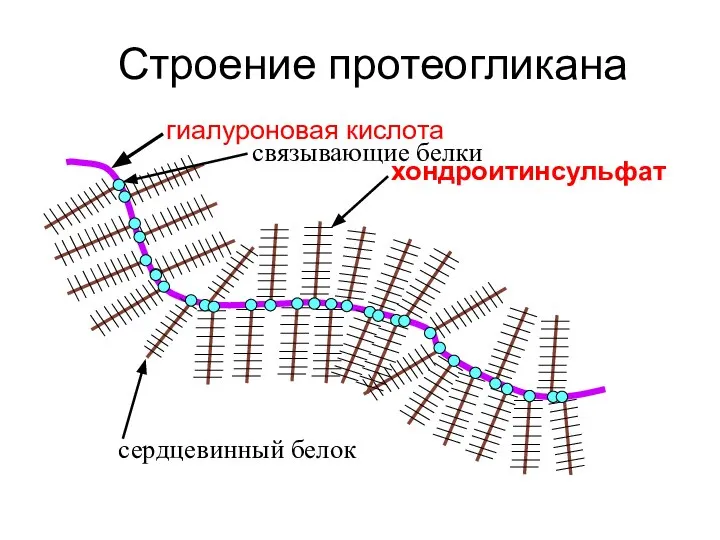
- 156. Строение протеогликана гиалуроновая кислота связывающие белки сердцевинный белок хондроитинсульфат
- 157. Роль протеогликанов в организме человека Повышает прочность оболочек клеток (плазматической мембраны); Проявляет свойство универсального клея. В
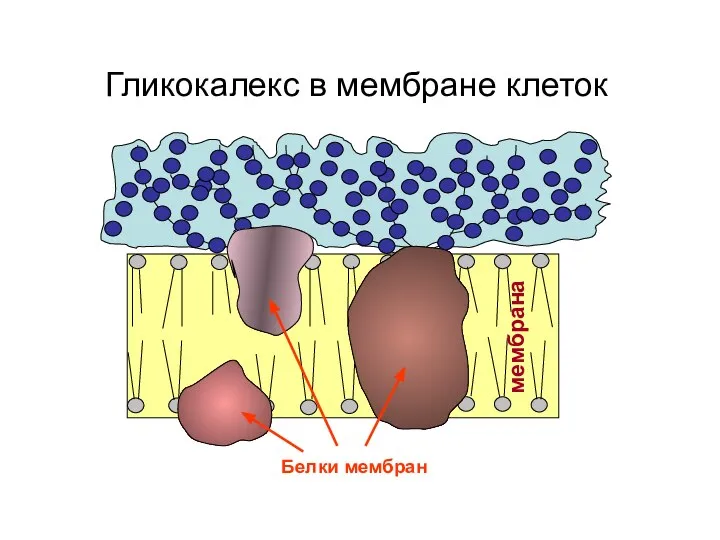
- 158. Гликокалекс в мембране клеток мембрана Белки мембран
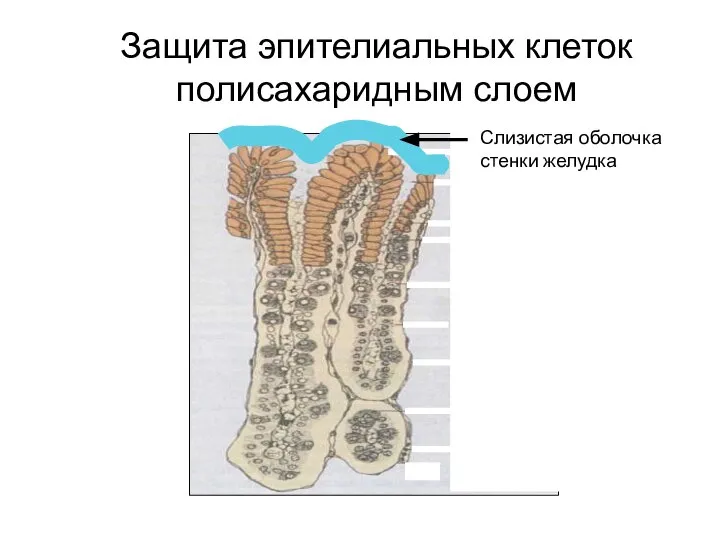
- 159. Защита эпителиальных клеток полисахаридным слоем Слизистая оболочка стенки желудка
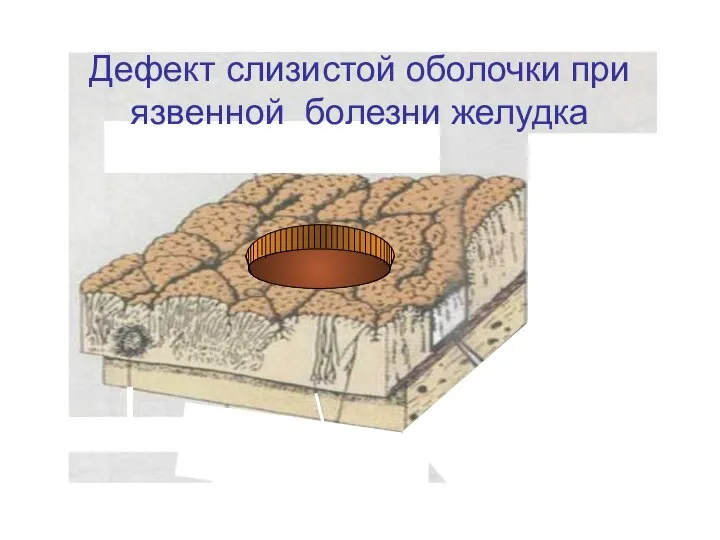
- 160. Дефект слизистой оболочки при язвенной болезни желудка
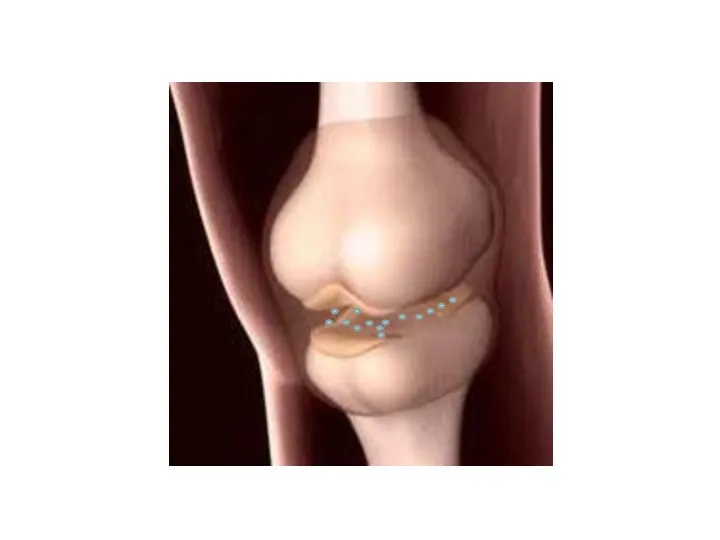
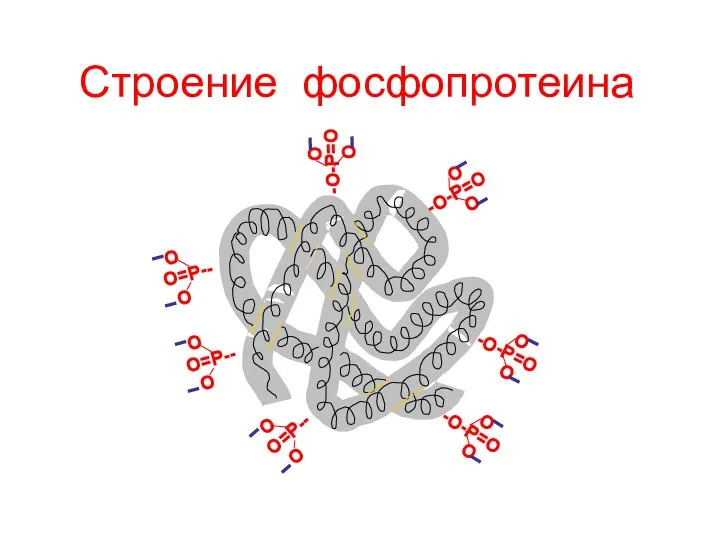
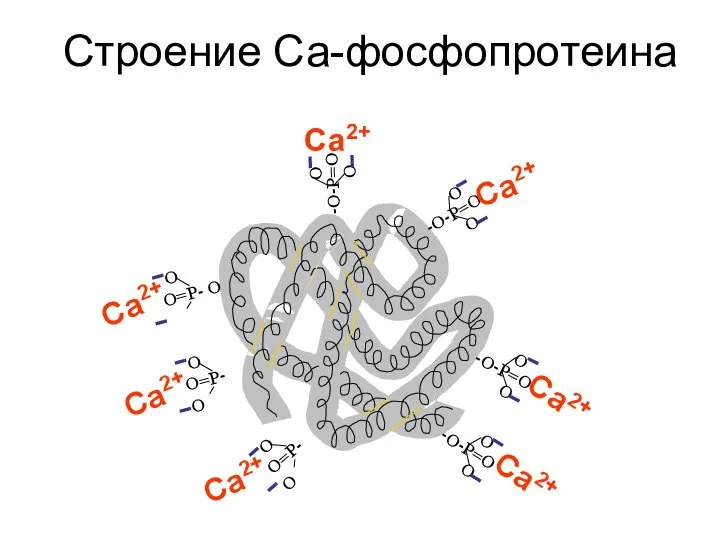
- 162. Фосфопротеины
- 163. -О-Р=О О О -О-Р=О О О -О-Р=О О О -О-Р=О О О О=Р-- О О О=Р--
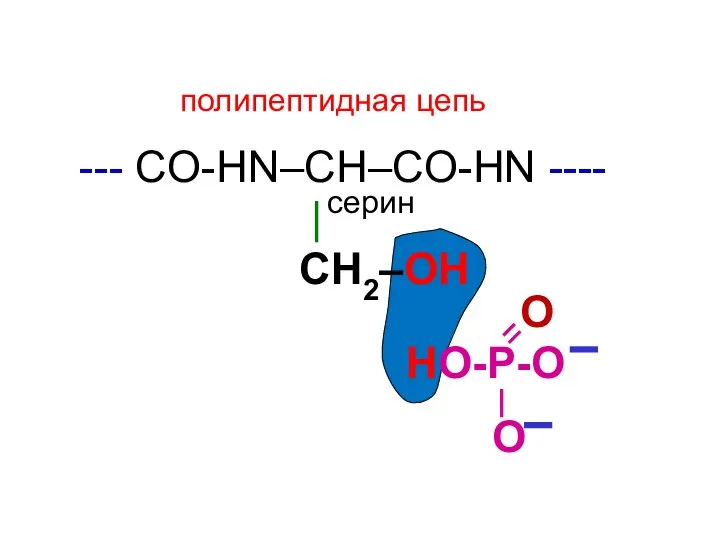
- 164. --- CO-HN–CH–CO-НN ---- | СН2–ОН НО-Р-О О О полипептидная цепь серин
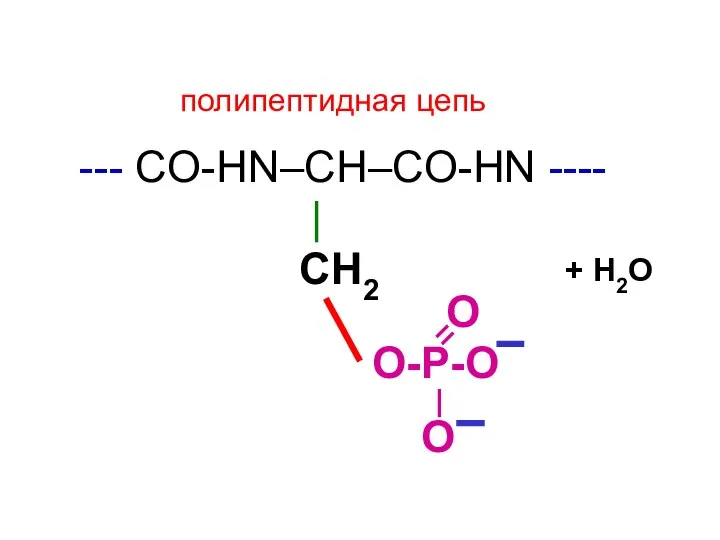
- 165. --- CO-HN–CH–CO-НN ---- | СН2 О-Р-О О О полипептидная цепь + Н2О
- 166. -О-Р=О О О -О-Р=О О О -О-Р=О О О -О-Р=О О О О=Р- О О О=Р-О
- 168. Скачать презентацию












































 Презентация на тему Хромосомные болезни
Презентация на тему Хромосомные болезни  Восковой плющ или хойя. Черенкование
Восковой плющ или хойя. Черенкование Огород на подоконнике (Выращивание фасоли в домашних условиях)
Огород на подоконнике (Выращивание фасоли в домашних условиях) Саморегуляция в экосистеме. Условия устойчивости биогеоценоза
Саморегуляция в экосистеме. Условия устойчивости биогеоценоза Характеристика особенностей размножения кустарниковой и малоазийской полевок в природных и экспериментальных условиях
Характеристика особенностей размножения кустарниковой и малоазийской полевок в природных и экспериментальных условиях Змеи Удмуртской республики
Змеи Удмуртской республики Образование половых клеток и оплодотворение
Образование половых клеток и оплодотворение Трудные вопросы биологии
Трудные вопросы биологии Рыбы. Строение рыб
Рыбы. Строение рыб Единство гидросферы
Единство гидросферы строение_НС
строение_НС Презентация на тему Виды пингвинов
Презентация на тему Виды пингвинов  Бактериофаги и их применение в вирусологии и биотехнологии
Бактериофаги и их применение в вирусологии и биотехнологии Редкие птицы
Редкие птицы Опорно-двигательная система человека
Опорно-двигательная система человека Толстая кишка
Толстая кишка Принципы транскрипции. Структура промотора прокариот
Принципы транскрипции. Структура промотора прокариот Позахромосомна спадковість у людини
Позахромосомна спадковість у людини Производственная структура питомника
Производственная структура питомника Система обоняния человека
Система обоняния человека Презентация на тему Птичьи разговоры
Презентация на тему Птичьи разговоры  50323-46
50323-46 Интерактивный контроль знаний студентов по теме Центральная нервная система и органы чувств
Интерактивный контроль знаний студентов по теме Центральная нервная система и органы чувств День птиц
День птиц Тайны цветов. Загадочный марафон
Тайны цветов. Загадочный марафон Отряд Однопроходные
Отряд Однопроходные Понятия генетики (9 класс)
Понятия генетики (9 класс) Подцарство простейшие
Подцарство простейшие