Содержание
- 2. SARS-CoV-2 является седьмым по счету известным коронавирусом, обнаруживаемым у людей. Среди описанных коронавирусов SARS-CoV, MERSCoV и
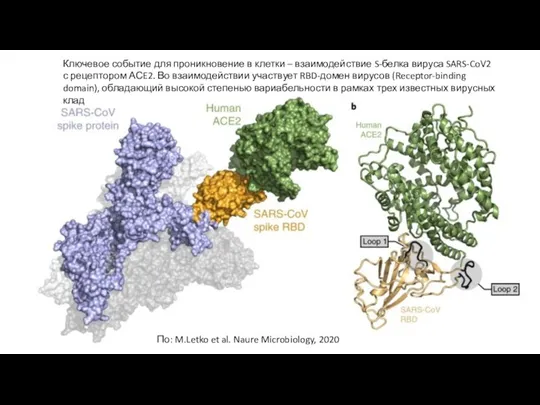
- 3. Ключевое событие для проникновение в клетки – взаимодействие S-белка вируса SARS-CoV2 с рецептором АСE2. Во взаимодействии
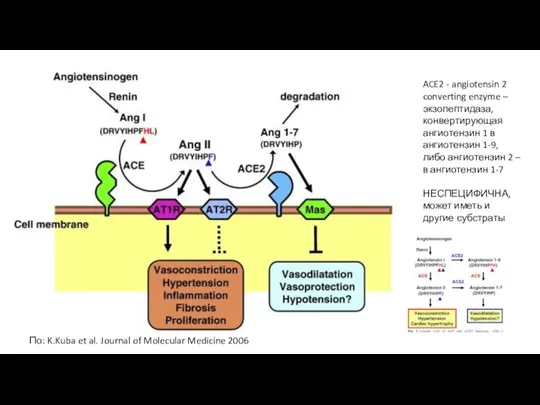
- 4. ACE2 - angiotensin 2 converting enzyme – экзопептидаза, конвертирующая ангиотензин 1 в ангиотензин 1-9, либо ангиотензин
- 5. (а) АСЕ2 и ACE являются ключевыми регуляторами ренин-ангиотензиновой системы, которая контролирует функции ССС, поддерживая кровяное давление
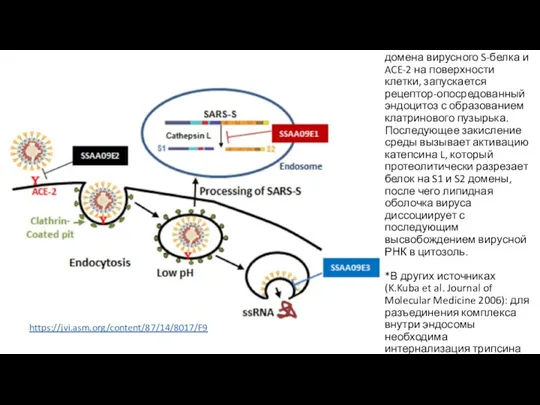
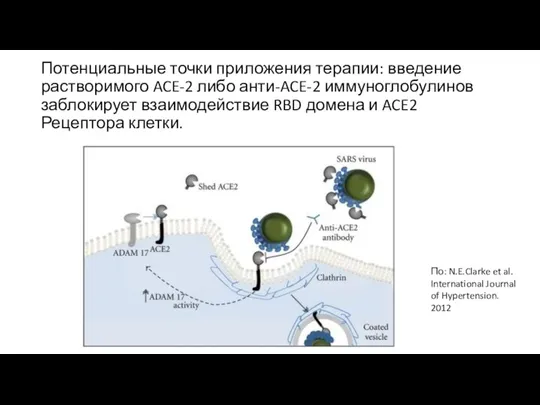
- 6. После взаимодействия RBD-домена вирусного S-белка и ACE-2 на поверхности клетки, запускается рецептор-опосредованный эндоцитоз с образованием клатринового
- 7. Особенности генома вируса SARS-CoV-2 На основании геномных исследований были выделены следующие особенности генома вируса SARS-CoV-2: 1
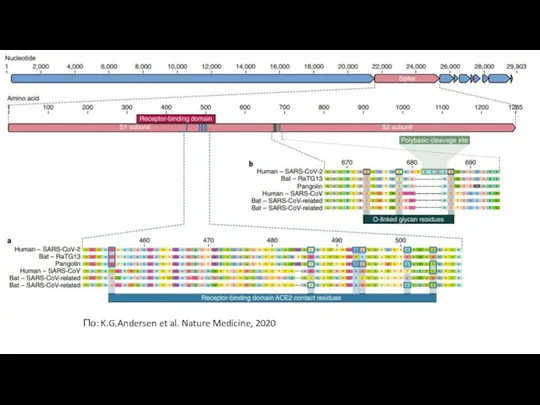
- 8. По: K.G.Andersen et al. Nature Medicine, 2020
- 9. RBD домен вируса SARS-CoV2 6 аминокислот RBD домена обуславливают взаимодействие с рецептором ACE2. У вируса- «предшественника»
- 10. Сайт разрезания S-белка Последовательность (RRAR) является сайтом распознавания для неспецифических протеаз (фурин, катепсин), благодаря чему S-
- 11. Возможные варианты происхождения вируса SARS-CoV-2 1) Мутагенез и селекция внутри животных-хозяев с последующим зоонозным переносом 2)
- 12. Вариант 1. Мутагенез и селекция внутри животных-хозяев с последующим зоонозным переносом Большинство первых выявленных случаев были
- 13. Вариант 1. Мутагенез и селекция внутри животных-хозяев с последующим зоонозным переносом Вероятный резервуар – летучие мыши
- 14. У панголинов домен RBD вируса идентичен такому же домену в вируче человека ? могла произойти передача
- 15. Вариант 3. Мутагенез с последующей селекцией в ходе работы с клеточными культурами в рамках лабораторных исследований
- 16. Потенциальные точки приложения терапии: введение растворимого ACE-2 либо анти-ACE-2 иммуноглобулинов заблокирует взаимодействие RBD домена и ACE2
- 18. Скачать презентацию










 Ткани. Эпителиальные, соединительные, мышечные, нервная ткани. Строение и функция нейрона. Синапс. Образование тканей
Ткани. Эпителиальные, соединительные, мышечные, нервная ткани. Строение и функция нейрона. Синапс. Образование тканей Кости лицевого черепа
Кости лицевого черепа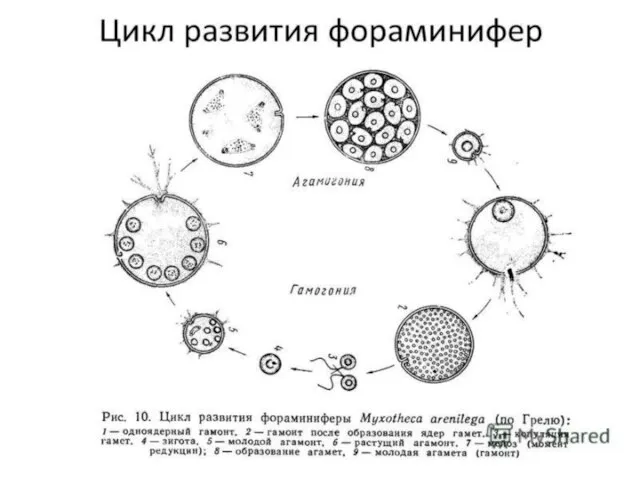 Цикл развития фораминифер
Цикл развития фораминифер Цветок. Строение и значение цветка. 6 класс. Часть 2
Цветок. Строение и значение цветка. 6 класс. Часть 2 Класс ракообразные
Класс ракообразные Эволюция и нанотехноогии
Эволюция и нанотехноогии Презентация на тему Этапы эволюции человека
Презентация на тему Этапы эволюции человека  Породы собак (фотографии)
Породы собак (фотографии) Вегетативная нервная система
Вегетативная нервная система Питомник немецкого охотничьего терьера
Питомник немецкого охотничьего терьера Фотосинтез
Фотосинтез Животные родного края
Животные родного края Обобщение и систематизация знаний по теме Организм и среда. Вид и популяция. Экосистемы
Обобщение и систематизация знаний по теме Организм и среда. Вид и популяция. Экосистемы Анатомо-физиологические механизмы безопасности и защиты человека от негативных факторов
Анатомо-физиологические механизмы безопасности и защиты человека от негативных факторов Строение клетки - основные органоиды
Строение клетки - основные органоиды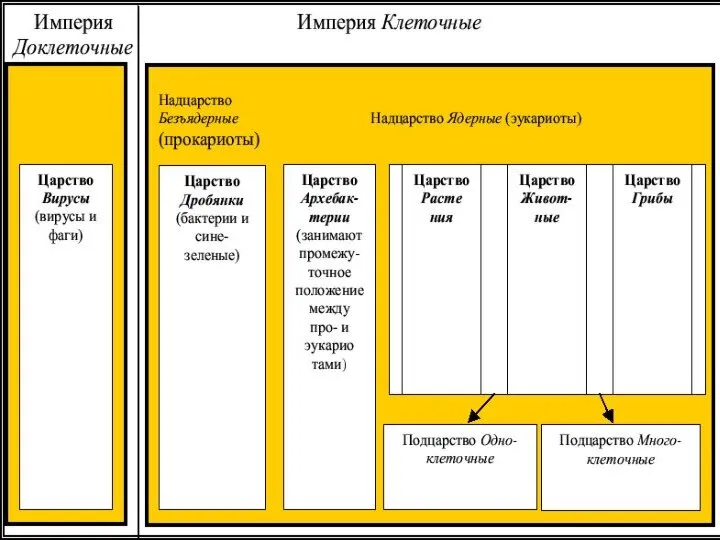 Надцарство Прокариоты
Надцарство Прокариоты Стебли растений
Стебли растений Презентация на тему КАК РАБОТАЕТ ОРГАНИЗМ ЧЕЛОВЕКА
Презентация на тему КАК РАБОТАЕТ ОРГАНИЗМ ЧЕЛОВЕКА  Underwater
Underwater Автоволновые процессы в активновозбудимых средах
Автоволновые процессы в активновозбудимых средах Интересные домашние животные в нашем мире
Интересные домашние животные в нашем мире Какие растения нас одевают?
Какие растения нас одевают? Нуклеиновые кислоты АТФ. 10 класс
Нуклеиновые кислоты АТФ. 10 класс Гипотезы происхождения человека
Гипотезы происхождения человека Организация сообществ у голых землекопов
Организация сообществ у голых землекопов Размножение
Размножение Животные известные, очень интересные!
Животные известные, очень интересные! Биологические особенности лошадей
Биологические особенности лошадей