Содержание
- 2. Различные симптомы шизофрении связаны со специфичными областями мозга - аномально функционирующими нейронными контурами. Нейронный контур -
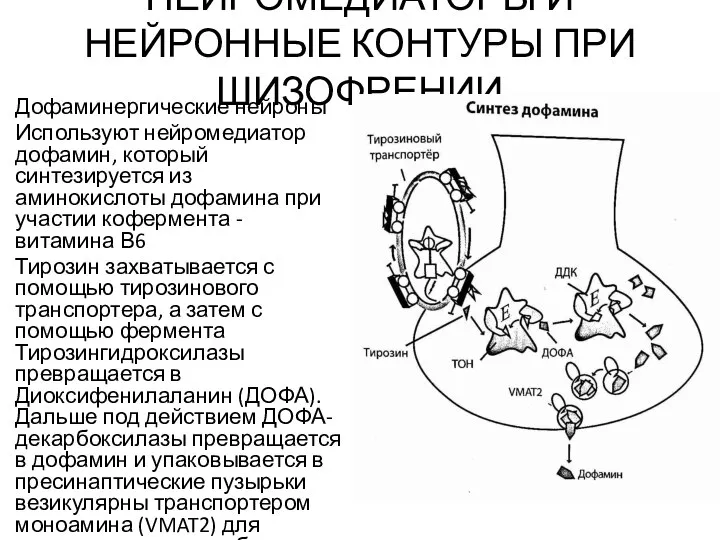
- 3. НЕЙРОМЕДИАТОРЫ И НЕЙРОННЫЕ КОНТУРЫ ПРИ ШИЗОФРЕНИИ Дофаминергические нейроны Используют нейромедиатор дофамин, который синтезируется из аминокислоты дофамина
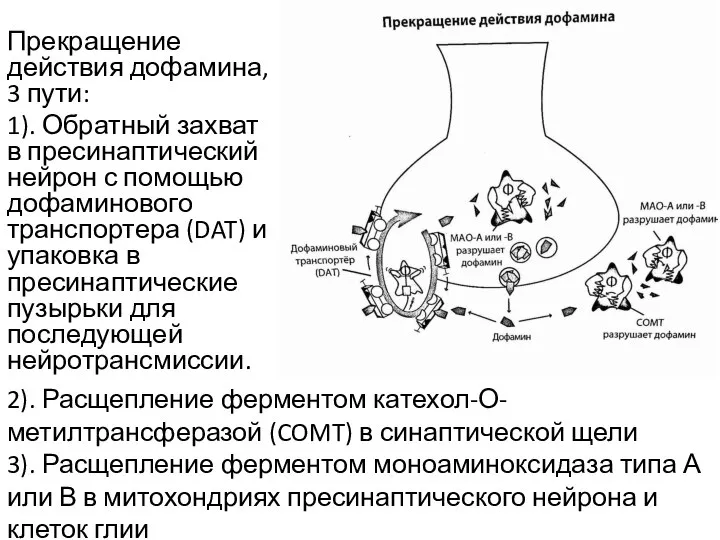
- 4. Прекращение действия дофамина, 3 пути: 1). Обратный захват в пресинаптический нейрон с помощью дофаминового транспортера (DAT)
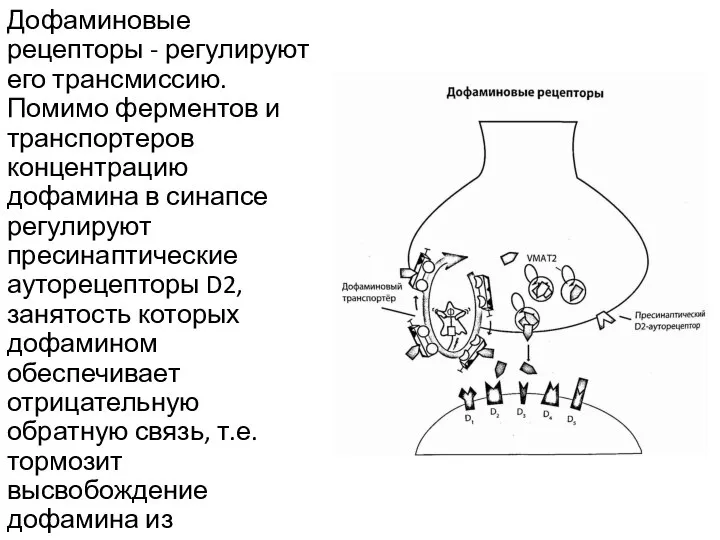
- 5. Дофаминовые рецепторы - регулируют его трансмиссию. Помимо ферментов и транспортеров концентрацию дофамина в синапсе регулируют пресинаптические
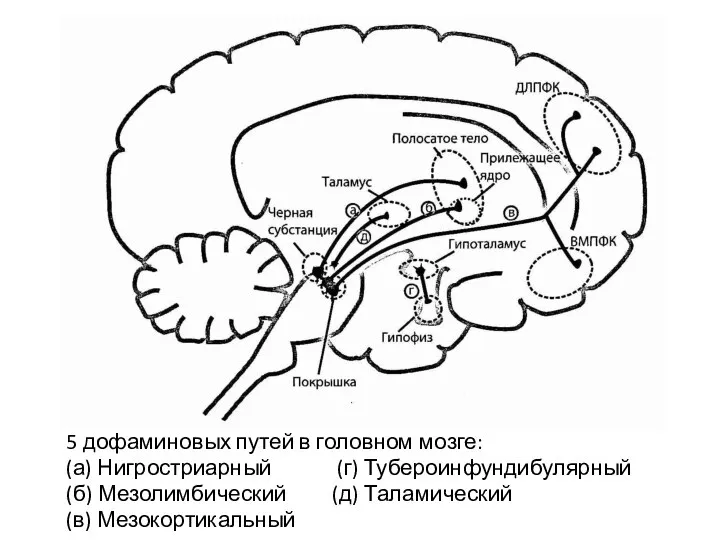
- 6. 5 дофаминовых путей в головном мозге: (а) Нигростриарный (г) Тубероинфундибулярный (б) Мезолимбический (д) Таламический (в) Мезокортикальный
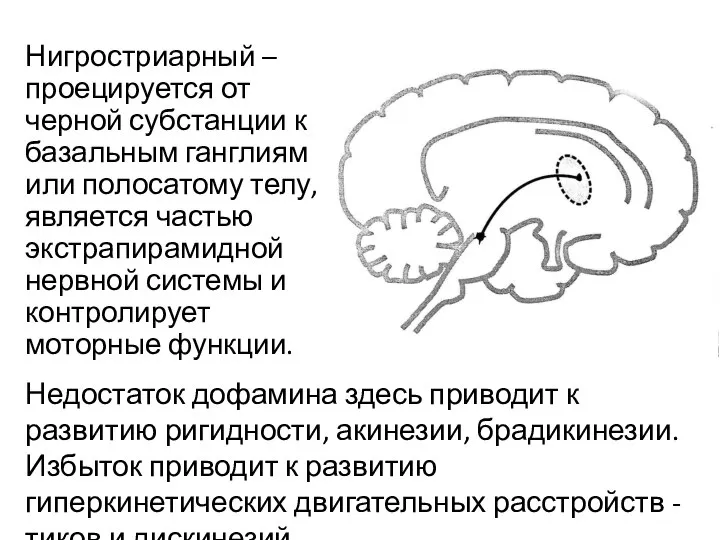
- 7. Нигростриарный – проецируется от черной субстанции к базальным ганглиям или полосатому телу, является частью экстрапирамидной нервной
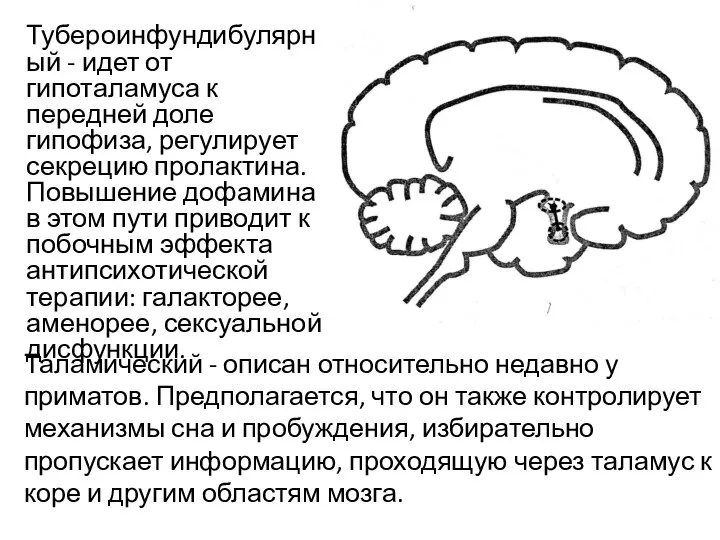
- 8. Тубероинфундибулярный - идет от гипоталамуса к передней доле гипофиза, регулирует секрецию пролактина. Повышение дофамина в этом
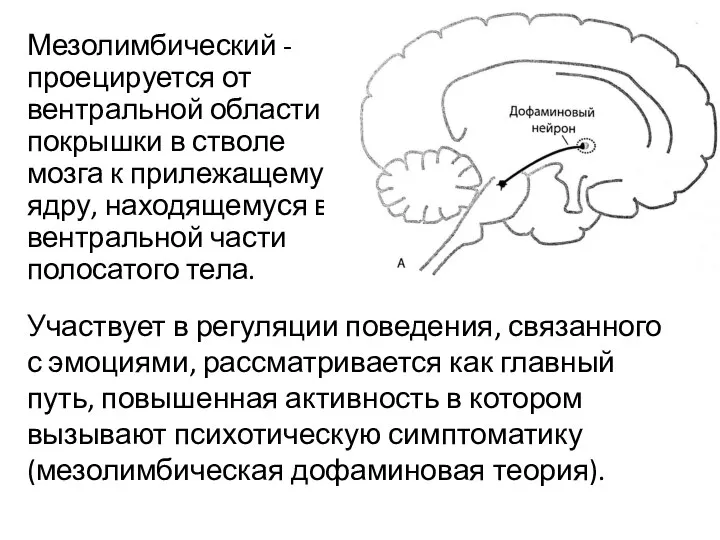
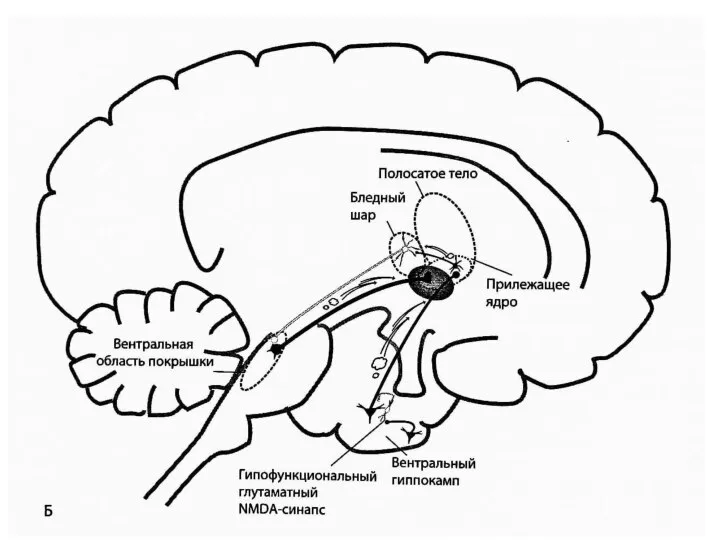
- 9. Мезолимбический - проецируется от вентральной области покрышки в стволе мозга к прилежащему ядру, находящемуся в вентральной
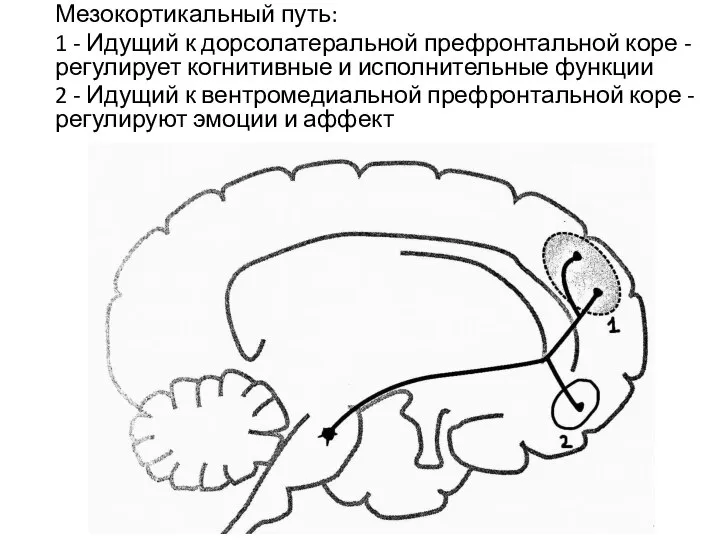
- 10. Мезокортикальный путь: 1 - Идущий к дорсолатеральной префронтальной коре - регулирует когнитивные и исполнительные функции 2
- 11. Негативные симптомы при шизофрении и состояние поведенческого дефицита обуславливаются недостаточной активностью или ненадлежащим функционированием мезокортикальных дофаминовых
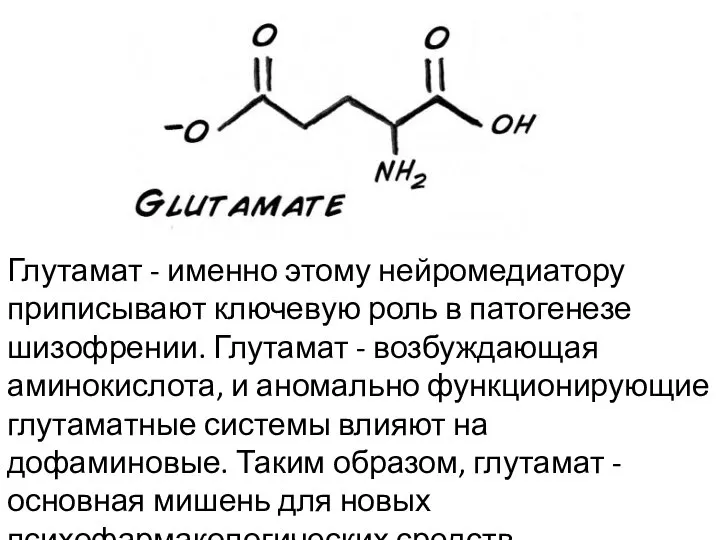
- 12. Глутамат - именно этому нейромедиатору приписывают ключевую роль в патогенезе шизофрении. Глутамат - возбуждающая аминокислота, и
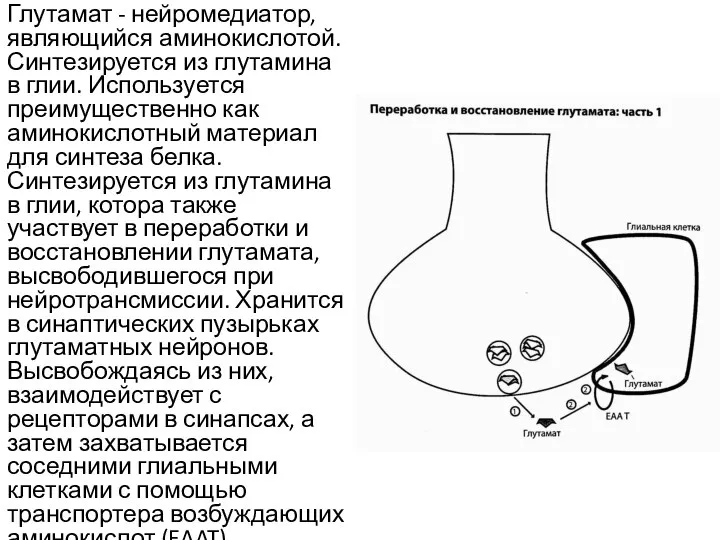
- 13. Глутамат - нейромедиатор, являющийся аминокислотой. Синтезируется из глутамина в глии. Используется преимущественно как аминокислотный материал для
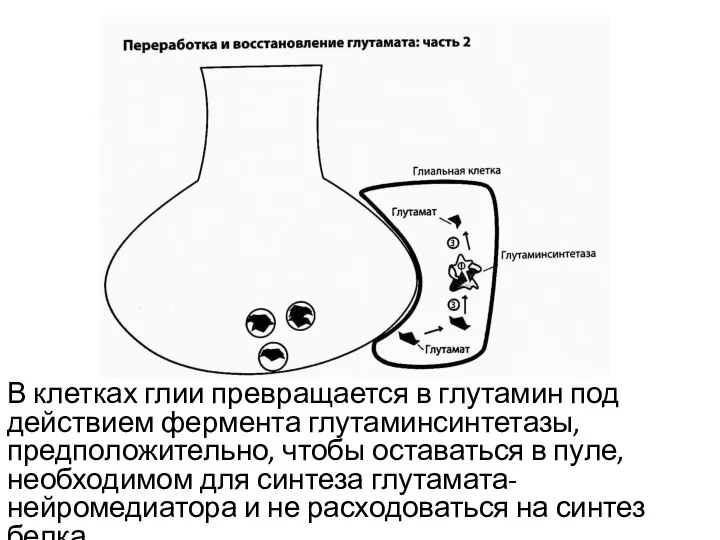
- 14. В клетках глии превращается в глутамин под действием фермента глутаминсинтетазы, предположительно, чтобы оставаться в пуле, необходимом
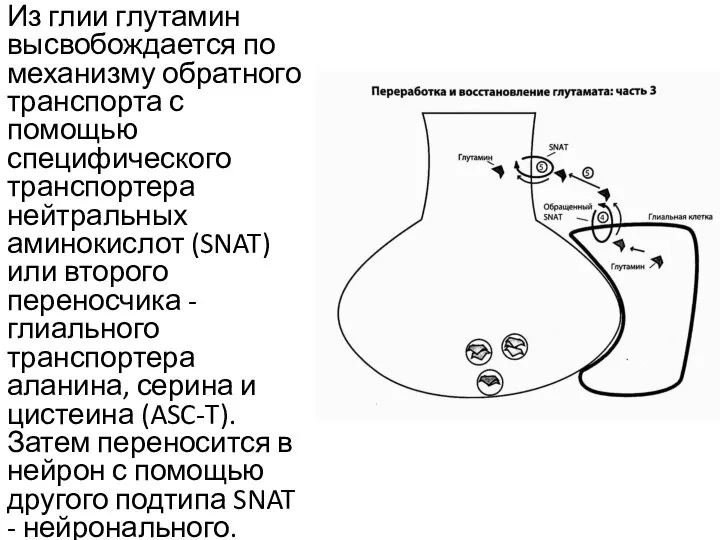
- 15. Из глии глутамин высвобождается по механизму обратного транспорта с помощью специфического транспортера нейтральных аминокислот (SNAT) или
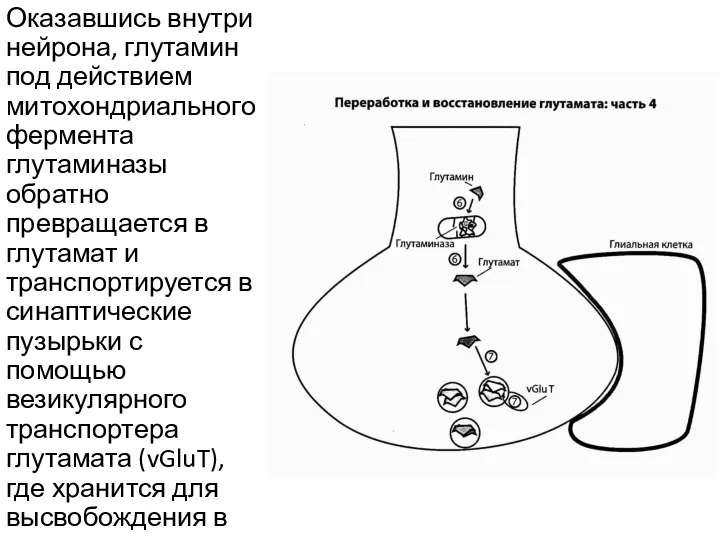
- 16. Оказавшись внутри нейрона, глутамин под действием митохондриального фермента глутаминазы обратно превращается в глутамат и транспортируется в
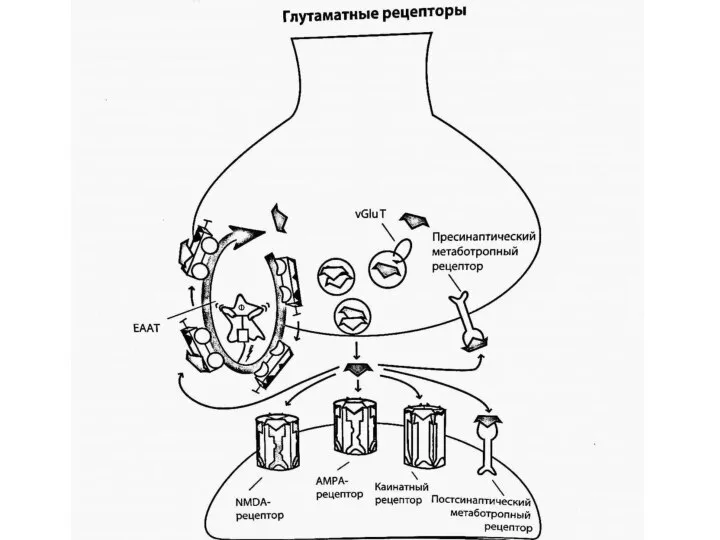
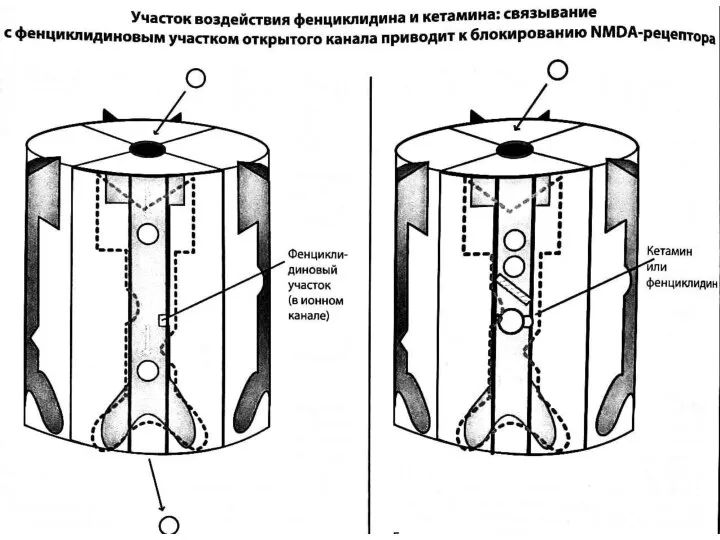
- 18. В глутаматергической нейротрансмиссии задействованы 4 подтипа глутаматных рецепторов, названия которых происходят от связывающихся с ними агонистов:
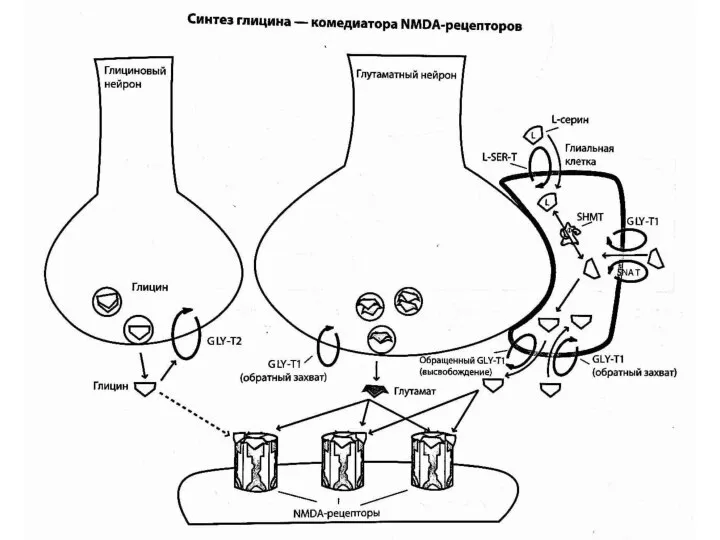
- 20. Глицин - комедиатор NMDA-рецепторов Действие глутамата на NMDA-рецепторы частично зависит от наличия комедиаторов - глицина или
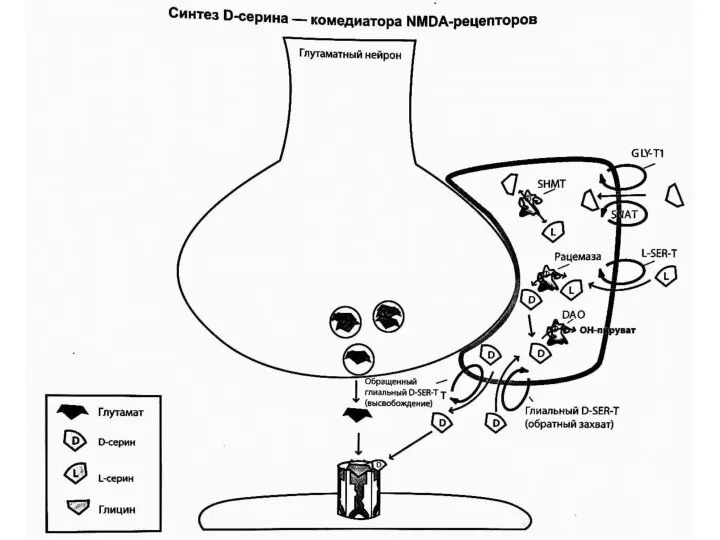
- 22. D-серин - комедиатор NMDA-рецепторов. L-серин попадает в глиальные клетки с помощью транспортера L-серина, и фермент серин-рацемаза
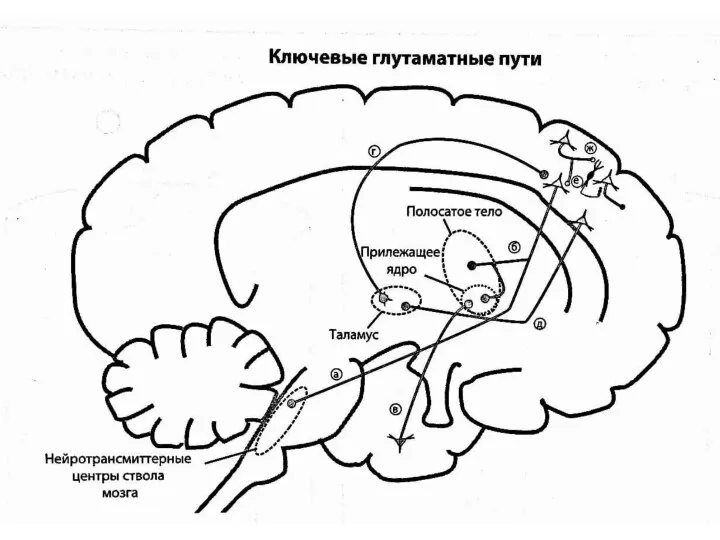
- 24. Хотя глутамат как возбуждающий нейромедиатор может оказывать воздействие практически на все нейроны в головном мозге, существуют
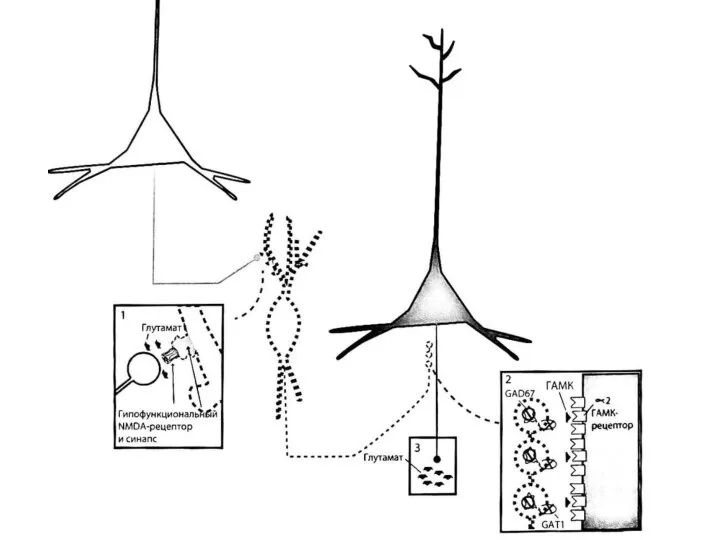
- 26. Гипотеза о гипофункции NMDA-рецепторов при шизофрении - основная современная нейрохимическая гипотеза шизофрении, согласно которой глутаматная активность
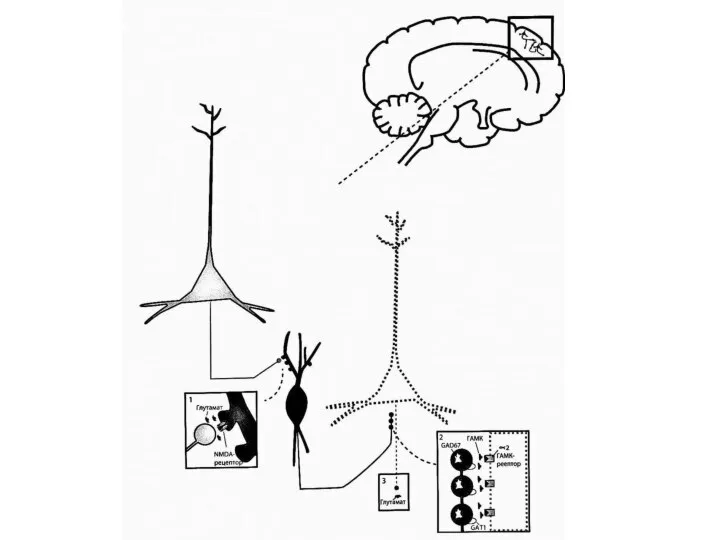
- 28. Гипотетический участок глутаматной дисфункции при шизофрении - на некоторых вставочных ГАМКергических нейронах коры. По всей видимости,
- 30. В парвальбумин-содержащих вставочных ГАМКергических нейронах префронтальной коры головного мозга пациентов с шизофренией имеются и другие дефекты,
- 32. Кортико-стволовые глутаматные пути регулируют выход глутамата из коры в нейротрансмиттерный центр ствола мозга (вентральную область покрышки),
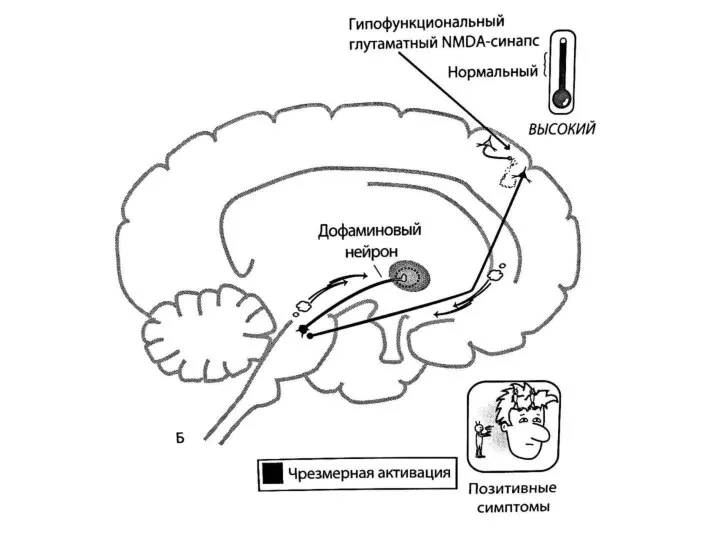
- 34. Гипофункция NMDA-рецепторов глутаматергических синапсов в вентральном гиппокампе тоже может приводить к мезолимбической дофаминовой гиперактивности. В норме
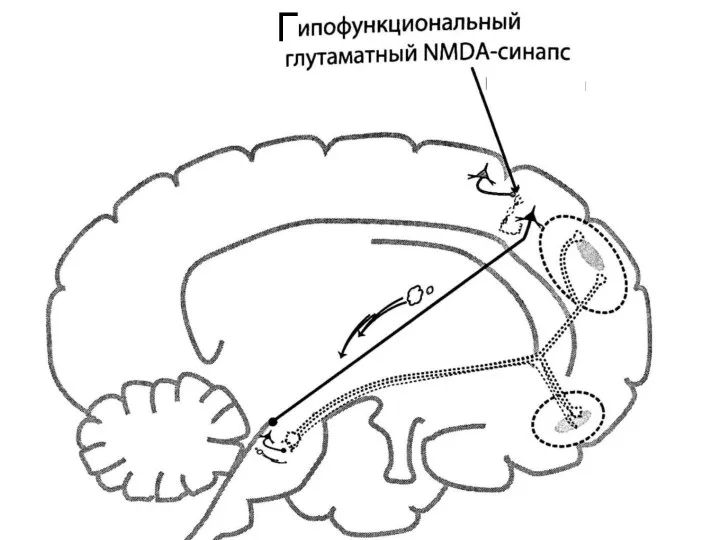
- 35. Г
- 36. Связь гипотезы о гипофункции NMDA-рецепторов при шизофрении с дофаминовой гипотизой: негативные симптомы Корково-стволовой глутаматный путь посредством
- 38. Скачать презентацию












 Интересные факты о черепахах
Интересные факты о черепахах Строение инфузории и амебы
Строение инфузории и амебы dnk_i_rnk_-_nukleinovye_kisloty
dnk_i_rnk_-_nukleinovye_kisloty Ordering flowers
Ordering flowers Летний лес - полный чудес
Летний лес - полный чудес Терморегуляция. Закаливание. Выделение пота
Терморегуляция. Закаливание. Выделение пота Сибирский багульник
Сибирский багульник Птицы удмуртского края
Птицы удмуртского края Мейоз. Гаметогенез
Мейоз. Гаметогенез Ткани животных и человека
Ткани животных и человека морфология анатомия листа
морфология анатомия листа Понятие изменчивости
Понятие изменчивости Прародина человека
Прародина человека Как зимуют звери в лесу
Как зимуют звери в лесу Плесневые грибы и дрожжи
Плесневые грибы и дрожжи Анаболизм. Автотрофное питание. Фотосинтез. II стадия фотосинтеза - темновая
Анаболизм. Автотрофное питание. Фотосинтез. II стадия фотосинтеза - темновая Памятники природы
Памятники природы Sprache und Gehirn. Anatomische Grundlagen
Sprache und Gehirn. Anatomische Grundlagen 11. Биосинтез углеводов — фотосинтез
11. Биосинтез углеводов — фотосинтез Жизнь в пресных водах
Жизнь в пресных водах Сортоиспытание огурца в открытом грунте на Сергачском государственном сортоиспытательном участке
Сортоиспытание огурца в открытом грунте на Сергачском государственном сортоиспытательном участке Клеточное строение листа
Клеточное строение листа Особенности строения черепа разных групп млекопитающих
Особенности строения черепа разных групп млекопитающих Плейотропия.. Взаимодействие генов
Плейотропия.. Взаимодействие генов Теория эволюции. Первые организмы на Земле и их эволюция
Теория эволюции. Первые организмы на Земле и их эволюция Përçuarja e ujit nëpër bimë
Përçuarja e ujit nëpër bimë Презентация на тему Хвойные леса умеренного пояса и их обитатели
Презентация на тему Хвойные леса умеренного пояса и их обитатели  Радость и печаль Жердевской осени
Радость и печаль Жердевской осени