Содержание
- 2. План лекции Уровни структурной организации белковой молекулы Физико – химические свойства белков и белковых растворов Практическое
- 3. УРОВНИ СТРУКТУРНОЙ ОРГАНИЗАЦИИ БЕЛКОВОЙ МОЛЕКУЛЫ
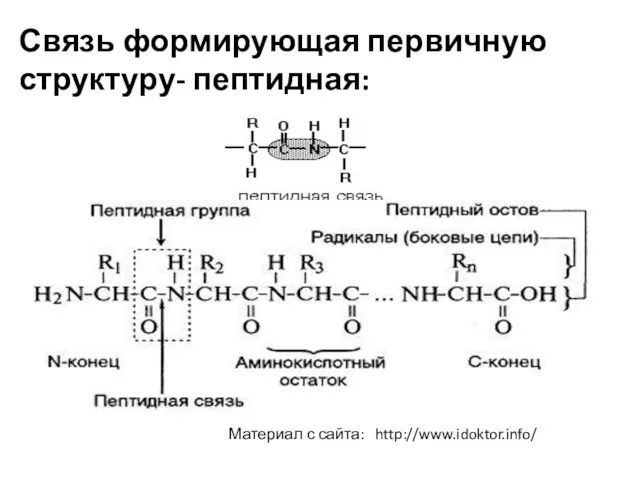
- 4. Первичная структура белка - представляет собой линейную последовательность аминокислотных остатков (свыше 50), связанных пептидными связями в
- 5. Связь формирующая первичную структуру- пептидная: Материал с сайта: http://www.idoktor.info/
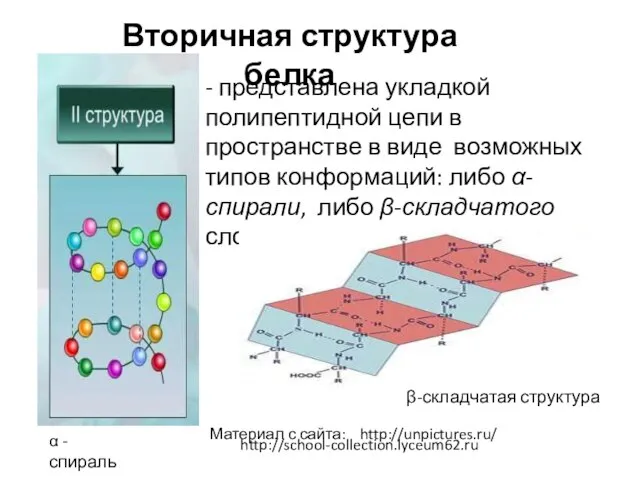
- 6. - представлена укладкой полипептидной цепи в пространстве в виде возможных типов конформаций: либо α-спирали, либо β-складчатого
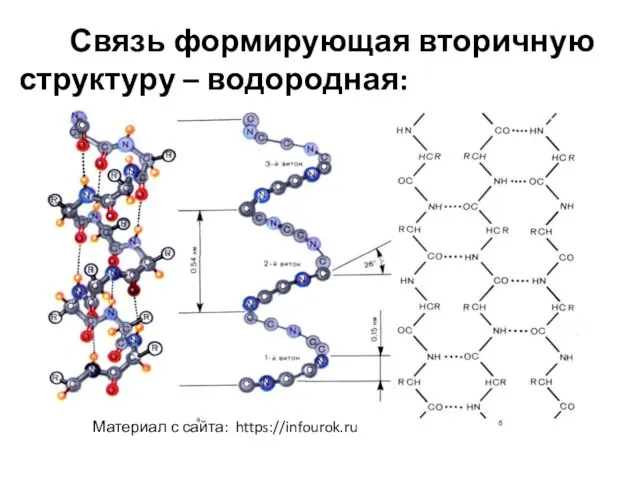
- 7. Связь формирующая вторичную структуру – водородная: Материал с сайта: https://infourok.ru
- 8. называют трехмерную пространственную структуру, образующуюся за счет взаимодействий между радикалами аминокислот полипептидной цепи, расположенных на значительном
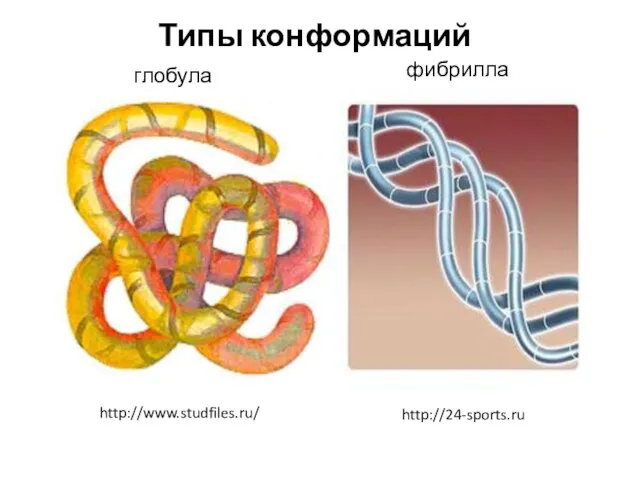
- 9. глобула фибрилла http://www.studfiles.ru/ http://24-sports.ru Типы конформаций
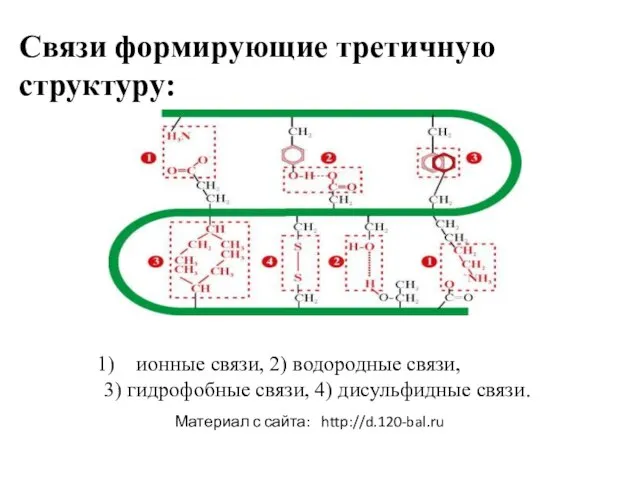
- 10. Связи формирующие третичную структуру: ионные связи, 2) водородные связи, 3) гидрофобные связи, 4) дисульфидные связи. Материал
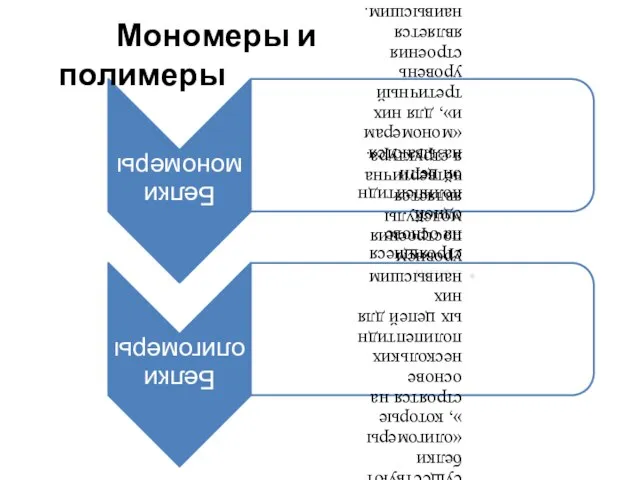
- 11. Мономеры и полимеры
- 12. – это способ укладки в пространстве отдельных полипептидных цепей, обладающих одинаковой третичной структурой (глобулярной или фибриллярной),
- 13. Физико – химическим свойствам белков
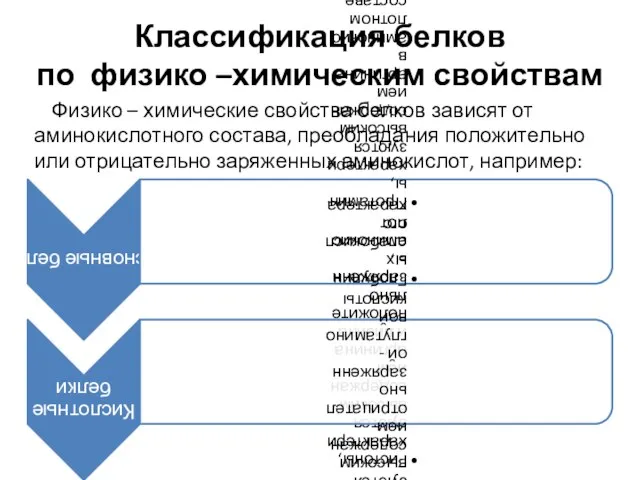
- 14. Классификация белков по физико –химическим свойствам Физико – химические свойства белков зависят от аминокислотного состава, преобладания
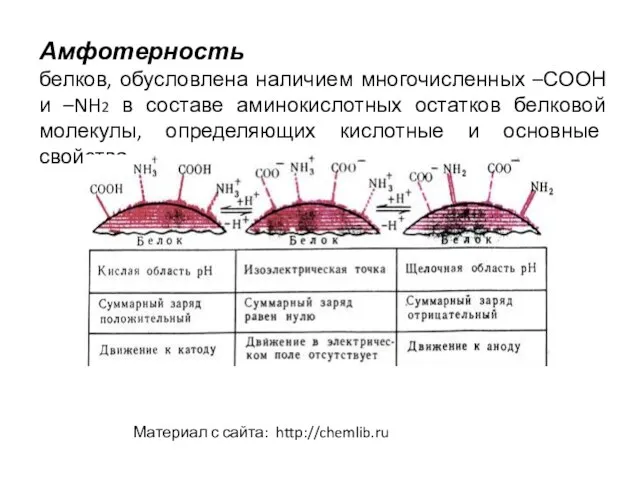
- 15. Амфотерность белков, обусловлена наличием многочисленных –СООН и –NH2 в составе аминокислотных остатков белковой молекулы, определяющих кислотные
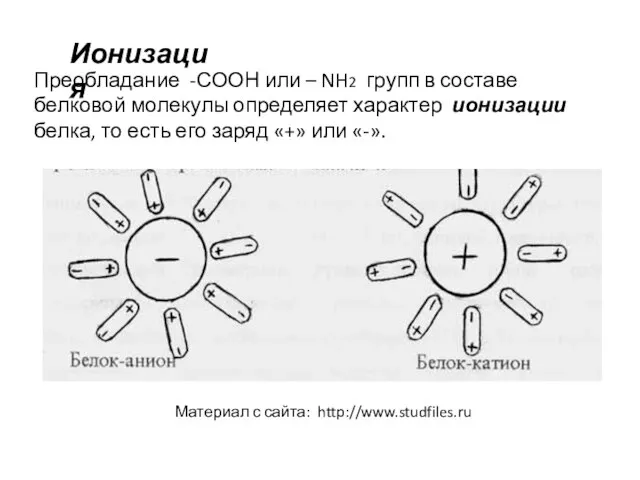
- 16. Преобладание -СООН или – NH2 групп в составе белковой молекулы определяет характер ионизации белка, то есть
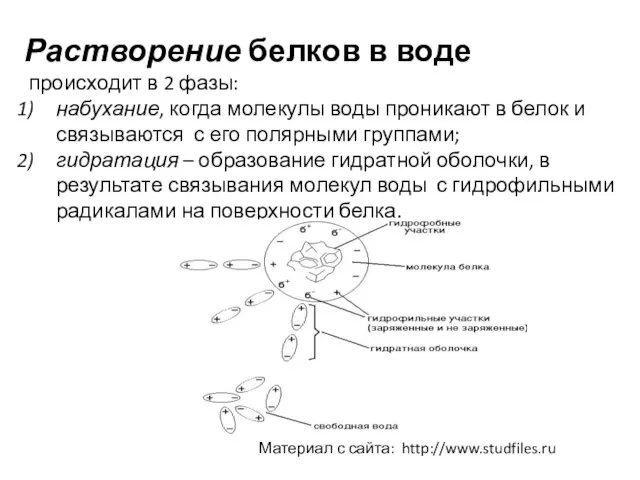
- 17. Растворение белков в воде происходит в 2 фазы: набухание, когда молекулы воды проникают в белок и
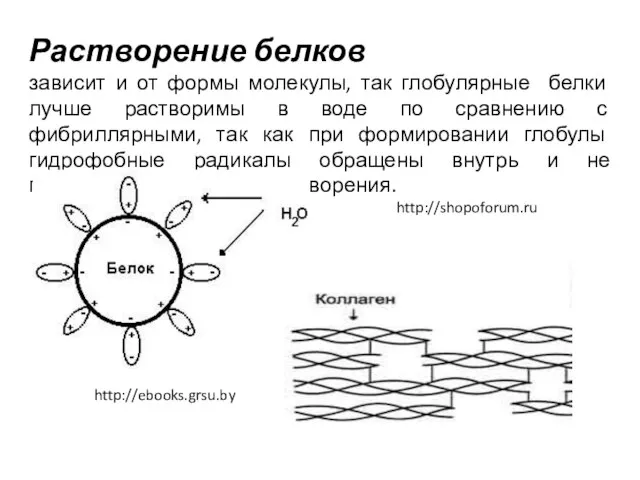
- 18. Растворение белков зависит и от формы молекулы, так глобулярные белки лучше растворимы в воде по сравнению
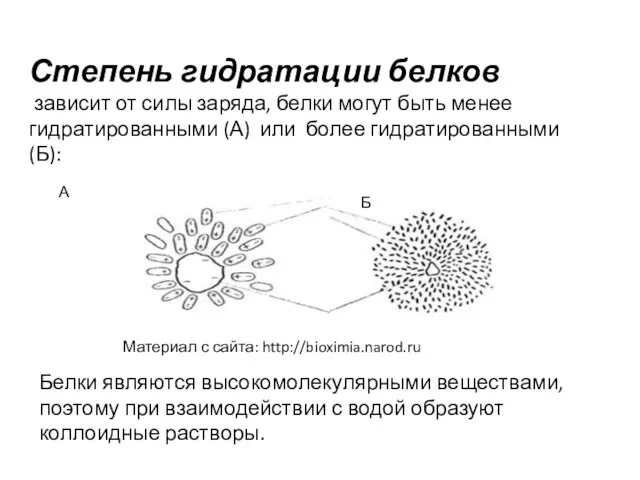
- 19. Степень гидратации белков зависит от силы заряда, белки могут быть менее гидратированными (А) или более гидратированными
- 20. Свойства коллоидных растворов: Опалесценция растворов (способность рассеивать луч видимого света) Малая скорость диффузии Неспособность проникать через
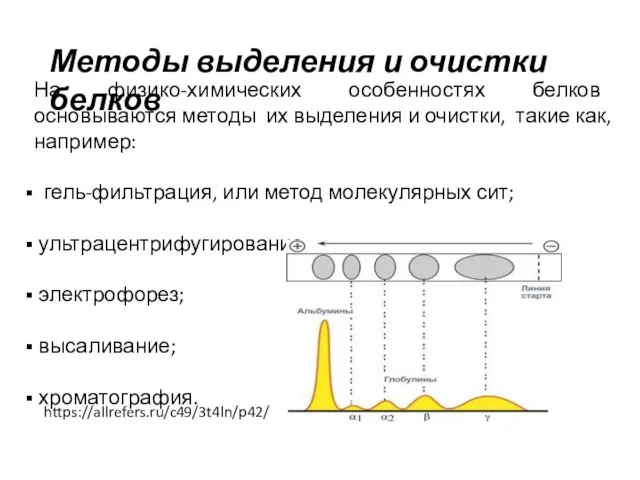
- 21. На физико-химических особенностях белков основываются методы их выделения и очистки, такие как, например: гель-фильтрация, или метод
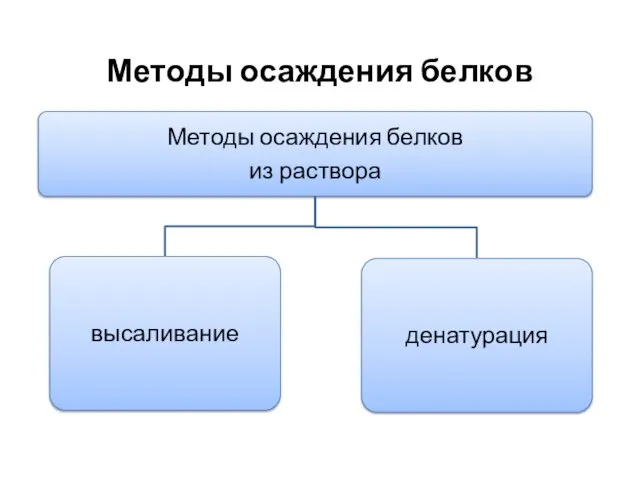
- 22. Методы осаждения белков
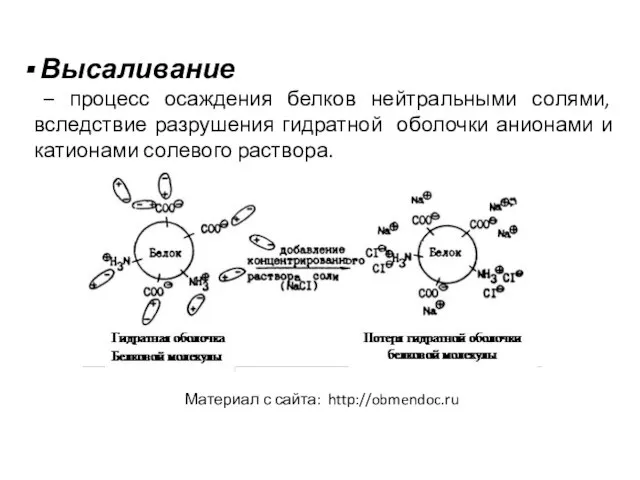
- 23. Высаливание – процесс осаждения белков нейтральными солями, вследствие разрушения гидратной оболочки анионами и катионами солевого раствора.
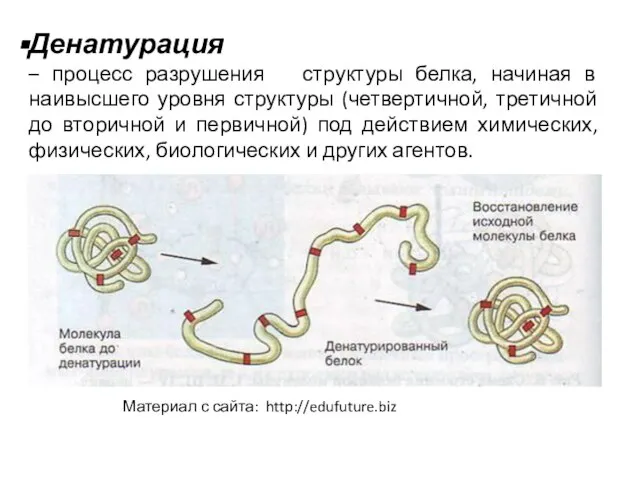
- 24. Денатурация – процесс разрушения структуры белка, начиная в наивысшего уровня структуры (четвертичной, третичной до вторичной и
- 25. Практическое применение денатурации в медицине
- 26. Практическое применение денатурации
- 27. Антисептические средства Материал с сайта: http://saf-14.ru/
- 28. Стерильные растворы Материал с сайта: http://mo.r-b.ru/
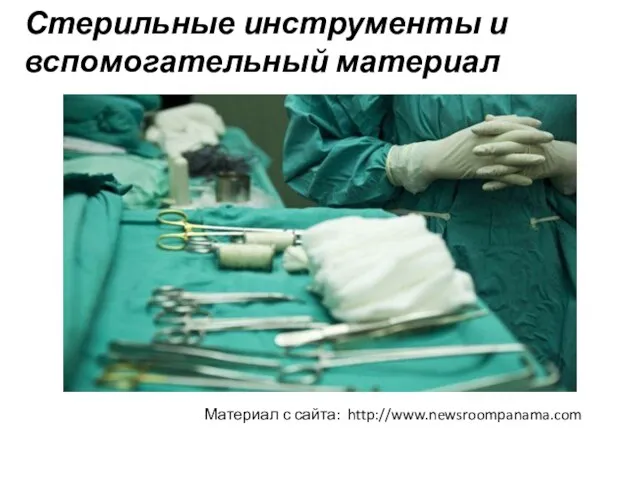
- 29. Стерильные инструменты и вспомогательный материал http://matopat.ru/ Материал с сайта: http://www.newsroompanama.com
- 30. Дезинфицирующие средства Материал с сайта: http://www.palmsbeachresort.net/
- 32. Скачать презентацию












 Биосинтез нуклеиновых кислот (анаболизм). Репликация
Биосинтез нуклеиновых кислот (анаболизм). Репликация Класс птицы
Класс птицы Орхидеи Вьетнама
Орхидеи Вьетнама Дыхание
Дыхание Транскрипция. Молекулярная биотехнология. Часть 2
Транскрипция. Молекулярная биотехнология. Часть 2 Виды рептилий
Виды рептилий Познавательные (когнитивные) процессы
Познавательные (когнитивные) процессы Земляника нейтрального светового дня. Голландская селекционная компания АBZ Seeds
Земляника нейтрального светового дня. Голландская селекционная компания АBZ Seeds Хамелеон. 7 клас
Хамелеон. 7 клас Мак опийный
Мак опийный Презентация на тему Сердце
Презентация на тему Сердце  Дикие животные и их детёныши
Дикие животные и их детёныши Класс насекомые. Отряд бабочки
Класс насекомые. Отряд бабочки Животные левши или правши?
Животные левши или правши? Тонус сосудов и его регуляция
Тонус сосудов и его регуляция Адаптации. Возникновение приспособлений
Адаптации. Возникновение приспособлений Ультразвук в природе
Ультразвук в природе mypresentation.ru
mypresentation.ru Ферменты
Ферменты Презентация на тему ВНЕШНЕЕ СТРОЕНИЕ ЛИСТА
Презентация на тему ВНЕШНЕЕ СТРОЕНИЕ ЛИСТА  “Ctenophora-sister” – гипотеза появления многоклеточности
“Ctenophora-sister” – гипотеза появления многоклеточности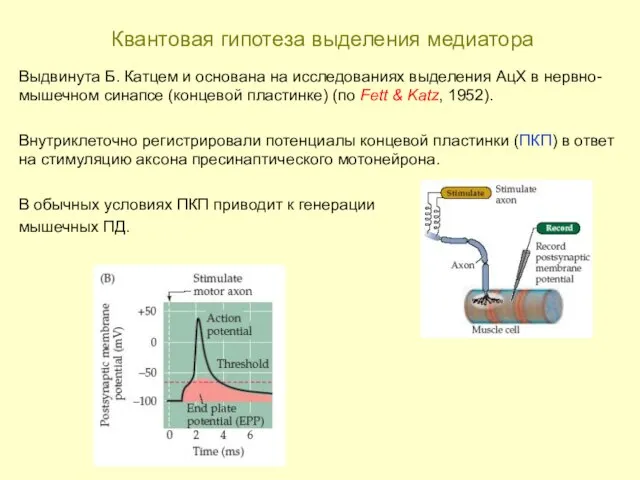 Квантовая гипотеза выделения медиатора
Квантовая гипотеза выделения медиатора List - nadzemný orgán rastliny
List - nadzemný orgán rastliny ЦНС человека и некоторые параметры обследования организма
ЦНС человека и некоторые параметры обследования организма Применение аналитической химии в биоинженерии
Применение аналитической химии в биоинженерии Белка
Белка Собака - друг человека!
Собака - друг человека! Размножение и оплодотворение у растений
Размножение и оплодотворение у растений