Слайд 2…
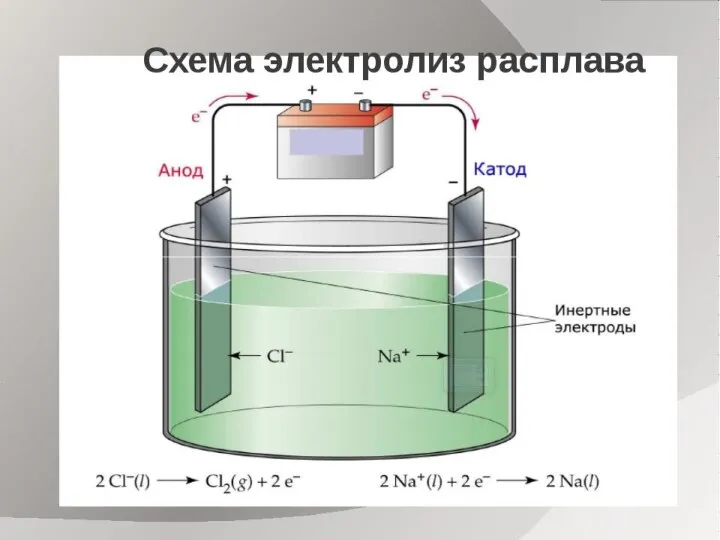
Электро́лиз — физико-химический процесс, состоящий в выделении на электродах составных частей растворённых веществ или других

веществ, являющихся результатом вторичных реакций на электродах , который возникает при прохождении электрического тока через раствор, либо расплав электролита.
Слайд 4Постоянный ток - это направленный поток электронов, исходящий от любого источника электричества.

Электролит - вещество, раствор которого способен проводить электрический ток. Электроды - пластинки из определенных материалов, соединенные между собой, которые пропускают электричество через себя (анод и катод). Окислительно-восстановительная реакция - это процесс, при котором происходит изменение степеней окисления участников. То есть одни ионы окисляются и повышают значение степени окисления, другие, напротив, восстанавливаются, понижая ее.
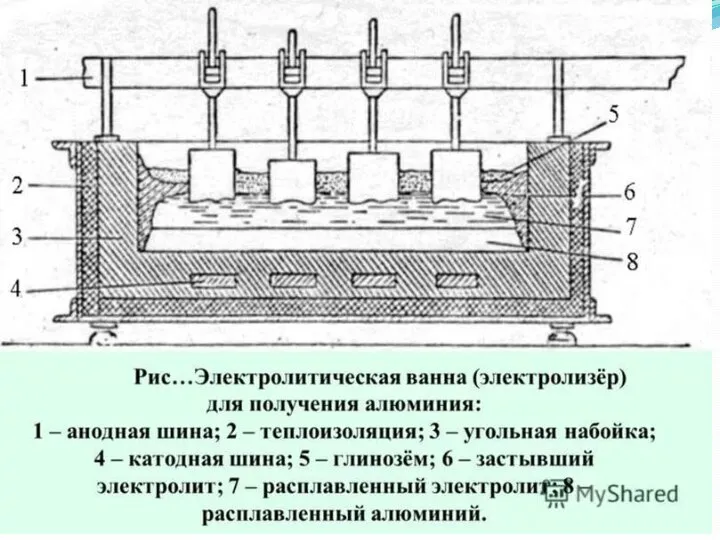
Слайд 5Явление электролиза широко применяется в современной промышленности. В частности, электролиз является одним из

способов промышленного получения алюминия, водорода, а также натрия, хлора, хлорорганических соединений, диоксида марганца[2], пероксида водорода. Также электролиз является основным процессом, благодаря которому функционирует химический источник тока.
Слайд 7Не все вещества будут электролизироваться при пропускании электрического тока. Существуют некоторые закономерности

и правила.




 Наблюдения и опыты на уроках физики
Наблюдения и опыты на уроках физики Давление. Свойства и сила давления
Давление. Свойства и сила давления Система питания дизельного двигателя
Система питания дизельного двигателя Оптика. Основные законы оптики
Оптика. Основные законы оптики Светодиоды. Применение светодиодов
Светодиоды. Применение светодиодов Из чего состоит велосипед
Из чего состоит велосипед Роль гидрогазодинамики в учебном процессе
Роль гидрогазодинамики в учебном процессе Постійний електричний струм
Постійний електричний струм Напряженность электрического поля. Принцип суперпозиции электрических полей
Напряженность электрического поля. Принцип суперпозиции электрических полей Моделирование процессов преобразования сигналов и помех линейными и нелинейными звеньями
Моделирование процессов преобразования сигналов и помех линейными и нелинейными звеньями О науке, Земле и физике
О науке, Земле и физике Презентация на тему Ядерные реакции (11 класс)
Презентация на тему Ядерные реакции (11 класс)  Современное состояние прецизионной кварцевой стабилизации частоты применительно к задачам частотно-временного обеспечения
Современное состояние прецизионной кварцевой стабилизации частоты применительно к задачам частотно-временного обеспечения Газовые законы
Газовые законы Специальность автомехеник
Специальность автомехеник Презентация на тему Простые механизмы (7 класс)
Презентация на тему Простые механизмы (7 класс)  Презентация на тему Условия плавания тел
Презентация на тему Условия плавания тел  Типовой расчет ТР2-ОС
Типовой расчет ТР2-ОС Наблюдение сплошного и линейчатых спектров
Наблюдение сплошного и линейчатых спектров Zakon_vsemirnogo_tyagotenia
Zakon_vsemirnogo_tyagotenia Лазеры
Лазеры Lek_02_Elek_22
Lek_02_Elek_22 Tlak v kvapalinách
Tlak v kvapalinách Работа газа. 10 класс
Работа газа. 10 класс Физическая кинетика явления переноса (лекция № 15)
Физическая кинетика явления переноса (лекция № 15) Презентация на тему Урок решения задач на плавление и кристаллизацию тел
Презентация на тему Урок решения задач на плавление и кристаллизацию тел  Масс-спектрометрия
Масс-спектрометрия Строение атома. Опыт Резерфорда
Строение атома. Опыт Резерфорда