Содержание
- 2. Инфракрасная спектроскопия ИКС – раздел молекулярной оптической спектроскопии, излучающей спектры поглощения и отражения электромагнитных волн в
- 3. Колебательно-вращательный спектр ИК-Спектры возникают в результате переходов между колебательными уровнями основного электронного состояния изучаемой системы. При
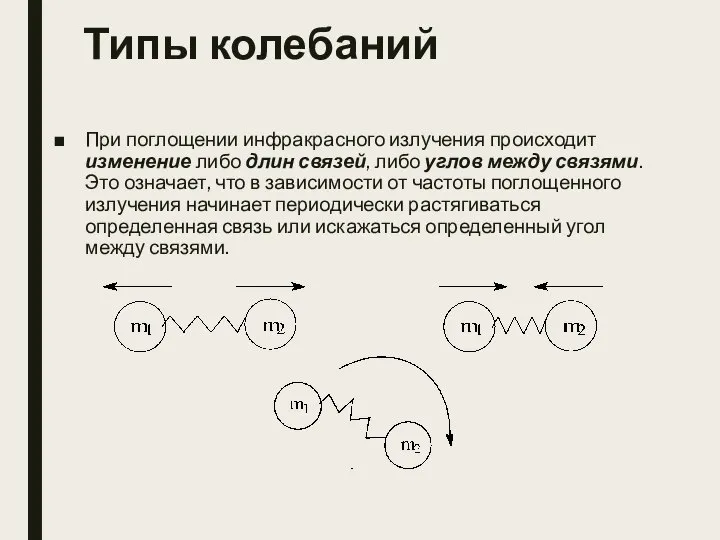
- 4. Типы колебаний При поглощении инфракрасного излучения происходит изменение либо длин связей, либо углов между связями. Это
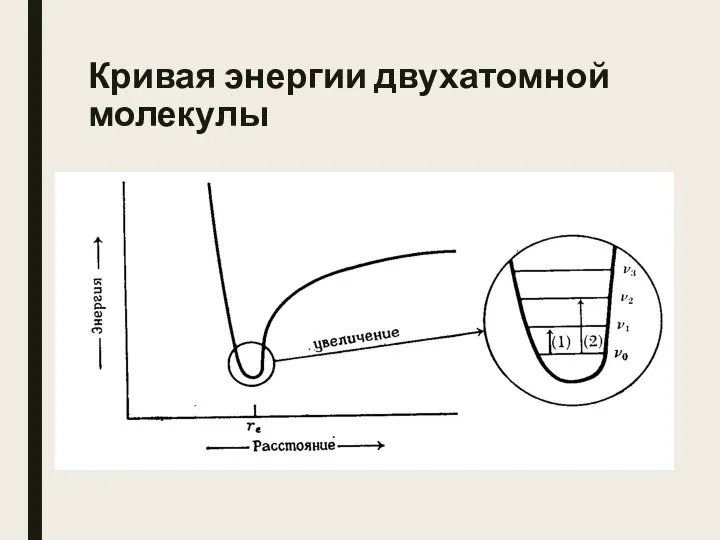
- 5. Кривая энергии двухатомной молекулы
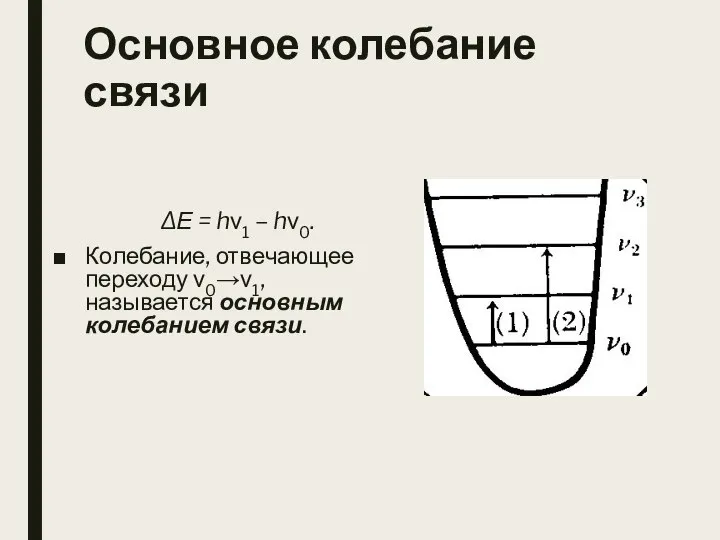
- 6. Основное колебание связи ΔЕ = hν1 – hν0. Колебание, отвечающее переходу ν0→ν1, называется основным колебанием связи.
- 7. ИК-спектр Колебательные уровни молекул квантованы, энергия переходов между ними и, следовательно, частоты колебаний могут иметь только
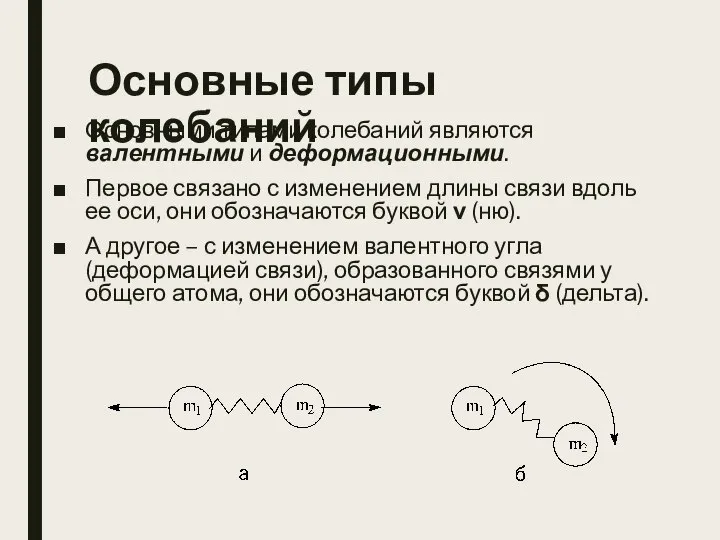
- 8. Основные типы колебаний Основными типами колебаний являются валентными и деформационными. Первое связано с изменением длины связи
- 9. Число колебаний В многоатомных молекулах, где имеется множество связей, соответственно возрастает и число теоретически возможных колебаний.
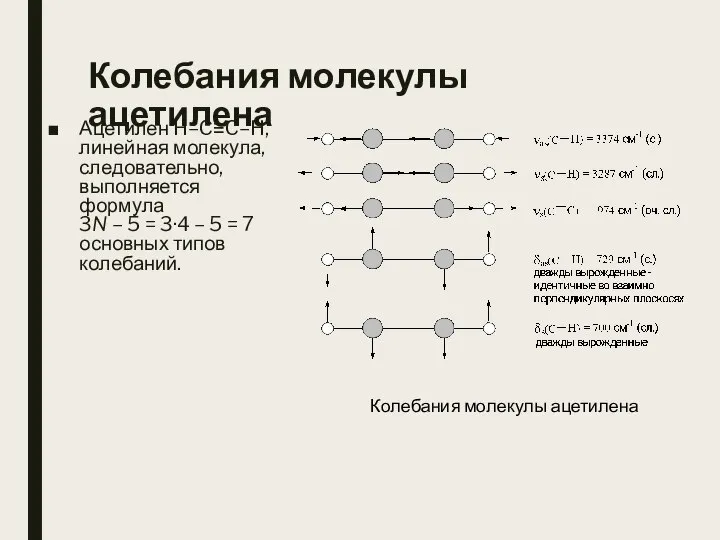
- 10. Колебания молекулы ацетилена Ацетилен H–C≡C–H, линейная молекула, следовательно, выполняется формула 3N – 5 = 3·4 –
- 11. Типы колебаний активных и неактивных в ИК-спектрах
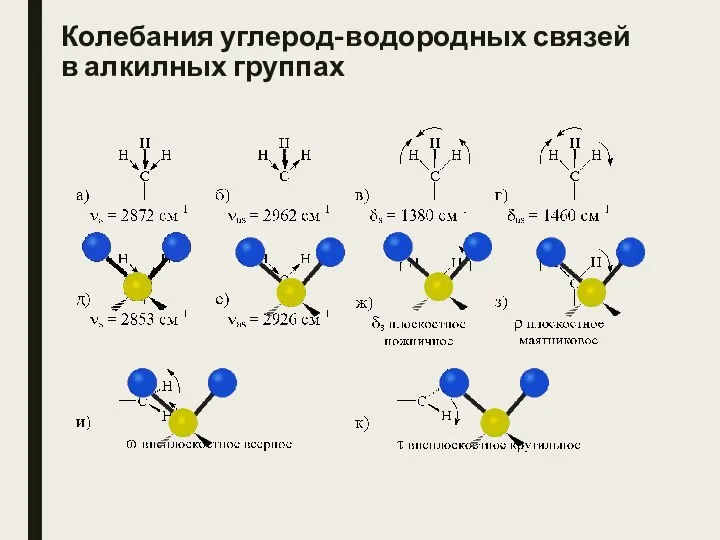
- 12. Колебания углерод-водородных связей в алкилных группах
- 13. Колебательное взаимодействие и обертоны Другие полосы поглощения, соответствующие переходам (возбуждениям) на более высокие уровни (например, переход
- 14. Колебательное взаимодействие и обертоны Третий обертон обнаружить обычно не удается. Обертоны встречаются на частотах, приближенно кратных
- 15. Число полос в спектре Таким образом, число полос в спектре не всегда равно числу степеней свободы
- 16. Частота и интенсивность поглощения В идеальном варианте валентное колебание связи описывается законом Гука, согласно которому степень
- 17. Валентные силовые постоянные химических связей Силовые константы для простой (4,5–8)·105, двойной (8–12)·105 и тройной связи (13–18)·105
- 18. Задача: Рассчитайте силовую константу валентных колебаний с частотой 1742 см–1 для карбонильной группы в циклопентаноне. Основываясь
- 19. Решение: mC = 12,0/6,02·1023 = 1,99·10–23, mO = 16,0/6,02·1023 = 2,66·10–23, μ = 1,14·10–23 k =
- 20. Основные закономерности, влияющие на частоту колебаний Энергия колебательного перехода, как и частота данного колебания, прямо пропорциональна
- 21. Основные закономерности, влияющие на частоту колебаний Таким образом, каждая функциональная группа имеет собственную, присущую ей частоту
- 22. Интенсивность полос поглощения Абсолютная интенсивность полос поглощения в инфракрасной спектроскопии не столь важна, как в электронной
- 23. ИНФРАКРАСНАЯ СПЕКТРОСКОПИЯ Практическое применение инфракрасной спектроскопии
- 24. Применение ИКС для обнаружения определенных функциональных групп в молекуле изучаемого соединения; для анализа смесей и идентификации
- 25. Применение ИКС для получение сведений о параметрах молекулярных моделей для идентификации пространственных и конформационных изомеров, изучения
- 26. Диапазоны волновых чисел Наличие изолированной функциональной группы или сочетания нескольких функциональных групп в одной молекуле обусловливает
- 27. Диапазоны волновых чисел Чаще всего наиболее важны диапазоны спектра от 4000 по 2500 см–1 и от
- 28. Решение конкретных задач обратите внимание на способ подготовки образца и отметьте полосы поглощения, обусловленные растворителем и
- 30. Скачать презентацию





















 Работа по перемещению заряда в электрическом поле
Работа по перемещению заряда в электрическом поле Электрический ток в вакууме
Электрический ток в вакууме Информационно-коммуникационные технологии на уроках физики
Информационно-коммуникационные технологии на уроках физики Резерв
Резерв Револьверный станок
Револьверный станок Движение тел. Плотность
Движение тел. Плотность Индукция. Самоиндукция. Интерактивный кроссворд Автор: Апрельская Валентина Ивановна, учитель физики МБОУ « СОШ № 11» ИМРСК,
Индукция. Самоиндукция. Интерактивный кроссворд Автор: Апрельская Валентина Ивановна, учитель физики МБОУ « СОШ № 11» ИМРСК,  Агрегатные состояния вещества
Агрегатные состояния вещества Равноускоренное движение
Равноускоренное движение Светофор. Внеклассное мероприятие по физике
Светофор. Внеклассное мероприятие по физике Использование элементов развивающего обучения на уроках физики по сингапурской системе обучения
Использование элементов развивающего обучения на уроках физики по сингапурской системе обучения Трехфазный переменный ток. Мощность трехфазной цепи
Трехфазный переменный ток. Мощность трехфазной цепи Активное и реактивное сопротивления в цепи перемен тока
Активное и реактивное сопротивления в цепи перемен тока Разработка технологии установки, эксплуатации и ремонта судовых аккумуляторов
Разработка технологии установки, эксплуатации и ремонта судовых аккумуляторов Метрология. Выборочный контроль
Метрология. Выборочный контроль Презентация на тему Спектроскоп
Презентация на тему Спектроскоп  Первый закон термодинамики. Применение первого закона термодинамики к изопроцессам
Первый закон термодинамики. Применение первого закона термодинамики к изопроцессам Как измеряются разводы и чем
Как измеряются разводы и чем Система питания двигателей автомобиля от газобаллонных установок
Система питания двигателей автомобиля от газобаллонных установок Виды движения
Виды движения Определение коэффициента силы трения
Определение коэффициента силы трения Ньютон. Совершенны ли законы Ньютона?
Ньютон. Совершенны ли законы Ньютона? Преломление света
Преломление света Постоянный ток. Сила тока. Сопротивление. Закон Ома для участка цепи. Виды соединения проводников
Постоянный ток. Сила тока. Сопротивление. Закон Ома для участка цепи. Виды соединения проводников Переменный электрический ток
Переменный электрический ток Переменный электрический ток
Переменный электрический ток Прикладная оптика. Лекция 2
Прикладная оптика. Лекция 2 Презентация на тему Постоянные магниты. Магнитное поле Земли
Презентация на тему Постоянные магниты. Магнитное поле Земли