Слайд 2 Молекулярная физика
Используя соотношения и , получим:
и . Полученную формулу

называют формулой Больцмана. Для давления будем иметь
, где и при Eпот=0.
В поле силы тяжести вблизи поверхности Земли
,
где m0 – масса молекулы газа, M – его молярная
масса. Последнюю формулу называют барометри-
ческой. Зависимость давления от высоты z над
поверхностью земли при разных температурах и молярных массах представлена на рисунке.
Слайд 3 Молекулярная физика
Распределение молекул по скоростям. Распределение Максвелла.
В связи с тем, что

в макроскопических объемах газа содержится ас-трономическое число молекул, бессмысленно говорить об опреде-лении точного значения скорости каждой из них. С одной стороны, это сложно осуществить технически, а с другой стороны, молекулы, постоянно сталкиваясь, меняют величину и направление скорости. При таком большом количестве частиц можно говорить лишь о вероятности того, что определенная часть молекул имеет скорости лежащие в некотором интервале от до . Решением подобных задач занимается статистическая физика.
Введем понятие вероятности. Вероятностью называется относитель-ная частота выпадения того или иного события. Игральная кость при падении оказывается одной гранью вверх. Вероятность выпа-дения, например, числа 3 равна числу выпадения тройки, отнесен-ному к общему числу бросаний
Слайд 4 Молекулярная физика
Сумма выпадения всех возможных 6 чисел равна .
Пусть из общего

числа молекул N скорости, лежащие в интервале от v до v + dv имеют dN молекул. Вероятность dP того, что молекулы имеют скорости, лежащие в этих пределах пропорцио-нальна , т.е. равна , где вероятность выражена через величину интервала скоростей , а функция называется функцией распределения молекул по скоростям.
Будем искать , используя формулу Больцмана. Для этого рассмотрим идеальный газ в состоянии теплового равновесия в однородном гравитационном поле и будем следить только за z компонентой скоростей его молекул. Пусть число молекул в единице объема со скоростями, лежащими в интервале от
до равно . Рассмотрим бесконечно тонкий слой газа площадью S толщиной dz на высоте z. В его объеме содержится молекул, где n(z) -
Слайд 5 Молекулярная физика
плотность газа на высоте z. Через некоторое время молекулы этого

слоя при тепловом движении сместится на другую высоту z’ и изменит свою толщину от до , а скорости под действием сил поля изменятся и перейдут в интервал от до . Число молекул в этом объеме можно представить в виде .
Поскольку число молекул осталось неизменным, то
.
В поле силы тяжести горизонтальные составляющие скорости не меняются, и закон сохранения энергии примет вид:
Дифференцируя при постоянных z и z’, получим:
, .
Откуда и .
Слайд 6 Молекулярная физика
Используя формулу Больцмана, получим:
Из закона сохранения энергии следует:
.
Тогда и

.
В результате получено равновесное распределение молекул по значениям только одной компоненты скорости . Доля молекул, обладающих тремя определенными значениями скорости получается перемножением долей
молекул, обладающих каждой из компонент в отдельности.
Слайд 7 Молекулярная физика
Таким образом, число молекул dN со скоростями, лежащими в интервалах

от до , от до и от до равно
.
если перейти к сферическим координатам и проинтегрировать по
, то .
Константа определяется из соотношения ,
Означающего очевидное утверждение, что молекула имеет какую-то скорость в интервале от 0 до бесконечности. Это событие является достоверным, поэтому его вероятность равна 1.
Функция распределения равна
Слайд 8 Молекулярная физика
Число молекул dN, движущихся в интервале скоростей от v до
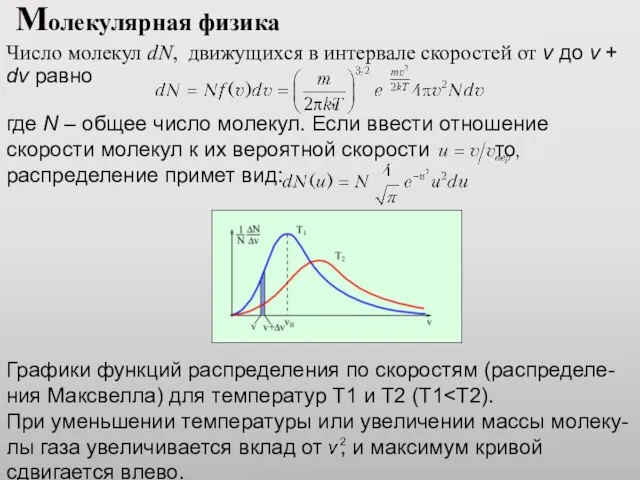
v + dv равно
,
где N – общее число молекул. Если ввести отношение скорости молекул к их вероятной скорости то распределение примет вид:
Графики функций распределения по скоростям (распределе-ния Максвелла) для температур Т1 и Т2 (Т1<Т2).
При уменьшении температуры или увеличении массы молеку-лы газа увеличивается вклад от , и максимум кривой сдвигается влево.
Слайд 9 Молекулярная физика
1.Наиболее вероятная скорость соответствует максимуму кривой
распределения Максвелла.
,
,

где - масса молекулы, M – молярная масса.
2.Средняя скорость молекул .
3.Среднеквадратичная скорость молекул
Пример. Средняя скорость движения молекул
кислорода.
м/с
Распределение молекул по скоростям
Экспериментальное подтверждение распределе-
ния Максвелла получено в опытах Штерна и
Ламмерта.
Слайд 10 Молекулярная физика
Примеры решения задач
Задача 62. Найдите суммарную кинетическую энергию вращательного

движения молекул углекислого газа (с жесткими связями) массой 88 г при температуре 300 К, молярная масса углекислого газа .
Решение. Молекула углекислого газа CO2 является треха-томной с 6 степенями свободы, три из которых приходятся на вращательное движение. Суммарная кинетическая энергия вращательного движения молекул 88 г (двух молей) CO2 равна
7479 Дж.
Задача 63. При какой температуре Т средняя квадратичная скорость молекул азота больше их наиболее вероятной скорости на
м/с?
Решение. Вычитая из выражения для средней квадратичной скорости наиболее вероятную скорость, получим:
Слайд 11 Молекулярная физика
откуда
Задача 64. Найти скорость при которой пересекаются кривые распределения

Максвелла молекул по скоростям при температурах Т и 2Т, если наиболее вероятная скорость при температуре 2Т равна.
Решение. В точке пересечения (рис.5) функций распределения (плотностей вероятности) они равны:
,
откуда и
Задача 65. Какая часть молекул кислорода при t = 0°С обладает скоростями от 100 до 110 м/с?
Решение. Запишем распределение Максвелла молекул по
скоростям в виде , где -
относительная скорость, , . Тогда
Слайд 12 Молекулярная физика
Задача 66. Найдите разность давлений в салоне самолета, летящего на

высоте = 8300 м и за бортом. В салоне поддерживается давление воздуха, соответствующее высоте
=2700 м. Ускорение свободного падения и температура 0°С наружного воздуха от высоты не зависят. Давление на поверхности Земли = 100 кПа, молярная масса воздуха M = 29кг/м3.
Решение. Зависимость давления от высоты над поверхностью Земли дается распределением Больцмана . Тогда давление в салоне равно кПа, а за бортом
кПа. Разность давлений составляет 36 кПа.
Задача 67. Вблизи поверхности Земли отношение объемных концентраций кислорода и азота в воздухе Считая ускорение свободного падения не зависящим от высоты, а темпера-туру атмосферы постоянной и равной 0°С, определить это отношение на высоте h = 10 км.
,











 Строения атомов
Строения атомов Svobodnoe_padenie_tel_Dvizhenie_s_uskoreniem_svobodnogo_padenia
Svobodnoe_padenie_tel_Dvizhenie_s_uskoreniem_svobodnogo_padenia Ремонт и покраска велосипеда
Ремонт и покраска велосипеда Движение тела по наклонной плоскости. Решение задач
Движение тела по наклонной плоскости. Решение задач Полупроводник как активная среда
Полупроводник как активная среда Физика вокруг на
Физика вокруг на Тепловые явления в природе
Тепловые явления в природе Презентация Механика Лекция 4
Презентация Механика Лекция 4 Презентация на тему Электромагнитная индукция. Опыты Фарадея
Презентация на тему Электромагнитная индукция. Опыты Фарадея  Явления тяготения. Сила тяжести
Явления тяготения. Сила тяжести Презентация на тему Физика плазмы
Презентация на тему Физика плазмы  Tesla
Tesla Методы расчёта разветвленных цепей постоянного тока
Методы расчёта разветвленных цепей постоянного тока Тепловые машины. Практическое занятие
Тепловые машины. Практическое занятие Перфора́тор
Перфора́тор Линзы. Оптические приборы. Практическая работа
Линзы. Оптические приборы. Практическая работа Реактивная сила
Реактивная сила Количественный анализ
Количественный анализ Рідинні термометри
Рідинні термометри Введение в волновую оптику. Энергия ЭМ волн. Вектор Пойнтинга. Лекция 2с 8 (1)
Введение в волновую оптику. Энергия ЭМ волн. Вектор Пойнтинга. Лекция 2с 8 (1) Проводники и диэлектрики в электрическом поле
Проводники и диэлектрики в электрическом поле Работа и мощность постоянного тока
Работа и мощность постоянного тока Питание
Питание Історія вивчення магнетизму
Історія вивчення магнетизму Сила тяжести
Сила тяжести Фи́зика твёрдого те́ла
Фи́зика твёрдого те́ла Голография и ее применение
Голография и ее применение Катушка с ферромагнитным сердечником. Лекция 06
Катушка с ферромагнитным сердечником. Лекция 06