Содержание
- 3. Фотографии атомов под микроскопом Атомы углерода на поверхности графита Атомы солнечной батареи
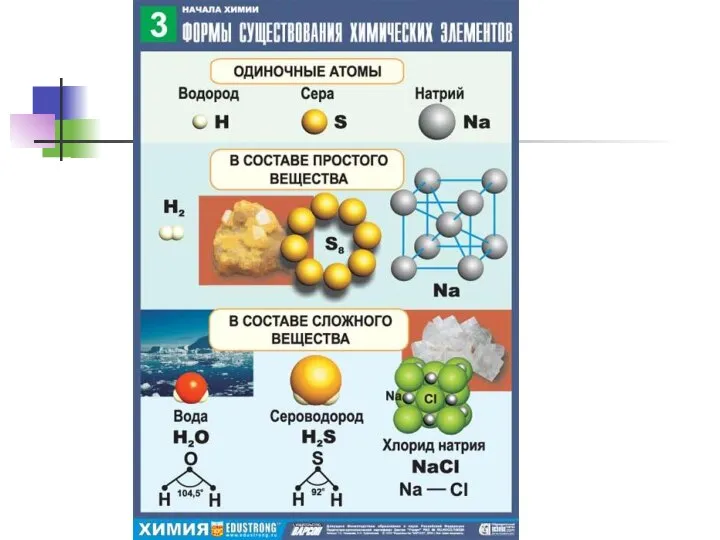
- 4. Первая форма существования химических элементов – свободные атомы. Понятие атом возникло в античном мире для обозначения
- 5. Открытие электрона В 1891 г.на основании опытов пришел к выводу, что электричество переносится мельчайшими частицами –
- 6. Характеристики электрона Доказали, что скорость движения электрона – 300 000 км/сек. Масса электрона в 2000 раз
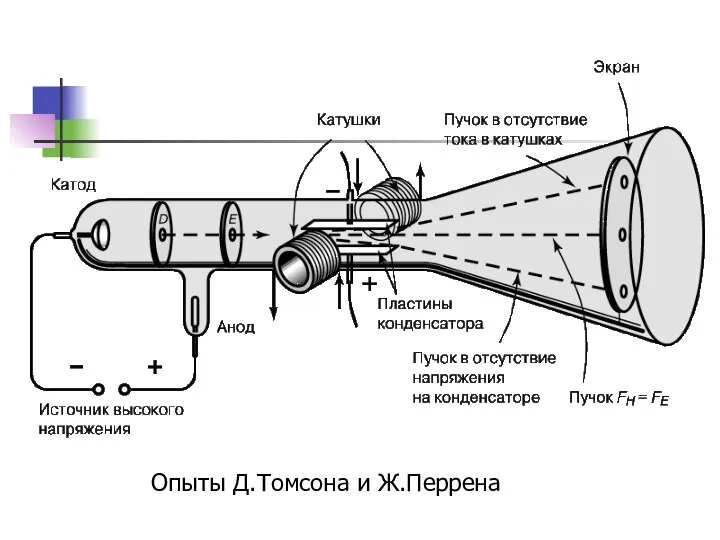
- 7. Опыты Д.Томсона и Ж.Перрена
- 8. Катодная трубка Томсона и катодные лучи осцилограф
- 9. Физик Анри Беккерель обнаружил, что соли урана испускают невидимое излучение, засвечивая фотопластинки, закрытые от света. Это
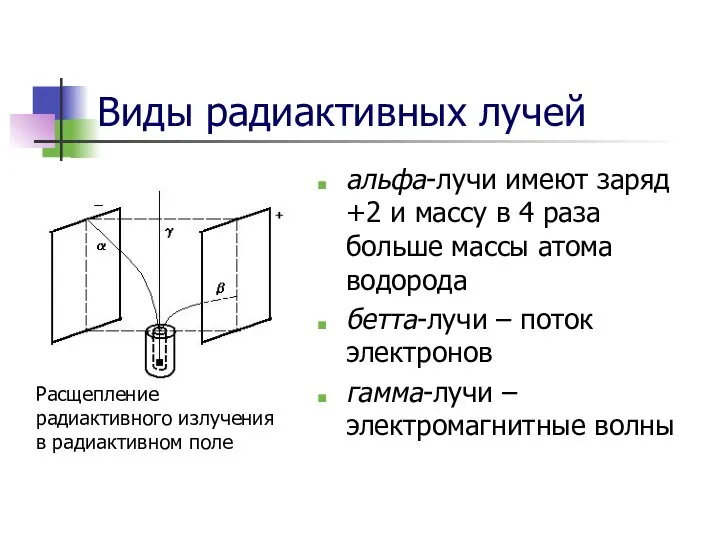
- 10. Виды радиактивных лучей альфа-лучи имеют заряд +2 и массу в 4 раза больше массы атома водорода
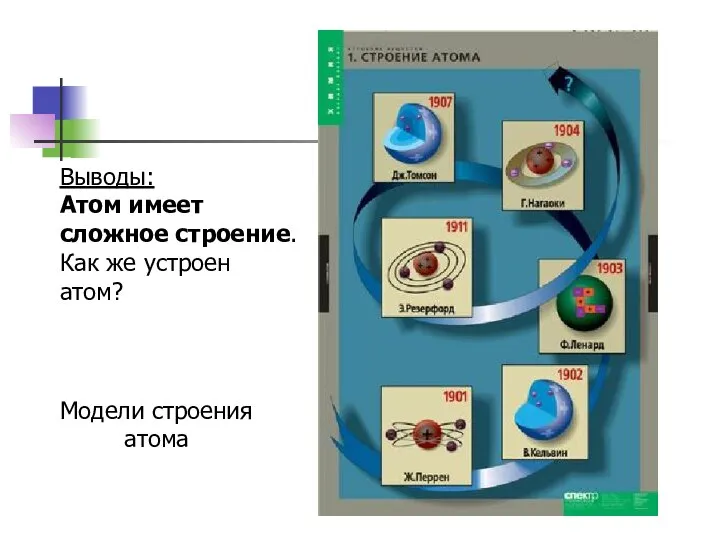
- 12. Выводы: Атом имеет сложное строение. Как же устроен атом? Модели строения атома
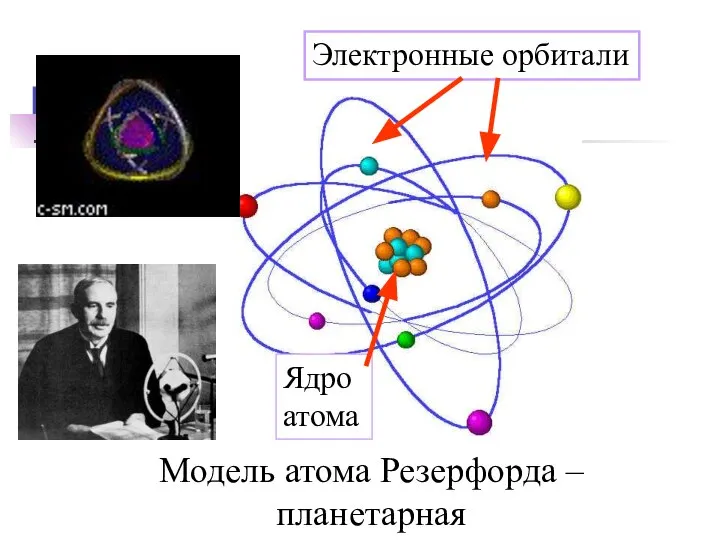
- 14. Модель атома Резерфорда – планетарная Ядро атома Электронные орбитали
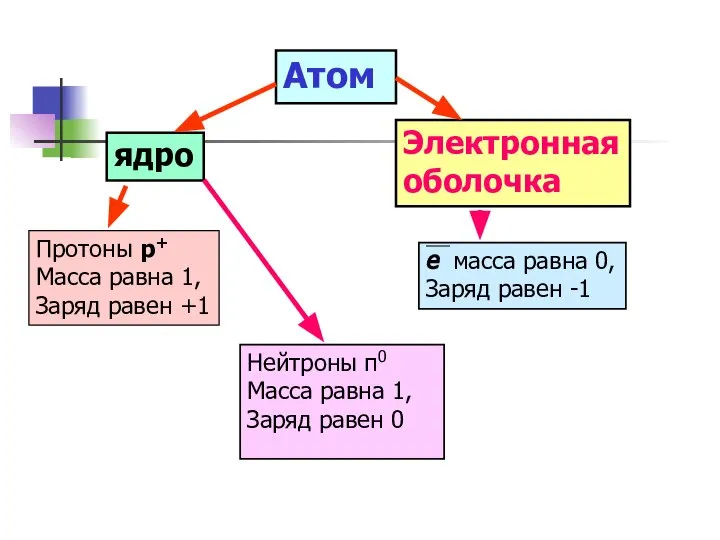
- 15. Атом ядро Электронная оболочка е масса равна 0, Заряд равен -1 Протоны р+ Масса равна 1,
- 16. Запомни ! Атом – электронейтрален, так как содержит одинаковое число протонов и электронов, равное порядковому номеру
- 17. Запомни! Вся масса атома сосредоточена в его ядре, так как массой электрона можно пренебречь. Радиус ядра
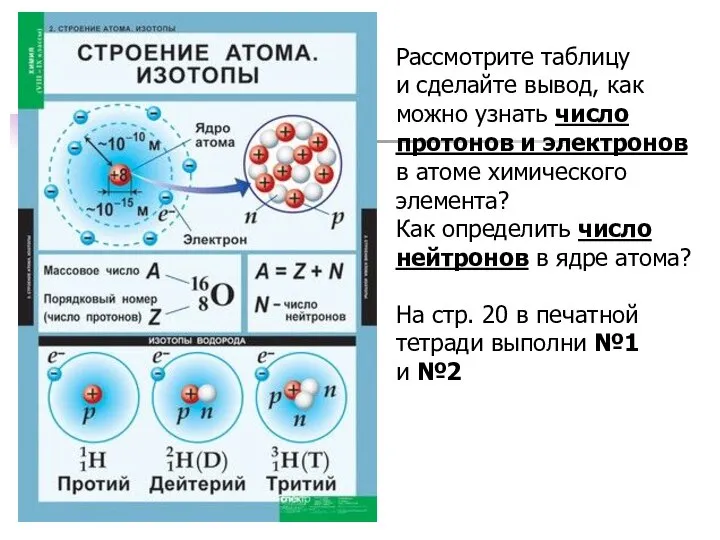
- 18. Рассмотрите таблицу и сделайте вывод, как можно узнать число протонов и электронов в атоме химического элемента?
- 19. Заполните таблицу №3 «Состав атомов химических элементов» на стр.21. в печатной тетради. Пользуйтесь Периодической системой химических
- 21. Скачать презентацию











 Физические задачи с литературным содержанием
Физические задачи с литературным содержанием Кипение. Температура кипения
Кипение. Температура кипения Электромагнитная индукция. Опыты Фарадея
Электромагнитная индукция. Опыты Фарадея Гидравлические системы. 2 класс
Гидравлические системы. 2 класс Волшебные свойства воды
Волшебные свойства воды “Методы регистрации заряженных частиц
“Методы регистрации заряженных частиц Антифрикционные сплавы
Антифрикционные сплавы Презентация на тему Электронно-лучевая трубка (10 класс)
Презентация на тему Электронно-лучевая трубка (10 класс)  Динамика судна. Общие понятия гидромеханики
Динамика судна. Общие понятия гидромеханики Организация участковой системы ведения путевого хозяйства на западно-сибирской железной дороге
Организация участковой системы ведения путевого хозяйства на западно-сибирской железной дороге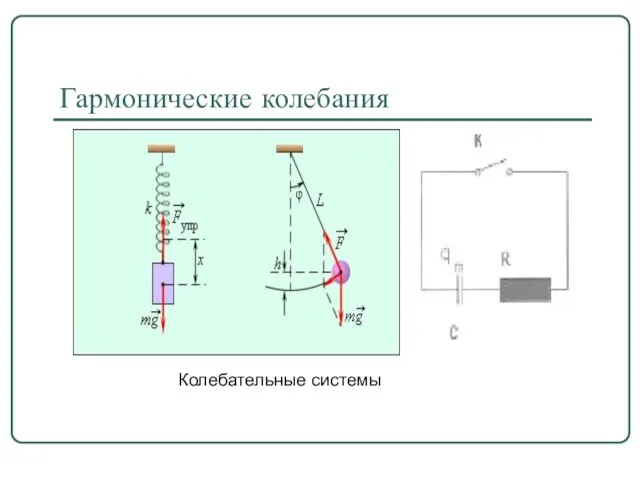 Гармонические колебания. Колебательные системы
Гармонические колебания. Колебательные системы Сила трения 7 класс
Сила трения 7 класс Вековые вариации геомагнитного поля
Вековые вариации геомагнитного поля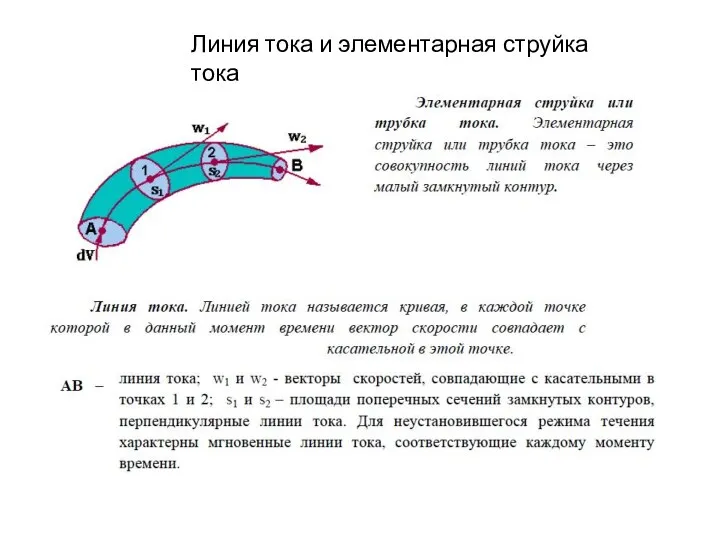 2.Уравнение Бернулли. Давление жидкости на плоские и криволинейные поверхности
2.Уравнение Бернулли. Давление жидкости на плоские и криволинейные поверхности Правила работы с микроскопом
Правила работы с микроскопом Конкурс Интерактивная мозаика. 7 - 8 классы
Конкурс Интерактивная мозаика. 7 - 8 классы Закон всемирного тяготения
Закон всемирного тяготения Переменный ток
Переменный ток Элективный курс физика и искусство
Элективный курс физика и искусство P-N переход
P-N переход Термохимические ячейки
Термохимические ячейки Использование теплового действия электрического тока в устройстве теплиц и инкубаторов
Использование теплового действия электрического тока в устройстве теплиц и инкубаторов Определение остаточных внутренних сил при разгрузке статически неопределимой балки
Определение остаточных внутренних сил при разгрузке статически неопределимой балки Неравномерное движение (9 класс)
Неравномерное движение (9 класс)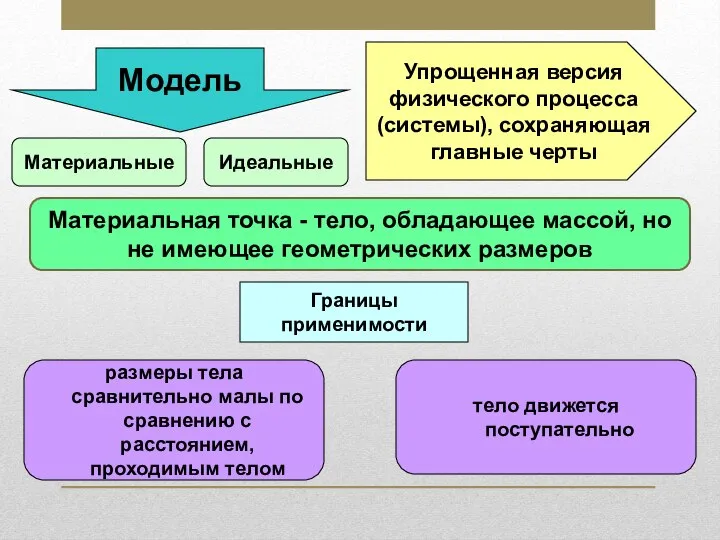 Материальная точка
Материальная точка Презентация на тему Трансформаторы (11 класс)
Презентация на тему Трансформаторы (11 класс)  Радиоактивность. Правило равенства сумм индесов
Радиоактивность. Правило равенства сумм индесов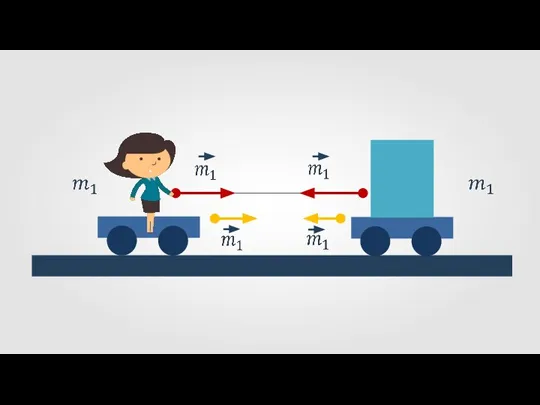 Напряжённость электрического поля
Напряжённость электрического поля