Слайд 2Испарение и конденсация
Испарение – процесс превращения жидкости в пар
Конденсация – процесс превращения

пара в жидкость
Испарение и Конденсация – взаимно компенсирующие процессы.
Слайд 3Насыщенный пар
Насыщенный пар – пар, находящийся в динамическом равновесии со своей жидкостью.
Динамическое

равновесие – когда число молекул, покидающих поверхность жидкости за некоторый промежуток времени, будет равно в среднем числу молекул пара, возвратившихся за то же время в жидкость.
Слайд 4Давление насыщенного пара
Концентрация молекул насыщенного пара при постоянной температуре не зависит от

его объёма.
Так как давление пропорционально концентрации молекул(p=nkT), то из этого следует, что давление насыщенного пара не зависит от занимаемого им объёма.
Давление насыщенного пара(pн.п.) – такое давление пара, при котором жидкость находится в равновесии со своим паром.
Слайд 5Ненасыщенный пар
Ненасыщенный пар – когда при постепенном сжатии пара, превращения в жидкость(конденсации)

не происходит.
Однако пар превращается в жидкость не при любой температуре. Если температура выше некоторого значения, то, как бы мы ни сжимали газ, он никогда не превратится в жидкость(такая норма называется критической температурой).
Критическая температура(Ткр.) – максимальная температура, при которой пар ещё может превратиться в жидкость. У каждого вещества своя Ткр.
Т>Ткр(газ); Т<Ткр(пар);
Слайд 6Зависимость давления насыщенного пара от температуры.
Кипение.

Слайд 7Зависимость давления насыщенного пара от температуры
С ростом температуры давление растёт. Так как

давление насыщенного пара не зависит от объёма, то, следовательно, оно зависит только от температуры.
При нагревании жидкости в закрытом сосуде часть жидкости превращается в пар. В результате, согласно формуле(p=nkT), давление насыщенного пара растет не только вследствие повышения температуры, но и вследствие увеличения концентрации молекул(плотности) пара.
Слайд 8
Главное различие в поведении идеального газа и насыщенного пара состоит в том,

что при изменении температуры в закрытом сосуде (или при изменении объёма при постоянной температуре) меняется масса пара. Жидкость частично превращается в пар, или, напротив, пар частично конденсируется. С идеальным газом ничего подобного не происходит.
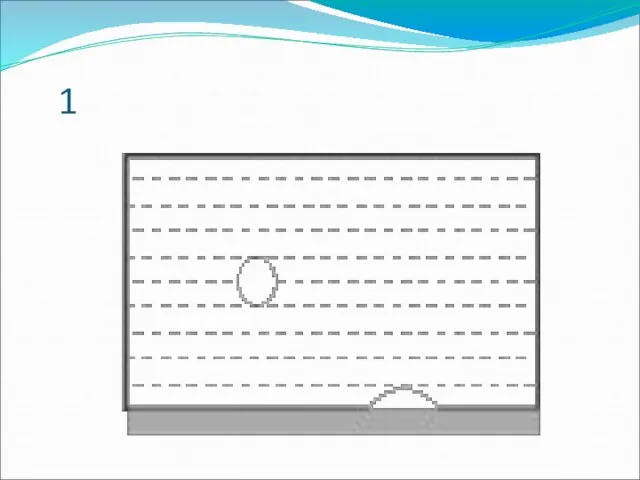
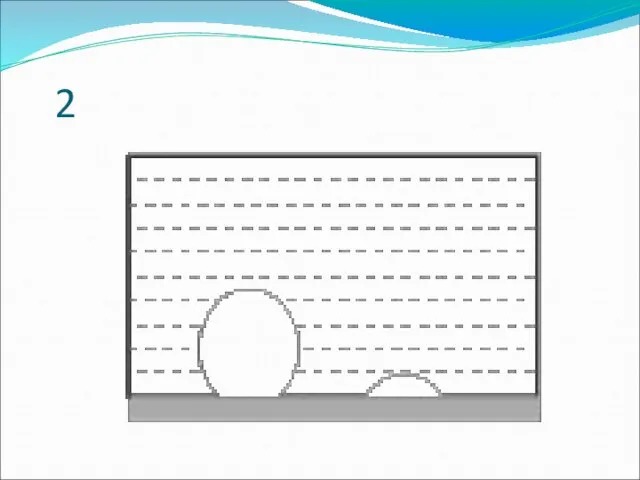
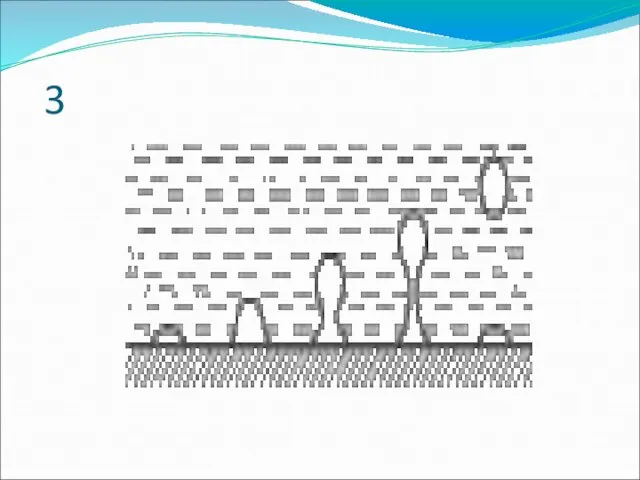
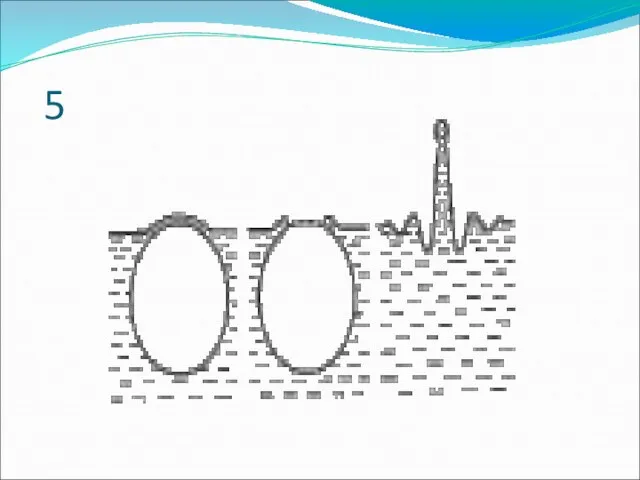
Слайд 9Кипение
Кипение - превращение жидкости в пар по всему объёму жидкости при постоянной

температуре.
Зависимость температуры кипения от давления.
Жидкость кипит тогда, когда давление её насыщенного пара = внешнему давлению.
Температура кипения - температура жидкости, при которой давление её насыщенного пара равно или превышает внешнее давление.
Слайд 10Особенности жидкости при кипении:
1)при постоянном внешнем давлении Т жидкости постоянна.
2)с

повышением внешнего давления температура кипения повышается, с понижением – понижается.
3)температура кипения зависит от наличия примесей.











 Биомеханика. Кинематика. Относительность движения
Биомеханика. Кинематика. Относительность движения Постоянный электрический ток и его характеристики
Постоянный электрический ток и его характеристики Ядерный реактор
Ядерный реактор Презентация на тему Солнце и другие звезды
Презентация на тему Солнце и другие звезды  Презентация на тему Термометр
Презентация на тему Термометр  Уравнение неразрывности. Лекция 5
Уравнение неразрывности. Лекция 5 Молекулярно-кинетический подход применительно к расчету тепловой нагрузки при пленочном кипении
Молекулярно-кинетический подход применительно к расчету тепловой нагрузки при пленочном кипении Презентация на тему Электрическое поле (8 класс)
Презентация на тему Электрическое поле (8 класс)  Расчет производительности экструдеров
Расчет производительности экструдеров Как уменьшить силу трения
Как уменьшить силу трения Электрическая цепь и её составная часть
Электрическая цепь и её составная часть Тепловое движение
Тепловое движение Презентация к уроку _Инерциальные системы отсчета
Презентация к уроку _Инерциальные системы отсчета Видимое и ультрафиолетовое излучение
Видимое и ультрафиолетовое излучение рух по колу
рух по колу Автор: Тараканова Светлана школа № 14, 8 А класс
Автор: Тараканова Светлана школа № 14, 8 А класс Закон Снеллиуса (отражения) для монотипных волн
Закон Снеллиуса (отражения) для монотипных волн Электромагнитная совместимость в электроэнергетике
Электромагнитная совместимость в электроэнергетике Наглядное пособие для изучения шпоночного и штифтового соединений
Наглядное пособие для изучения шпоночного и штифтового соединений Электрический ток. Задачи
Электрический ток. Задачи Электрический ток в различных средах
Электрический ток в различных средах Явление электромагнитной индукции (эми). 11 класс
Явление электромагнитной индукции (эми). 11 класс Солнечная лаборатория
Солнечная лаборатория Результаты измерений. Лабораторная работа №3 по биофизике
Результаты измерений. Лабораторная работа №3 по биофизике Сила
Сила Изменение агрегатных состояний
Изменение агрегатных состояний Основы медицинской и биологической физики. Лекция 4. Часть 1
Основы медицинской и биологической физики. Лекция 4. Часть 1 Динамика фотоионизации атомов благородных газов между первым и вторым порогом ионизации
Динамика фотоионизации атомов благородных газов между первым и вторым порогом ионизации