Содержание
- 2. Термодинамика – теория тепловых явлений, в которой не учитывается молекулярное строение тел. Выводы термодинамики опираются на
- 3. Если термодинамическая система была подвержена внешнему воздействию, то в конечном итоге она перейдет в другое равновесное
- 4. Если процесс протекает достаточно медленно (в пределе бесконечно медленно), то система в каждый момент времени оказывается
- 5. С точки зрения молекулярно-кинетической теории внутренняя энергия вещества = кинетическая энергия всех атомов и молекул +
- 6. внутренняя энергия U тела определяется макроскопическими параметрами, характеризующими состояние тела.
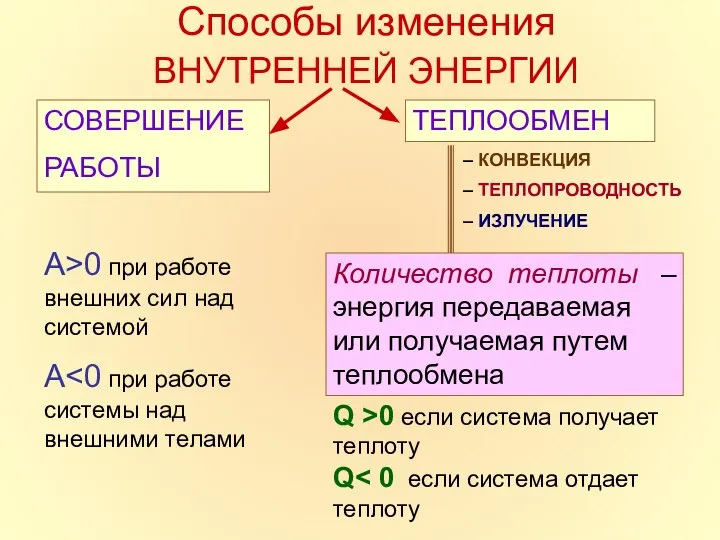
- 7. Способы изменения ВНУТРЕННЕЙ ЭНЕРГИИ СОВЕРШЕНИЕ РАБОТЫ ТЕПЛООБМЕН – КОНВЕКЦИЯ – ТЕПЛОПРОВОДНОСТЬ – ИЗЛУЧЕНИЕ Количество теплоты –
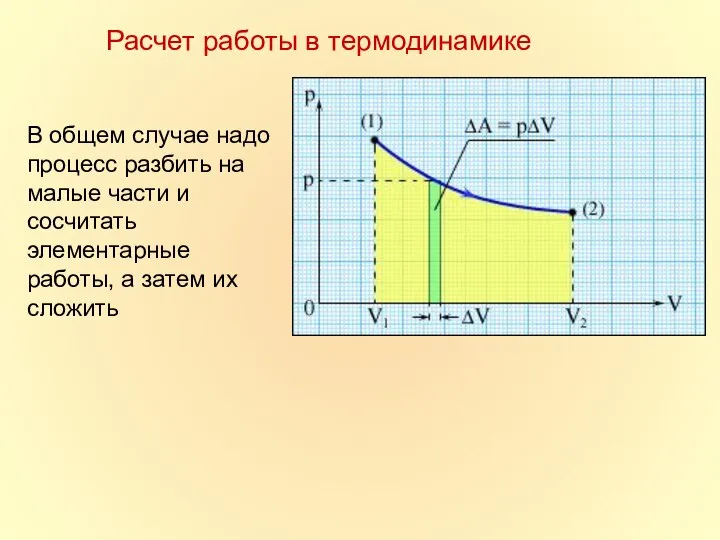
- 8. Расчет работы в термодинамике
- 9. В общем случае надо процесс разбить на малые части и сосчитать элементарные работы, а затем их
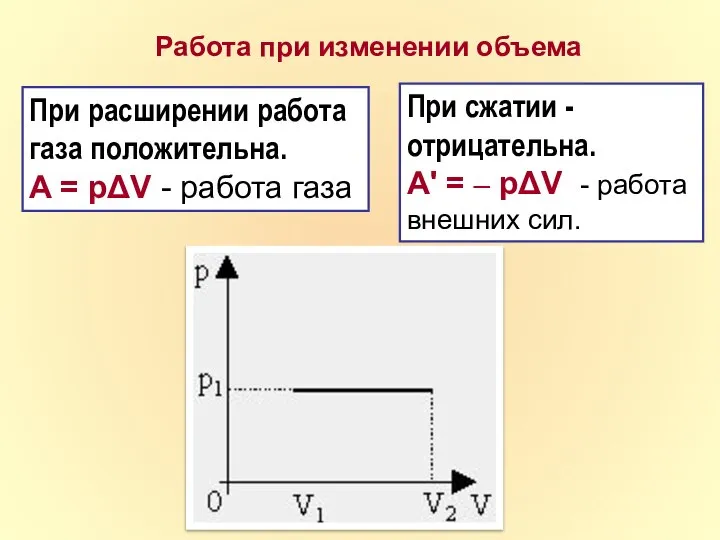
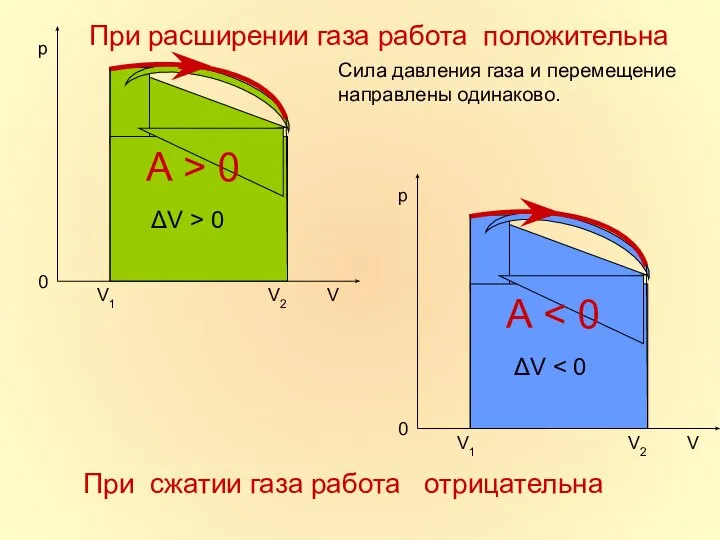
- 10. Работа при изменении объема При расширении работа газа положительна. A = pΔV - работа газа При
- 11. Используя уравнение Менделеева-Клапейрона, получим:
- 12. В изохорном процессе объем не меняется, следовательно, в изохорном процессе работа не совершается!
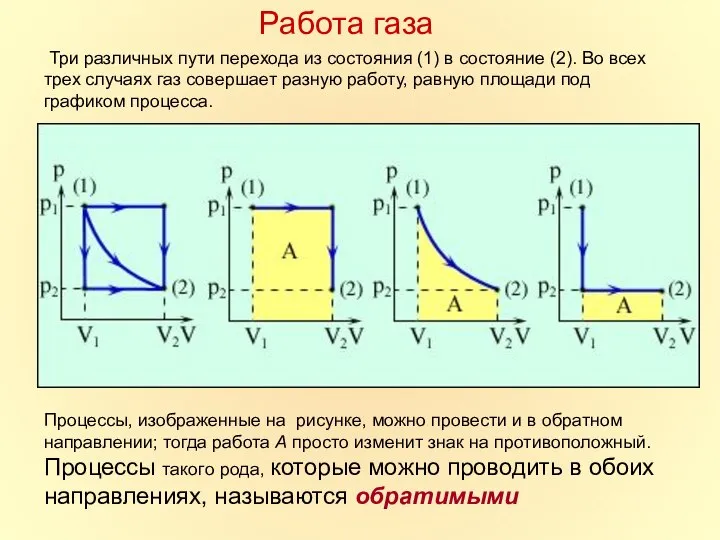
- 13. Три различных пути перехода из состояния (1) в состояние (2). Во всех трех случаях газ совершает
- 14. При расширении газа работа положительна Сила давления газа и перемещение направлены одинаково. При сжатии газа работа
- 15. Первый закон термодинамики является обобщением закона сохранения и превращения энергии для термодинамической системы. Изменение ΔU внутренней
- 16. Другая форма записи соотношение, выражающего первый закон термодинамики: Количество теплоты, полученное системой, идет на изменение ее
- 17. Первый закон термодинамики является обобщением опытных фактов. Согласно этому закону, энергия не может быть создана или
- 18. АДИАБАТНЫЙ ПРОЦЕСС
- 19. Наряду с изохорным, изобарным и изотермическим процессами в термодинамике часто рассматриваются процессы, протекающие в отсутствие теплообмена
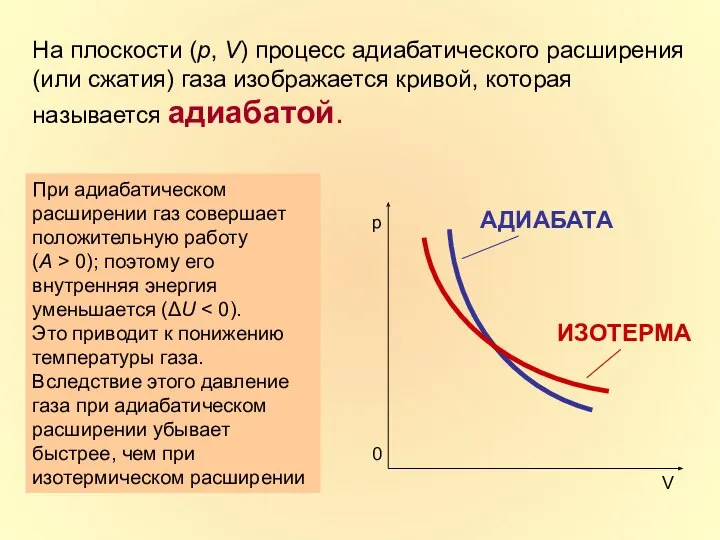
- 20. На плоскости (p, V) процесс адиабатического расширения (или сжатия) газа изображается кривой, которая называется адиабатой. При
- 21. Опыт "воздушное огниво". Возьмем толстостенный стеклянный цилиндр с поршнем. На дно цилиндра насыплем измельченной "серы" от
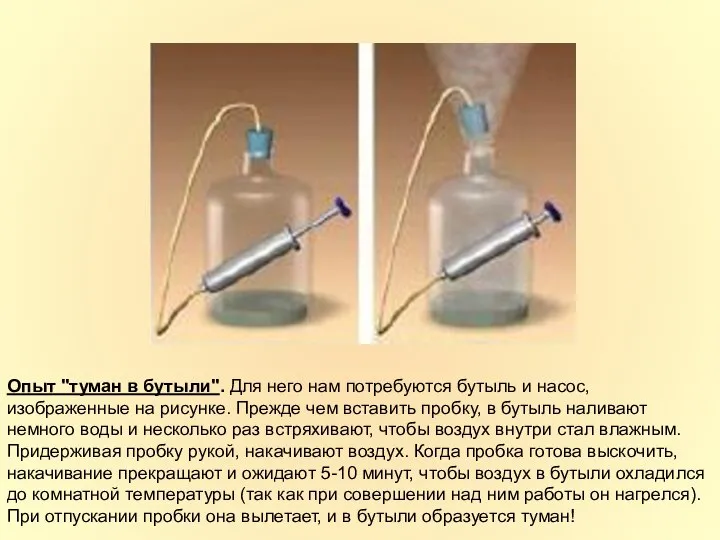
- 22. Опыт "туман в бутыли". Для него нам потребуются бутыль и насос, изображенные на рисунке. Прежде чем
- 24. Применение первого закона термодинамики к изопроцессам
- 25. ı закон термодинамики Q = ΔU + A Изобарный процесс A = p ΔV Изотермический процесс
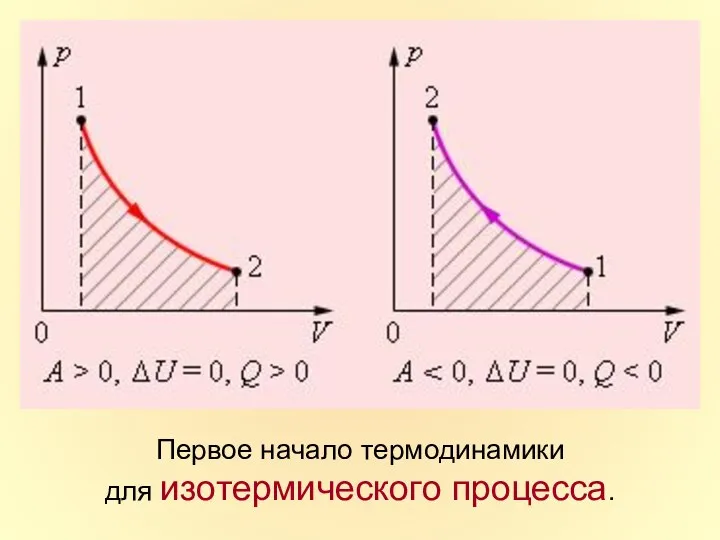
- 26. Изотермический процесс
- 27. Первое начало термодинамики для изотермического процесса.
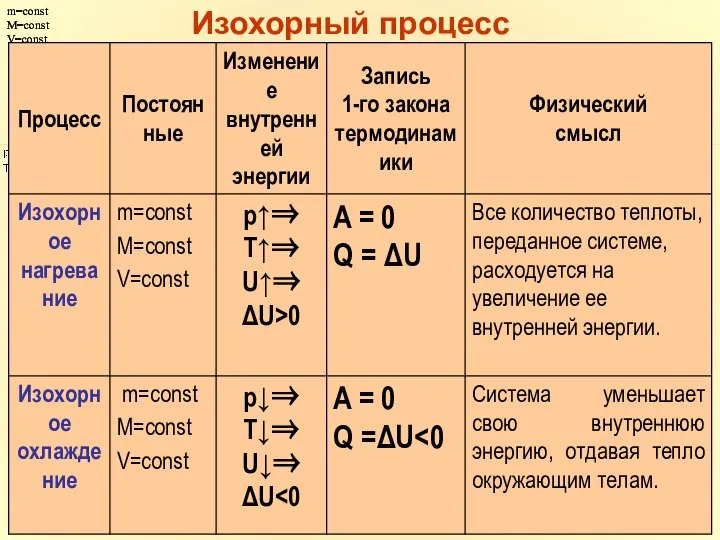
- 28. m=const M=const V=const m=const M=const V=const Изохорный процесс
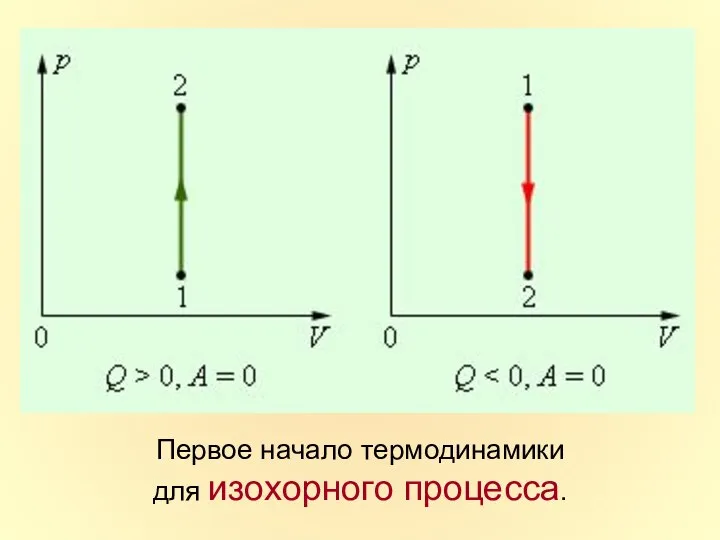
- 29. Первое начало термодинамики для изохорного процесса.
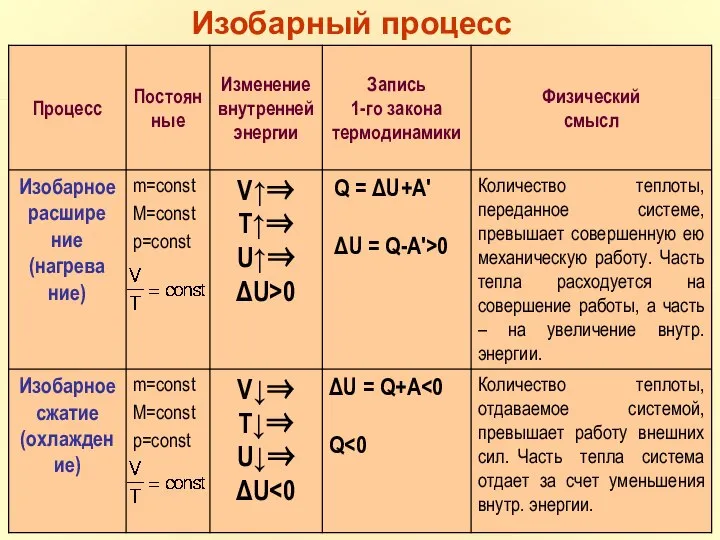
- 30. m=const M=const p=const Изобарный процесс
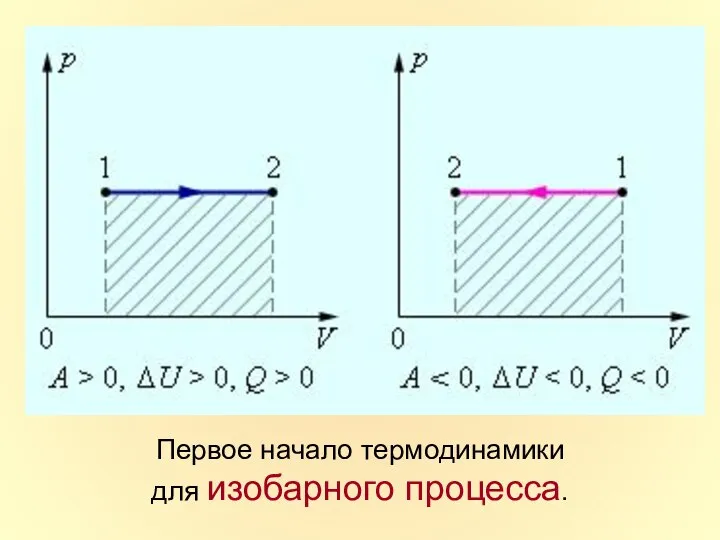
- 31. Первое начало термодинамики для изобарного процесса.
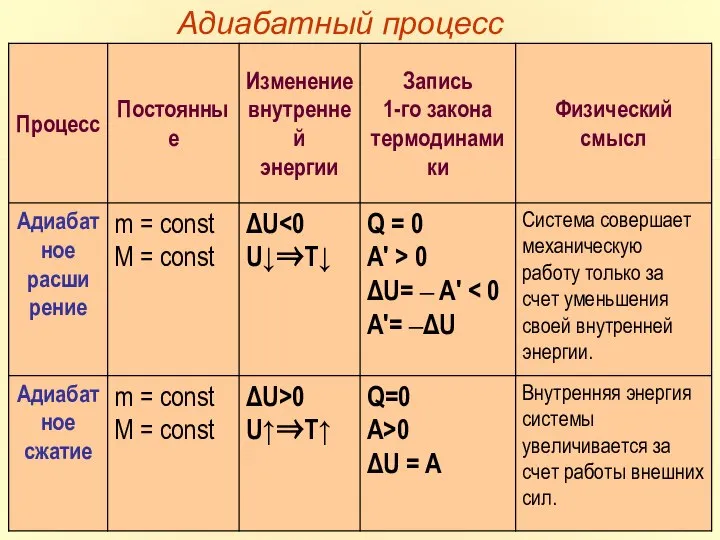
- 32. Адиабатный процесс
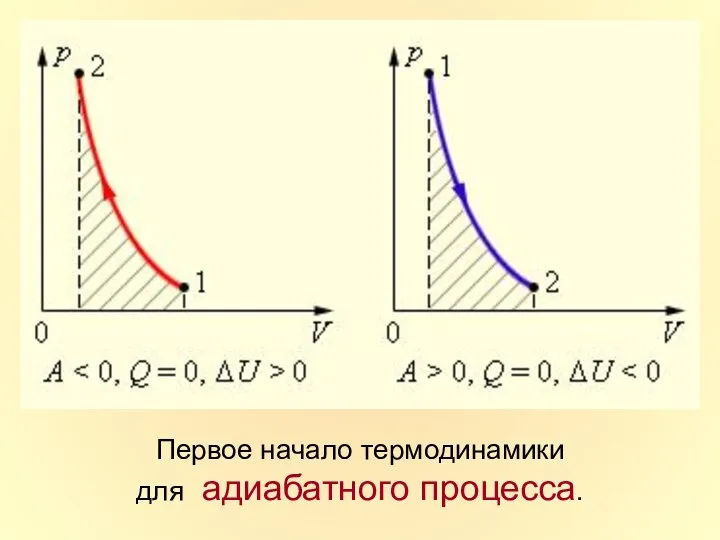
- 33. Первое начало термодинамики для адиабатного процесса.
- 34. Практическая работа на тему «Работа газа»
- 36. Скачать презентацию


















 Физика вокруг нас Подготовили: обучающиеся 10 класса
Физика вокруг нас Подготовили: обучающиеся 10 класса Простые механизмы
Простые механизмы Приемы разрешения ТП ГСА
Приемы разрешения ТП ГСА Ферромагнитные динамические амортизаторы
Ферромагнитные динамические амортизаторы Технология монтажа и технического обслуживания измерительных приборов
Технология монтажа и технического обслуживания измерительных приборов Тормозной путь
Тормозной путь Дискретные случайные процессы (тема 7)
Дискретные случайные процессы (тема 7) Экспериментальное решение проблемы течи гидроблока МТА
Экспериментальное решение проблемы течи гидроблока МТА Ветровой электрогенератор challenergy
Ветровой электрогенератор challenergy Теория механизмов и машин. Лекция 6
Теория механизмов и машин. Лекция 6 Работа совершаемая при термодинамических процессах. Количество теплоты. Теплоемкость
Работа совершаемая при термодинамических процессах. Количество теплоты. Теплоемкость Строение твердых тел, жидкостей и газов
Строение твердых тел, жидкостей и газов Графическое представление физического процесса - функция
Графическое представление физического процесса - функция Делимость электрического заряда
Делимость электрического заряда ИГЭС 2 семестр-Волны Лекция 2
ИГЭС 2 семестр-Волны Лекция 2 Найважливіші відкриття Ніколи Тесли
Найважливіші відкриття Ніколи Тесли Последовательное соединение проводников
Последовательное соединение проводников Дисперсия света
Дисперсия света Механические колебания и волны
Механические колебания и волны Понятие смены скорости - ось. Модели расширения и сужения
Понятие смены скорости - ось. Модели расширения и сужения Астрофизика итоги. 2021г
Астрофизика итоги. 2021г Изобретения радио А.С. Поповым
Изобретения радио А.С. Поповым Механические передачи
Механические передачи Исследование процесса образования ядер капель и кристаллов в атмосфере. Лабораторная работа №2
Исследование процесса образования ядер капель и кристаллов в атмосфере. Лабораторная работа №2 Электрический ток в металлах. Электрический ток в полупроводниках
Электрический ток в металлах. Электрический ток в полупроводниках Отчет о прохождении производственной практики
Отчет о прохождении производственной практики Способы изменения внутренней энергии
Способы изменения внутренней энергии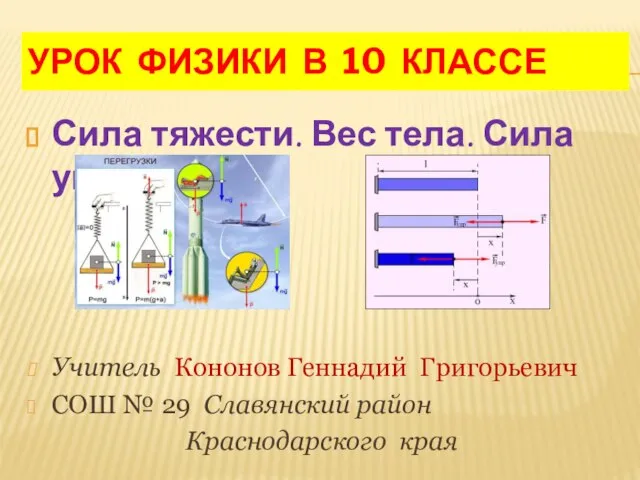 Презентация на тему Сила тяжести. Вес тела. Сила упругости
Презентация на тему Сила тяжести. Вес тела. Сила упругости