Слайд 2УРАВНЕНИЕ СОСТОЯНИЯ ИДЕАЛЬНОГО ГАЗА.
Состояние данной массы газа характеризуется тремя макроскопическими параметрами:
Давлением

p,
Объемом V,
Температурой T.
Слайд 3уравнение состояния
Уравнение состояния идеального газа
= 8,31 Дж/моль*К

Слайд 4
- универсальная газовая постоянная
- молекулярная масса
- масса молекулы

- давление
- объем
-температура
Слайд 5ГАЗОВЫЕ ЗАКОНЫ
С помощью уравнения состояния идеального
газа можно исследовать процессы, в которых

масса газа и один из трех параметров –давление,
объем или температура – остается неизменными.
Количественные зависимости между двумя
параметрами газа при фиксированном значении
третьего параметра называют газовыми
законами.
Слайд 6изопроцессы
Процессы, протекающие при неизменном
значении одного из параметров, называют
изопроцессами.
Изопроцесс – это

идеализированная
Модель реального процесса, которая
Только приближенно отражает
действительность.
Слайд 7Существует три вида изопроцессов
Изотермический
Изобарный
Изохорный

Слайд 8Изотермический процесс
Процесс изменения состояния термодинамической системы макроскопических тел при постоянной температуре называют

изотермическими.
Согласно уравнению состояния идеального газа в любом состоянии с неизменной температурой произведение давления газа на его объем остается постоянным:
Слайд 9Закон Бойля-Мариотта
при
Для газа данной массы произведение давление газа на

его объем постоянно, если температура газа не меняется.
Слайд 10График изотермы
Зависимость давления газа от объема при постоянной температуре графически изображается
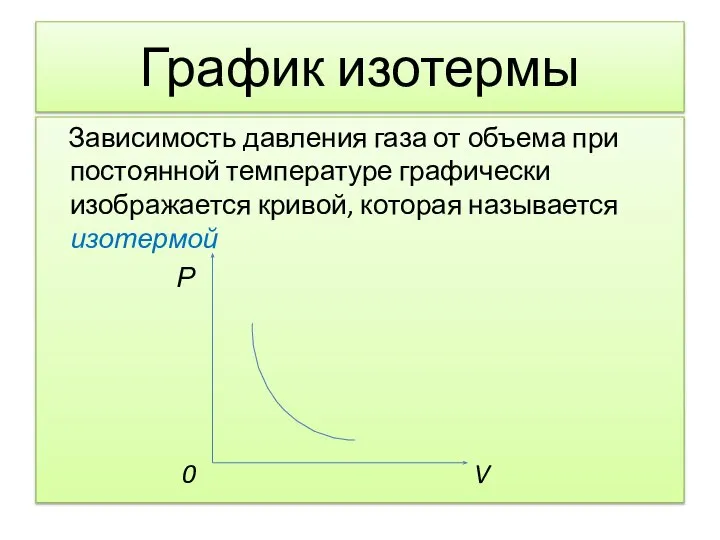
кривой, которая называется изотермой
Р
0 V
Слайд 11Изобарный процесс
Процесс изменения состояния термодинамической системы при постоянном давлении называют изобарным.
Согласно уравнению

в любом состоянии газа с неизменным давлением отношение объема газа к его температуре остается постоянным:
Слайд 12Закон Гей-Люссака
при
Для газа данной массы отношение объема к температуре постоянно, если

давление газа не меняется.
Слайд 13График изобары
Зависимость объема от температуры при постоянной давлении изображается прямой, которая
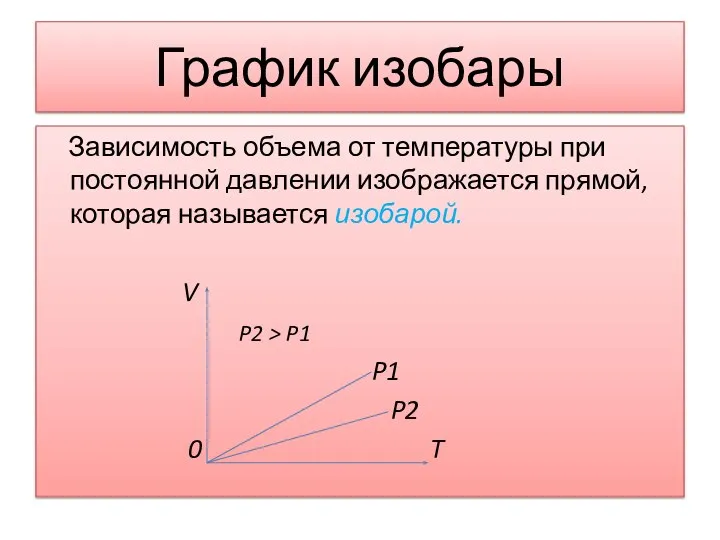
называется изобарой.
V
P2 > P1
P1
P2
0 T
Слайд 14Изохорный процесс
Процесс изменения состояния термодинамической системы при постоянном объеме называют изохорным.
Из

уравнения состояния вытекает, что в любом состоянии газа с неизменным объемом отношение давления газа к его температуре остается постоянным:
Слайд 15Закон Шарля
при
Для газа данной массы отношение давления к температуре постоянно, если

объем не меняется.














 Гравитационное взаимодействие
Гравитационное взаимодействие Работа. Энергия. 8 класс
Работа. Энергия. 8 класс Законы сохранения в механике. Решение задач
Законы сохранения в механике. Решение задач Плоская система пар сил и условие её равновесия
Плоская система пар сил и условие её равновесия Вычислительная теплофизика. Лекция 1 [2]
Вычислительная теплофизика. Лекция 1 [2] Презентация на тему Ультрафиолетовые лучи
Презентация на тему Ультрафиолетовые лучи  Система обнаружения и блокировки излучения радиосигнала
Система обнаружения и блокировки излучения радиосигнала Презентация на тему Решение задач по теме «Фотоэффект»
Презентация на тему Решение задач по теме «Фотоэффект»  Электризация в быту
Электризация в быту Механічні властивості матеріалів при розтяганні і стисканні. Лекція № 4
Механічні властивості матеріалів при розтяганні і стисканні. Лекція № 4 Тема 5. Нормирование шер-ти поверх-ти, точности формы и расположение поверх-й
Тема 5. Нормирование шер-ти поверх-ти, точности формы и расположение поверх-й Микроволновая химия. Часть 1
Микроволновая химия. Часть 1 Световые кольца. Лазер
Световые кольца. Лазер Атомно-абсорбционные методы. АSS
Атомно-абсорбционные методы. АSS Электромагнитные явления
Электромагнитные явления Физическая величина
Физическая величина Движение по окружности. Решение задач
Движение по окружности. Решение задач Законы сохранения энергии и импульса
Законы сохранения энергии и импульса Механические волны
Механические волны Понятие о машине и механизме
Понятие о машине и механизме Равноуск. движение
Равноуск. движение Законы Ньютона. Закон всемирного тяготения
Законы Ньютона. Закон всемирного тяготения Электронный нос или что может заменить нос собаки
Электронный нос или что может заменить нос собаки Помпаж. Способы повышения запасов ГДЛУ (борьба с помпажом)
Помпаж. Способы повышения запасов ГДЛУ (борьба с помпажом) Накопление механической энергии
Накопление механической энергии Количество теплоты, обобщающий урок-практикум, 8, 10 класс
Количество теплоты, обобщающий урок-практикум, 8, 10 класс Геометрическая оптика. Свет. Источники света
Геометрическая оптика. Свет. Источники света Электроемкость, конденсаторы
Электроемкость, конденсаторы