Содержание
- 2. Основные пути биотрансформации чужеродных соединений. 1. Окисление: а) микросомальное – алифатичекое или ароматическое гидроксилирование, – эпоксидирование,
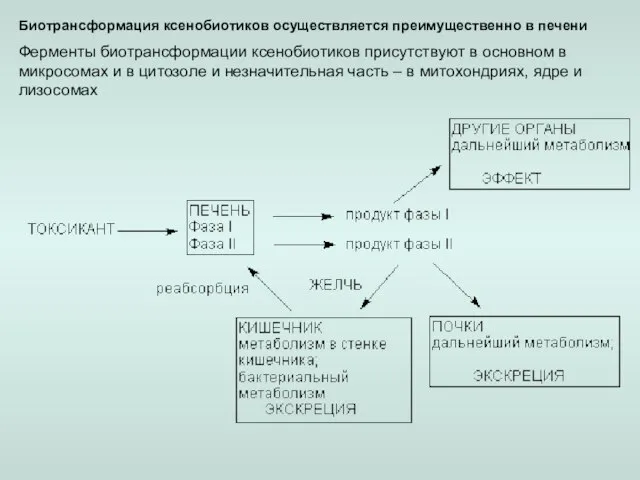
- 3. Биотрансформация ксенобиотиков осуществляется преимущественно в печени Ферменты биотрансформации ксенобиотиков присутствуют в основном в микросомах и в
- 4. Ферментативные реакции 1-й фазы биотрансформации ксенобиотиков карбоксилэстераза, ацетилхолинэстераза псевдохолинэстераза эпоксидная гидролаза 1. Гидролиз при биотрансформации X
- 5. 2. Восстановление при биотрансформации Некоторые металлы альдегиды, кетоны, дисульфиды, сульфоксиды, хиноны, алкены, азо- и нитросоединеня Коферменты
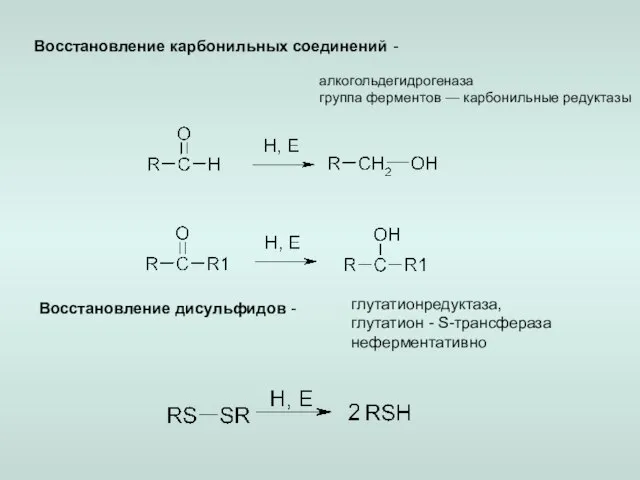
- 6. Восстановление карбонильных соединений - алкогольдегидрогеназа группа ферментов — карбонильные редуктазы Восстановление дисульфидов - глутатионредуктаза, глутатион -
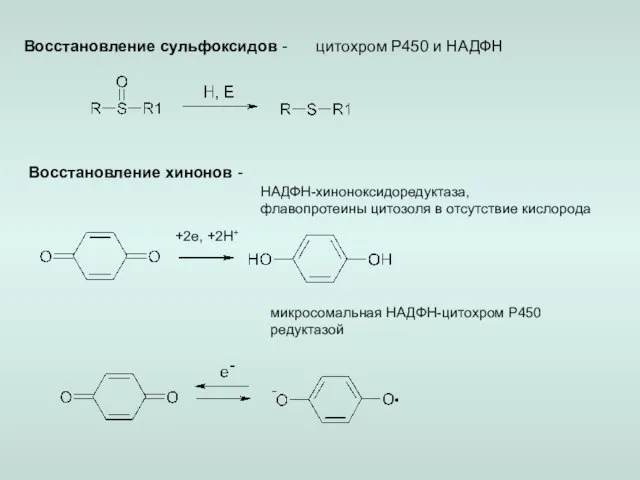
- 7. Восстановление сульфоксидов - цитохром Р450 и НАДФН Восстановление хинонов - +2e, +2H+ НАДФН-хиноноксидоредуктаза, флавопротеины цитозоля в
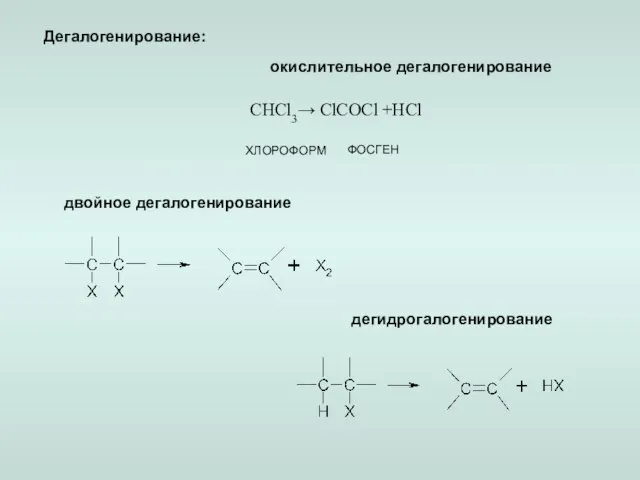
- 8. Дегалогенирование: окислительное дегалогенирование двойное дегалогенирование дегидрогалогенирование ХЛОРОФОРМ ФОСГЕН CHCl3→ ClCOCl +HCl
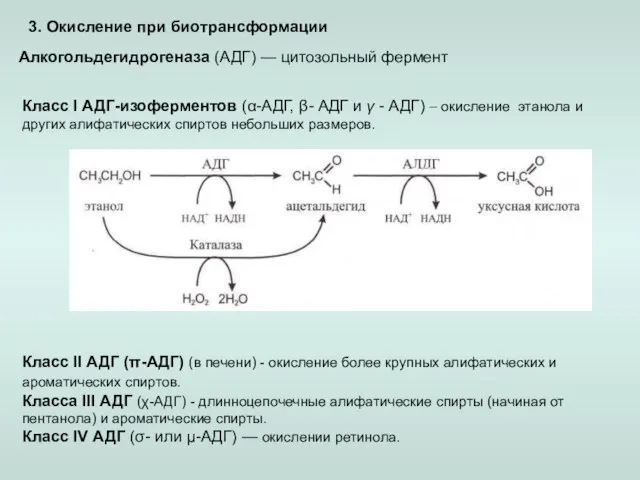
- 9. 3. Окисление при биотрансформации Алкогольдегидрогеназа (АДГ) — цитозольный фермент Класс I АДГ-изоферментов (α-АДГ, β- АДГ и
- 10. Альдегид-дегидрогеназа (АЛДГ) - окислении альдегидов до карбоновых кислот (кофактор НАД+). Дигидродиолдегидрогеназа - окисление полициклических ароматических углеводородов.
- 11. Пероксидаза-зависимое окисление превращение ксенобиотиков в токсичные метаболиты прямой перенос пероксидного кислорода к ксенобиотику Тох → ТохО
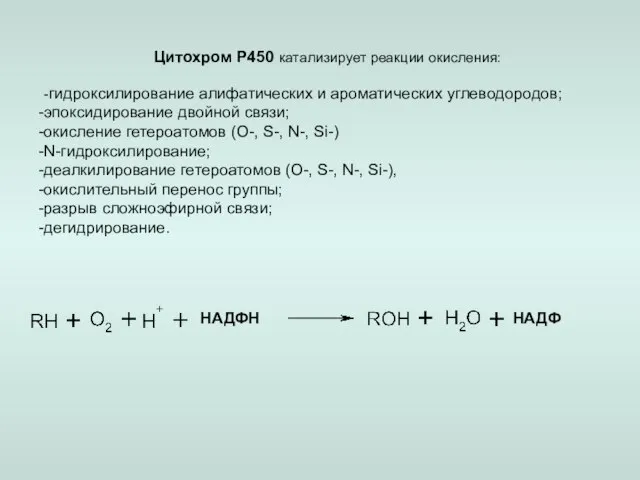
- 12. Цитохром Р450 катализирует реакции окисления: -гидроксилирование алифатических и ароматических углеводородов; эпоксидирование двойной связи; окисление гетероатомов (О-,
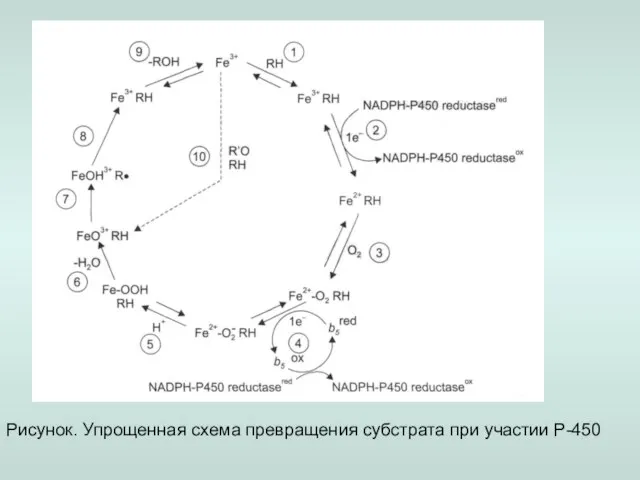
- 13. Рисунок. Упрощенная схема превращения субстрата при участии Р-450
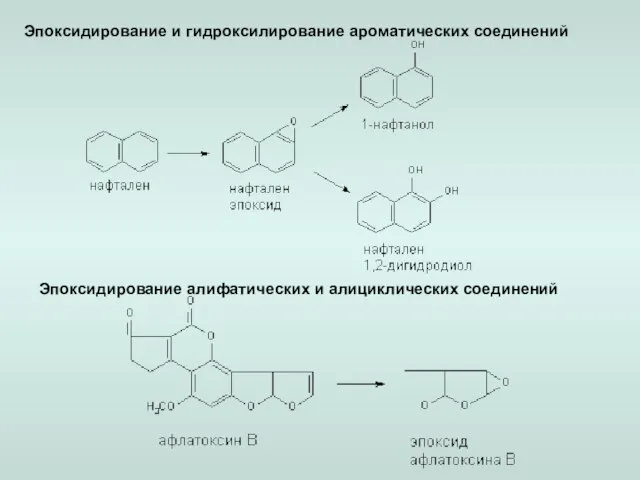
- 14. Эпоксидирование и гидроксилирование ароматических соединений Эпоксидирование алифатических и алициклических соединений
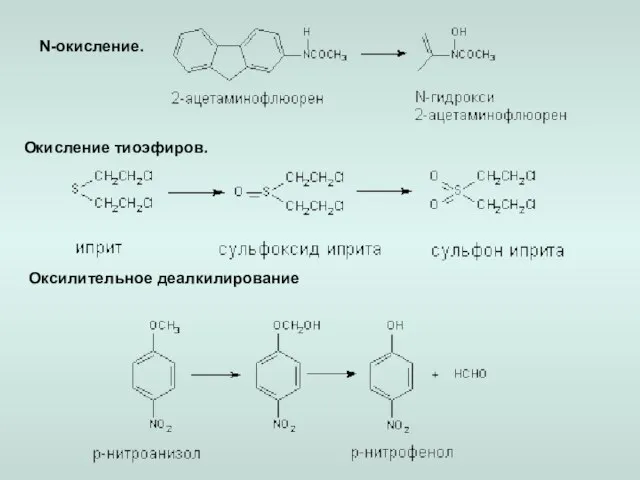
- 15. N-окисление. Оксилительное деалкилирование Окисление тиоэфиров.
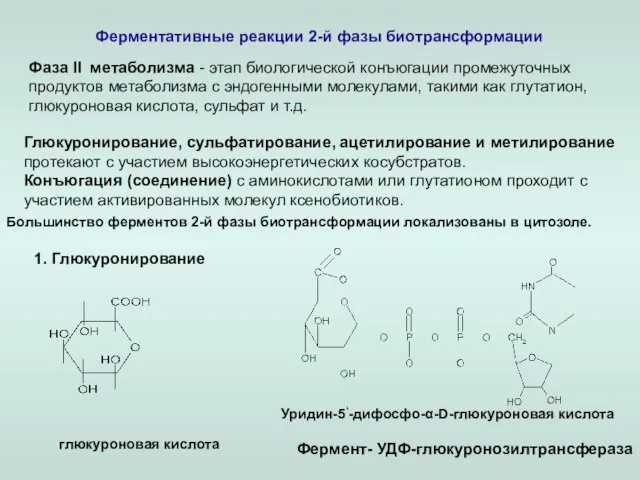
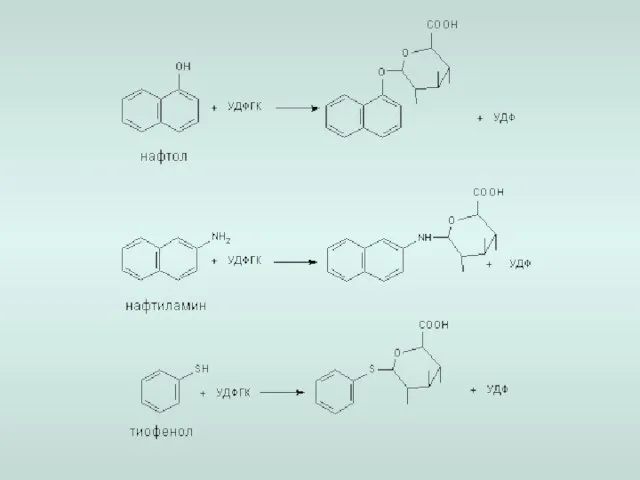
- 16. Ферментативные реакции 2-й фазы биотрансформации Фаза ll метаболизма - этап биологической конъюгации промежуточных продуктов метаболизма с
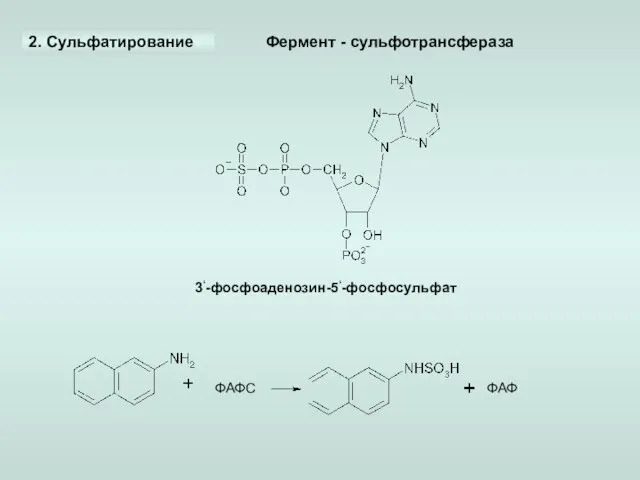
- 18. 2. Сульфатирование 3‘-фосфоаденозин-5‘-фосфосульфат ФАФС ФАФ Фермент - сульфотрансфераза
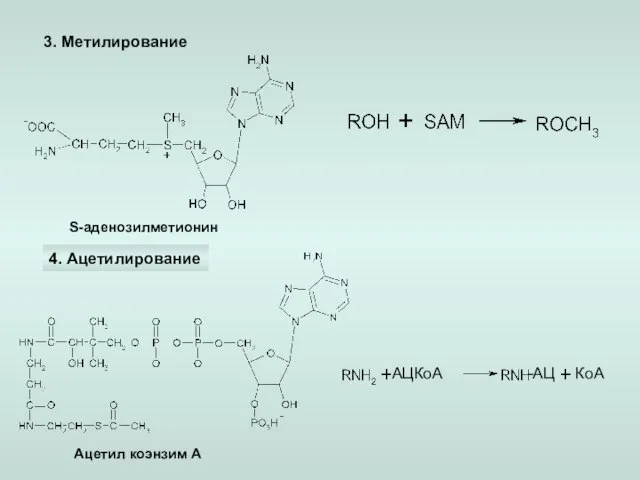
- 19. 3. Метилирование 4. Ацетилирование S-аденозилметионин Ацетил коэнзим А КоА АЦКоА -АЦ
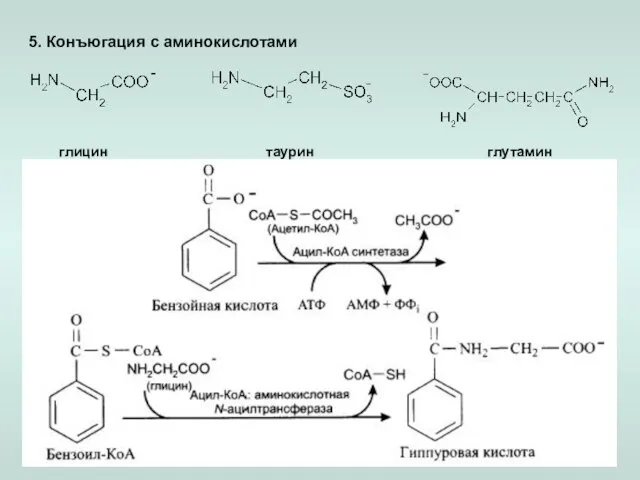
- 20. 5. Конъюгация с аминокислотами глицин таурин глутамин
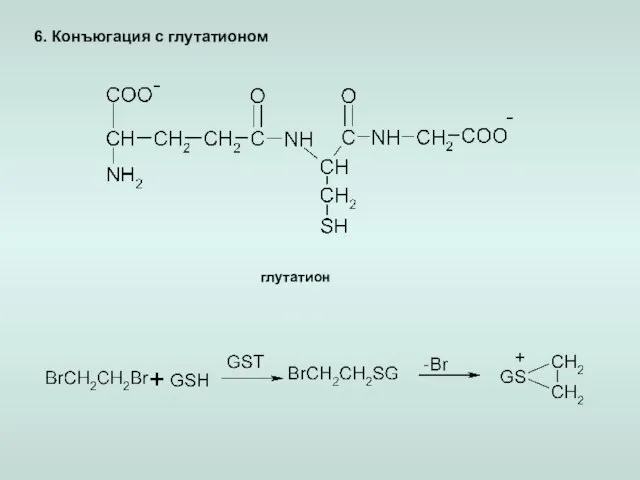
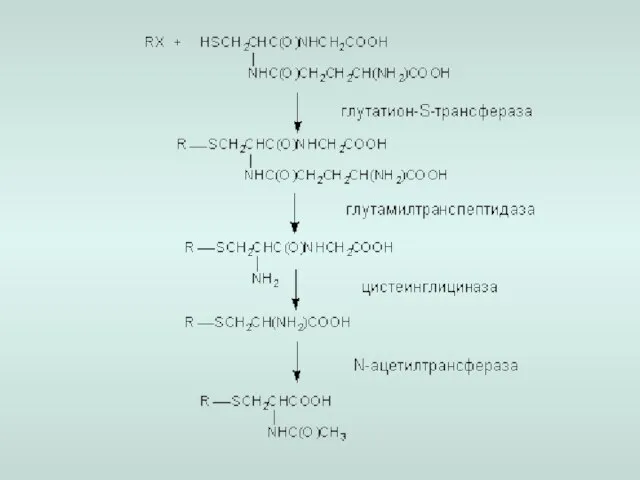
- 21. 6. Конъюгация с глутатионом глутатион
- 24. Скачать презентацию





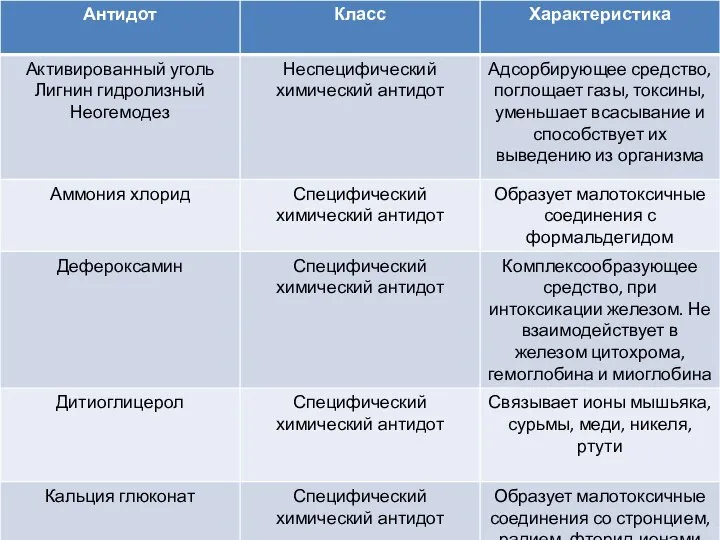 Антидоты. Класс. Характеристика
Антидоты. Класс. Характеристика valentnost
valentnost Обобщить и систематизировать знания учащихся о кислотах неорганических и органических, о их составе и свойствах
Обобщить и систематизировать знания учащихся о кислотах неорганических и органических, о их составе и свойствах Презентации 1 строение атома
Презентации 1 строение атома Наноматеріали. Тіт Лукрецій Кар
Наноматеріали. Тіт Лукрецій Кар Решение задач
Решение задач Bioenergetyka syntezy glutaminy
Bioenergetyka syntezy glutaminy Белки-1 2020
Белки-1 2020 Презентация на тему Коррозия
Презентация на тему Коррозия  Классификация и номенклатура ОС
Классификация и номенклатура ОС Электролитическая диссоциация
Электролитическая диссоциация Изменение химмотологических свойств цетанповышающей присадки в процессе хранения
Изменение химмотологических свойств цетанповышающей присадки в процессе хранения Homecredit Bank. Показатели и зоны роста
Homecredit Bank. Показатели и зоны роста Типы кристаллических решёток
Типы кристаллических решёток Алюминий
Алюминий Натрий, свойства атома, химические и физические свойства
Натрий, свойства атома, химические и физические свойства Определение Кофеина в Кофе
Определение Кофеина в Кофе Углеводороды. Алканы
Углеводороды. Алканы Изучение адсорбции аминокислот на поверхности гидроксилапатита при варьировании рН
Изучение адсорбции аминокислот на поверхности гидроксилапатита при варьировании рН Каучук негізіндегі материалдар
Каучук негізіндегі материалдар минералы_4_блеск
минералы_4_блеск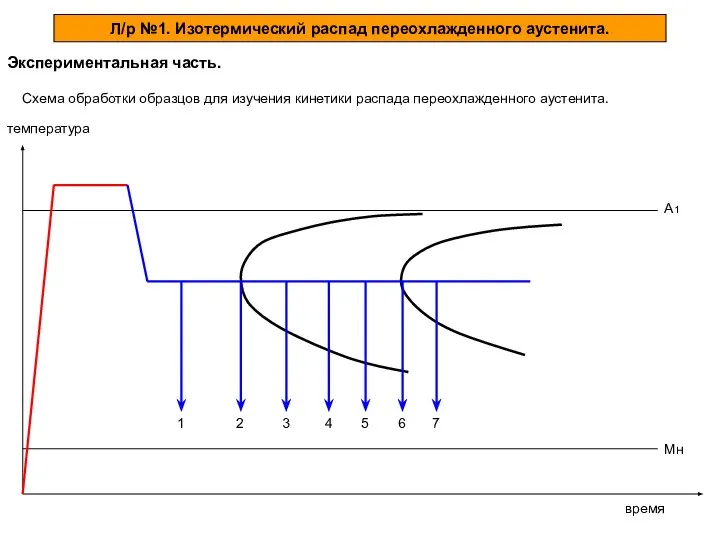 Изотермический распад переохлажденного аустенита. Экспериментальная часть
Изотермический распад переохлажденного аустенита. Экспериментальная часть Скорость протекания химических реакций
Скорость протекания химических реакций Составление формул по валентности. Понятие
Составление формул по валентности. Понятие Презентация на тему Гидролиз солей
Презентация на тему Гидролиз солей  Металлы
Металлы Адсорбция. Механизмы адсорбции. Термодинамика адсорбции. Лекция 5
Адсорбция. Механизмы адсорбции. Термодинамика адсорбции. Лекция 5 Вода-растворитель. Растворы
Вода-растворитель. Растворы