Содержание
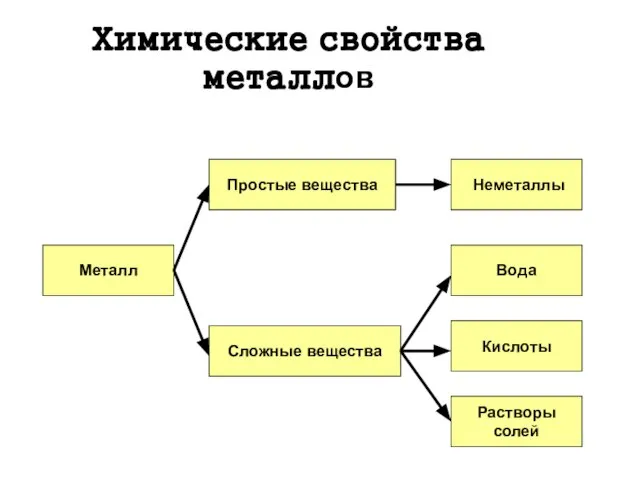
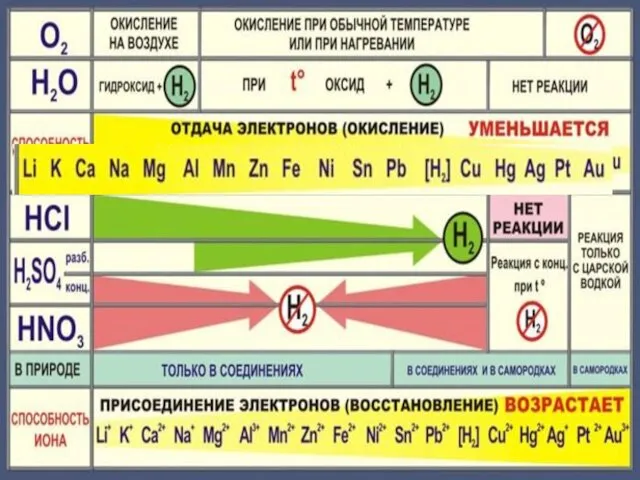
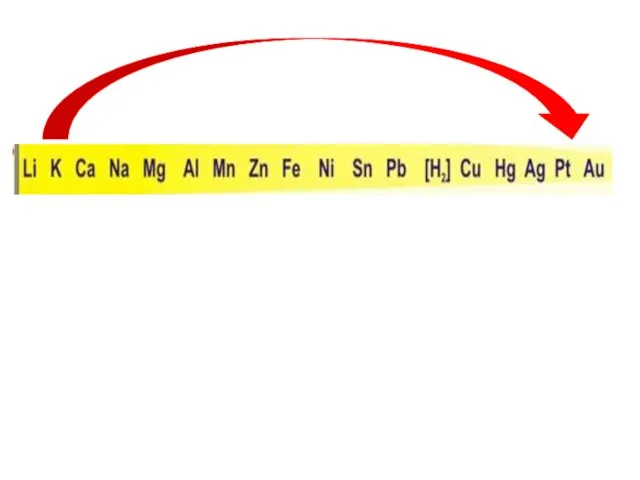
- 5. Химические свойства металлов Металл Простые вещества Сложные вещества Неметаллы Вода Кислоты Растворы солей
- 6. Cu + Cl2 =CuCl2 2Mg + CO2 = 2MgO + C С неметаллами С кислотными оксидами
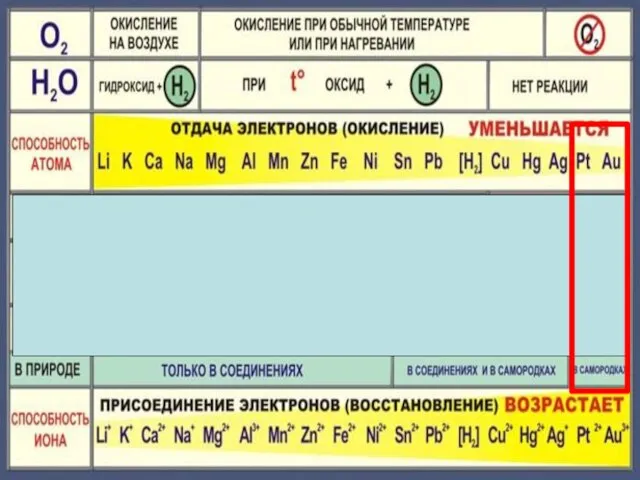
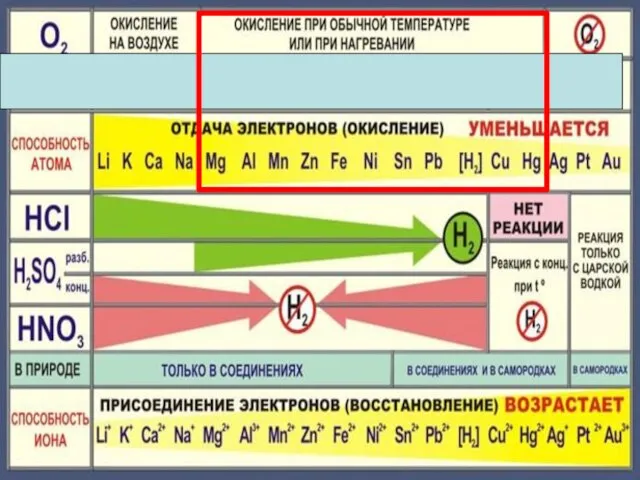
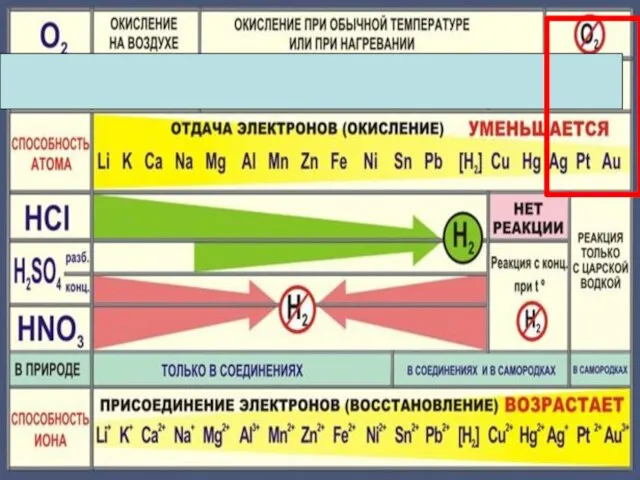
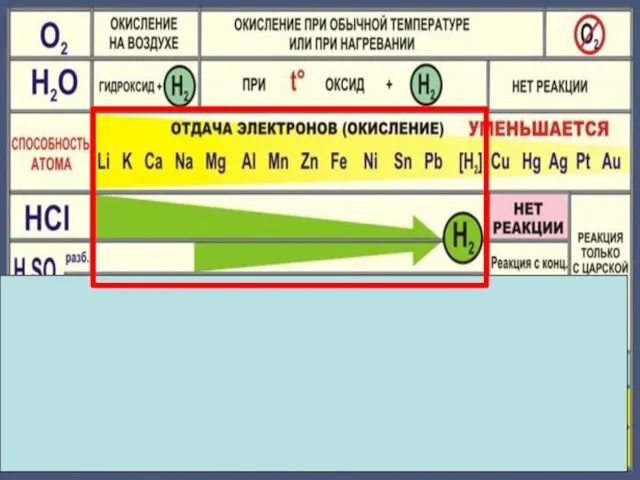
- 10. 4Na + O2 = 2Na2O 2Mg + O2 = 2MgO при нагревании 4Ag + O2 =
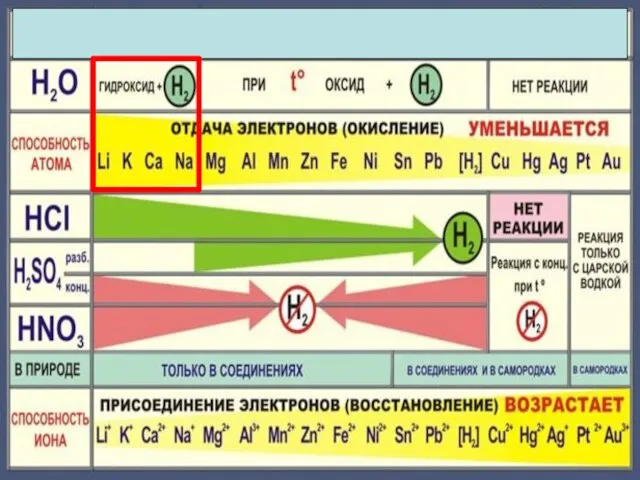
- 12. 2Na + 2H2O ? 2NaOH +H2 2K + 2H2O = 2KOH + H2
- 14. 3Fe + 4H2O = Fe3O4+4 H2
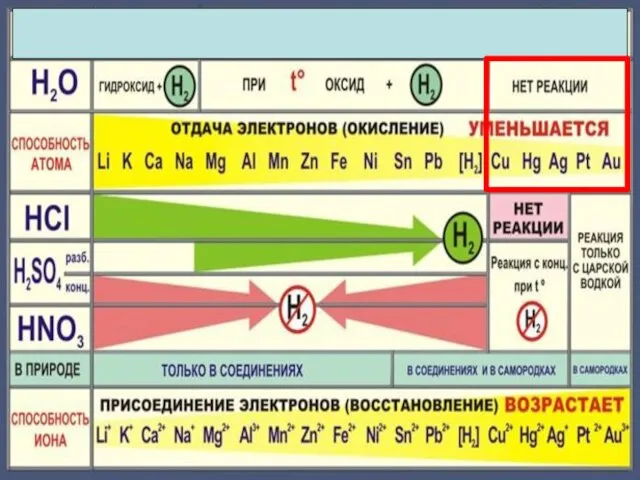
- 16. Cu + H2О = реакция не идет
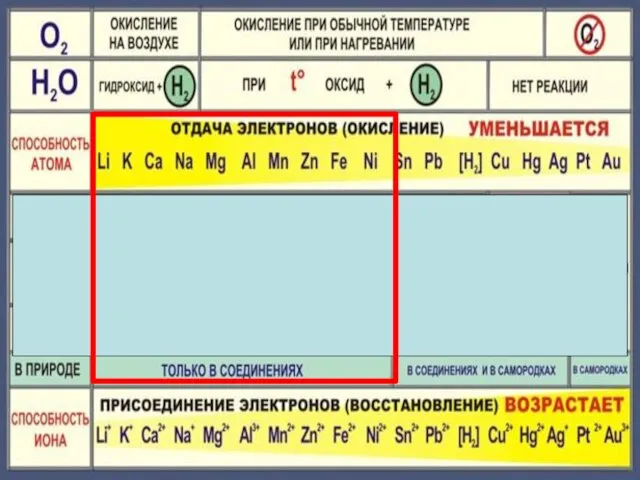
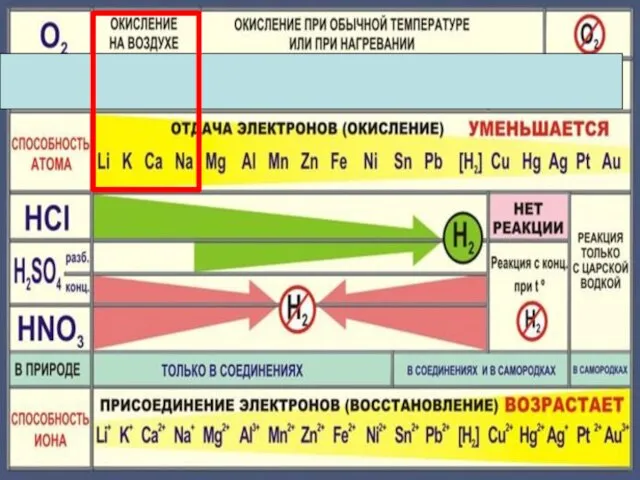
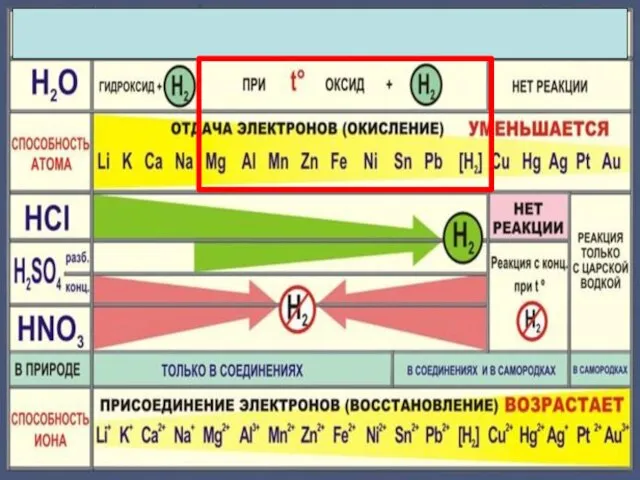
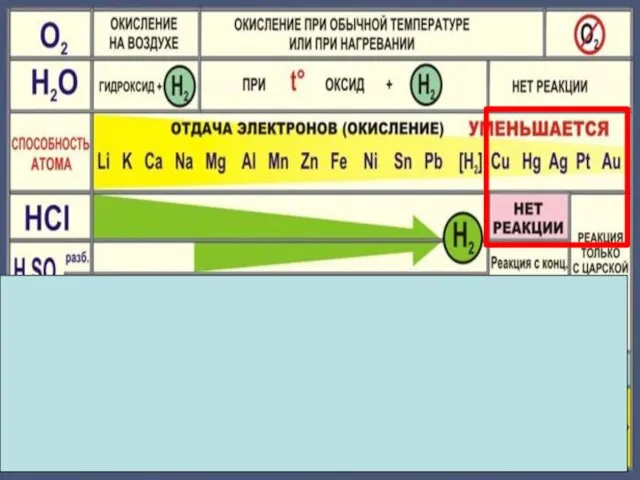
- 18. Zn + 2HCl = ZnCl2 + H2 Fe + 2HCl = FeCl2 + H2 Cu +
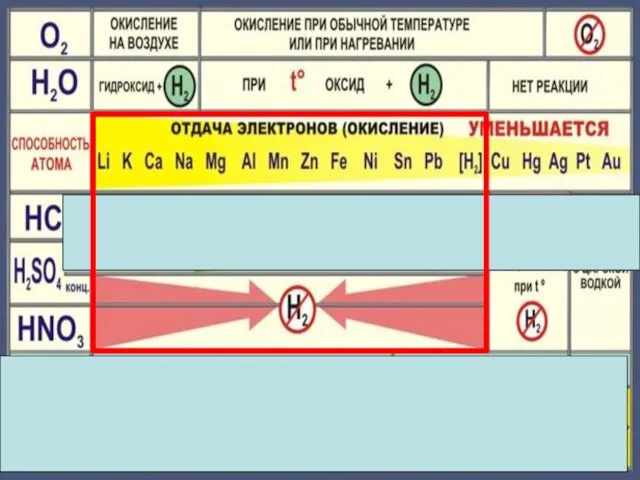
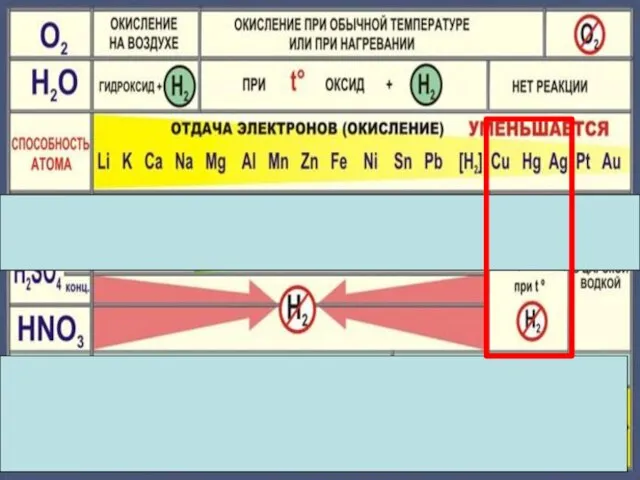
- 22. Cu + 2H2 SO4конц. = Cu SO4 +SO2 +2H2 O Cu + 4HNO3 конц. = Cu(NO3)2
- 23. Состав «царской водки»: смесь концентрированных азотной HNO3 (65-68 % масс.) и соляной HCl (32-35 % масс.)
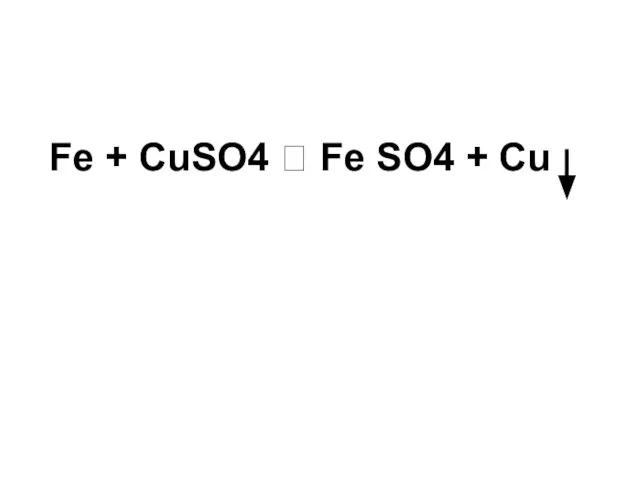
- 26. Fe + CuSO4 ? Fe SO4 + Cu
- 28. Скачать презентацию



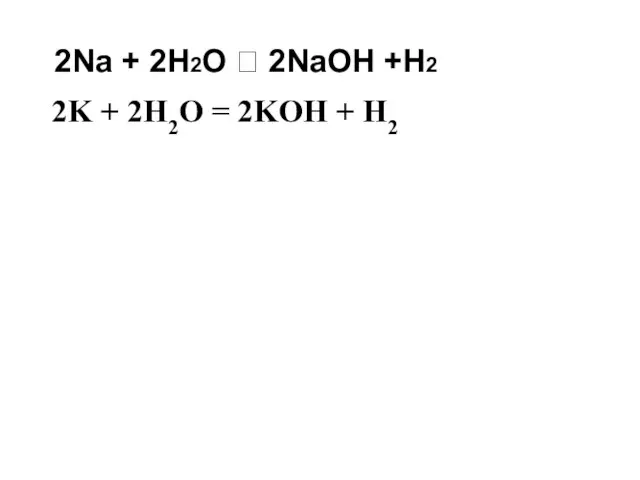


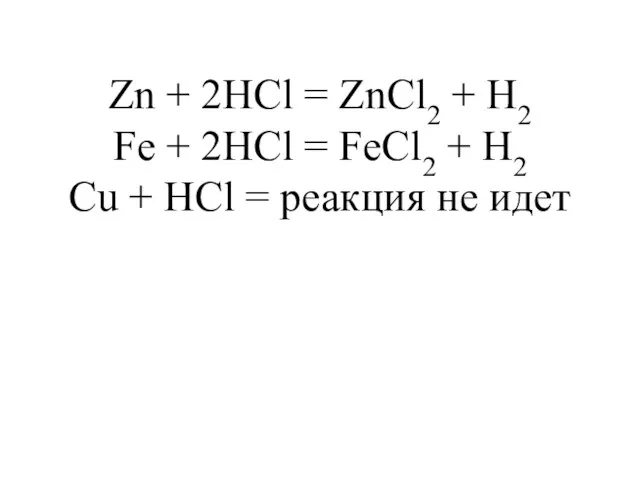
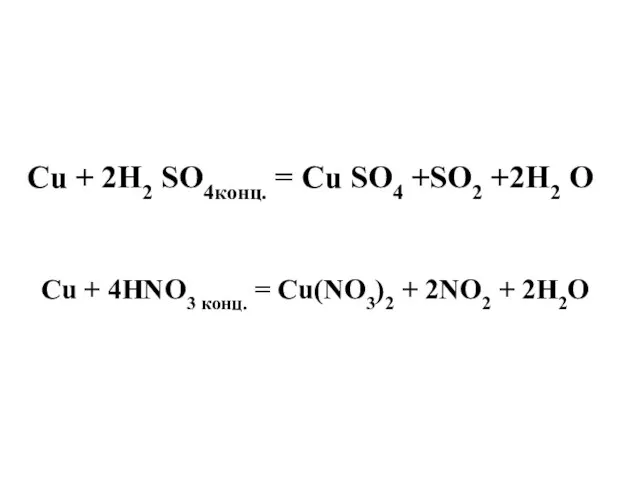

 Цианоакрилатовая камера для выявления жировых следов
Цианоакрилатовая камера для выявления жировых следов Кислоты. состав, номенклатура и их их классификация
Кислоты. состав, номенклатура и их их классификация Судьба углеродного скелета аминокислот
Судьба углеродного скелета аминокислот Строение атома
Строение атома Техника безопасности при использовании различных видов топлива. Практическая работа № 3
Техника безопасности при использовании различных видов топлива. Практическая работа № 3 Общие свойства неметаллов
Общие свойства неметаллов Пиримидин (шестичленный гетероцикл с двумя атомами азота)
Пиримидин (шестичленный гетероцикл с двумя атомами азота) Презентация на тему Соли: свойства, получение, применение (8 класс)
Презентация на тему Соли: свойства, получение, применение (8 класс)  Презентация на тему Применение кислорода
Презентация на тему Применение кислорода  Презентация на тему Кремний в природе
Презентация на тему Кремний в природе  Неорганические вещества
Неорганические вещества Окислительно-восстановительные реакции
Окислительно-восстановительные реакции Презентация на тему Жиры, их строение и свойства
Презентация на тему Жиры, их строение и свойства  Horenie
Horenie Основания. 8 класс
Основания. 8 класс Ионная связь
Ионная связь Презентация по Химии "Строении атомов. Химическая связь"
Презентация по Химии "Строении атомов. Химическая связь"  Виды нагрева и материалы резистивных нагревателей, их стойкость к температуре, ростовой атмосфере и расплаву
Виды нагрева и материалы резистивных нагревателей, их стойкость к температуре, ростовой атмосфере и расплаву Галогены. Элементы главной подгруппы 7 группы Периодической системы Менделеева
Галогены. Элементы главной подгруппы 7 группы Периодической системы Менделеева Простые вещества - неметаллы
Простые вещества - неметаллы Пропи́н (метилацетилен, аллилен)
Пропи́н (метилацетилен, аллилен) Практическая работа №5. Качественные реакции на анионы 1-3 групп
Практическая работа №5. Качественные реакции на анионы 1-3 групп Кислоты основания и соли как электролиты
Кислоты основания и соли как электролиты Тотығу - тотықсыздану реакциясы
Тотығу - тотықсыздану реакциясы Физико-химические свойства растворов ВМС
Физико-химические свойства растворов ВМС Учитель химии МАОУ СОШ № 61 города Тюмени Белова Н.В.
Учитель химии МАОУ СОШ № 61 города Тюмени Белова Н.В. Основные классы неорганических веществ
Основные классы неорганических веществ Презентация на тему Соли
Презентация на тему Соли