Содержание
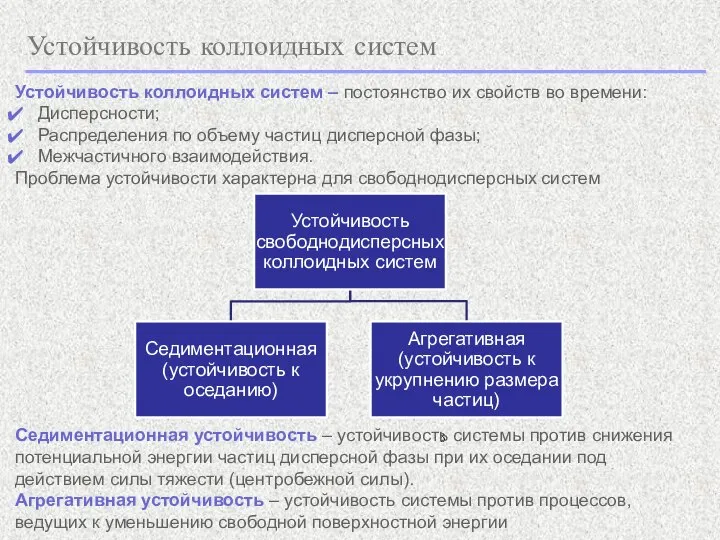
- 2. Устойчивость коллоидных систем Устойчивость коллоидных систем – постоянство их свойств во времени: Дисперсности; Распределения по объему
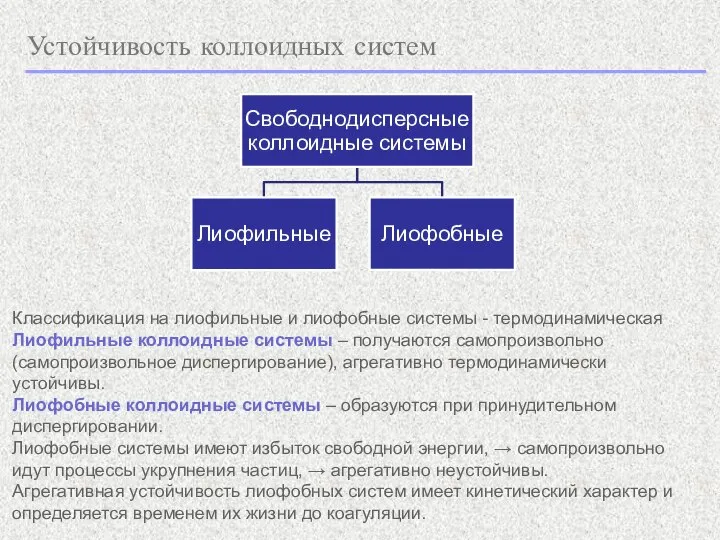
- 3. Устойчивость коллоидных систем Классификация на лиофильные и лиофобные системы - термодинамическая Лиофильные коллоидные системы – получаются
- 4. Лиофильные коллоидные системы Лиофильные коллоидные системы: Растворы ПАВ; Микроэмульсии; Растворы ВМС (???).
- 5. Термодинамика лиофильных систем
- 6. Термодинамика лиофильных систем - условие самопроизвольного диспергирования Если межфазное натяжение достаточно мало, то возможно самопроизвольное отщепление
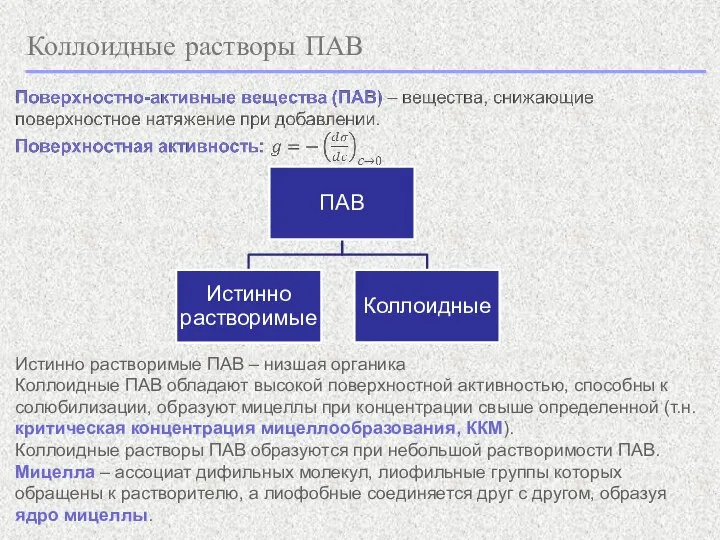
- 7. Коллоидные растворы ПАВ Истинно растворимые ПАВ – низшая органика Коллоидные ПАВ обладают высокой поверхностной активностью, способны
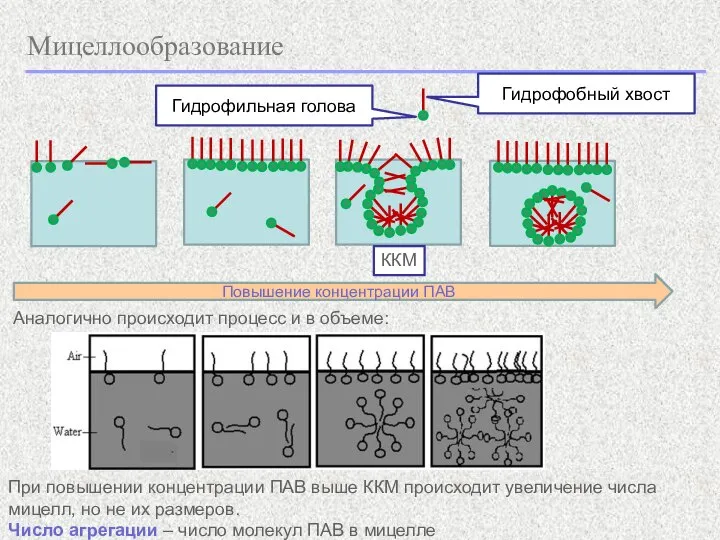
- 8. Мицеллообразование Гидрофобный хвост Гидрофильная голова Повышение концентрации ПАВ ККМ Аналогично происходит процесс и в объеме: При
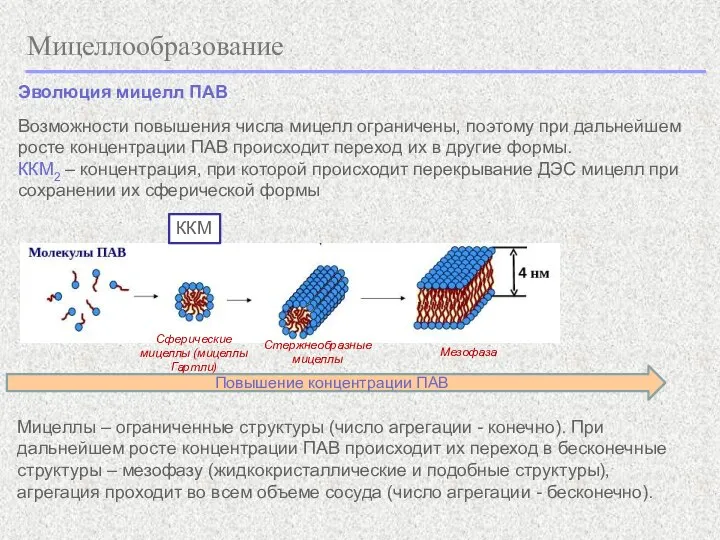
- 9. Мицеллообразование Эволюция мицелл ПАВ Повышение концентрации ПАВ ККМ Сферические мицеллы (мицеллы Гартли) Стержнеобразные мицеллы Мезофаза Возможности
- 10. Мицеллообразование Мицеллобразование в неводных средах В неполярных средах ПАВ не понижают поверхностное натяжение, но мицеллообразование все
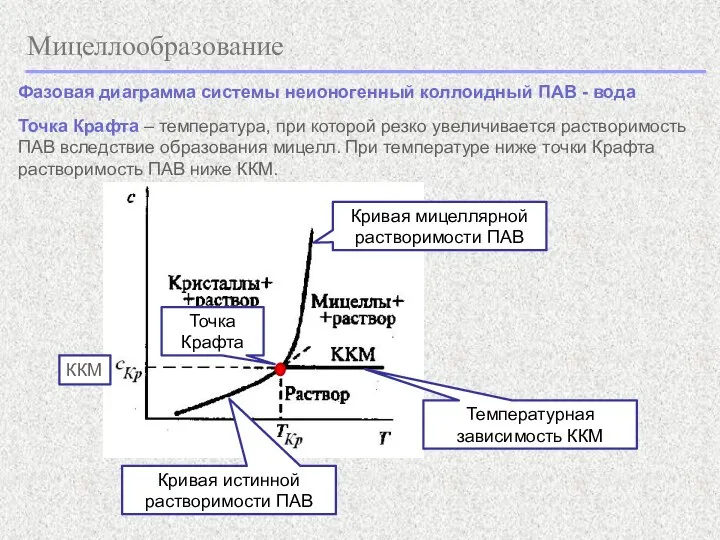
- 11. Мицеллообразование Фазовая диаграмма системы неионогенный коллоидный ПАВ - вода Точка Крафта – температура, при которой резко
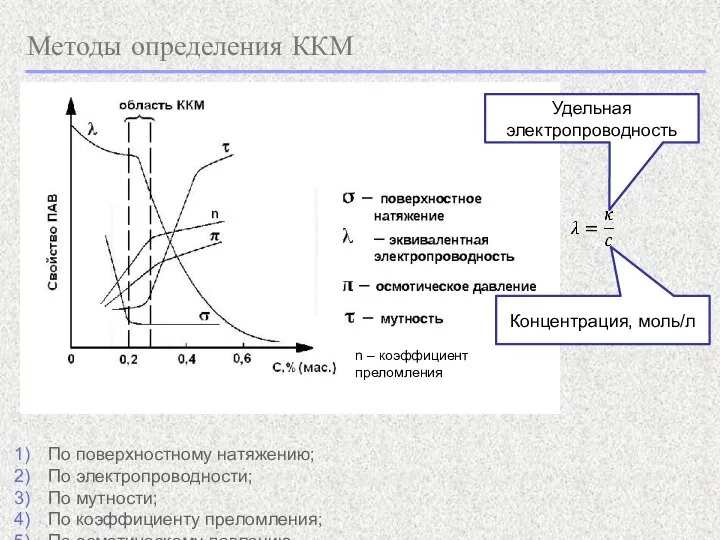
- 12. Методы определения ККМ n – коэффициент преломления По поверхностному натяжению; По электропроводности; По мутности; По коэффициенту
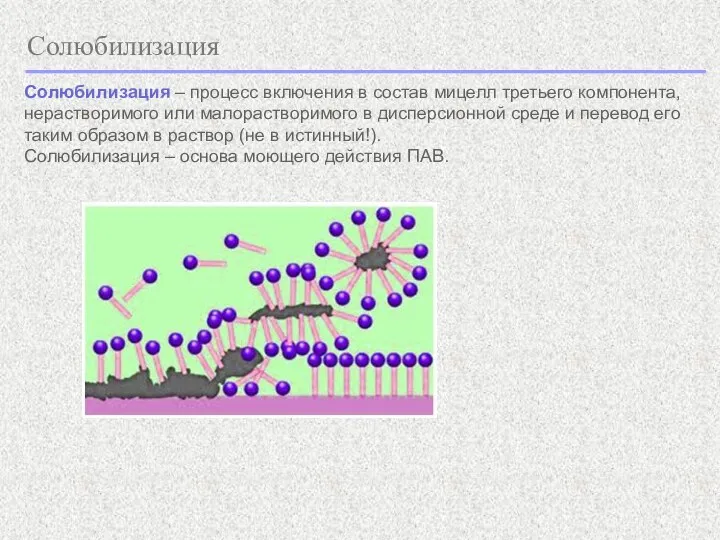
- 13. Солюбилизация Солюбилизация – процесс включения в состав мицелл третьего компонента, нерастворимого или малорастворимого в дисперсионной среде
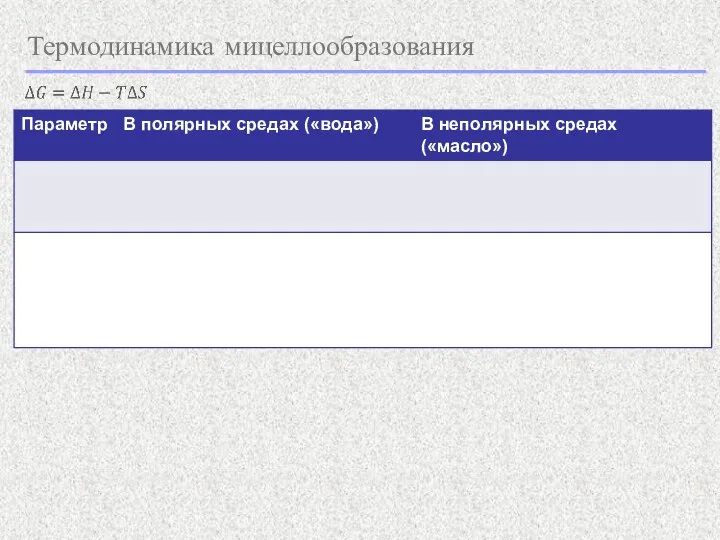
- 14. Термодинамика мицеллообразования
- 15. Термодинамика мицеллообразования Коэффициенты активности
- 16. Термодинамика мицеллообразования
- 17. Химия ПАВ Химическая структура и типы ПАВ
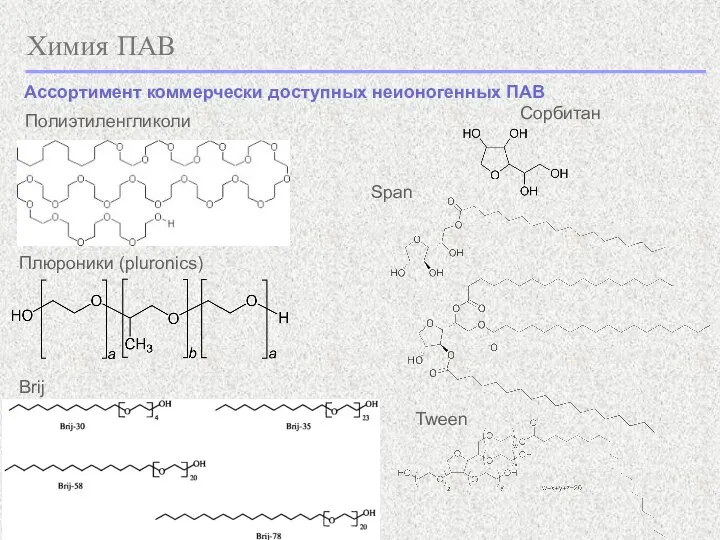
- 18. Химия ПАВ Ассортимент коммерчески доступных неионогенных ПАВ Полиэтиленгликоли Плюроники (pluronics) Brij Сорбитан Span Tween
- 19. Гидрофильно-липофильный баланс Гидрофобность Отношение растворимостей в водной и масляной фазах, коэффициент распределения
- 20. Принципы подбора ПАВ по ГЛБ Правила подбора ПАВ-эмульгатора: ПАВ должно обладать выраженной склонностью мигрировать к межфазной
- 21. Микроэмульсии Различия между эмульсиями и микроэмульсиями - условие самопроизвольного диспергирования
- 23. Скачать презентацию










 Алкины
Алкины Презентация на тему Кристаллическая решетка
Презентация на тему Кристаллическая решетка  Фосфорные удобрения
Фосфорные удобрения Предельные углеводороды (алканы)
Предельные углеводороды (алканы) Substanță chimică
Substanță chimică Уравнение материального баланса технологического процесса. (Лекция 3)
Уравнение материального баланса технологического процесса. (Лекция 3) Ориентация полимеров
Ориентация полимеров Язык естествознания. Химия
Язык естествознания. Химия Коштовне каміння
Коштовне каміння Буферлік жүйелер мен ерітінділер туралы түсініктер, олардың құрамы және жіктелуі
Буферлік жүйелер мен ерітінділер туралы түсініктер, олардың құрамы және жіктелуі Скорость химической реакции
Скорость химической реакции Составитель: Денисова В.Г.
Составитель: Денисова В.Г. Химия и география. Блиц-опрос. 7 класс
Химия и география. Блиц-опрос. 7 класс Метилэтилкетон. Его применение и процесс получения
Метилэтилкетон. Его применение и процесс получения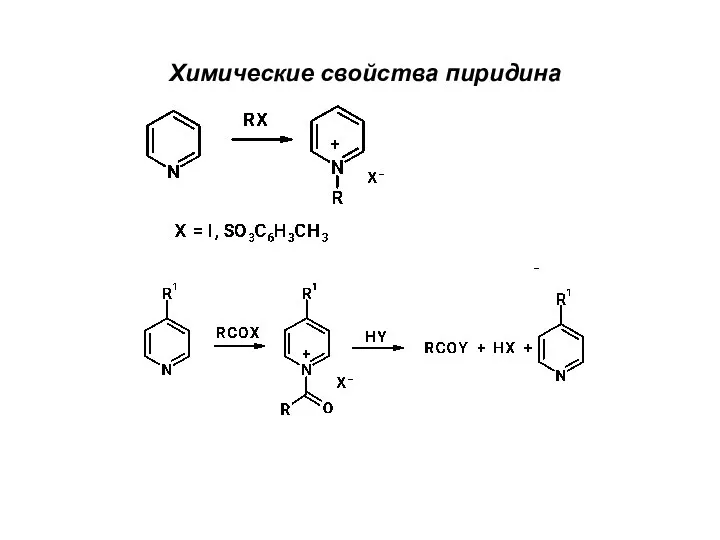 Химические свойства пиридина
Химические свойства пиридина Основные классы неорганических соединений. Общие формулы оксидов, оснований, кислот, солей
Основные классы неорганических соединений. Общие формулы оксидов, оснований, кислот, солей Карбоновые кислоты
Карбоновые кислоты Химический состав клетки
Химический состав клетки Правила ТБ при работе в кабинете химии. Приёмы обращения с лабораторным оборудованием
Правила ТБ при работе в кабинете химии. Приёмы обращения с лабораторным оборудованием Электролитическая диссоциация
Электролитическая диссоциация Характеристика химических элементов IV А группа. Углерод
Характеристика химических элементов IV А группа. Углерод Химическое равновесие и способы его смещения. Принцип Ле Шателье. 9 класс
Химическое равновесие и способы его смещения. Принцип Ле Шателье. 9 класс Активизация познавательной деятельности на уроках химии при работе с МГП (малыми графическими пособиями)
Активизация познавательной деятельности на уроках химии при работе с МГП (малыми графическими пособиями) Тренажер. Типы химических реакций
Тренажер. Типы химических реакций Галогены
Галогены Химическая связь
Химическая связь Неметаллы. Обобщение и систематизация знаний
Неметаллы. Обобщение и систематизация знаний Графит. 9 класс
Графит. 9 класс