Содержание
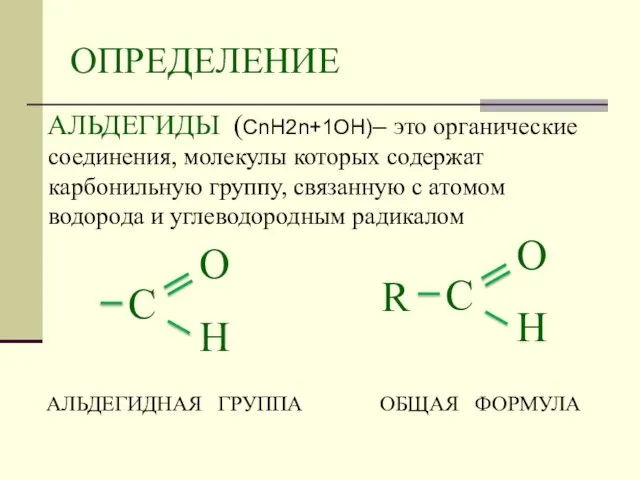
- 2. ОПРЕДЕЛЕНИЕ АЛЬДЕГИДЫ (СnH2n+1OН)– это органические соединения, молекулы которых содержат карбонильную группу, связанную с атомом водорода и
- 3. КЕТОНЫ КЕТОНЫ – органические вещества, в молекулах которых карбонильная группа связана с двумя углеводородными радикалами R1
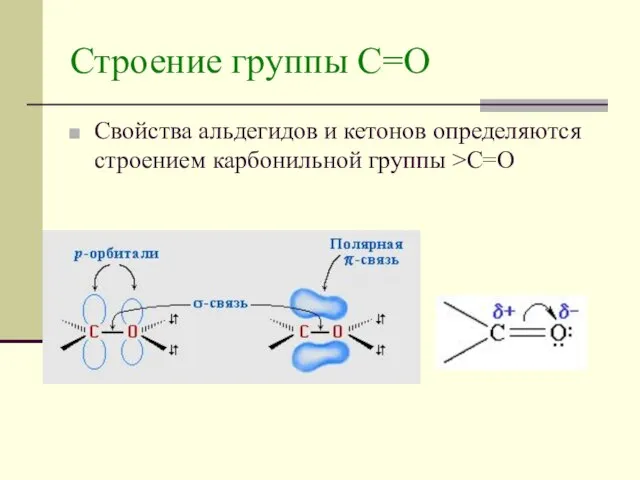
- 4. Строение группы С=О Свойства альдегидов и кетонов определяются строением карбонильной группы >C=O
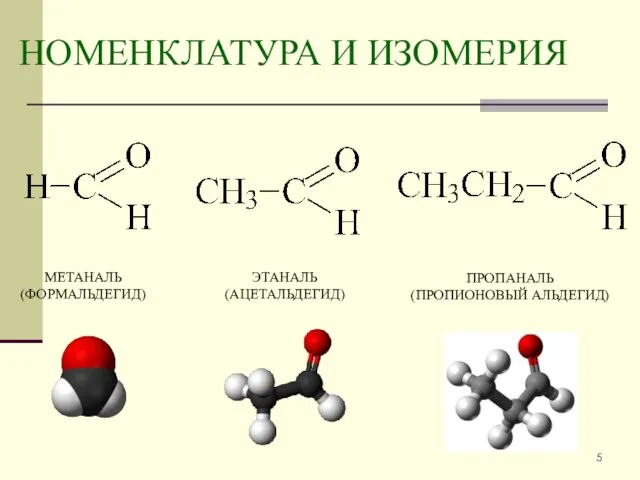
- 5. НОМЕНКЛАТУРА И ИЗОМЕРИЯ МЕТАНАЛЬ (ФОРМАЛЬДЕГИД) ЭТАНАЛЬ (АЦЕТАЛЬДЕГИД) ПРОПАНАЛЬ (ПРОПИОНОВЫЙ АЛЬДЕГИД)
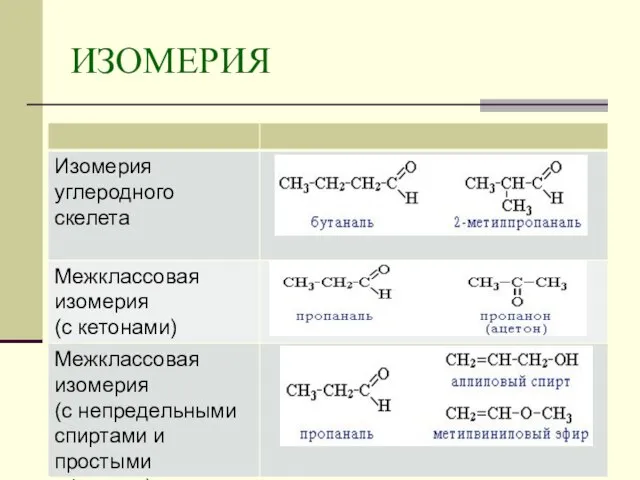
- 6. ИЗОМЕРИЯ
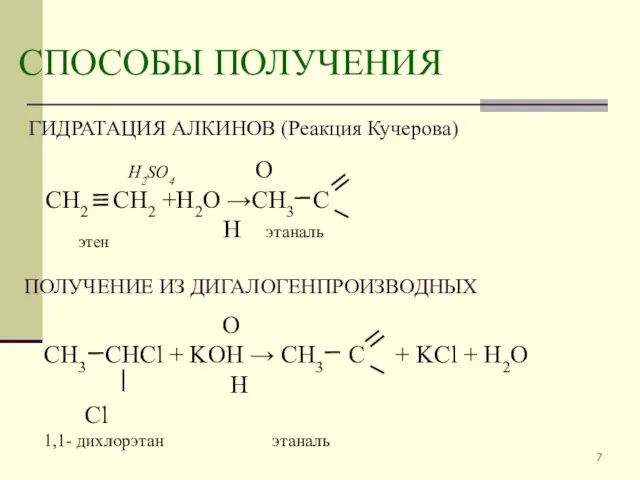
- 7. СПОСОБЫ ПОЛУЧЕНИЯ ГИДРАТАЦИЯ АЛКИНОВ (Реакция Кучерова) ПОЛУЧЕНИЕ ИЗ ДИГАЛОГЕНПРОИЗВОДНЫХ H2SO4 О СН2 СН2 +Н2О →СН3 С
- 8. СПОСОБЫ ПОЛУЧЕНИЯ ДЕГИДРИРОВАНИЕ СПИРТОВ O Cu,t // CH3 – CH2 – CH2 – OH → СH3
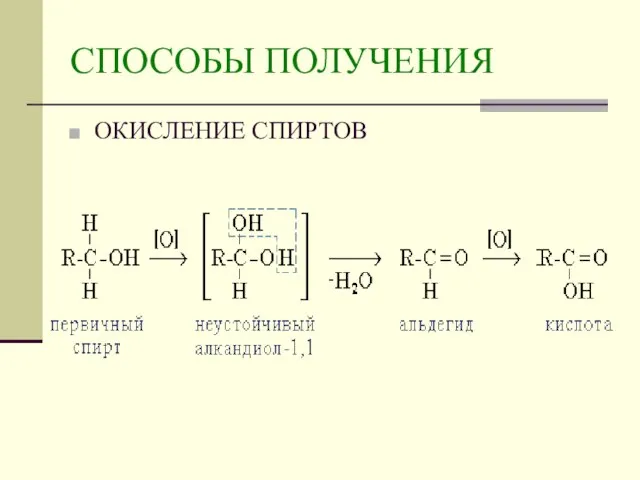
- 9. СПОСОБЫ ПОЛУЧЕНИЯ ОКИСЛЕНИЕ СПИРТОВ
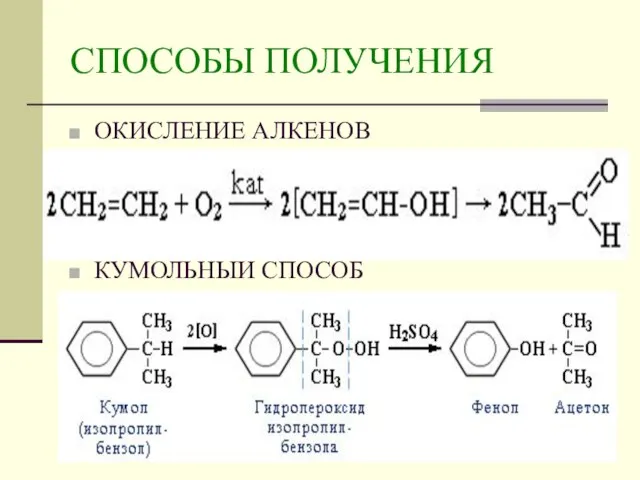
- 10. СПОСОБЫ ПОЛУЧЕНИЯ ОКИСЛЕНИЕ АЛКЕНОВ КУМОЛЬНЫЙ СПОСОБ
- 11. ХИМИЧЕСКИЕ СВОЙСТВА РЕАКЦИИ ОКИСЛЕНИЯ Реакция серебряного зеркала О О СН3 С + 2[Ag(NH3)2]OH → СН3 С
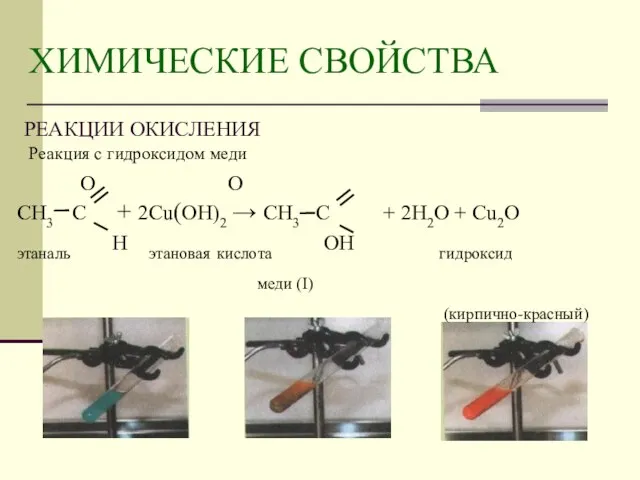
- 12. Реакция с гидроксидом меди О О СН3 С + 2Cu(OH)2 → СН3 С + 2H2O +
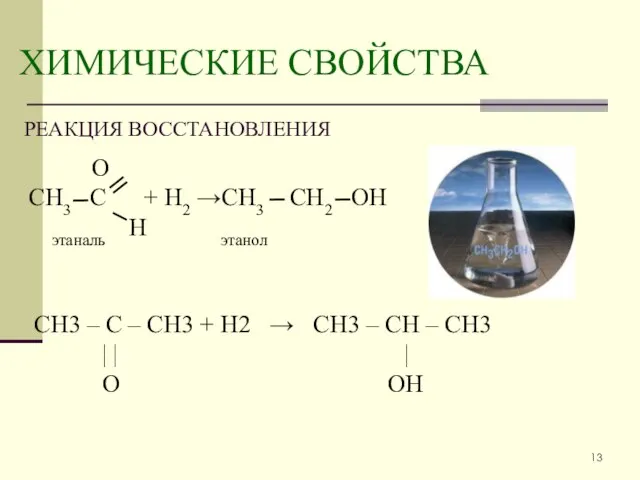
- 13. ХИМИЧЕСКИЕ СВОЙСТВА РЕАКЦИЯ ВОССТАНОВЛЕНИЯ О СН3 С + Н2 →СН3 СН2 ОН этаналь Н этанол CH3
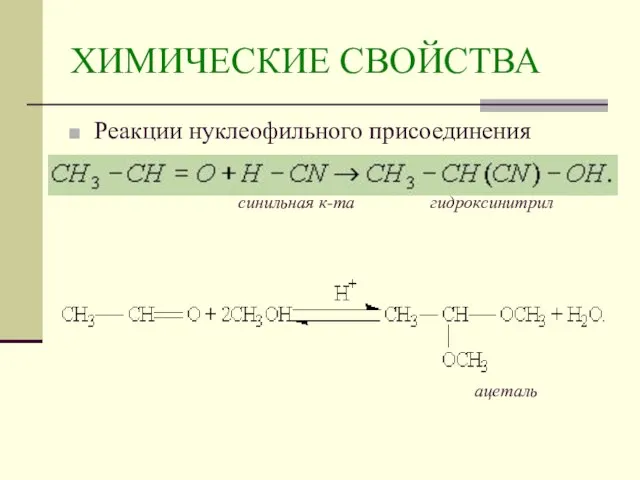
- 14. ХИМИЧЕСКИЕ СВОЙСТВА Реакции нуклеофильного присоединения синильная к-та гидроксинитрил ацеталь
- 15. ХИМИЧЕСКИЕ СВОЙСТВА Присоединение гидросульфитов Реактив Гриньяра
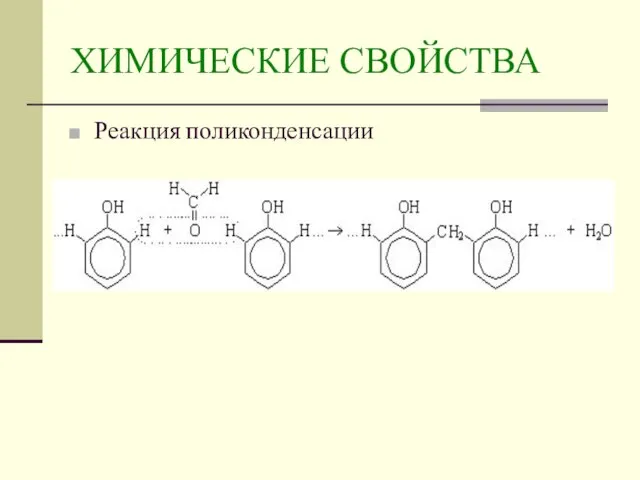
- 16. ХИМИЧЕСКИЕ СВОЙСТВА Реакция поликонденсации
- 17. ПРИМЕНЕНИЕ АЛЬДЕГИДОВ ПАРФЮМЕРИЯ Альдегид анисовый, обепин – жидкость с приятным запахом мимозы Альдегид дециловый, деканаль –
- 18. ПРИМЕНЕНИЕ АЛЬДЕГИДОВ ПОЛИМЕРНЫЕ МАТЕРИАЛЫ Фенолформальдегидные смолы
- 20. Скачать презентацию






 Корейская война
Корейская война Святослав Игоревич – Великий полководец древней Руси.
Святослав Игоревич – Великий полководец древней Руси. Материнская плата
Материнская плата Предприятие EcoCorp
Предприятие EcoCorp БАЗЫ ДАННЫХ
БАЗЫ ДАННЫХ Авторы: Вабищевич Мария Владимировна, учитель химии МОУСОШ № 37 г. Шахты
Авторы: Вабищевич Мария Владимировна, учитель химии МОУСОШ № 37 г. Шахты Живая память
Живая память Coffeе-art Сладкая фантазия
Coffeе-art Сладкая фантазия Живи здраво (о ВИЧ и не только)
Живи здраво (о ВИЧ и не только) Смеситель металлический
Смеситель металлический Order Letter
Order Letter Изменения в налоговом законодательстве осенняя сессия 2011 г.
Изменения в налоговом законодательстве осенняя сессия 2011 г. «Принципы и направления развития таможенных органов.» Работу выполнили студентки 1-го курса ФТД группы Т-116 Сафонова Эллина и Панк
«Принципы и направления развития таможенных органов.» Работу выполнили студентки 1-го курса ФТД группы Т-116 Сафонова Эллина и Панк Как опубликовать сообщение в блоге
Как опубликовать сообщение в блоге Искусство графики
Искусство графики Свойства нервной системы в профессиональной деятельности
Свойства нервной системы в профессиональной деятельности Ядерная сделка с Ираном
Ядерная сделка с Ираном Русская народная одежда
Русская народная одежда Описание предмета Городецкая роспись
Описание предмета Городецкая роспись Minsk. Capitale de Bielorussie
Minsk. Capitale de Bielorussie Пейзажная лирика Ф.И.Тютчева
Пейзажная лирика Ф.И.Тютчева Презентация на тему Профилактика ВИЧ и СПИД
Презентация на тему Профилактика ВИЧ и СПИД Защита зоны электродуговой сварки от окисления
Защита зоны электродуговой сварки от окисления Театральное искусство XVII – XVIII вв
Театральное искусство XVII – XVIII вв Колебания и волны
Колебания и волны Бизнес инсайт. Продвижение бренда при нулевом бюджете
Бизнес инсайт. Продвижение бренда при нулевом бюджете Формирование Совета Федерации
Формирование Совета Федерации AL-1035WH - - Произведение Искусств
AL-1035WH - - Произведение Искусств