Слайд 2До 85% всех случаев субарахноидальных кровоизлияний обусловлены разрывом аневризмы сосудов головного мозга.
Аневризма

- местное расширение просвета артерии вследствие изменения или повреждения ее стенки.
В настоящее время единой теории происхождения аневризм нет.
Большинство авторов считают, что происхождение аневризм зависит от 2-х причин: а) дегенеративных изменений сосудистой стенки б) факторов, их вызывающих.
Слайд 3Дефекты артериальной стенки, лежащие в основе формирования аневризмы:
- дефект мышечного слоя,
-

повреждения внутренней эластической
мембраны,
- гиперплазия интимы и атеромы артериального
ствола,
- повреждение коллагеновых волокон артерии,
- сочетание возрастающей ригидности стенки
артерии с уменьшением ее толщины.
Слайд 4Гемодинамическе факторы -
аневризмы чаще располагаются в области отхождения ветвей от артерии или

в месте изгибов артерии, т.к. эти участки испытывают наибольшее гемодинамическое воздействие.
Слайд 5Классификация аневризм по артерии,
на которой они расположены.
1. На передней мозговой

– передней
соединительной артериях (45%).
2. На внутренней сонной артерии (32%).
3. На средней мозговой артерии (19%).
4. На артериях вертебробазилярной системы (4%)
5. Множественные аневризмы – на двух и более
артериях (13%).
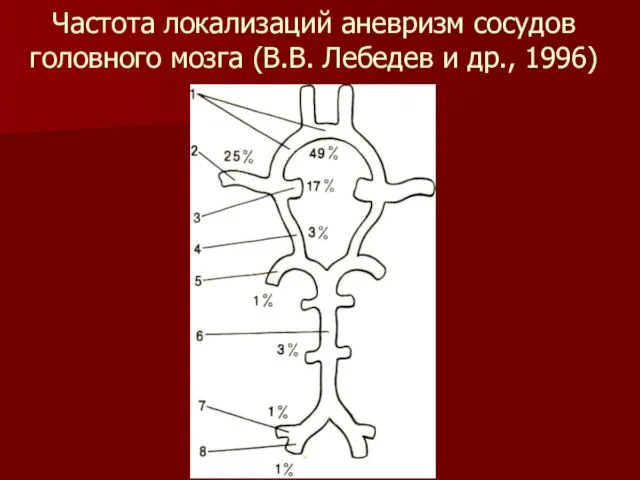
Слайд 6Частота локализаций аневризм сосудов головного мозга (В.В. Лебедев и др., 1996)
Слайд 7Классификация аневризмы по форме.
1. Мешотчатые (одно- или многокамерные).
2. Веретенообразные (фузиформные).

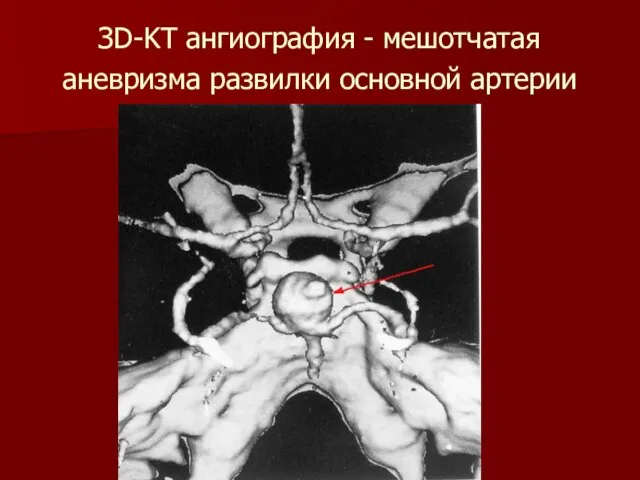
Слайд 8ЗD-KT ангиография - мешотчатая аневризма развилки основной артерии
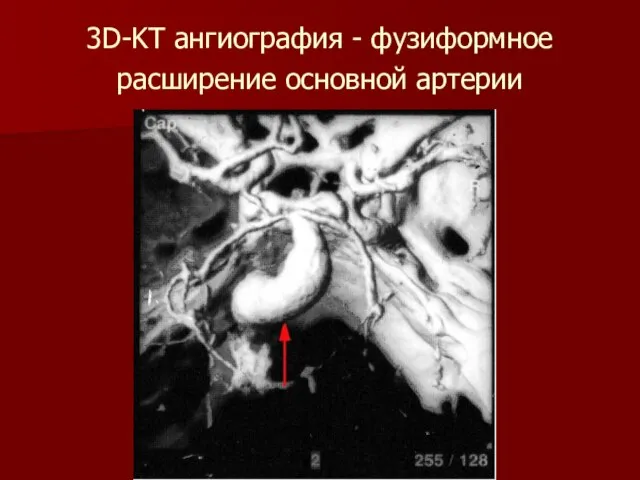
Слайд 93D-KT ангиография - фузиформное расширение основной артерии
Слайд 10Классификация аневризм по величине.
1. До 3 мм – милиарные.
2. 4 -

15 мм – обычные.
3. 16 - 25 мм – большие.
4. Более 25 мм – гигантские.
Слайд 11Вилизиев круг (артериальный круг головного мозга) с гигантской аневризмой внутренней сонной артерии

(слева)
Слайд 12Строение аневризм
Аневризма состоит из шейки, тела и купола.
Шейка – имеет трехслойное строение

церебральной артерии, это наиболее прочная часть аневризмы.
Тело аневризмы характеризуется отсутствием трехслойной сосудистой стенки (прежде всего мышечного слоя) и недоразвитием эластической мембраны.
Купол аневризмы представлен одним слоем интимы, он наиболее тонок, и кровотечение возникает именно отсюда.
В области аневризмы практически всегда имеются атероматозные изменения и разрыв ее часто возникает на месте этих изменений.
Слайд 13Распространенность аневризм
Аневризма может стать причиной внутричерепного кровоизлияния в любой период жизни человека,

но чаще в возрасте от 40 до 60 лет.
Встречаемость разрыва аневризм возрастает с 3 на 100 000 населения среди лиц до 30 лет,
30 на 100 000 населения среди лиц старше 60 лет.
Факторами риска разрыва аневризм являются артериальная гипертензия, курение и возраст.
Слайд 14Клинические формы разрыва аневризм
Неосложненное субарахноидальное кровоизлияние
Субарахноидально-паренхиматозное кровоизлияние
Субарахноидально-вентрикулярное кровоизлияние
Субарахноидально-паренхиматозно-вентрикулярное (смешанное) кровоизлияние
Субарахноидальное кровоизлияние с

оболочечными гематомами
Слайд 15Клиническая картина разрыва аневризмы сосудов головного мозга
Типичная клиническая картина САК развивается у

72% больных.
У остальных возможны следующие варианты клинического проявления разрыва аневризм в зависимости от ведущего клинического синдрома:
1) мигренеподобный (7%),
2) ложновоспалительный (6%),
3) ложногипертонический (9%),
4) ложнорадикулярный (2%),
5) ложнопсихотический (2%),
6) ложнотоксический (2%).
Слайд 16Мигренеподобный вариант (7%)
Внезапное появление головной боли без утраты сознания и рвоты
Общее состояние

удовлетворительное
АД не более 140/90 мм рт. ст.
Температура субфебрильная
Менингеальный синдром слабо выражен
Слайд 17Ложновоспалительный вариант (6%)
Остро развивается головная боль, которая сопровождается рвотой
У 25% больных кратковременная

потеря сознания
У всех пациентов сопровождается повышением температуры (у ¼ сразу с головной болью, у ¾ на 2-3 день заболевания)
Сознание сохранено
Менингеальные знаки
Слайд 18Ложногипертонический вариант (9%)
Большинство больных – страдают артериальной гипертензией
В начале заболевания отмечается повышение

АД
Сознание ясное
Менингеальный синдром слабо выражен (или появляется на 2-3 сутки)
Слайд 19Ложнорадикулярный вариант (2%)
Начало с острой головной боли, без утраты сознания и рвоты
Интенсивность

головной боли быстро снижается
начинают преобладать жалобы на боль в поясничной области, шее, ногах (менингеальный синдром)
Слайд 20Ложнопсихотический вариант (2%)
Развивается при аневризмах передней мозговой – передней соединительной артерии
В клинике

на первом плане дезориентация, делирий, психомоторное возбуждение
Менингеальный синдром не удается исследовать или же его просто игнорируют
Слайд 21Ложнотоксикационный вариант (2%)
Головная боль
Неукротимая рвота
Сознание ясное
АГ отсутствует
Заболевание обычно связывают с приемом недоброкачественной

пищи
Слайд 22Клинические периоды
В клиническом проявлении разрыва аневризм принципиально выделяют два периода
острый (первые

14 дней после разрыва аневризмы)
холодный – спустя 2 нед от начала заболевания.
В остром периоде наиболее высок риск повторного разрыва аневризмы, что отягощает течение заболевания. Спустя 2 нед. у части больных наступает регресс патологической реакции на кровоизлияние и состояние пациентов стабилизируется.
Слайд 24Летальность и риск повторного кровоизлияния
Летальность в течение первых 2–3 нед после разрыва

аневризмы колеблется от 20 до 30%, инвалидами становятся около 20% пациентов.
Повторное кровоизлияние из аневризмы является основной причиной высокой летальности и инвалидности.
Риск повторного разрыва аневризмы в течение первых 2 нед заболевания достигает 20%, в течение 1-го месяца – 33% и в течение 6 мес – 50%.
Далее риск повторного разрыва аневризм значительно уменьшается и составляет примерно 3% в год.
Слайд 25Летальность от повторного разрыва аневризм очень высокая и достигает 40–50%.
От первичных

разрушений мозга, обусловленных кровоизлиянием, умирает каждый третий больной –
25–35%.
Слайд 26Осложнения, развивающиеся в остром периоде разрыва аневризмы:
1. Повторное кровотечения из аневризмы.
2.

Сосудистый спазм, который развивается в 100% случаев (пик развития спазма на 3-14 сутки), ишемия мозга вследствие ангиоспазма развивается в 64% случаев.
3. Внутримозговая гематома – 22%.
4. Внутрижелудочковое кровоизлияние – 14%.
В настоящее время ведущие нейрохирурги всего мира склоняются к ранним операциям при разрывах аневризм сосудов головного мозга. Таким образом, проводится профилактика повторного кровоизлияния, сосудистого спазма и гидроцефалии.
Слайд 27Диагностика
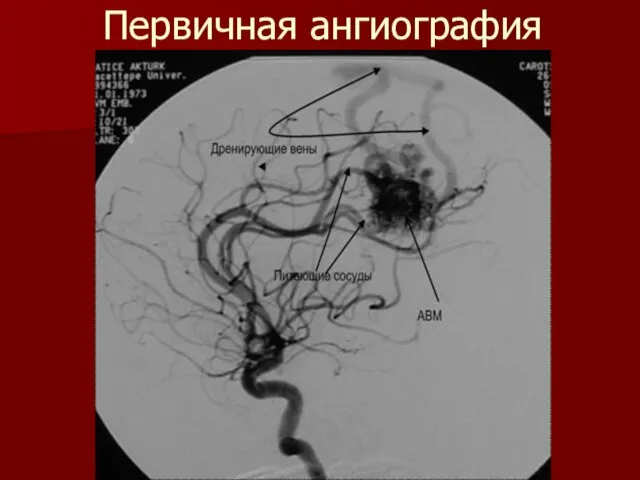
1) церебральная ангиография (определяет причины кровоизлияния, устанавливает локализацию, форму и размеры аневризмы;
2)

КТ головного мозга (определяет тип кровоизлияния в зависимости от его анатомической формы);
3) КТА - чувствительность трехмерной КТ-ангиографии (КТА) при аневризмах не менее 2 мм в диаметре достигает 88–97%, а специфичность – 95–100%. КTА особенно важно проводить в нейрохирургической клинике, это позволяет получать трехмерное изображение и определять взаиморасположение артерий и аневризмы с близлежащими костными структурами, что необходимо для планирования доступа к аневризме.
Слайд 28Диагностика
4) МРА - чувствительность магнитно-резонансной ангиографии (МРА) в определении аневризм головного мозга

достигает 74–100%.
5) транскраниальную допплерографию и определение индекса Линденгаарда (отношение линейной средней скорости кровотока в СМА и во ВСА той же стороны в норме менее 3, при наличии сосудистого спазма равно 3–6 и более).
Слайд 29Целью внутричерепного (открытого) вмешательства на аневризме является выключение ее из кровотока при

сохранении проходимости несущего и окружающих сосудов, удаление крови из субарахноидального пространства.
Эти операции относятся к ряду наиболее сложных операций в нейрохирургии.
Операция должна быть минимально травматична, что обеспечивается выполнением оптимальных хирургических доступов, микрохирургической техники и одномоментным клипированием шейки аневризмы.
Для выполнения операции используется операционный микроскоп, специальный микрохирургический инструмент.
При открытом вмешательстве, проведенных в условиях специализированных отделений крупных центров, летальность после операции в остром периоде кровоизлияния составляет 8-16%, а в холодном периоде кровоизлияния (через 1 месяц после него) – не более 2-3%.
Слайд 30Микрохирургическое клипирование аневризмы
А. Типичный разрез кожи и трепанационный доступ.
Б. На шейку аневризмы
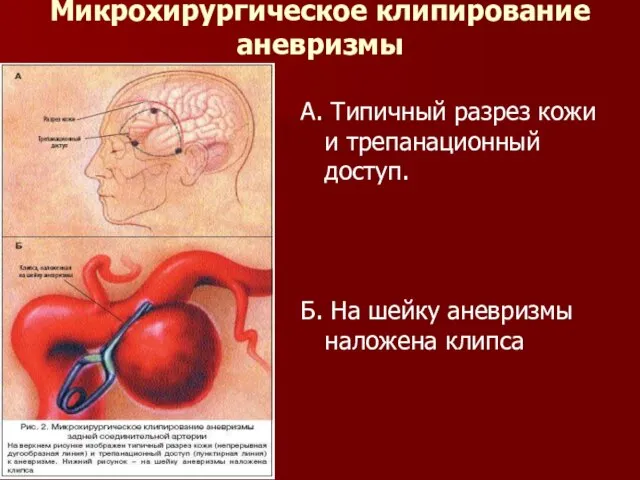
наложена клипса
Слайд 31Наложение клипсы на аневризму сосуда мозга

Слайд 32“Пломбирование” микроспиралями
Простые по анатомическому строению аневризмы, с не широкой шейкой возможно закрыть

простым “пломбированием” микроспиралями, без применения дополнительных методик.
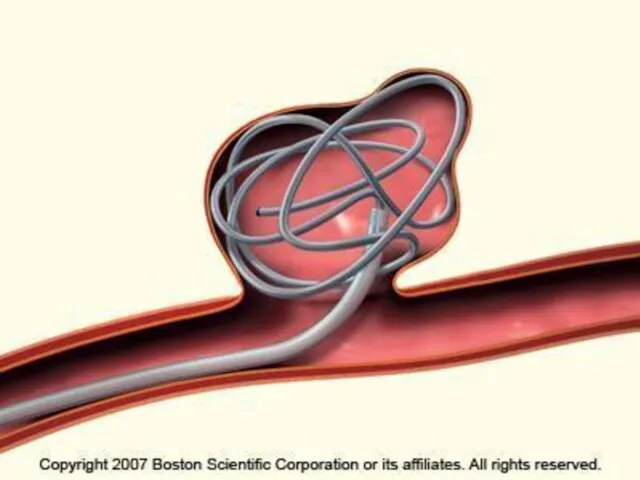
Микрокатетер проводится по сосудам головного мозга в питающий сосуд и конец микрокатетера вводится в полость аневризмы и, через микрокатетер, вводятся микроспирали, которые постепенно заполняют полость аневризмы.
Слайд 33Эндоваскулярная окклюзия аневризмы микроспиралями Джуглиелми
А. Проведение микрокатетера через правую бедренную артерию, аорту
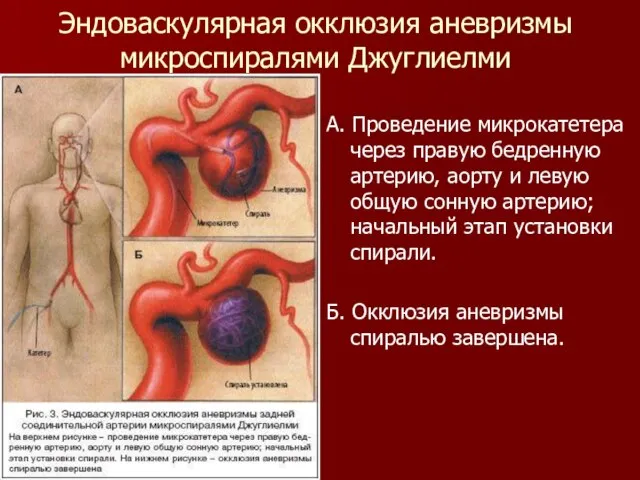
и левую общую сонную артерию; начальный этап установки спирали.
Б. Окклюзия аневризмы спиралью завершена.
Слайд 35Процедура введения микроспиралей проводится под постоянным радиологическим контролем по особым методикам, позволяющим

контролировать расположение спиралей в полости аневризмы и полноту заполнения полости аневризмы.
Слайд 36Микрокатетер введён в полость аневризмы и введена первая микроспираль
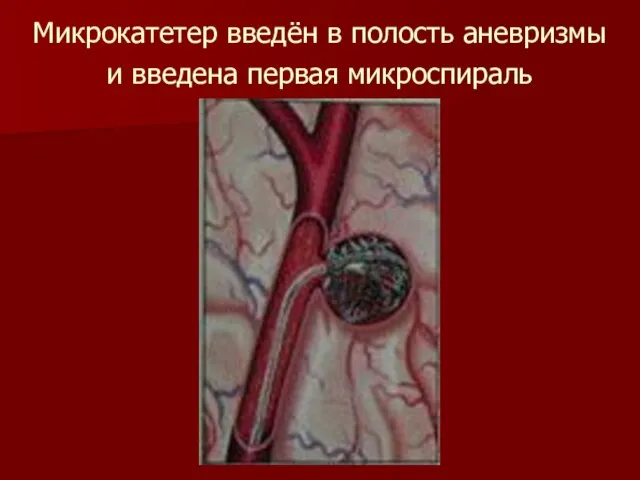
Слайд 37Продолжение заполнения полости аневризмы
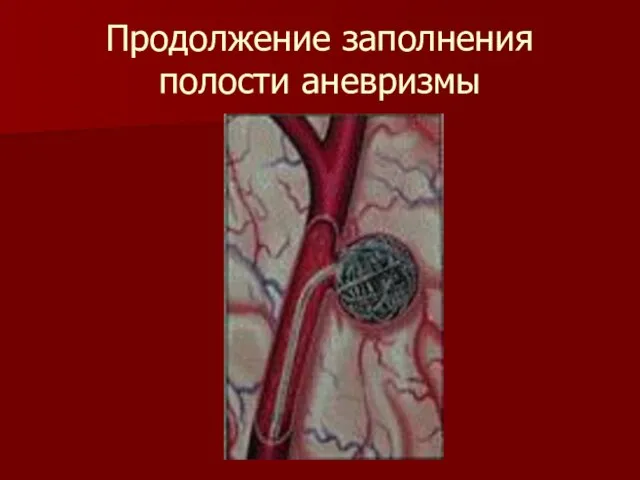
Слайд 38После того, как контрольные ангиограммы показывают полное закрытие аневризмы, микрокатетер удаляется.
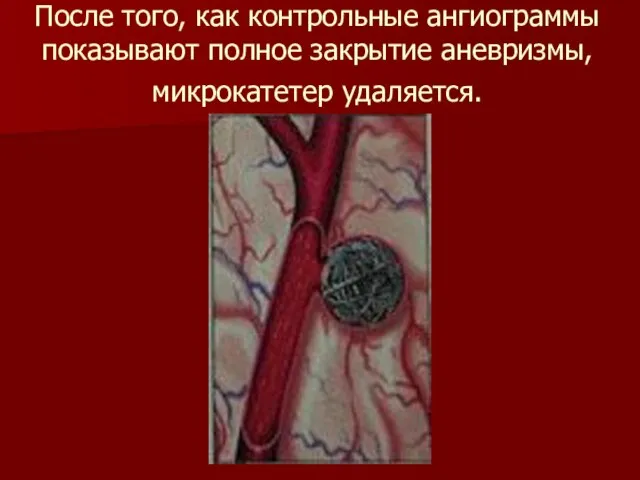
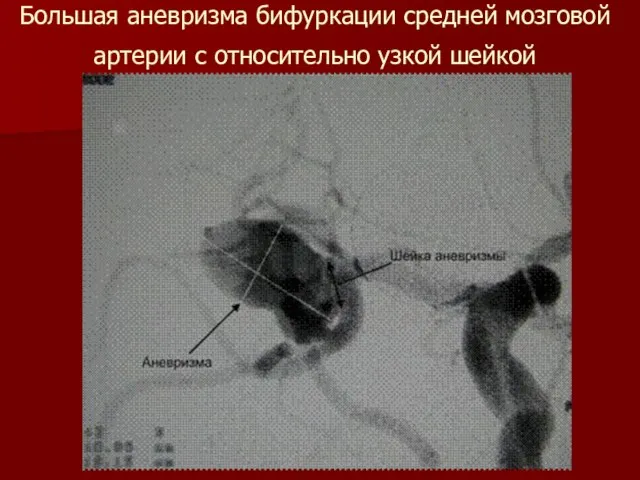
Слайд 39Большая аневризма бифуркации средней мозговой артерии с относительно узкой шейкой
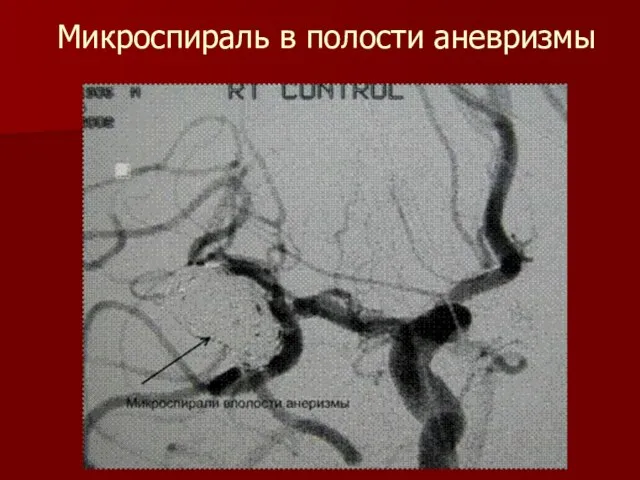
Слайд 40Микроспираль в полости аневризмы
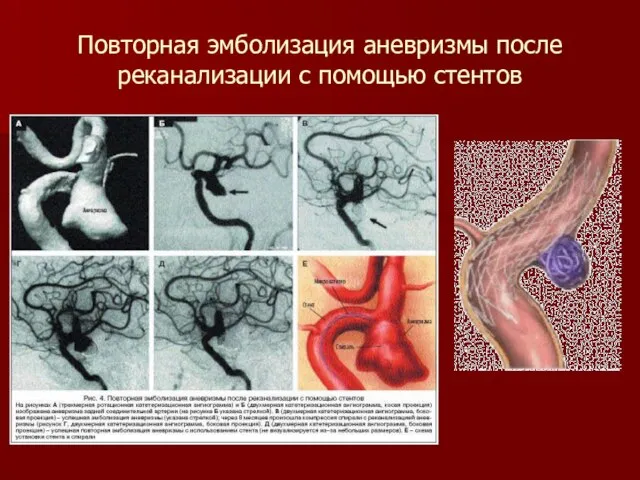
Слайд 41Повторная эмболизация аневризмы после реканализации с помощью стентов
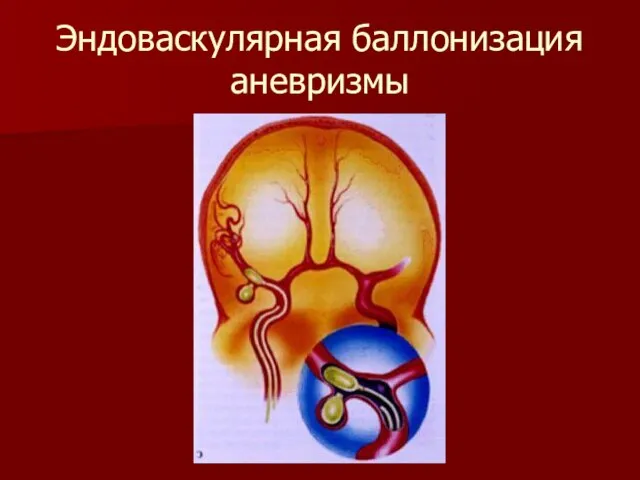
Слайд 43Эндоваскулярная баллонизация аневризмы
Слайд 44Суммарный «технический» успех эндоваскулярных операций варьирует от 65% до 98% в зависимости

от анатомической и клинической ситуации.
Слайд 45АРТЕРИОВЕНОЗНЫЕ МАЛЬФОРМАЦИИ (АВМ)
являются врожденной аномалией развития сосудистой системы головного мозга и представляют

собой различной формы и величины клубки, образованные вследствие беспорядочного переплетения патологических сосудов.
Слайд 46Статистика АВМ
Суммарная частота ангиоматозных пороков развития составляет 19 на 100000 населения в

год.
Артериовенозные мальформации (АВМ) в 5% - 10% являются причиной нетравматического субарахноидального кровоизлияния.
Разрыв АВМ, обычно, происходит в возрасте 20 - 40 лет.
Слайд 47Типы сосудистых мальформаций
А) артериальная, В) артериовенозная фистулезная,
С) артериовенозная рацемозная (75%),
D) артериовенозная микромальформация
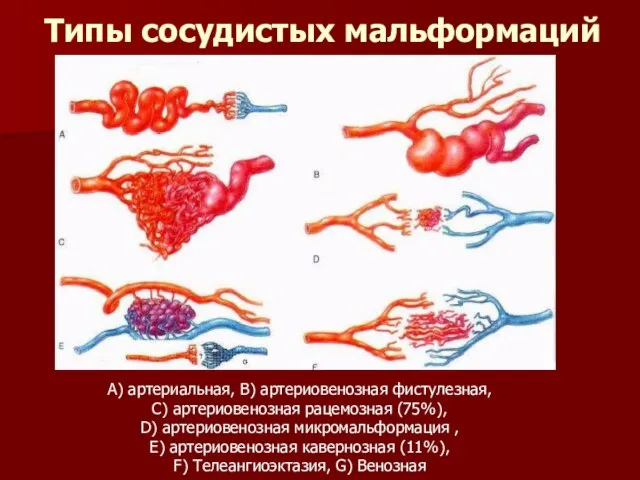
,
Е) артериовенозная кавернозная (11%),
F) Телеангиоэктазия, G) Венозная
Слайд 48Интраоперационный вид поверхностной АВМ
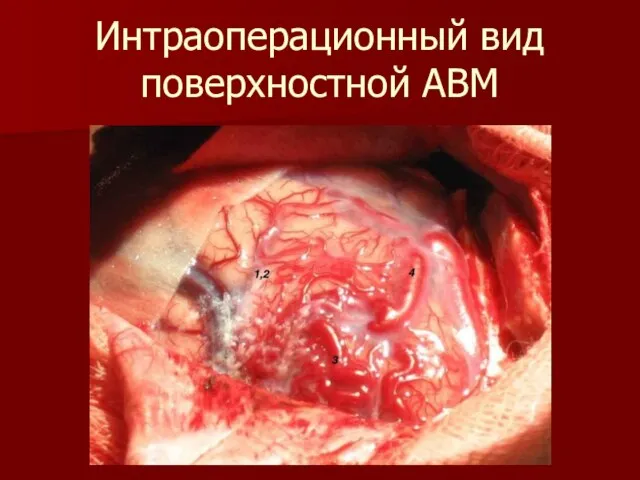
Слайд 49Типичная локализация артериовенозных мальформаций головного мозга

Слайд 50Классификация АВМ (по Spetzler-Martin, 1986)
1) по размеру:
менее 3 см — 1 балл,
3—6

см — 2 балла,
более 6 см — 3 балла;
2) по локализации:
вне функционально значимой зоны — 0 баллов,
в пределах функционально значимой зоны — 1 балл;
3) подразделение АВМ по характеру дренирования:
отсутствие глубоких дренирующих вен — 0 баллов,
наличие глубоких дренирующих вен — 1 балл.
Слайд 51Классификация АВМ (по Spetzler-Martin, 1986)
По данной градации АВМ разделяются на 3 типа:
1,

2 балла — АВМ низкого риска;
3 балла — промежуточные АВМ;
4, 5 баллов — АВМ высокого риска.
Слайд 52Клиника артериовенозных мальформаций
Геморрагический тип течения заболевания – в 50 – 70 %

случаев. Для этого типа течения характерно наличие у больного артериальной гипертензии, небольшой размер узла мальформации, дренаж ее в глубокие вены, а так же АВМ задней черепной ямки.
Торпидный тип течения, характерен для больных с АВМ больших размеров, локализацией ее в коре, кровоснабжение ветвями средней мозговой артерии.
Слайд 53Геморрагический тип
В 50% случаев является первым симптомом проявления АВМ, что обусловливает летальный

исход у 10 -15% и инвалидизацию 20 – 30 % больных. (N. Martin et al.,1994).
Ежегодный риск кровоизлияния из АВМ составляет 1,5 – 3%. В течение первого года после кровоизлияния риск повторного - 6% и увеличивается с возрастом. (R. Braun et al.,1990).
В течение жизни повторное кровоизлияние случается у 34% больных, выживших после первого, а среди перенесших второе (летальность до 29%) - 36% страдают от третьего. (G. Rasmussen 1996).
Кровотечение из АВМ является причиной 5 -12% всей материнской смертности, 23% всех внутричерепных кровоизлияний у беременных. (B. Karlsson et al.,1997)
Картина субарахноидального кровоизлияния наблюдается у 52 % больных (Лебедев В. В., Крылов В. В., 2000).
У 47% пациентов возникают осложненные формы кровоизлияния: с формированием внутримозговых (38%), субдуральных (2%) и смешанных (13%) гематом, гемотомпанада желудочков развивается у 47%.
Слайд 54Торпидный тип
Судорожный синдром (у 26 – 67% больных с АВМ)
Кластерные головные боли
Прогрессирующий

неврологический дефицит, как при опухолях головного мозга или в связи с ишемическими нарушениями из –за синдрома “ обкрадывания“
Слайд 55Лечение АВМ
Основной задачей любого вида вмешательства при артериовенозной мальформации является полная облитерация

сосудистой сети мальформации.
В настоящее время применяются следующие методы:
хирургическое вмешательство (радикальная экстирпация АВМ),
эндоваскулярная эмболизация,
радиохирургия – по отдельности или в комбинации
Слайд 56Хирургическое вмешательство открытым способом
радикальная экстирпация АВМ проводится пациентам с приемлемым риском неврологических

осложнений, при поверхностных АВМ и вне функционально значимых зон головного мозга
Удаление АВМ градации 4 – 5 по шкале Spetzler-Martin сопряжено с большими техническими сложностями, очень высоким риском глубокой инвалидизации и летального исхода
АВМ расположенные в глубинных отделах, стволе мозга – недоступны
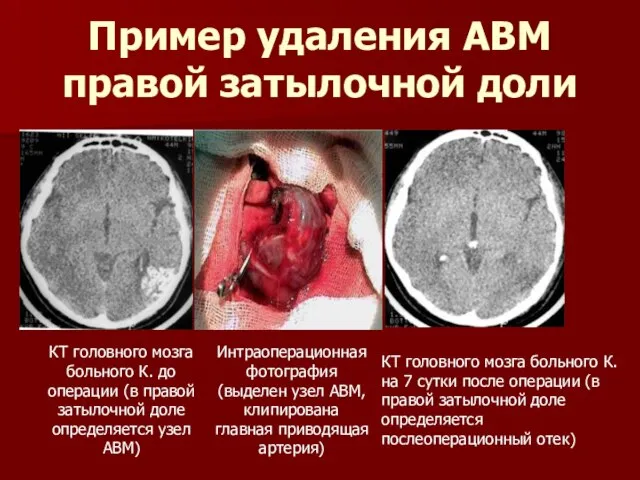
Слайд 58Пример удаления АВМ правой затылочной доли
Пример удаления АВМ правой затылочной доли
Слайд 59Эндоваскулярная процедура
малоинвазивна
величина, локализация АВМ не влияют на риск процедуры.
появление нового эмболизирующего

материала – ONYX – (поли-винил-алкоголь кополимера), обладающего высоким пенетрационным потенциалом, позволяет производить хорошо контролируемую и длительную иньекцию
появление специального микрокатетера для работы с этим материалом, катетер Sonic с отделяющимся наконечником, даёт возможность проводить длительную (до 2 – 3 часов) инъекцию и нетравматичное удаление катетера после окончания инъекции.
Слайд 60Этапы эндоваскулярной операции
Процедура проводится под общей анестезией
Производится прокол бедренной артерии, мягкий катетер

проводится в сосуды, кровоснабжающие головной мозг.
Микрокатетер проводится в питающий сосуд и далее в сосуды узла АВМ.
Под радиологическим контролем производится иньекция эмболизирующего материала.
После заполнения узла АВМ микрокатетер удаляется и производится контрольная ангиография.
При сложном строении АВМ – большая, состоящая из нескольких узлов – процедура может быть разбита на 2 – 3 этапа.
Слайд 62Завершение процедуры – полная окклюзия АВМ
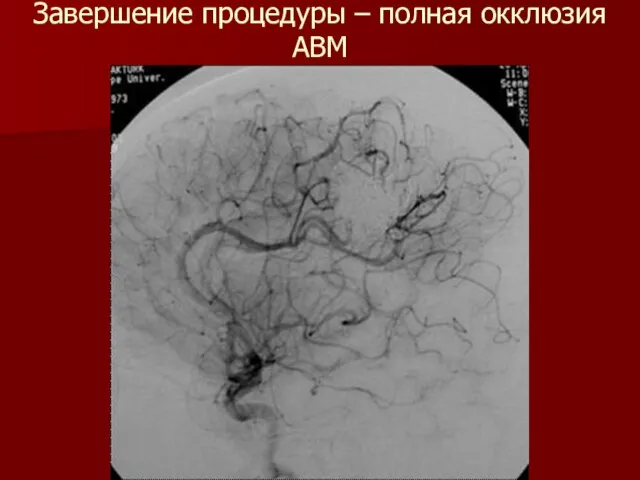
Слайд 63По завершении процедуры больной пробуждается от наркоза и переводится в палату где

находится под наблюдением ближайшие 24 часа после процедуры.
Затем больному разрешается вставать с постели и ходить и, как правило, на 3 день после процедуры больной выписывается из стационара.
Слайд 65Особенности радиохирургического лечения мальформаций гамма-ножом
Основное показание - мальформации до 3 см в

диаметре, расположенные в глубоких отделах мозга, т.е. зонах, имеющих большой риск осложнений для хирургии и эмболизации, а также остатки АВМ того же размера после прямых или эдовазальных операций
При радиохирургическом лечении не бывает таких осложнений как разрывы сосудов, повреждения мозговой ткани или ишемия.
После проведенной процедуры сосуды мальформации постепенно облитерируются и кровоток по мальформации прекращается. Происходит это постепенно, в течение 1 – 3 лет.
Эффективность радиохирургического лечения в виде достижения в конечном итоге тотальной облитерации АВМ (т.е. полного излечения больного) составляет 95 %.





























































 Проект Моё лицо
Проект Моё лицо Презентация на тему Компетенция должностных лиц по выявлению АП
Презентация на тему Компетенция должностных лиц по выявлению АП  Повестка родительского собрания от 26.01.2012года 1. Итоги 2 четверти 2. Задачи на 3 четверть 3. Знание и учёт возрастных особеннос
Повестка родительского собрания от 26.01.2012года 1. Итоги 2 четверти 2. Задачи на 3 четверть 3. Знание и учёт возрастных особеннос Презентация на тему Национальные костюмы народов России
Презентация на тему Национальные костюмы народов России Единицы площади. Обобщение
Единицы площади. Обобщение Программа добровольного медицинского страхования Доктор РЕСО. Екатеринбург
Программа добровольного медицинского страхования Доктор РЕСО. Екатеринбург Исследование бетонных конструкций методом ультразвукового зондирования поверхностного слоя
Исследование бетонных конструкций методом ультразвукового зондирования поверхностного слоя Великий русский писатель К.Д.Ушинский.
Великий русский писатель К.Д.Ушинский. ИНДИВИДУАЛЬНЫЕ СРЕДСТВА ЗАЩИТЫ (СИЗ)
ИНДИВИДУАЛЬНЫЕ СРЕДСТВА ЗАЩИТЫ (СИЗ) Микробиология на службе человека
Микробиология на службе человека Этюды овощей и фруктов. Живопись
Этюды овощей и фруктов. Живопись Применение солнечной энергетики в городском хозяйстве Москвы
Применение солнечной энергетики в городском хозяйстве Москвы Памятка для приезжающих в Ростовскую область из других регионов России
Памятка для приезжающих в Ростовскую область из других регионов России Текстология. Атрибуция текста, работа с рукописями
Текстология. Атрибуция текста, работа с рукописями 461 Спаситель мой живёт!
461 Спаситель мой живёт! Общая управленческая практика
Общая управленческая практика Вент& Винт. Вентиляционное оборудование
Вент& Винт. Вентиляционное оборудование Презентація_1662705410
Презентація_1662705410 1c7a5f862b5d4d6fb943f08d0af3ce8e
1c7a5f862b5d4d6fb943f08d0af3ce8e Направление Москва Юг. Дирекция Москва
Направление Москва Юг. Дирекция Москва Тематический семинар
Тематический семинар Бумажные картины Карлоса Мейра
Бумажные картины Карлоса Мейра Типы химических реакций
Типы химических реакций Презентация на тему Породы кроликов (4 класс)
Презентация на тему Породы кроликов (4 класс) Научно-практическая конференция 18 мая 2005г. Я – исследователь! Я открываю мир! МОУ Гимназия 30 им.Музалева Д.Н.
Научно-практическая конференция 18 мая 2005г. Я – исследователь! Я открываю мир! МОУ Гимназия 30 им.Музалева Д.Н. Такие разные мосты
Такие разные мосты Презентация на тему Русский язык
Презентация на тему Русский язык Концепция IOI
Концепция IOI