Содержание
- 2. И это всё о ней… Это вещество было описано в VIII веке арабским алхимиком Джабиром ибн
- 3. Знаете ли Вы, почему HNO3 назвали… к и с л о т о й ? взрывоопасной
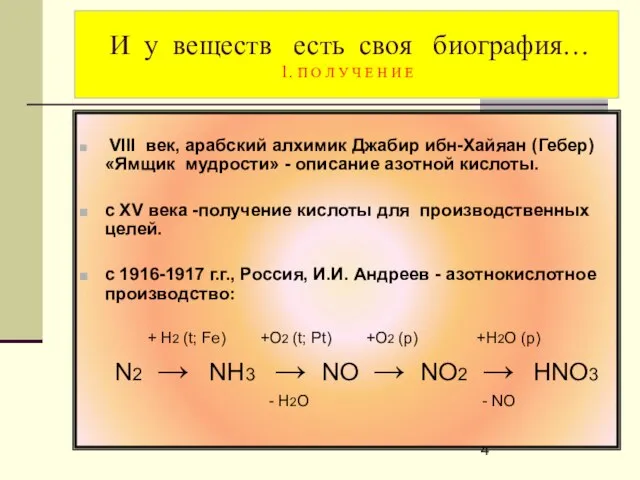
- 4. И у веществ есть своя биография… 1. П О Л У Ч Е Н И Е
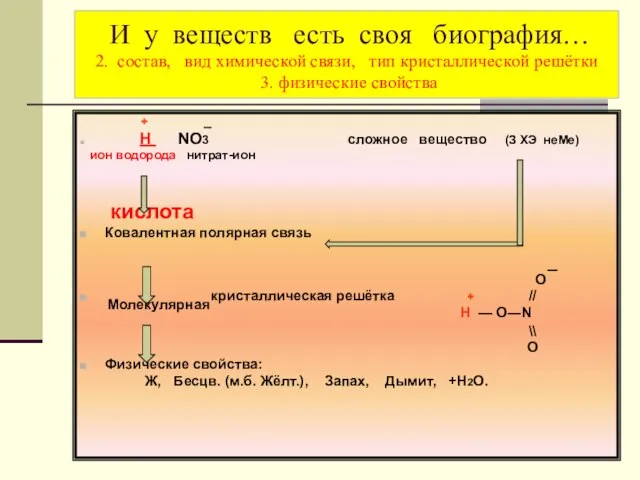
- 5. И у веществ есть своя биография… 2. состав, вид химической связи, тип кристаллической решётки 3. физические
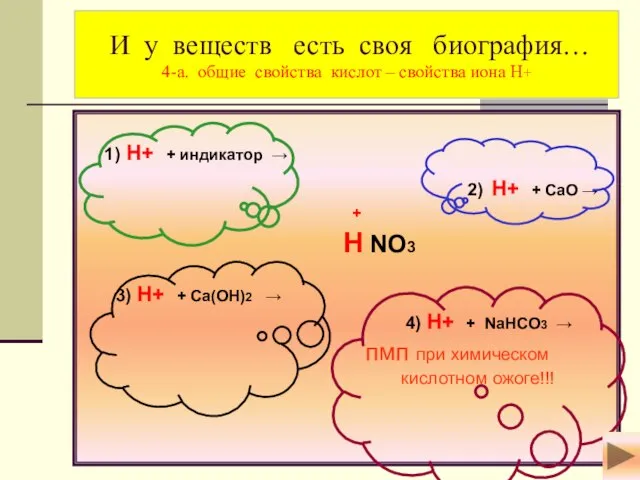
- 6. 1) H+ + индикатор → 2) H+ + СaO → + H NO3 3) H+ +
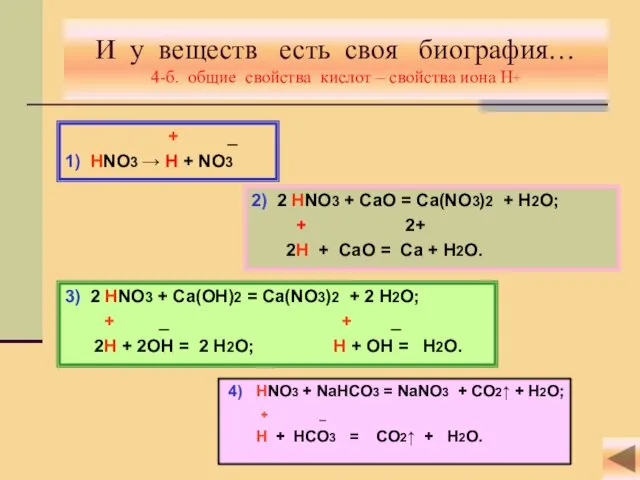
- 7. И у веществ есть своя биография… 4-б. общие свойства кислот – свойства иона Н+ + _
- 8. И у веществ есть своя биография… 5. особые свойства +5 -3, 0, +1, +2, +3, +4
- 9. И у веществ есть своя биография… 5-а. особое «царское» свойство 1 HNO3 + 3 HCl «Царская
- 10. И у веществ есть своя биография… 5-б. особое «взрывоопасное» свойство 4 HNO3 t 4 NO2 ↑
- 11. Эта страница для Ваших открытий… А пока … Д/З: § 27 (с.156-157), закончить и выучить записи
- 13. Скачать презентацию






 Презентация на тему My family (2 класс)
Презентация на тему My family (2 класс) Задачи на построение являются одними из основных задач школьного курса геометрии, которые формируют необходимые практические нав
Задачи на построение являются одними из основных задач школьного курса геометрии, которые формируют необходимые практические нав Аннотация проекта
Аннотация проекта С. Ю. Витте – личность и реформы
С. Ю. Витте – личность и реформы Каждый ребенок имеет право, ответственность и обязанность
Каждый ребенок имеет право, ответственность и обязанность Загадка
Загадка Lektsiya dlya vechernikov_ Upravlenie kontentom v organizatsii
Lektsiya dlya vechernikov_ Upravlenie kontentom v organizatsii Работа с дробями
Работа с дробями Мал шаруашылығы өнімдерінің ауыр металл тұздарымен ластануын анықтау және оларға қарсы ветсаншараларды ұйымдастыру
Мал шаруашылығы өнімдерінің ауыр металл тұздарымен ластануын анықтау және оларға қарсы ветсаншараларды ұйымдастыру Образ художника. Сюрреализм
Образ художника. Сюрреализм Программа «Paint»
Программа «Paint» Healthy Food
Healthy Food Лекция 1
Лекция 1 Расширенное Участие Trust Fund Кодексав деятельности Кодекса
Расширенное Участие Trust Fund Кодексав деятельности Кодекса Техническое задание. Фотографии
Техническое задание. Фотографии Инициативное бюджетирование для школьников: опыт Санкт-Петербурга
Инициативное бюджетирование для школьников: опыт Санкт-Петербурга Организационная встреча для участников ПМАМ 2021-22 уч.г
Организационная встреча для участников ПМАМ 2021-22 уч.г Геометрия египетских пирамид
Геометрия египетских пирамид VII Всероссийский конкурс учебно-исследовательских экологических проектов «Человек на Земле» Номинация №3 «Этнографические исс
VII Всероссийский конкурс учебно-исследовательских экологических проектов «Человек на Земле» Номинация №3 «Этнографические исс Основы метапредметного обучения русскому языку и формирование лингвистической компетентности всех участников образовательного
Основы метапредметного обучения русскому языку и формирование лингвистической компетентности всех участников образовательного  Цилиндр (задача В-9)
Цилиндр (задача В-9) Урок правовых знаний
Урок правовых знаний Мыши: внешний вид, образ жизни. Профилактика, средства избавления
Мыши: внешний вид, образ жизни. Профилактика, средства избавления Интуиция
Интуиция ООО «Инновационно-трастовая энергетическая компания»
ООО «Инновационно-трастовая энергетическая компания» История фотографии (9 класс)
История фотографии (9 класс) Мастер-класс: Техника Друдлы
Мастер-класс: Техника Друдлы СЛУЖБА СКОРОЙ МЕДИЦИНСКОЙ ПОМОЩИ В СИСТЕМЕ ОМС
СЛУЖБА СКОРОЙ МЕДИЦИНСКОЙ ПОМОЩИ В СИСТЕМЕ ОМС