Содержание
- 2. Химические элементы в живых системах Распространенность: Земная кора: O>Si>Al>Fe>Ca>Mg>Na>K>Ti>H>P Океаны: H>O>Cl>Na>Mg>S>Ca>K>C>Br>B Человек: H>O>C>N>Na>K>Ca>Mg>P>S>Cl
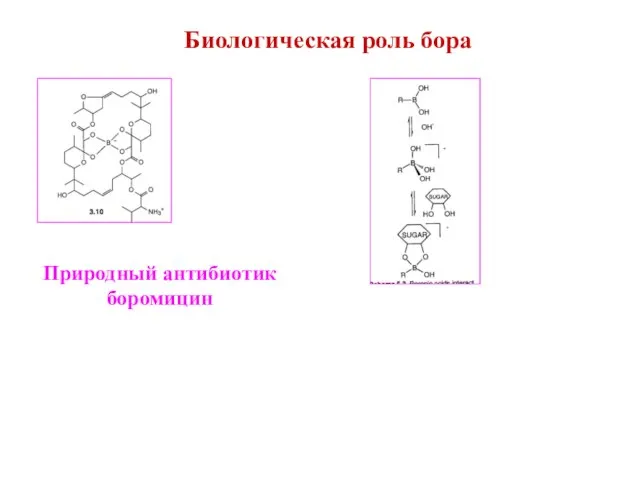
- 3. Биологическая роль бора Природный антибиотик боромицин
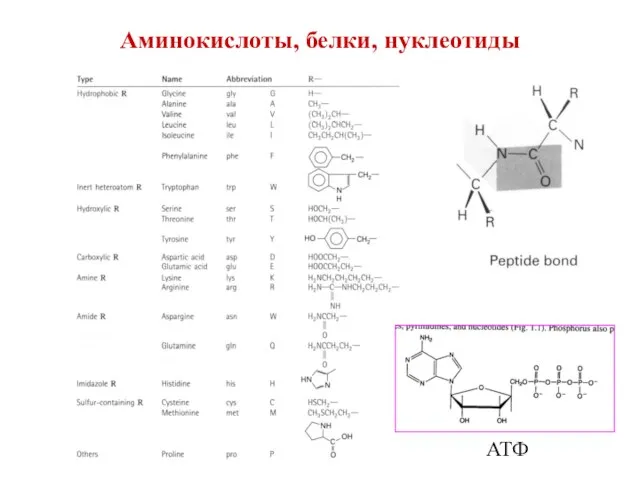
- 4. Аминокислоты, белки, нуклеотиды АТФ
- 5. Минералы в живых системах
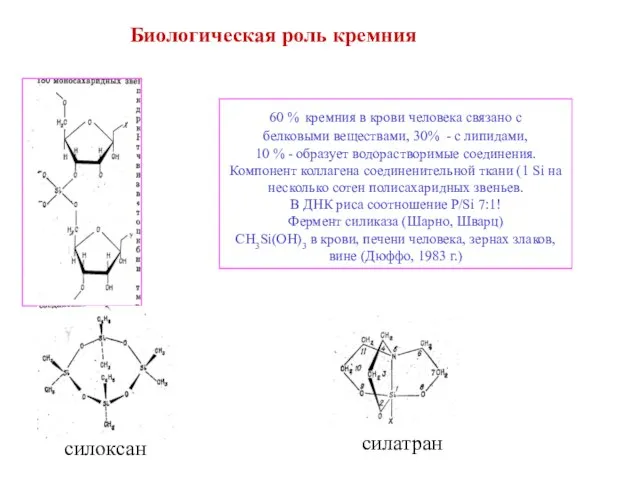
- 6. Биологическая роль кремния 60 % кремния в крови человека связано с белковыми веществами, 30% - с
- 7. Биологическая роль серы Ио – спутник Юпитера голожаберные моллюски H2SO4
- 8. СКУНС Жареный кофе Биологическая роль серы
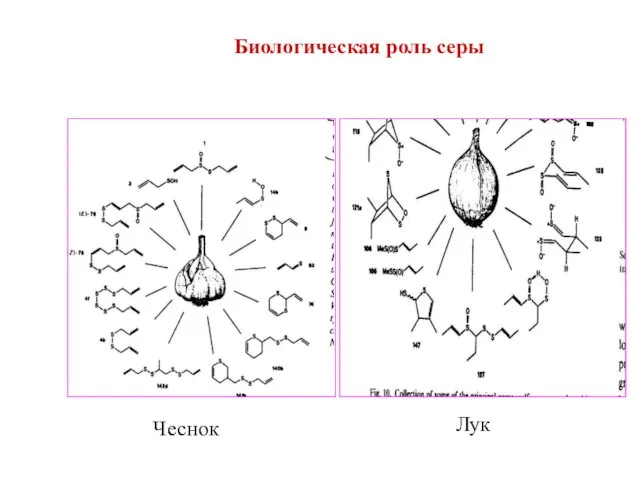
- 9. Чеснок Лук Биологическая роль серы
- 10. HNO3 и NO Оболочечник - HNO3 ! NO в организме животных передает сигналы, регулируя: Кровяное давление
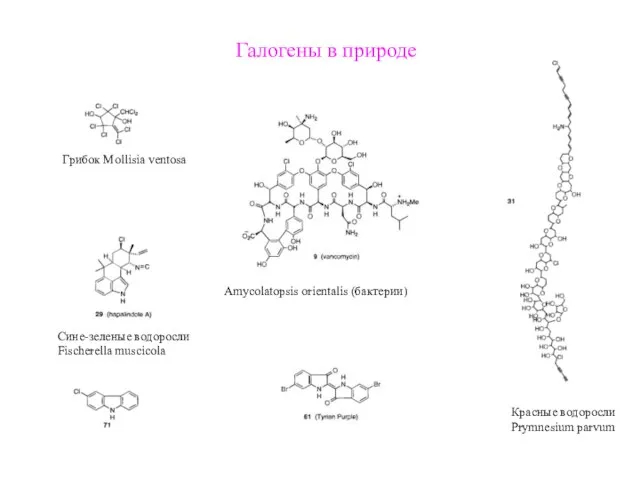
- 11. Галогены в природе Грибок Mollisia ventosa Amycolatopsis orientalis (бактерии) Сине-зеленые водоросли Fischerella muscicola Красные водоросли Prymnesium
- 12. Галогены в природе Феромон у клещей
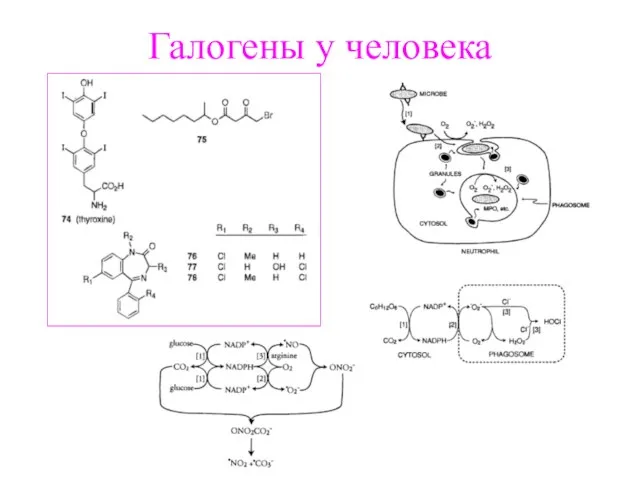
- 13. Галогены у человека
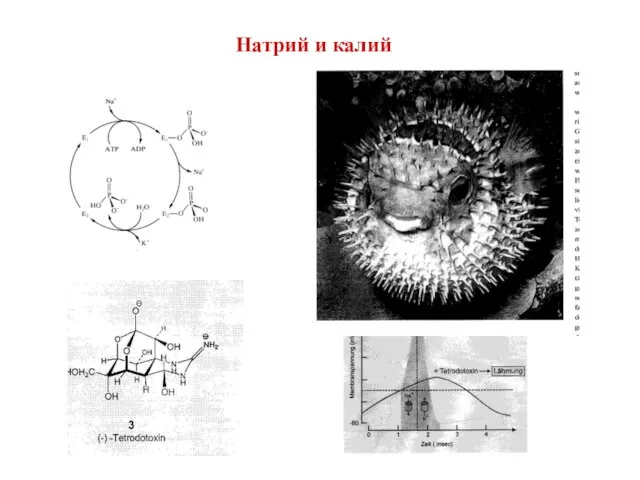
- 14. Натрий и калий
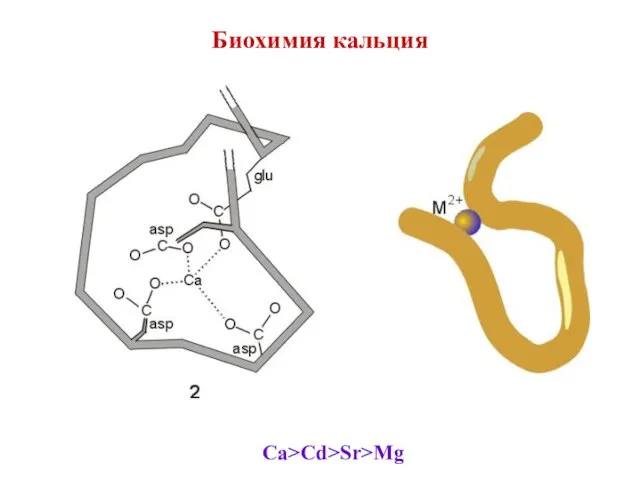
- 15. Биохимия кальция Ca>Cd>Sr>Mg
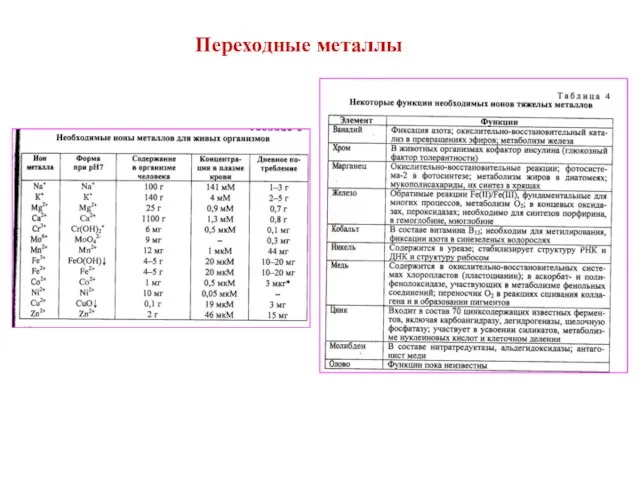
- 16. Переходные металлы
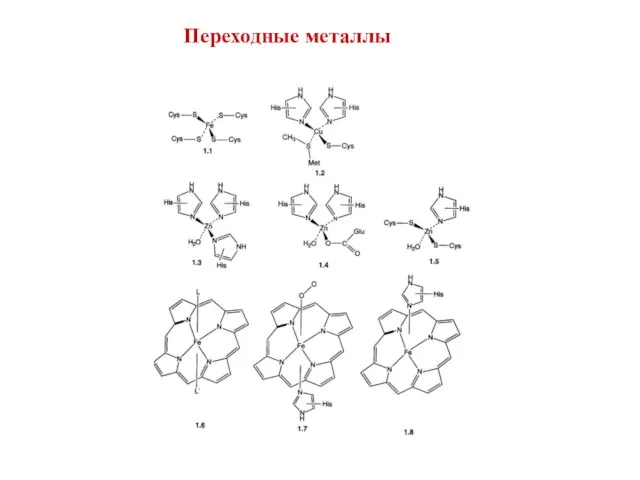
- 17. Переходные металлы
- 18. Переходные металлы
- 19. Гемоглобин – транспорт кислорода в плазме 4 атома железа (II) Миоглобин – хранение кислорода в мускулах
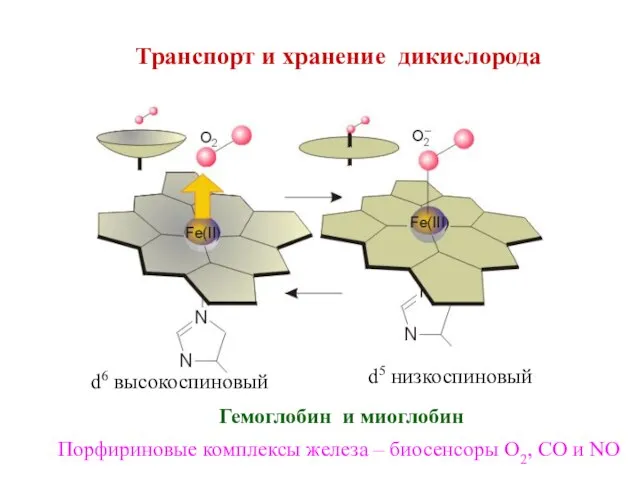
- 20. Транспорт и хранение дикислорода Гемоглобин и миоглобин d6 высокоспиновый d5 низкоспиновый Порфириновые комплексы железа – биосенсоры
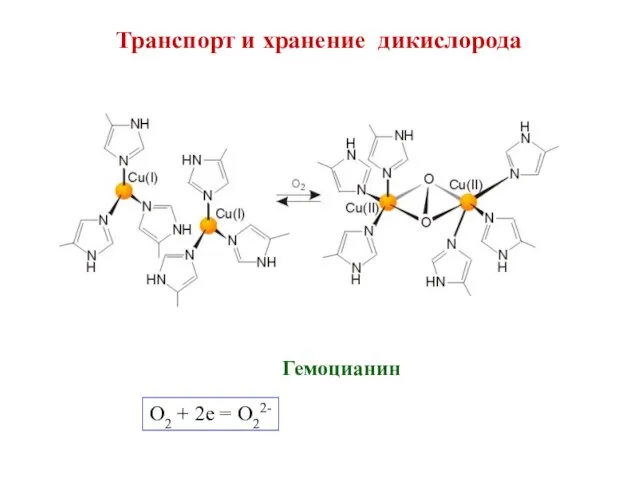
- 21. Транспорт и хранение дикислорода Гемоцианин O2 + 2e = O22-
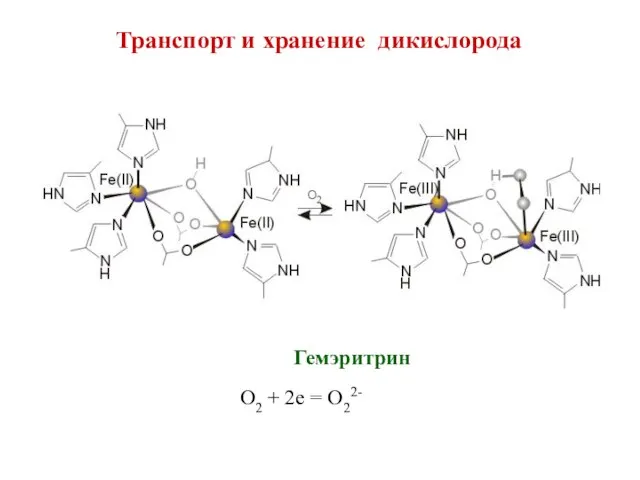
- 22. Транспорт и хранение дикислорода Гемэритрин O2 + 2e = O22-
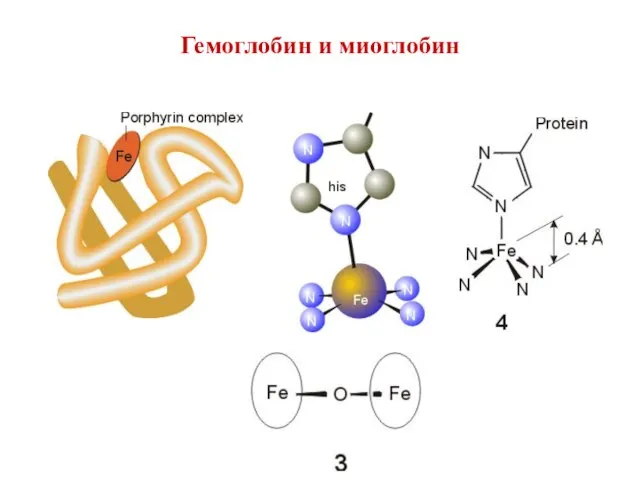
- 23. Гемоглобин и миоглобин
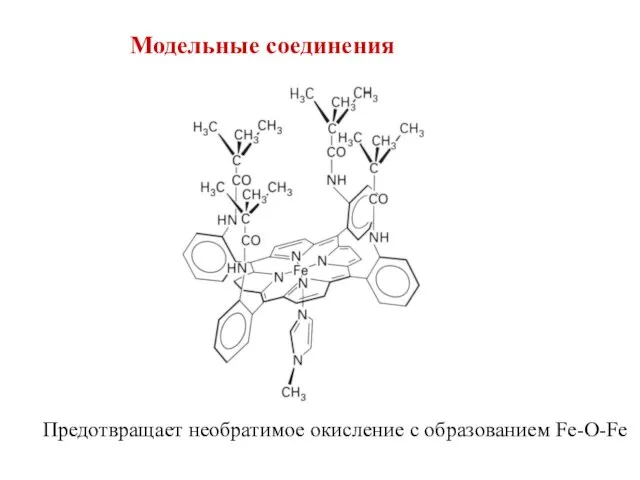
- 24. Модельные соединения Предотвращает необратимое окисление с образованием Fe-O-Fe
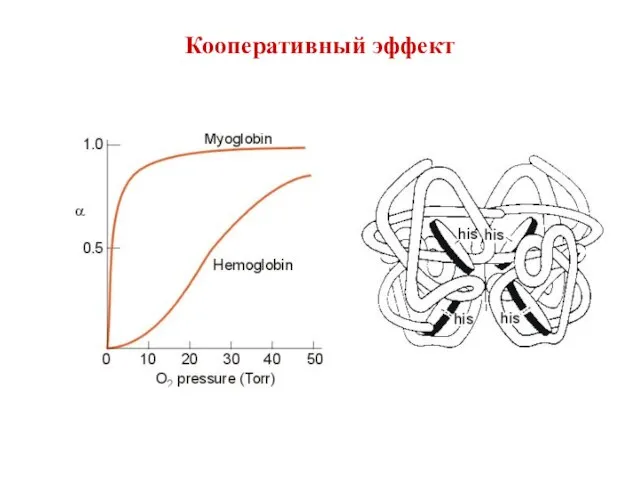
- 25. Кооперативный эффект
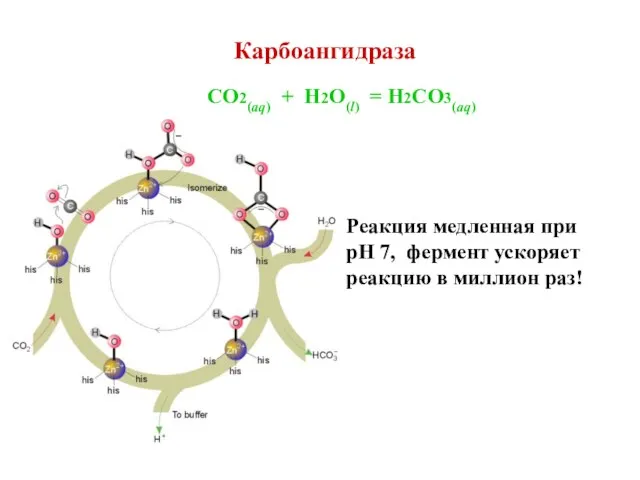
- 26. Карбоангидраза CO2(aq) + H2O(l) = H2CO3(aq) Реакция медленная при pH 7, фермент ускоряет реакцию в миллион
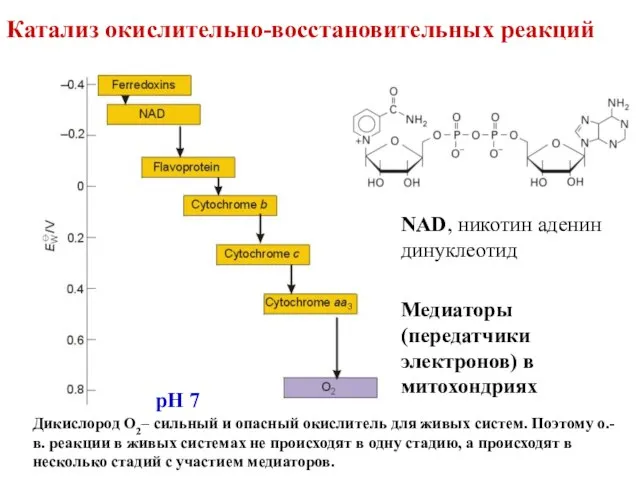
- 27. Катализ окислительно-восстановительных реакций pH 7 Медиаторы (передатчики электронов) в митохондриях NAD, никотин аденин динуклеотид Дикислород О2–
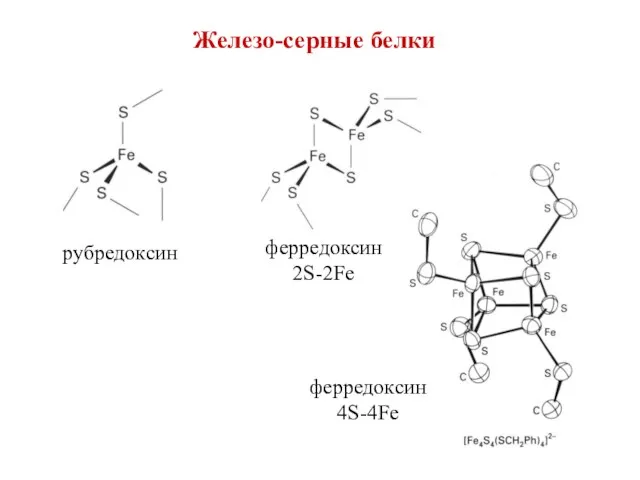
- 28. Железо-серные белки рубредоксин ферредоксин 2S-2Fe ферредоксин 4S-4Fe
- 29. [4Fe-4S] ферредоксины - небольшие (6-12 kDa) протеины, участвующие в разнообразных окислительно-восстановительных реакциях в живых системах. Они
- 30. Цитохромы и транспорт электронов
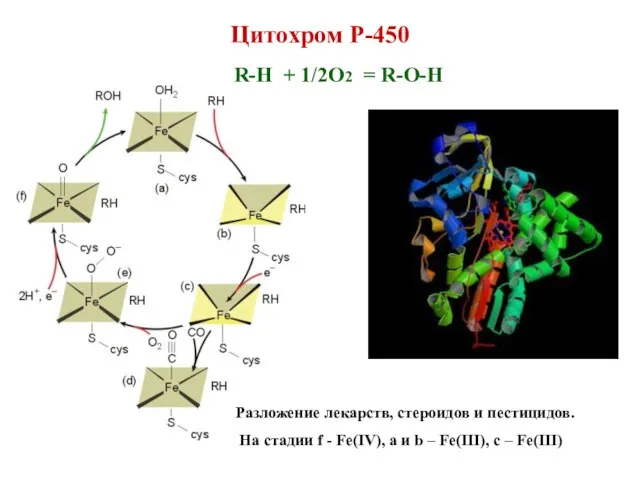
- 31. Цитохром Р-450 R-H + 1/2O2 = R-O-H Разложение лекарств, стероидов и пестицидов. На стадии f -
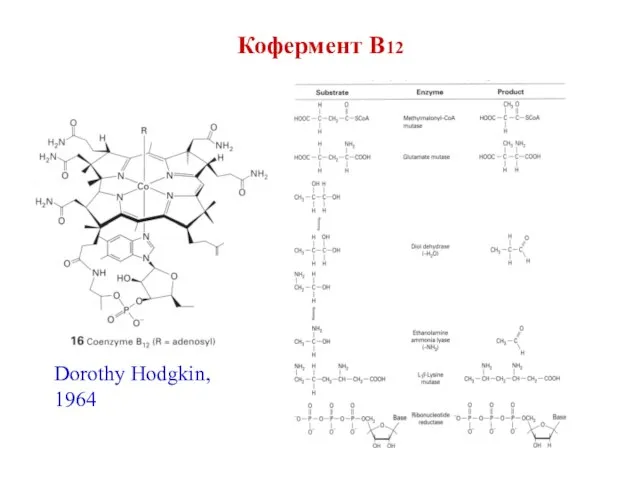
- 32. Кофермент В12 Dorothy Hodgkin, 1964
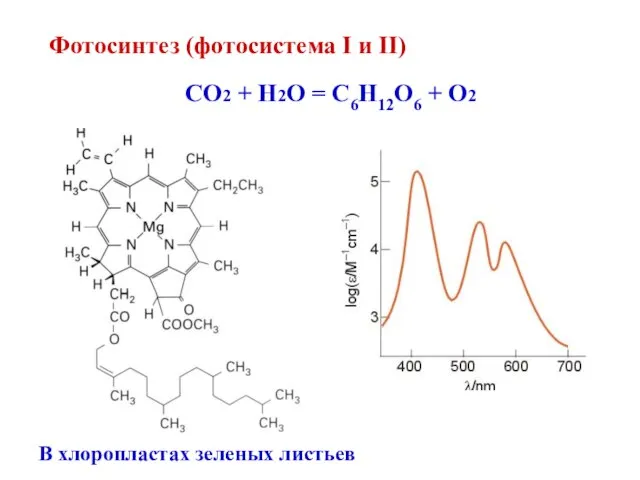
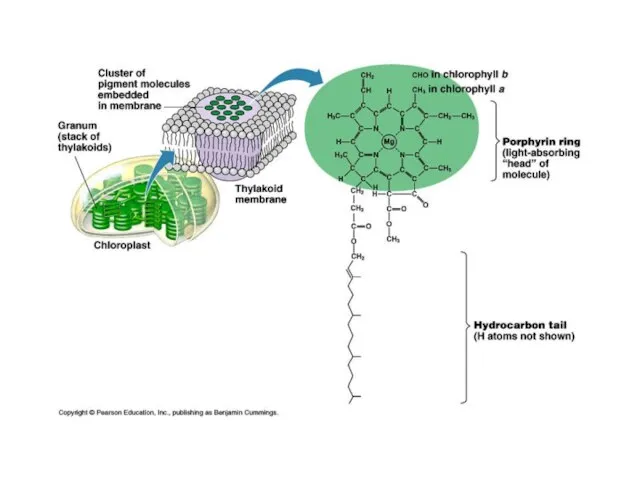
- 33. Фотосинтез (фотосистема I и II) CO2 + H2O = С6Н12О6 + O2 В хлоропластах зеленых листьев
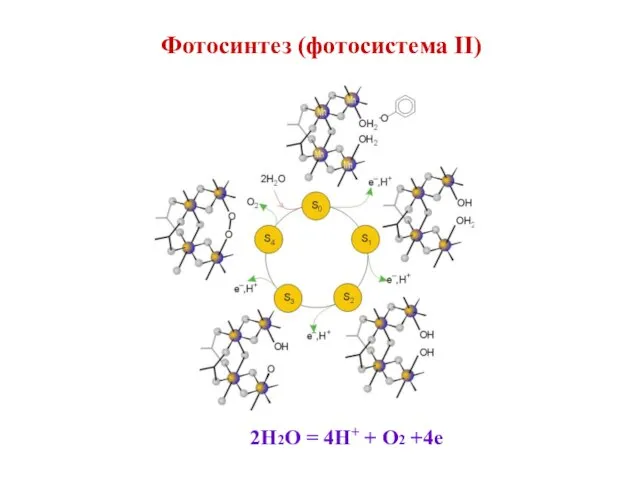
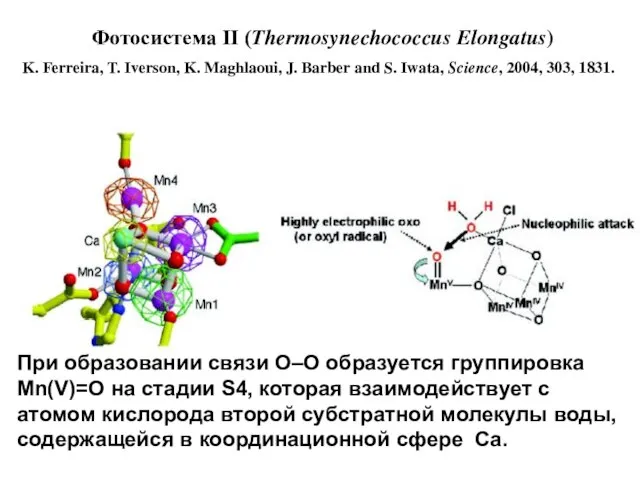
- 35. Фотосинтез (фотосистема II) 2H2O = 4H+ + O2 +4e
- 36. Фотосистема II (Thermosynechococcus Elongatus) K. Ferreira, T. Iverson, K. Maghlaoui, J. Barber and S. Iwata, Science,
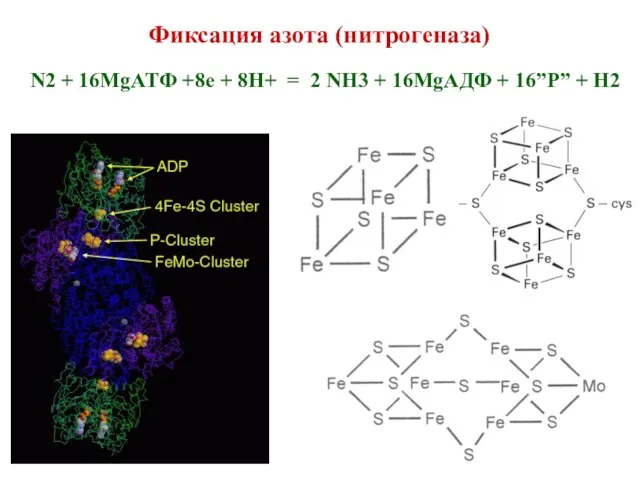
- 37. Фиксация азота (нитрогеназа) N2 + 16MgATФ +8e + 8H+ = 2 NH3 + 16MgAДФ + 16”P”
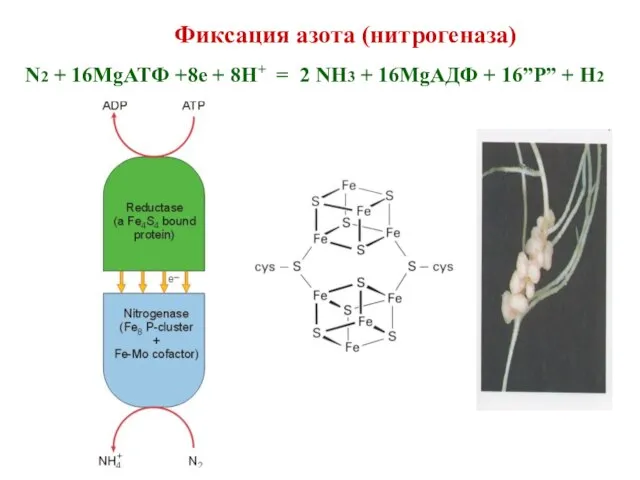
- 38. Фиксация азота (нитрогеназа) N2 + 16MgATФ +8e + 8H+ = 2 NH3 + 16MgAДФ + 16”P”
- 40. Скачать презентацию








![[4Fe-4S] ферредоксины - небольшие (6-12 kDa) протеины, участвующие в разнообразных окислительно-восстановительных реакциях](/_ipx/f_webp&q_80&fit_contain&s_1440x1080/imagesDir/jpg/441480/slide-28.jpg)

 Мозаики Ломоносова М.В.
Мозаики Ломоносова М.В. THE KAZAKHSTAN’S ARCHITECTURE of the Ancientry and the Middle Ages / STYLES OF THE KAZAKHSTAN’S ARCHITECTURE (by K.I.Samoilov)
THE KAZAKHSTAN’S ARCHITECTURE of the Ancientry and the Middle Ages / STYLES OF THE KAZAKHSTAN’S ARCHITECTURE (by K.I.Samoilov) Области педагогики, исследования в которых приобрели особую актуальность в связи с задачами непрерывного образования
Области педагогики, исследования в которых приобрели особую актуальность в связи с задачами непрерывного образования Красота своими руками. Работы бисером
Красота своими руками. Работы бисером Обеспечение практической реализации закона об энергосбережении и о повышении энергетической эффективности
Обеспечение практической реализации закона об энергосбережении и о повышении энергетической эффективности Валютный курс. Факторы и режимы валютного курса
Валютный курс. Факторы и режимы валютного курса Лабораторная работа №4.Тема. Строение зрительного анализатора.Цель: изучить строение органа зрения. Оборудование: ПК, презента
Лабораторная работа №4.Тема. Строение зрительного анализатора.Цель: изучить строение органа зрения. Оборудование: ПК, презента Спорт в моей жизни
Спорт в моей жизни Презентация на тему Характеристика щелочных металлов 9 класс
Презентация на тему Характеристика щелочных металлов 9 класс Презентация на тему Нефтяная промышленность России 9 класс
Презентация на тему Нефтяная промышленность России 9 класс Что такое симметрия
Что такое симметрия Презентация на тему Работа социального педагогам с детьми девиантного поведения
Презентация на тему Работа социального педагогам с детьми девиантного поведения Семейное право. Правовая связь членов семьи
Семейное право. Правовая связь членов семьи Город Зарайск
Город Зарайск Портрет парадный и лирический
Портрет парадный и лирический Правовой статус гражданина РФ
Правовой статус гражданина РФ Презентация на тему Иммануил Кант
Презентация на тему Иммануил Кант PREZENTATsIYa_soglashenie_o_namerenia
PREZENTATsIYa_soglashenie_o_namerenia Глобальные прогнозы
Глобальные прогнозы Презентация на тему: Понятие квадратного корня из неотрицательного числа
Презентация на тему: Понятие квадратного корня из неотрицательного числа Самоконтроль при занятиях физическими упражнениями. Лекция 1
Самоконтроль при занятиях физическими упражнениями. Лекция 1 Б. М. Кустодиев. (1878-1927)
Б. М. Кустодиев. (1878-1927) Жуков Дмитрий - кандидат в председатели комиссии по спортивной работе
Жуков Дмитрий - кандидат в председатели комиссии по спортивной работе «НАШ НОВЫЙ ДЕТСКИЙ САД»
«НАШ НОВЫЙ ДЕТСКИЙ САД» Политика и власть. 10 класс
Политика и власть. 10 класс Русская тема в художественной культуре периода оттепели
Русская тема в художественной культуре периода оттепели Николай Хмеленок. Тренажёры по английскому языку. Расположите по порядку. Части тела
Николай Хмеленок. Тренажёры по английскому языку. Расположите по порядку. Части тела КРИМИНОЛОГИЯ
КРИМИНОЛОГИЯ