Содержание
- 2. Внутренняя среда организма формируется совокупностью биологических жидкостей (кровь, лимфа, тканевая жидкость), омывающих клетки и структуры тканей.
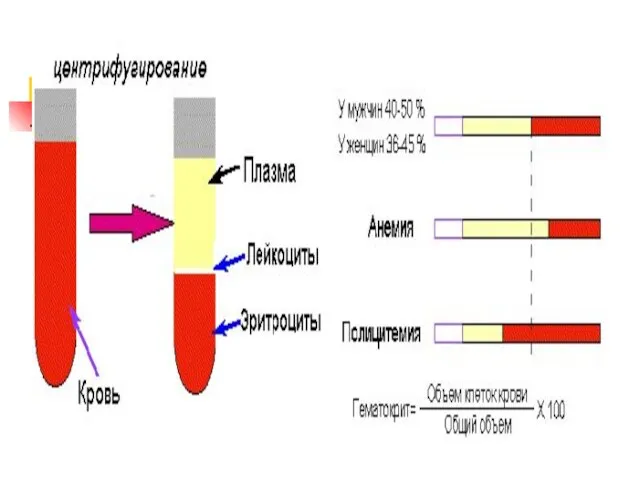
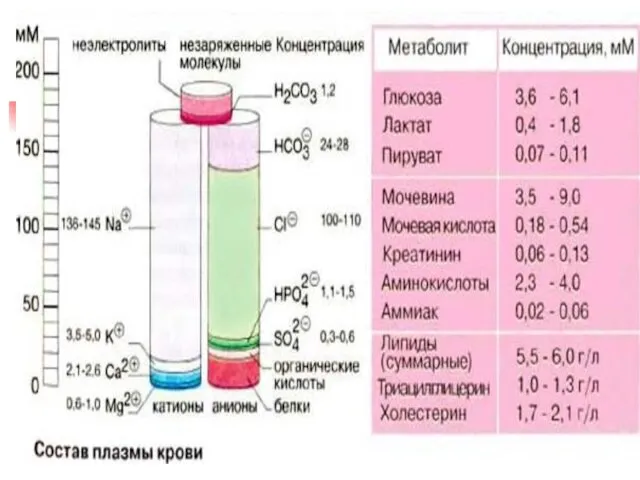
- 4. Химический состав плазмы
- 5. Функции крови Дыхательная -транспорт кислорода от легких к тканям и CO2 от тканей к легким Выделительная
- 6. Химический состав крови Большую часть этих функций выполняют компоненты плазмы крови. Плазма крови состоит на 90-93%
- 7. Характеристика белков плазмы крови содержатся в плазме крови синтезируются в печени или РЭС (реже в специализированных
- 8. Состав белков плазмы крови В плазме обнаружено более 100 разных белков соответствующих этим критериям, содержание которых
- 9. Остаточный азот Все азотсодержащие вещества плазмы образуют общий пул азота, состоящий из: Азота белкового – осаждаемого
- 10. Состав ОА Мочевина - 50% (главный компонент) АК - 25% (~ 10% ГЛУ и ГЛН) Ураты
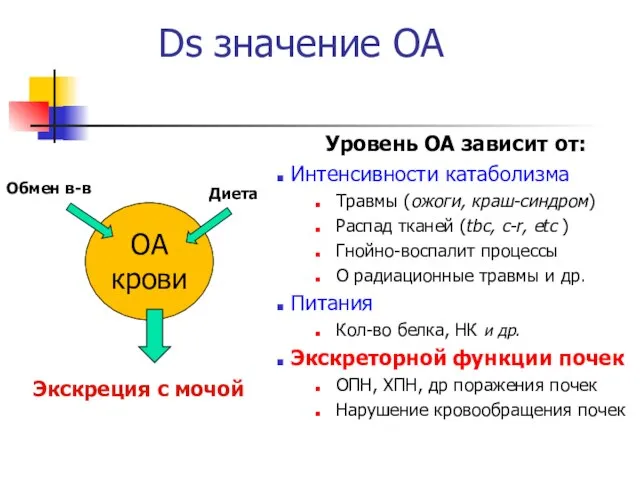
- 11. Ds значение ОА Уровень ОА зависит от: Интенсивности катаболизма Травмы (ожоги, краш-синдром) Распад тканей (tbc, c-r,
- 12. Азотемия - повышение уровня ОА в крови Ретенционная – задержка компонентов ОА в организме из-за нарушения
- 13. Общие понятия КОС КОС – система гомеостаза рН внутри- и внеклеточной среды организма. Единицы измерения :рН
- 14. рН – производное метаболизма За сутки организм hs образует 50-100 мМ [Н+] на 15-20л ВКЖ. Весь
- 15. Стабильный рН - необходимое условие метаболизма Изменение рН приводит к изменению: заряда и функции белков (ферментов,
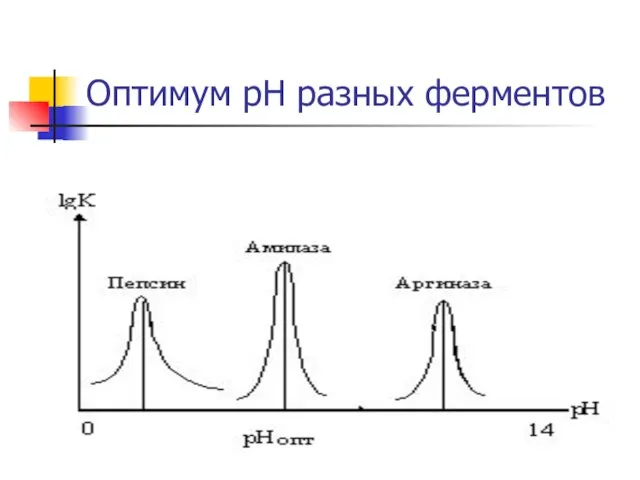
- 16. Оптимум рН разных ферментов
- 17. Изоосмолярность – осм. давление=310 осМ/л - const любые изменения должны поддерживать эту константу Электронейтральность – (по
- 19. Механизмы регуляции КОС Физико-хим – действует в автоматическом режиме и представлен: разбавлением т.е. выходом Н+ или
- 20. Классификация нарушений КОС рНО =7.40±0.04 рН = 7.35 и ниже – ацидоз рН = 7.45 и
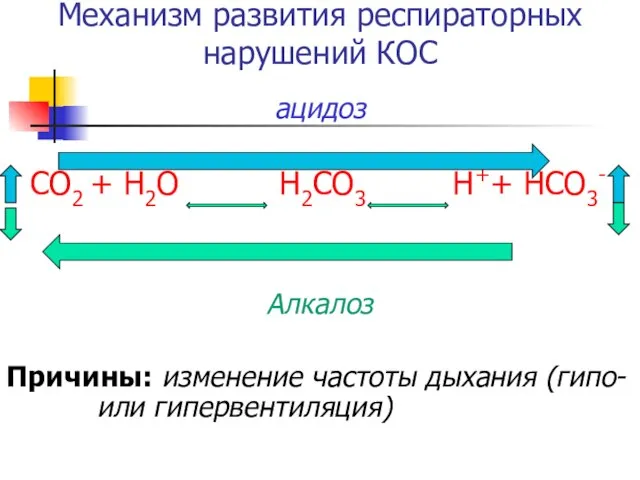
- 21. Механизм развития респираторных нарушений КОС ацидоз СО2 + Н2О Н2СО3 Н++ НСО3- Алкалоз Причины: изменение частоты
- 22. Межорганное взаимодействие в регуляции рН Если этих респираторных механизмов недостаточно, то активируются др.экскреторные системы. В печени
- 25. Эритропоэтин (Эпо) Эпо – цитокин, специфический регулятор эритропоэза в костном мозге Эпо человека – гликопротеид, состоит
- 26. Э общий обзор Кол-во Э у мужчин - 4.6-6.2 млн/мкл крови, а у женщин - 4.2-5.4
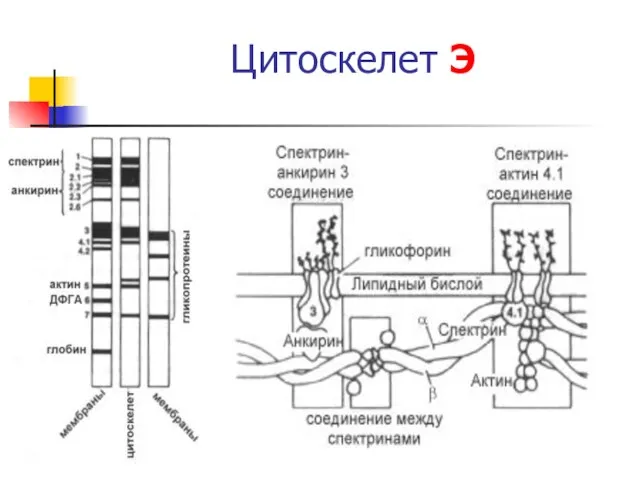
- 27. Цитоскелет Э
- 28. Структура цитоскелета Э Большинство мембран Э - интегральные Б, гликопротеиды. Б без углеводной части находятся на
- 29. Метаболизм глюкозы в Э Глюкоза в Э используется в: Гликолизе (90-95%) – образование АТФ ПФП (10-5%)
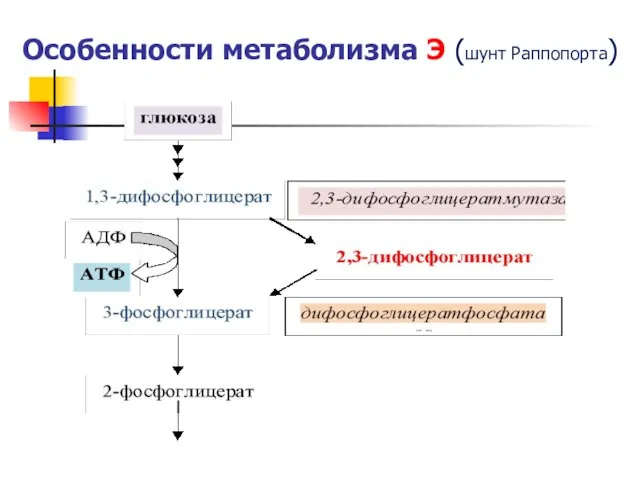
- 30. Особенности метаболизма Э (шунт Раппопорта)
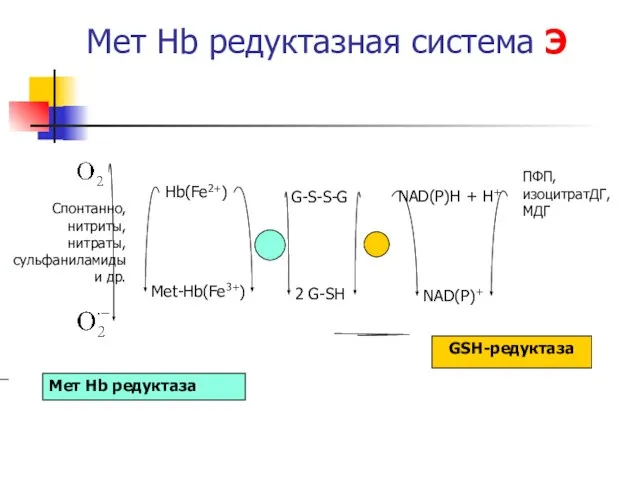
- 31. Мет Hb редуктазная система Э Hb(Fe2+) Met-Hb(Fe3+) 2 G-SH G-S-S-G NAD(P)H + H+ NAD(P)+ Мет Hb
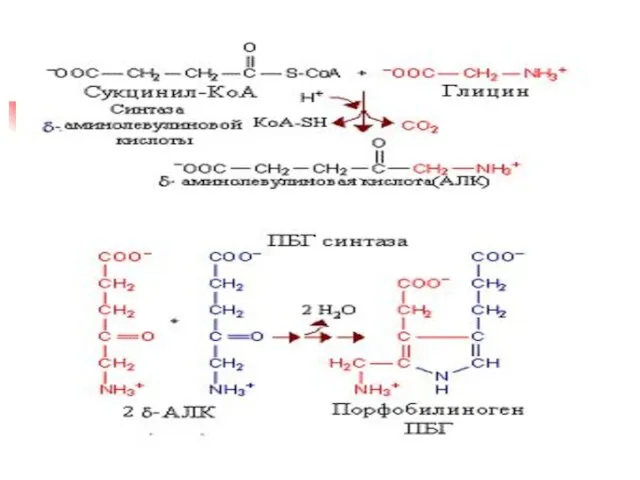
- 32. Синтез порфобилиногена и гема Первая реакция б/с гема происходит в Мх и происходит путем конденсации гли
- 34. Синтез порфобилиногена и гема (прод) Затем следует этап конденсации (голова-хвост) 4 молекул порфобилиногена с образованием линейного
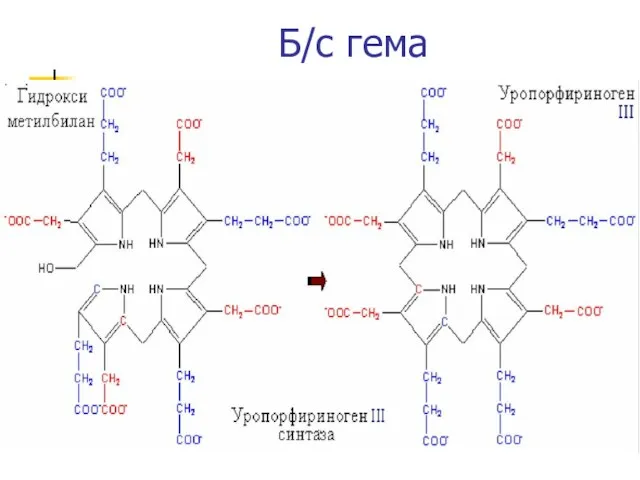
- 35. Б/с гема
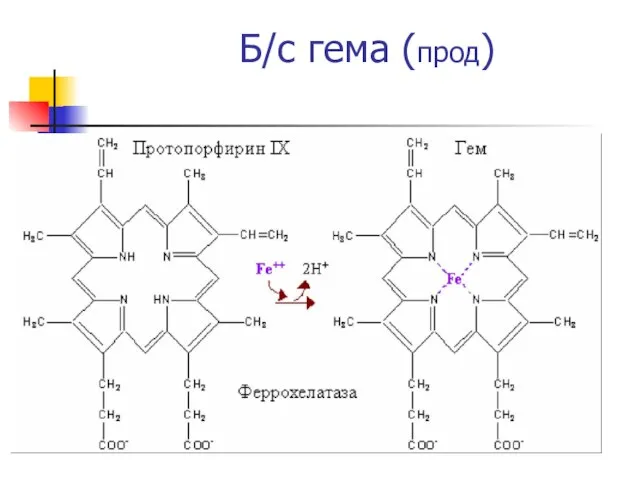
- 36. Б/с гема (прод)
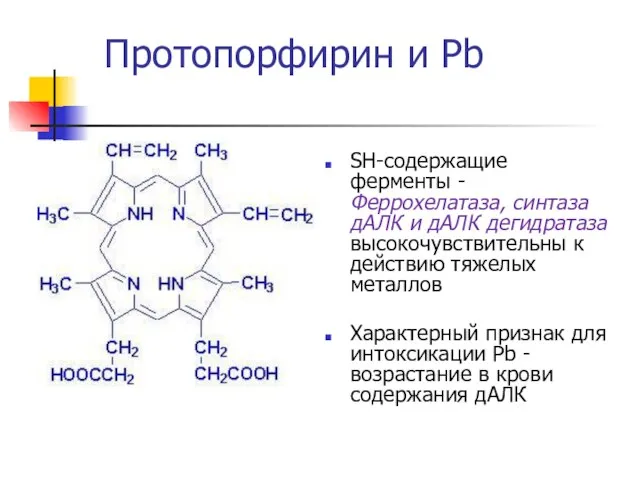
- 37. SH-содержащие ферменты - Феррохелатаза, синтаза дАЛК и дАЛК дегидратаза высокочувствительны к действию тяжелых металлов Характерный признак
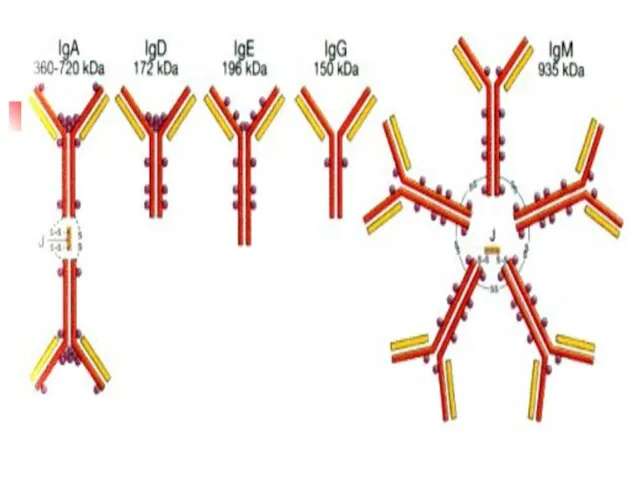
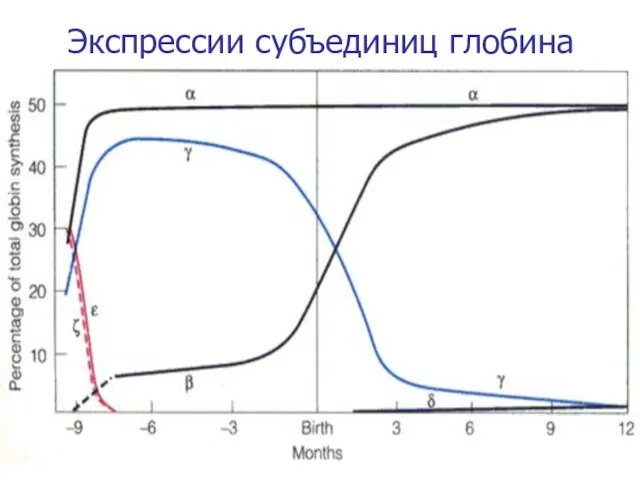
- 38. Экспрессии субъединиц глобина
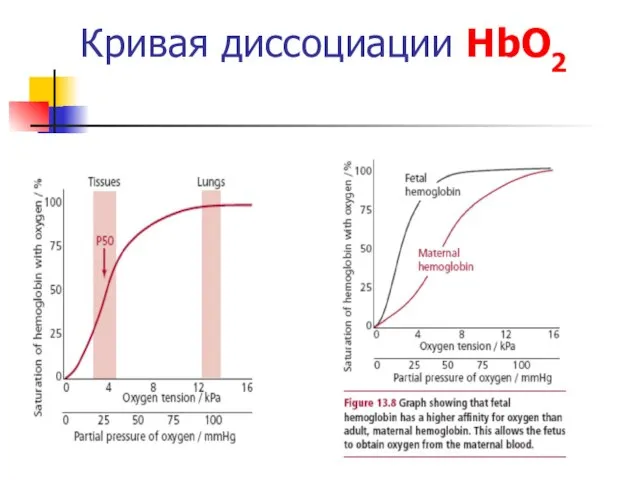
- 39. Кривая диссоциации HbО2
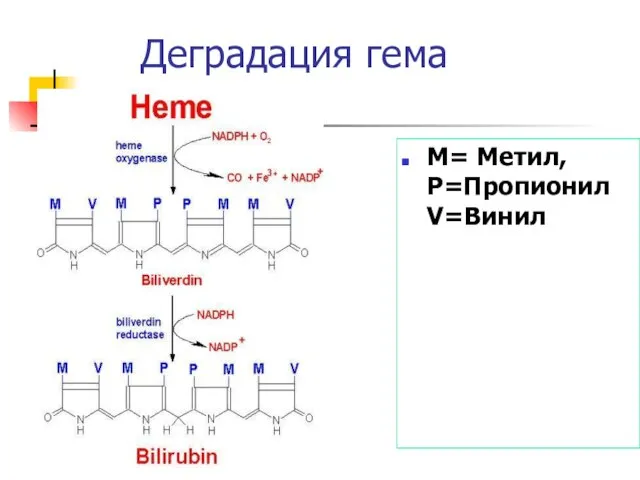
- 40. Распад гема Продолжительность жизни Э ~120 дней, ежедневный оборот Hb ~6 г/день. Гем из старых Э
- 41. Образование билирубина Следующий этап СН2 мост (между кольцами III и IV) биливердина восстанавливается биливердин редуктазой до
- 42. Деградация гема M= Метил, P=Пропионил V=Винил
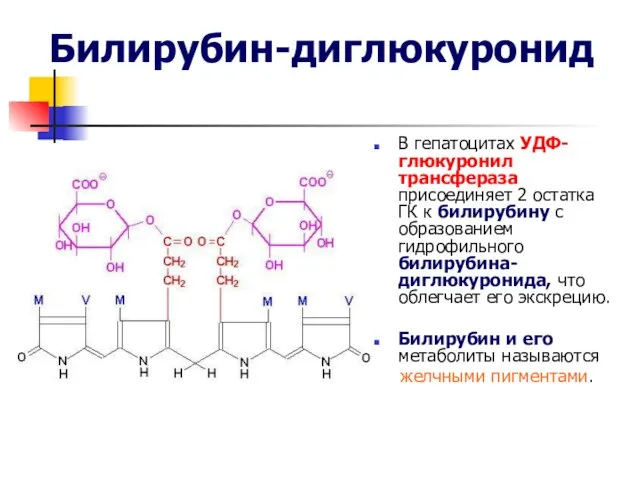
- 43. Билирубин-диглюкуронид В гепатоцитах УДФ-глюкуронил трансфераза присоединяет 2 остатка ГК к билирубину с образованием гидрофильного билирубина-диглюкуронида, что
- 44. Клинические аспекты метаболизма гема представлены в виде: Дефектов ферментов и нарушения б/с гема – порфирий, которые
- 45. Желтухи Гипербилирубинемия проявляется в виде желтух – желтой пигментации кожи и слизистых. В норме в кишечнике
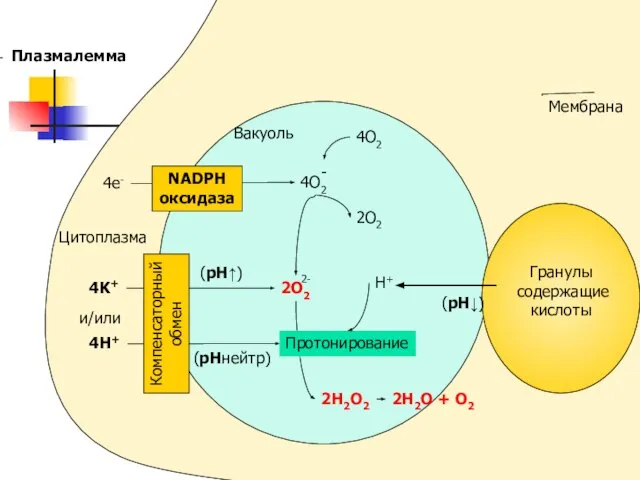
- 46. Нейтрофилы (гранулоциты) –полиморфноядерные лейкоциты: обладают выраженной способностью к фагоцитозу, Хорошо развитый, подвижный цитоскелет, Активное Мх и
- 47. 4O2 2O2 H+ 2H2O2 2H2O + O2 (pH↓) Цитоплазма 4e- Вакуоль 4K+ и/или 4H+ (pHнейтр) (pH↑)
- 49. Скачать презентацию










![рН – производное метаболизма За сутки организм hs образует 50-100 мМ [Н+]](/_ipx/f_webp&q_80&fit_contain&s_1440x1080/imagesDir/jpg/382117/slide-13.jpg)
















 Вышивка. Образ птицы
Вышивка. Образ птицы Орфографическая диктовка
Орфографическая диктовка Для сх
Для сх Натюрморт
Натюрморт Права несовершеннолетних
Права несовершеннолетних СТОП вырубке ёлок!
СТОП вырубке ёлок! Русский мир
Русский мир Исследование развития речи детей старшего дошкольного возраста в игровой деятельности
Исследование развития речи детей старшего дошкольного возраста в игровой деятельности Предпрофильная подготовка и профильное обучение. Государственная (итоговая) аттестация выпускников
Предпрофильная подготовка и профильное обучение. Государственная (итоговая) аттестация выпускников Физиология мотивации
Физиология мотивации Маркетинговая стратегия
Маркетинговая стратегия СОЦИАЛЬНАЯ МОБИЛЬНОСТЬ
СОЦИАЛЬНАЯ МОБИЛЬНОСТЬ  Иконы православных праздников
Иконы православных праздников Олимпийские игры в Древней Греции
Олимпийские игры в Древней Греции Бумажная филигрань Бумагокручение Квиллинг
Бумажная филигрань Бумагокручение Квиллинг Бенчмаркинг, как инструмент управления организацией
Бенчмаркинг, как инструмент управления организацией Стандартизация. Общие положения стандартизации
Стандартизация. Общие положения стандартизации «Поспорили однажды корень, стебель, лист – кто из них важнее?»
«Поспорили однажды корень, стебель, лист – кто из них важнее?» В море коварном товаров и цен. Бизнес-корабль ведёт…
В море коварном товаров и цен. Бизнес-корабль ведёт… ИНФОРМАЦИЯ. ИНФОРМАТИКА.ИНФОРМАТИЗАЦИЯ.
ИНФОРМАЦИЯ. ИНФОРМАТИКА.ИНФОРМАТИЗАЦИЯ. Служу Отечеству
Служу Отечеству Продукты для «1С:Предприятия»
Продукты для «1С:Предприятия» Dadaisms mērķis. Veidot izpratni par modernisma virzienu dadaismu
Dadaisms mērķis. Veidot izpratni par modernisma virzienu dadaismu Урок -путешествие
Урок -путешествие Прогнозирование и анализ временных рядов
Прогнозирование и анализ временных рядов هدف از معامله کردن در بازار فارکس
هدف از معامله کردن در بازار فارکس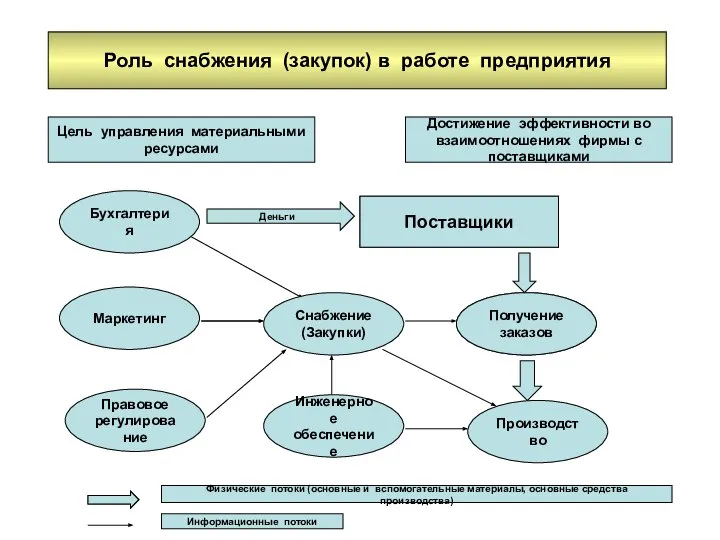 Роль снабжения, закупок в работе предприятия
Роль снабжения, закупок в работе предприятия Правописание о – е после шипящих и ц в окончаниях существительных 5 класс
Правописание о – е после шипящих и ц в окончаниях существительных 5 класс