Содержание
- 2. Что такое химия Химия – это наука, изучающая вещества, их свойства, взаимопревращения веществ, условия, при которых
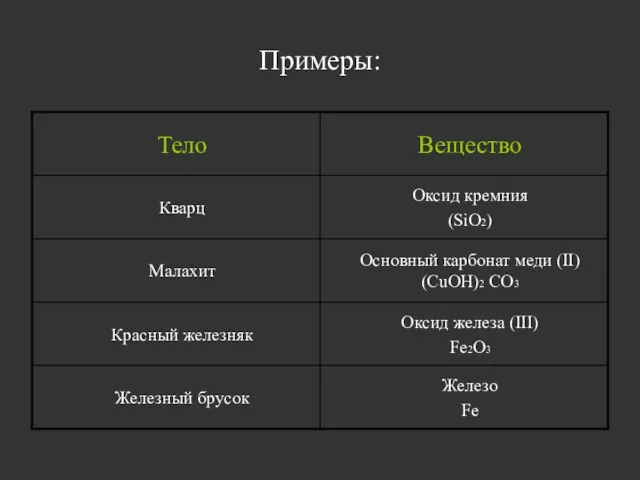
- 3. Примеры:
- 4. Свойства вещества Свойством вещества называется признак, по которому данное вещество может быть сходно, либо отличаться от
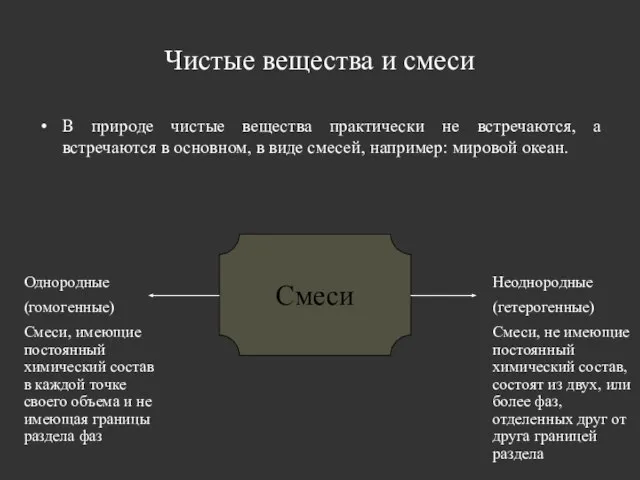
- 5. Чистые вещества и смеси В природе чистые вещества практически не встречаются, а встречаются в основном, в
- 6. Способы разделения гетерогенной смеси Разделение 2-х не смешанных жидкостей с помощью воронки С помощью магнита Фильтрование
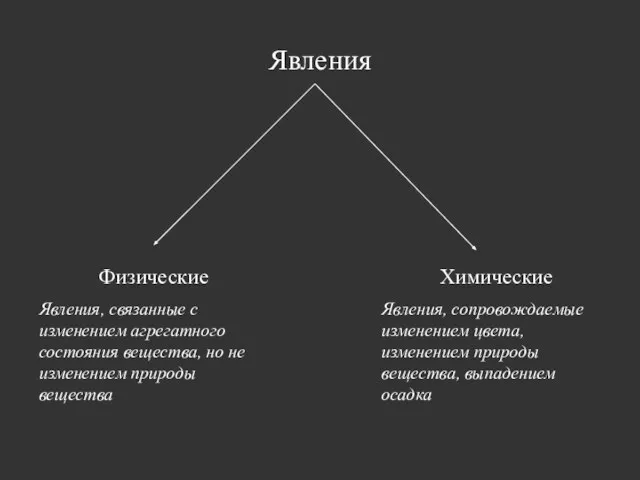
- 7. Явления Физические Явления, связанные с изменением агрегатного состояния вещества, но не изменением природы вещества Химические Явления,
- 8. Молекулы и атомы Молекула – мельчайшая частица вещества, обладающая всеми его свойствами, находящаяся в непрерывном, хаотичном
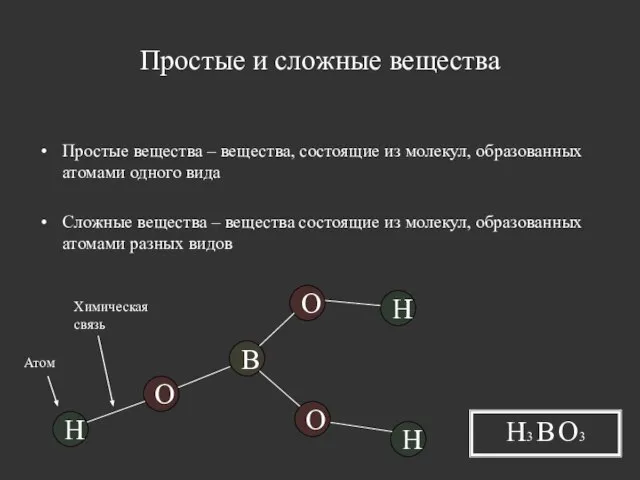
- 9. Простые и сложные вещества Простые вещества – вещества, состоящие из молекул, образованных атомами одного вида Сложные
- 10. Химический элемент Химический элемент – ключевое понятие химии, это определенный вид атомов Простое вещество состоит из
- 11. Относительная атомная масса Самый легкий атом – атом водорода (H) Атомная единица массы (а.е.м.) равна 1/12
- 12. Химическая формула 3CuCl2 Коэффициент Индекс Химическая формула – условная запись состава вещества посредством химических знаков и
- 13. Относительная молекулярная масса вещества Относительная молекулярная масса вещества показывает во сколько раз масса молекулы данного вещества
- 14. Задача на вычисление относительной молекулярной массы H2SO4 Решение: Для вычисления относительной молекулярной массы необходимо суммировать относительные
- 15. Валентность Это количество химических связей, которые образует атом в данном соединении с другими атомами. O O
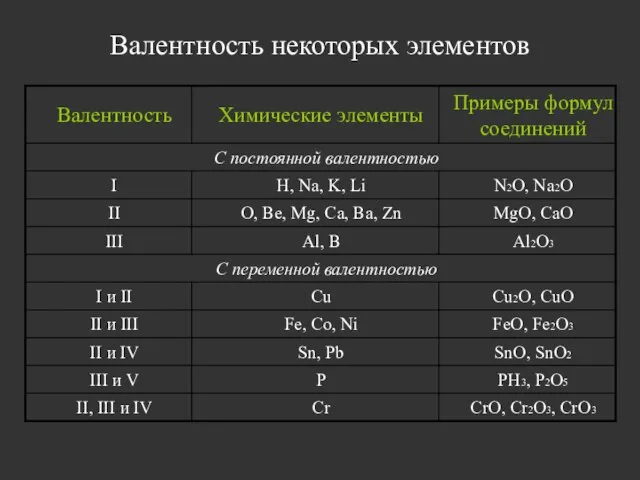
- 16. Валентность некоторых элементов
- 17. Структурная формула Формула, отражающая не только состав молекулы, но и ее строение, то есть взаимное расположение
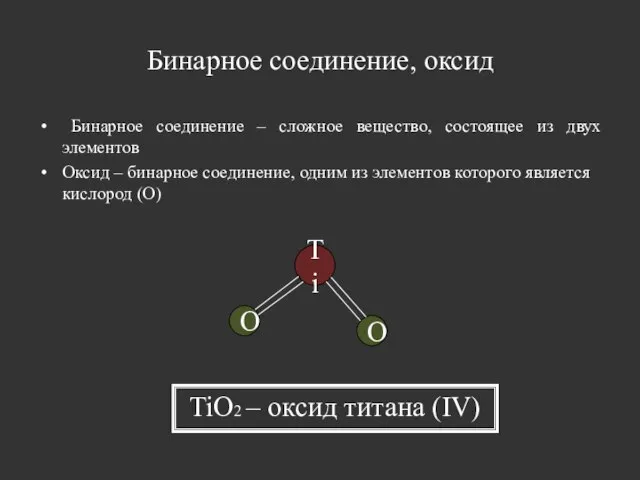
- 18. Бинарное соединение, оксид Бинарное соединение – сложное вещество, состоящее из двух элементов Оксид – бинарное соединение,
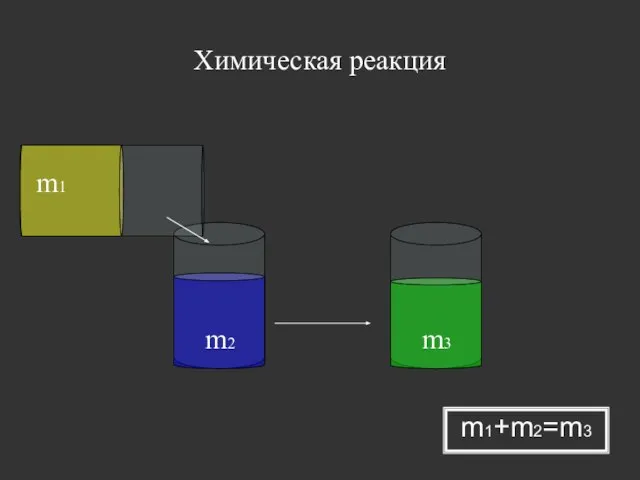
- 19. Закон сохранения массы веществ В ходе химической реакции, общая масса вещества не изменится, то есть, общая
- 20. m1 m2 m3 Химическая реакция m1+m2=m3
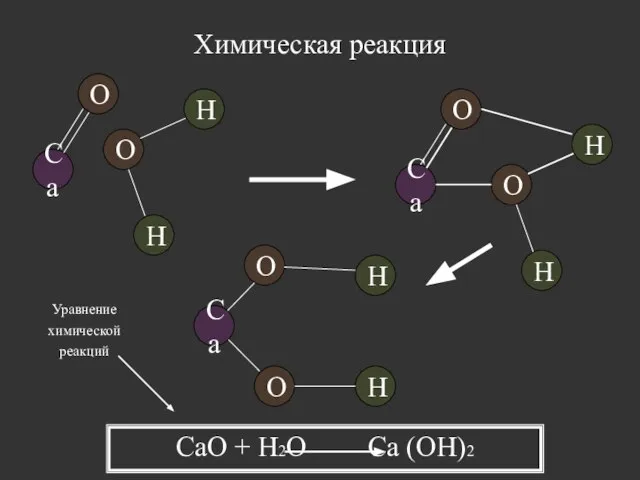
- 21. Химическая реакция Химическая Реакция – превращение одних веществ в другие Явление перегруппировки атомов, сопровождающееся разрушением одних
- 22. Химическая реакция O O H H Ca Ca O O H H O O H H
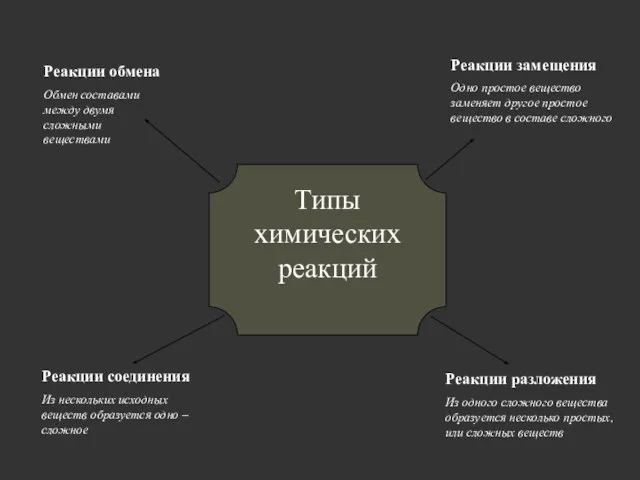
- 23. Типы химических реакций Реакции соединения Из нескольких исходных веществ образуется одно – сложное Реакции разложения Из
- 24. Моль. Молярная масса. Количество вещества. Моль – физическая величина показывающая количество вещества, равная количеству вещества содержащего
- 26. Скачать презентацию














 Основные направления инвестирования в Российской Федерации
Основные направления инвестирования в Российской Федерации  Учебная дисциплина. Психология
Учебная дисциплина. Психология Ачинск – город с историей
Ачинск – город с историей Презентация на тему Государства и народы доколумбовой Америки
Презентация на тему Государства и народы доколумбовой Америки  Сочинение с элементами описания внутреннего состояния по картине Н. Богданова-Бельского «У дверей школы»
Сочинение с элементами описания внутреннего состояния по картине Н. Богданова-Бельского «У дверей школы» Откройте для себя здоровую, юную кожу
Откройте для себя здоровую, юную кожу ПРАВАЧЕЛОВЕКА
ПРАВАЧЕЛОВЕКА Принципы организации судебной власти
Принципы организации судебной власти « У нас много замечательных и любимых не только нами, но и всем миром, писателей. Чехов занимает одно из первых мест среди них ». К. А.
« У нас много замечательных и любимых не только нами, но и всем миром, писателей. Чехов занимает одно из первых мест среди них ». К. А.  Музыкальная живопись и живописная музыка. Импрессионизм.
Музыкальная живопись и живописная музыка. Импрессионизм. Установка для повторного нанесения покрытия на аноды компании Каустик
Установка для повторного нанесения покрытия на аноды компании Каустик Rome Model United Nations Rome International Careers
Rome Model United Nations Rome International Careers  История Российского самодержавия
История Российского самодержавия Добро пожаловать на час общения «Поговорим о любви»
Добро пожаловать на час общения «Поговорим о любви» Технология моделирования в начальной школе Сложным является сообщение учащимся знаний, так как их объем из года в год увеличивает
Технология моделирования в начальной школе Сложным является сообщение учащимся знаний, так как их объем из года в год увеличивает Рациональное питание. Расчет меню
Рациональное питание. Расчет меню Планета дорог
Планета дорог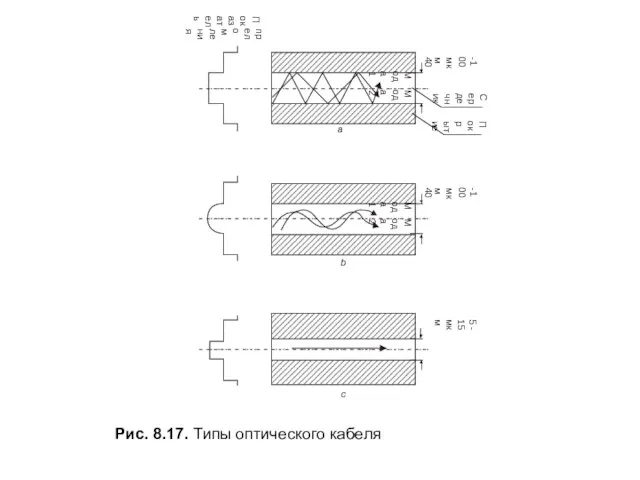 Рис. 8.17. Типы оптического кабеля
Рис. 8.17. Типы оптического кабеля Обширный информационный сервис по Европейскому Союзу, странам Европы и актульным событиям, происходящим в Европе
Обширный информационный сервис по Европейскому Союзу, странам Европы и актульным событиям, происходящим в Европе Идеал человеческого единства
Идеал человеческого единства Конкурс «Роялти – педагогу новатору»
Конкурс «Роялти – педагогу новатору» Современное состояние классовой борьбы в Австралии и Новой Зеландии
Современное состояние классовой борьбы в Австралии и Новой Зеландии Фото_Чек_лист_08_09_2022_ПВЗ_Октябрьское_поле
Фото_Чек_лист_08_09_2022_ПВЗ_Октябрьское_поле Причастия действительные и страдательные
Причастия действительные и страдательные Презентация на тему Природная зона тайги
Презентация на тему Природная зона тайги Multilayer model in optics. New analitic results.
Multilayer model in optics. New analitic results. Синтаксическая стилистика
Синтаксическая стилистика Презентация на тему Совесть и раскаяние (4 класс)
Презентация на тему Совесть и раскаяние (4 класс)