Содержание
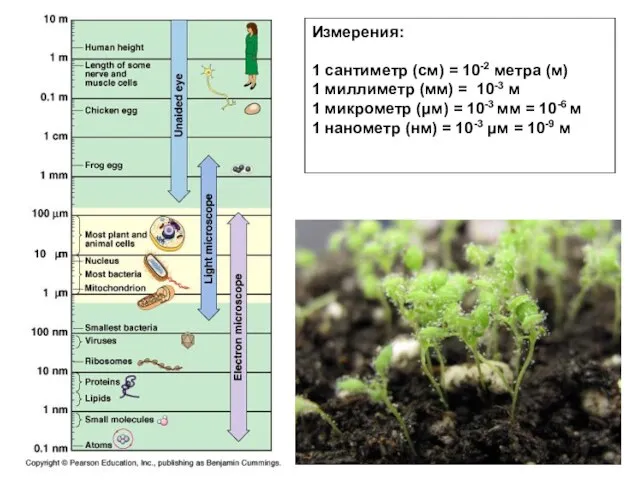
- 2. Измерения: 1 сантиметр (cм) = 10-2 метра (м) 1 миллиметр (мм) = 10-3 м 1 микрометр
- 3. Уровни организации (международная классификация, 2011 год): Atoms Molecules Assemblies Cells Tissue Organ Organ system Organism Population
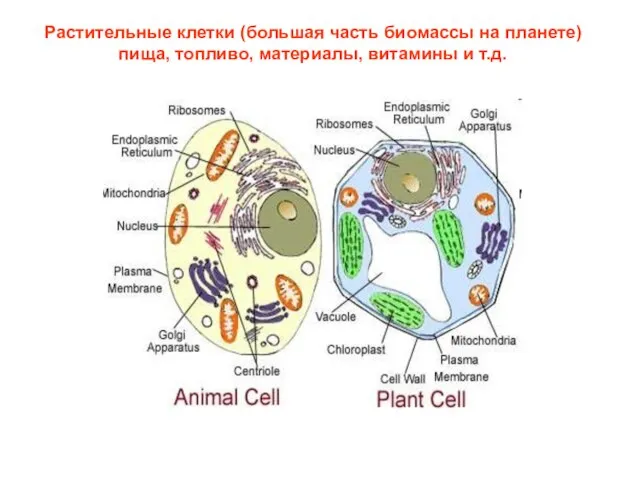
- 4. Растительные клетки (большая часть биомассы на планете) пища, топливо, материалы, витамины и т.д.
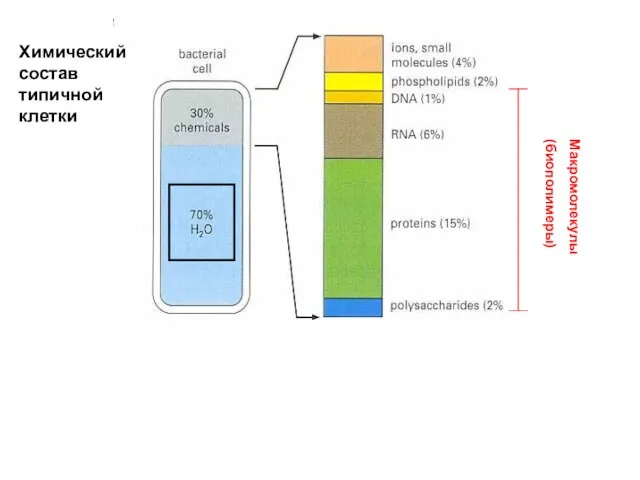
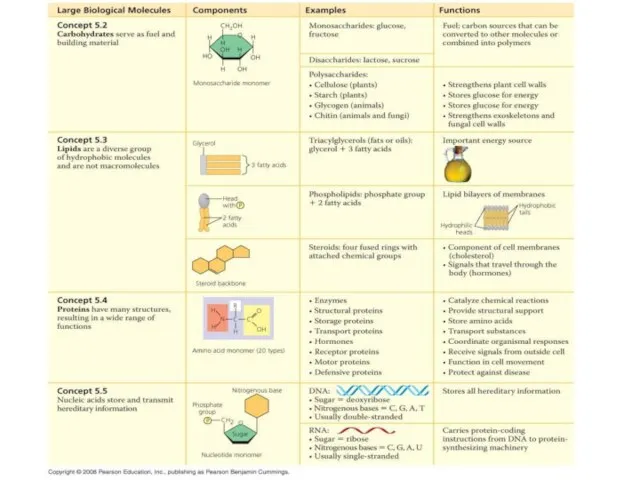
- 5. Химический состав типичной клетки Макромолекулы (биополимеры)
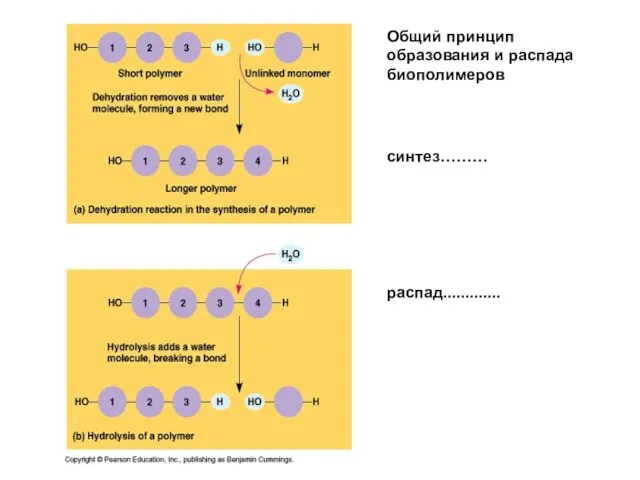
- 6. Общий принцип образования и распада биополимеров синтез……… распад.............
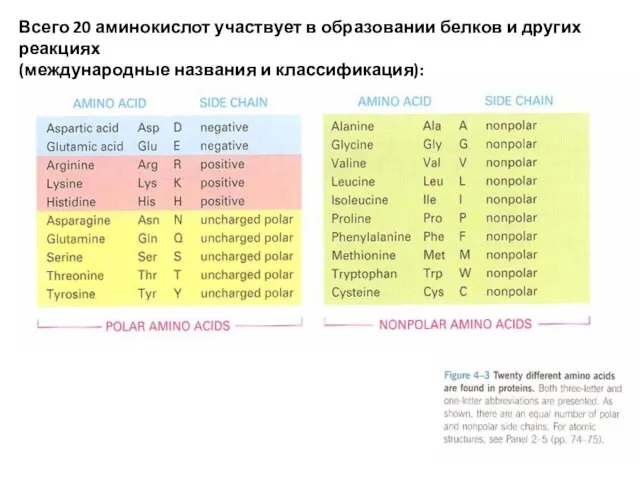
- 7. Всего 20 аминокислот участвует в образовании белков и других реакциях (международные названия и классификация):
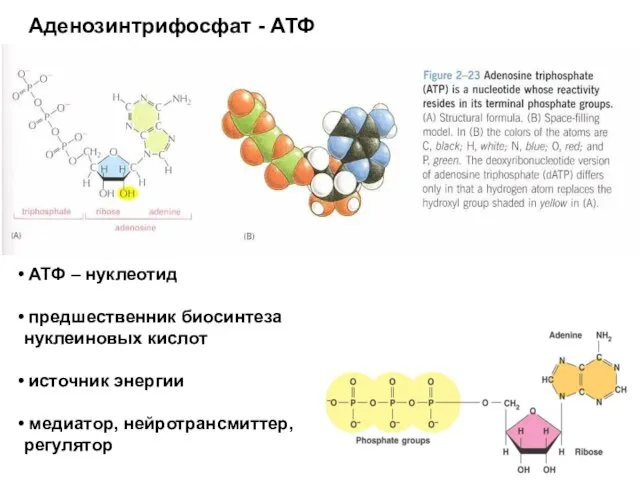
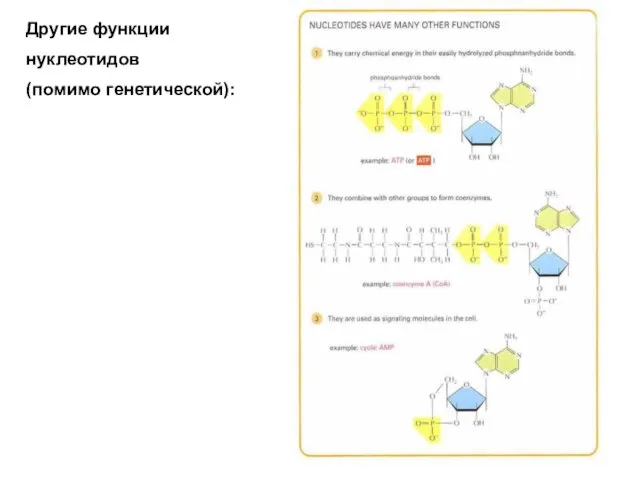
- 8. Аденозинтрифосфат - АТФ АТФ – нуклеотид предшественник биосинтеза нуклеиновых кислот источник энергии медиатор, нейротрансмиттер, регулятор
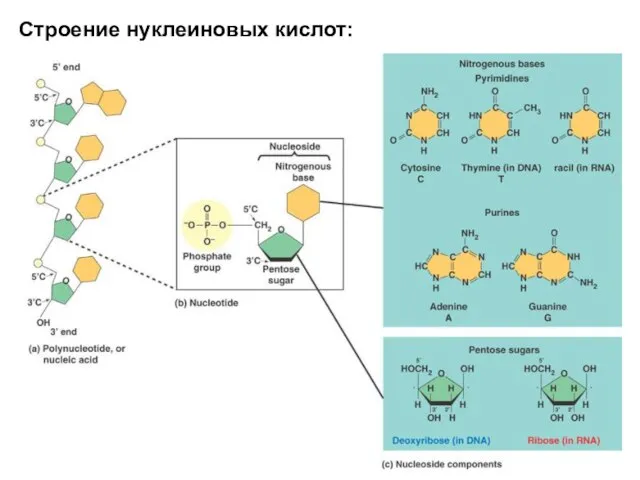
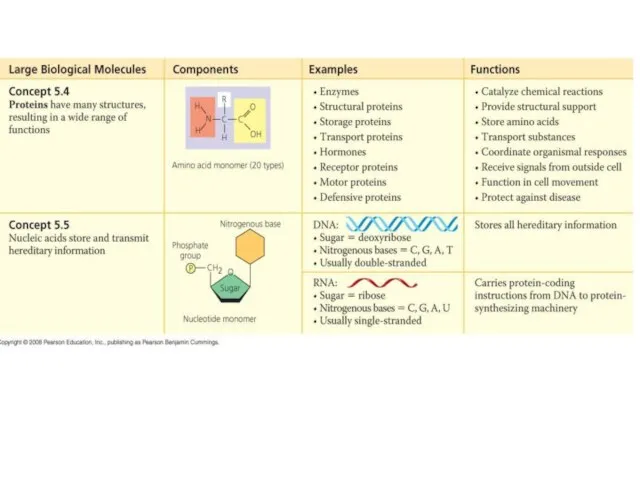
- 9. Строение нуклеиновых кислот:
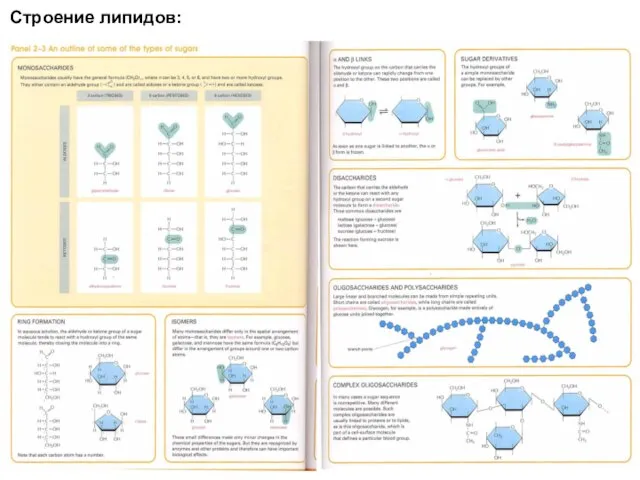
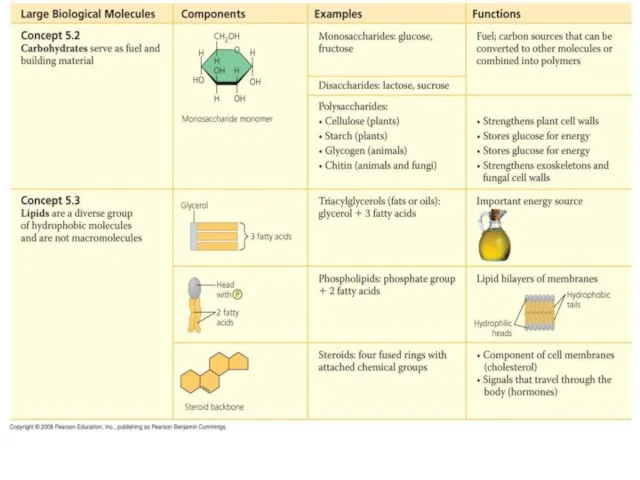
- 10. Строение липидов:
- 11. Строение липидов:
- 19. Разнообразие комбинаций трех полимеров определяет разнообразие живого на планете. Растения, животные и грибы имеют одинаковые «мономеры»
- 20. Семь функциональных групп, которые наиболее важны в биохимических процессах: Гидроксильная Карбонильная Карбоксильная Амино Сульфгидрильная Фосфатная Метильная
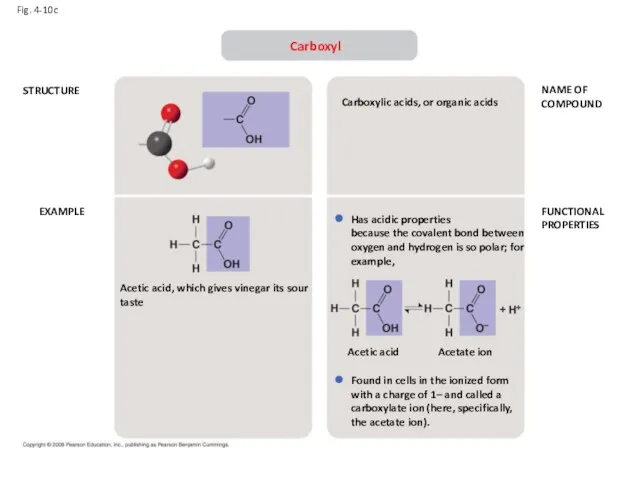
- 21. Fig. 4-10c STRUCTURE EXAMPLE NAME OF COMPOUND FUNCTIONAL PROPERTIES Carboxyl Acetic acid, which gives vinegar its
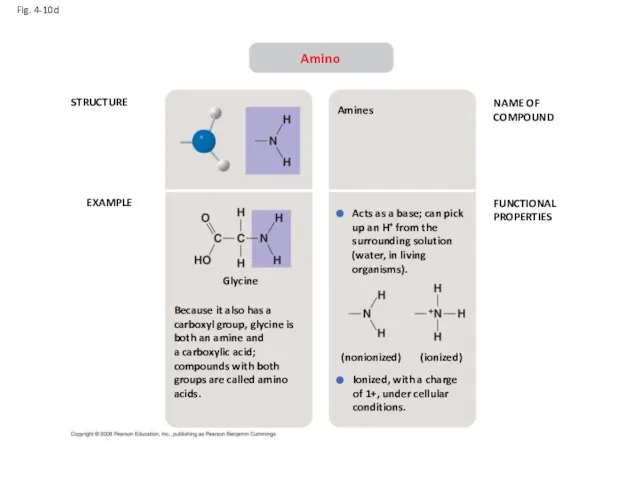
- 22. Fig. 4-10d STRUCTURE EXAMPLE NAME OF COMPOUND FUNCTIONAL PROPERTIES Amino Because it also has a carboxyl
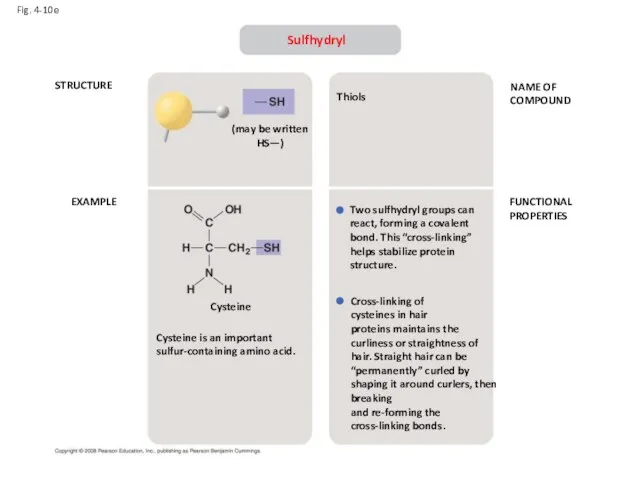
- 23. Fig. 4-10e STRUCTURE EXAMPLE NAME OF COMPOUND FUNCTIONAL PROPERTIES Sulfhydryl (may be written HS—) Cysteine Cysteine
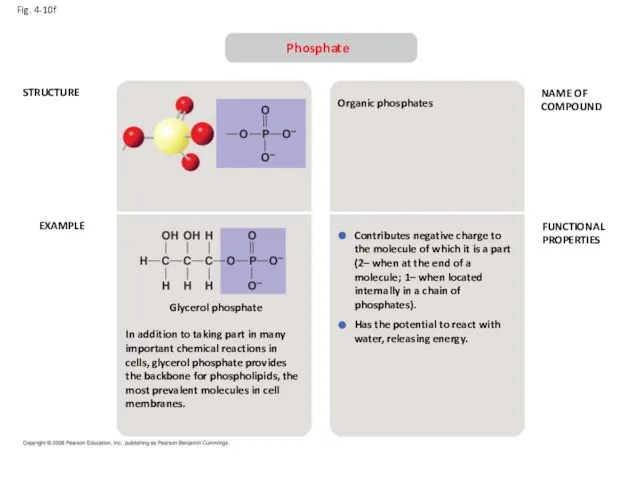
- 24. Fig. 4-10f STRUCTURE EXAMPLE NAME OF COMPOUND FUNCTIONAL PROPERTIES Phosphate In addition to taking part in
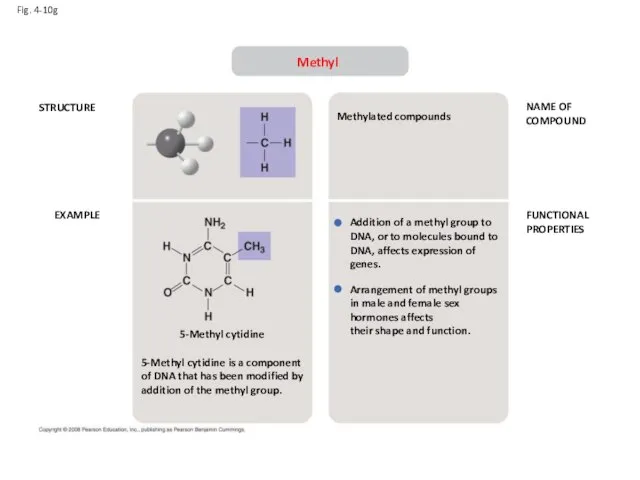
- 25. Fig. 4-10g STRUCTURE EXAMPLE NAME OF COMPOUND FUNCTIONAL PROPERTIES Methyl 5-Methyl cytidine is a component of
- 27. James Watson and Francis Crick, UK Erwin Chargaff, Ukraine Linus Pauling, USA Maurice Wilkins, NZ Rosalind
- 28. Первое правило Чаргафа: В природной ДНК количество единиц гуанина равно количеству единиц цитозина, тогда как количество
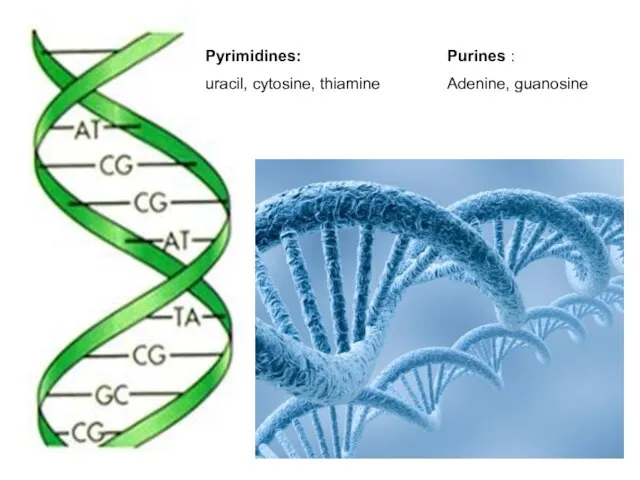
- 29. Pyrimidines: uracil, cytosine, thiamine Purines : Adenine, guanosine
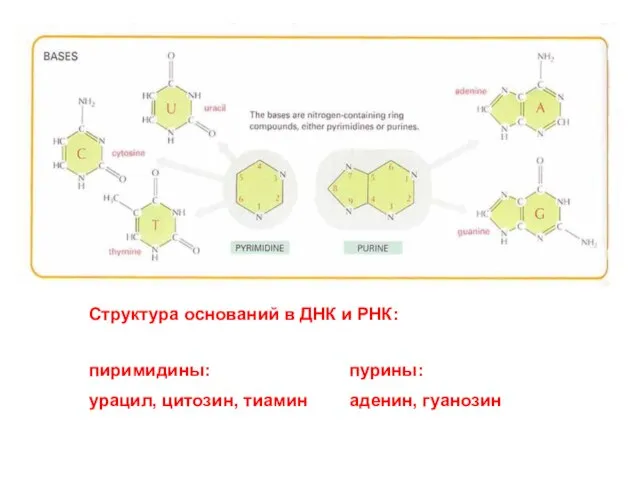
- 30. Структура оснований в ДНК и РНК: пиримидины: урацил, цитозин, тиамин пурины: аденин, гуанозин
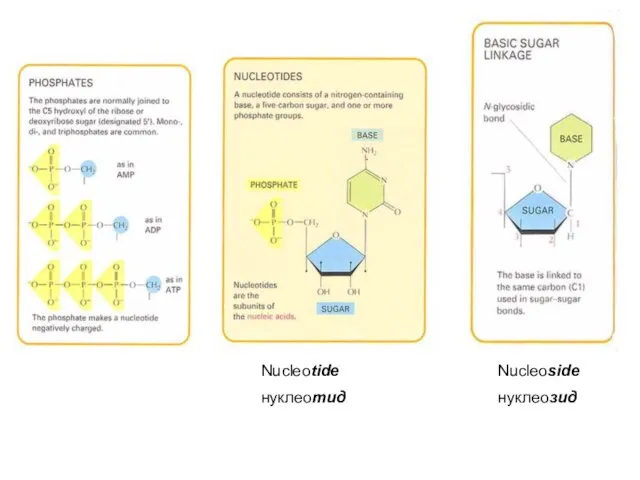
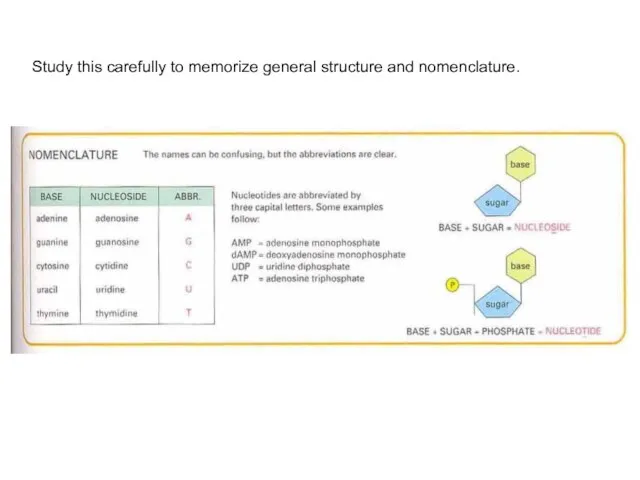
- 31. Nucleoside нуклеозид Nucleotide нуклеотид
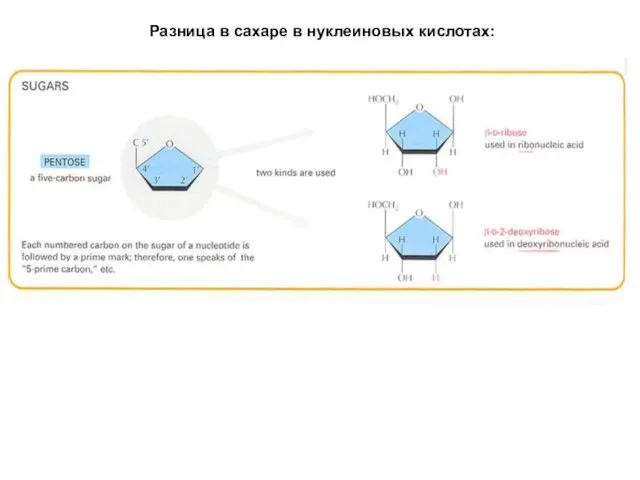
- 32. Разница в сахаре в нуклеиновых кислотах:
- 33. Другие функции нуклеотидов (помимо генетической):
- 34. Study this carefully to memorize general structure and nomenclature.
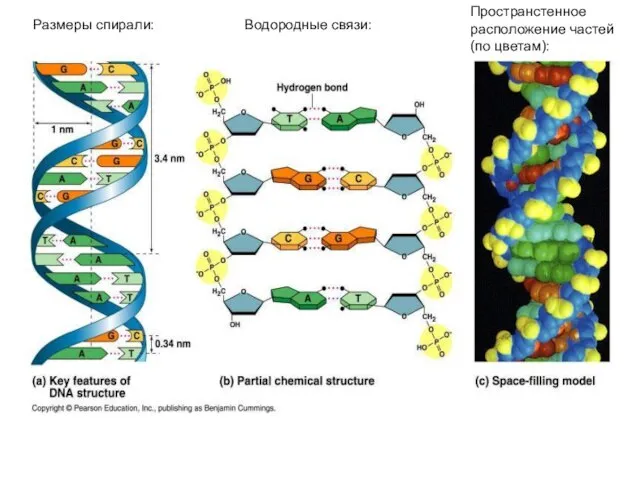
- 35. Размеры спирали: Водородные связи: Пространстенное расположение частей (по цветам):
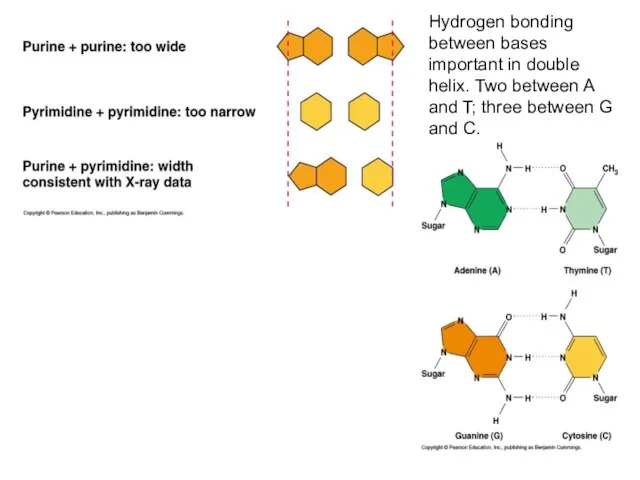
- 37. Hydrogen bonding between bases important in double helix. Two between A and T; three between G
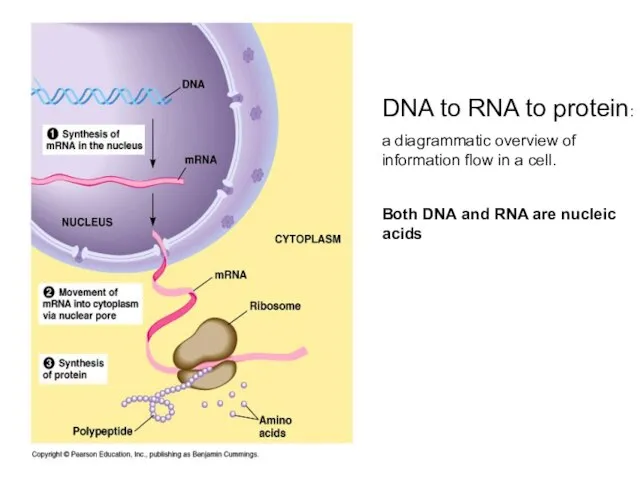
- 38. DNA to RNA to protein: a diagrammatic overview of information flow in a cell. Both DNA
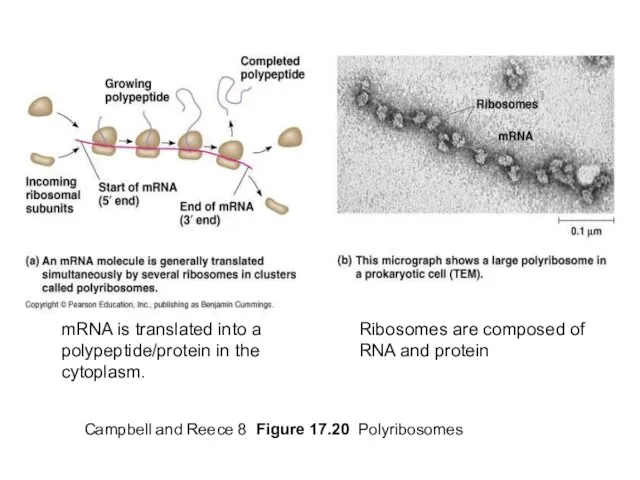
- 39. Campbell and Reece 8 Figure 17.20 Polyribosomes mRNA is translated into a polypeptide/protein in the cytoplasm.
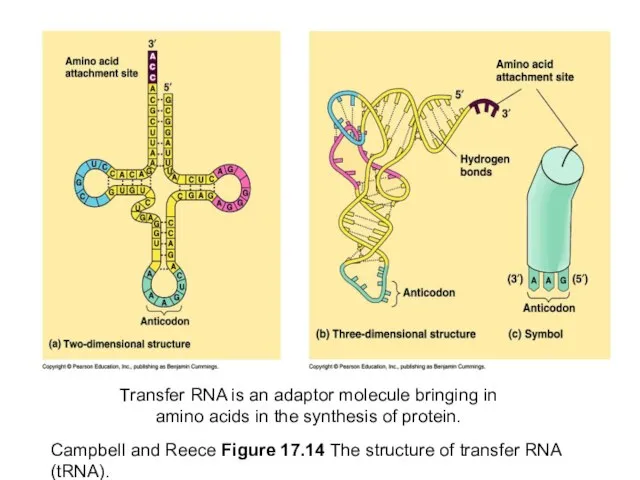
- 40. Campbell and Reece Figure 17.14 The structure of transfer RNA (tRNA). Transfer RNA is an adaptor
- 41. Campbell and Reece 8 Chapter 17 These first three are the types of RNA that you
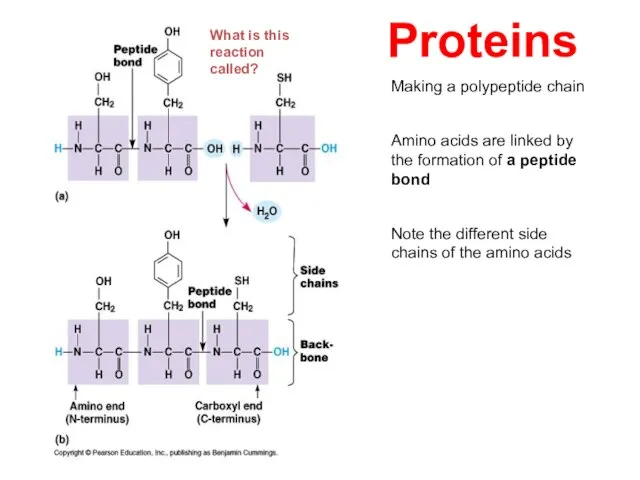
- 43. Making a polypeptide chain Amino acids are linked by the formation of a peptide bond Note
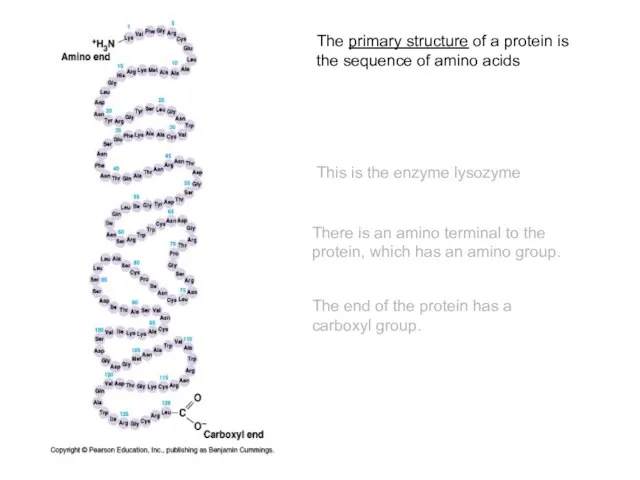
- 44. The primary structure of a protein is the sequence of amino acids This is the enzyme
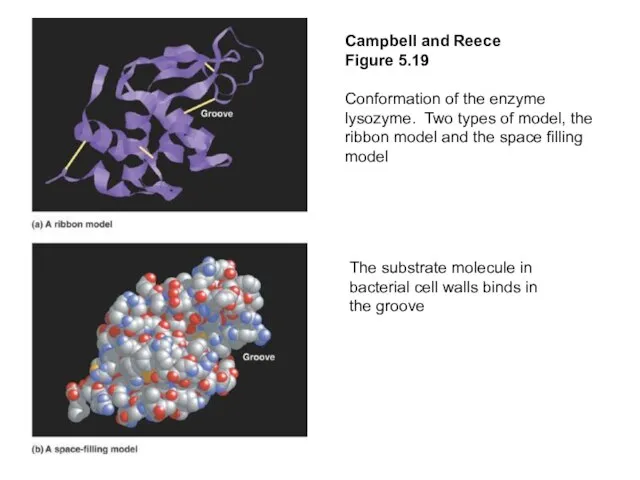
- 45. Campbell and Reece Figure 5.19 Conformation of the enzyme lysozyme. Two types of model, the ribbon
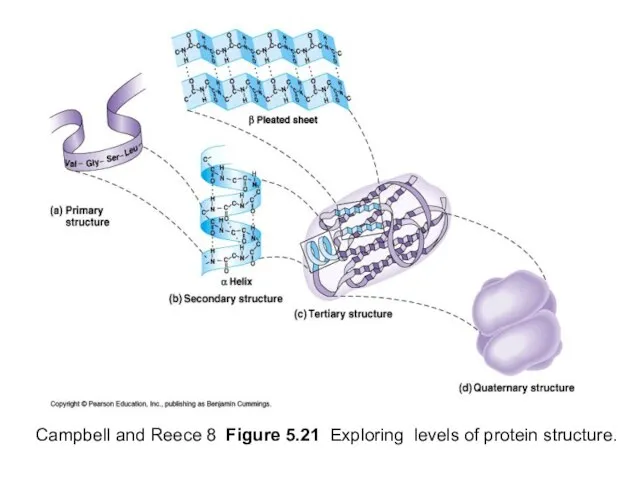
- 46. Campbell and Reece 8 Figure 5.21 Exploring levels of protein structure.
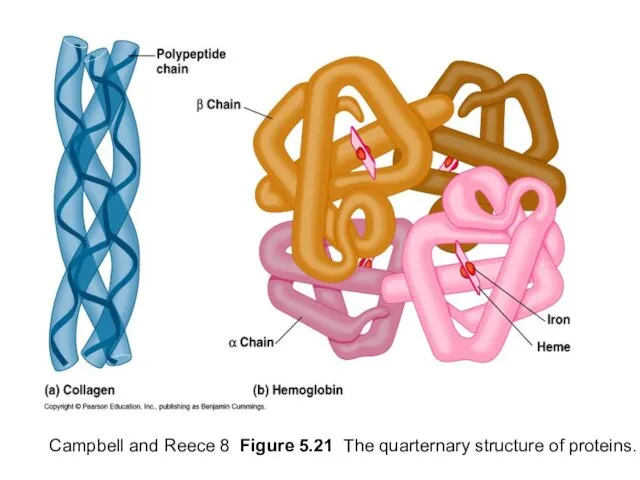
- 47. Campbell and Reece 8 Figure 5.21 The quarternary structure of proteins.
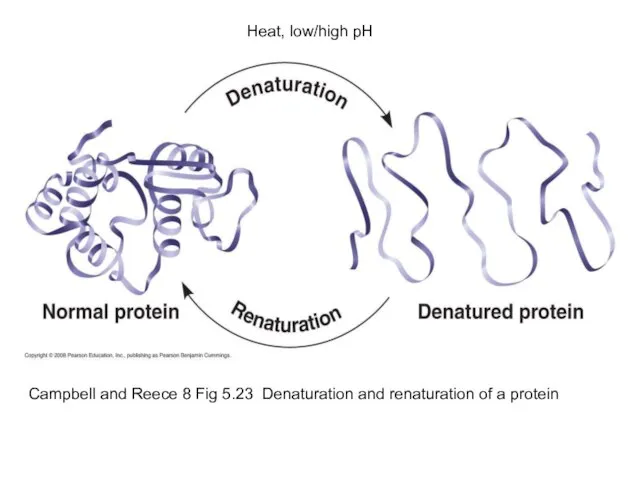
- 48. Campbell and Reece 8 Fig 5.23 Denaturation and renaturation of a protein Heat, low/high pH
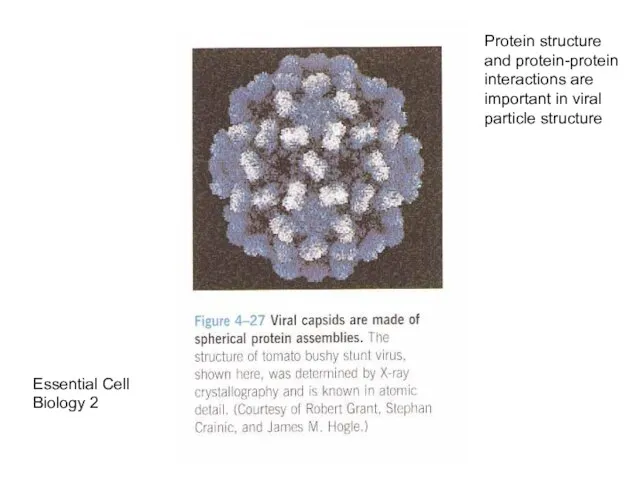
- 49. Essential Cell Biology 2 Protein structure and protein-protein interactions are important in viral particle structure
- 51. Скачать презентацию










 Презентация на тему Эдуард Мане
Презентация на тему Эдуард Мане  Правоохранительные органы Российской Федерации
Правоохранительные органы Российской Федерации Организация сопровождаемого проживания граждан с нарушениями
Организация сопровождаемого проживания граждан с нарушениями 学校
学校 Типы сварных швов
Типы сварных швов Отчет о размещении вакансий
Отчет о размещении вакансий СОВРЕМЕННОЕ ПРОФЕССИОНАЛЬНОЕ ОБРАЗОВАНИЕДЛЯ РОССИЙСКОЙ ИННОВАЦИОННОЙ СИСТЕМЫВ ОБЛАСТИ ЭЛЕКТРОНИКИ
СОВРЕМЕННОЕ ПРОФЕССИОНАЛЬНОЕ ОБРАЗОВАНИЕДЛЯ РОССИЙСКОЙ ИННОВАЦИОННОЙ СИСТЕМЫВ ОБЛАСТИ ЭЛЕКТРОНИКИ Сравнительный анализ развития лыжероллеров
Сравнительный анализ развития лыжероллеров Прыжки в длину
Прыжки в длину Презентация на тему Механические колебания 11 класс
Презентация на тему Механические колебания 11 класс  Понятия частей речи
Понятия частей речи Презентация Нагрузки и воздействия
Презентация Нагрузки и воздействия Презентация на тему Разнообразие животных
Презентация на тему Разнообразие животных  English theater
English theater  Класс Однодольные, характерные признаки растений семейства злаковых
Класс Однодольные, характерные признаки растений семейства злаковых Еңбек нормасы. Өнім нормасы
Еңбек нормасы. Өнім нормасы Формы и методы профессиональной ориентации
Формы и методы профессиональной ориентации e70f443261a743aba5fb4ba5defd798a
e70f443261a743aba5fb4ba5defd798a Функциональные стили речи
Функциональные стили речи Комплексная программа развития и воспитания дошкольников в Образовательной системе "Школа 2100"
Комплексная программа развития и воспитания дошкольников в Образовательной системе "Школа 2100" Презентация на тему Вельможи Древнего ЕГИПТА
Презентация на тему Вельможи Древнего ЕГИПТА  Маршалы Великой Отечественной войны
Маршалы Великой Отечественной войны Исторические лица земли Тверской, их жизнь и деяния, составляющие гордость региона
Исторические лица земли Тверской, их жизнь и деяния, составляющие гордость региона Природный газ
Природный газ Михайленко Юлия Борисовна учитель начальных классов ГБОУ гимназии № 1518 г. Москвы
Михайленко Юлия Борисовна учитель начальных классов ГБОУ гимназии № 1518 г. Москвы Оркестр. Инструменты симфонического оркестра
Оркестр. Инструменты симфонического оркестра МАТЕРИАЛЫ ДЛЯ ЖБК. АРМАТУРА
МАТЕРИАЛЫ ДЛЯ ЖБК. АРМАТУРА  Богиня Молва (Фама, Осса)
Богиня Молва (Фама, Осса)