Содержание
- 2. ЭЛЕКТРОЛИТЫ-вещества, обладающие ионной проводимостью; их называют проводниками второго рода – прохождение тока через них сопровождается переносом
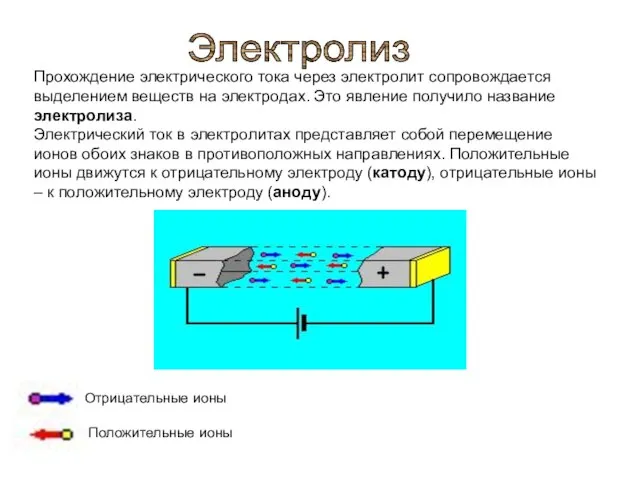
- 3. Прохождение электрического тока через электролит сопровождается выделением веществ на электродах. Это явление получило название электролиза. Электрический
- 4. Вольтамперная характеристика для электролитов. За счет явления поляризации график смещен. ЭДС поляризации имеет знак, противоположный знаку
- 6. Фарадей Майкл (22.IX.1791–25.VIII.1867) Английский физик и химик. Один из основателей количественной электрохимии. Установил (1833–1836) количественные законы
- 7. Ионы обоих знаков появляются в водных растворах солей, кислот и щелочей в результате расщепления части нейтральных
- 8. электролитическая диссоциация
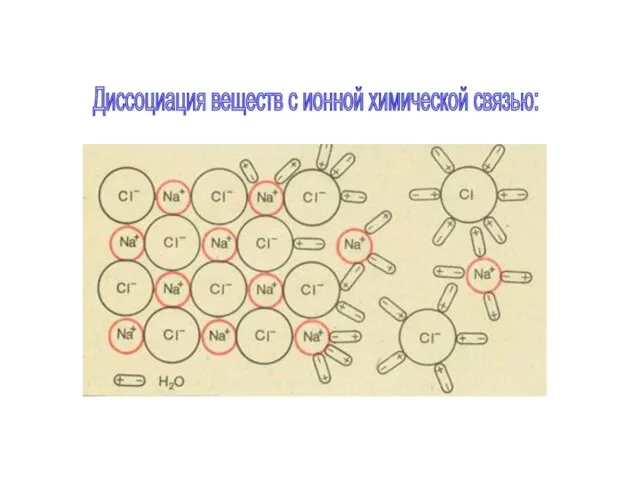
- 9. Диссоциация веществ с ионной химической связью:
- 10. Схема электролитической диссоциации на примере хлора и натрия
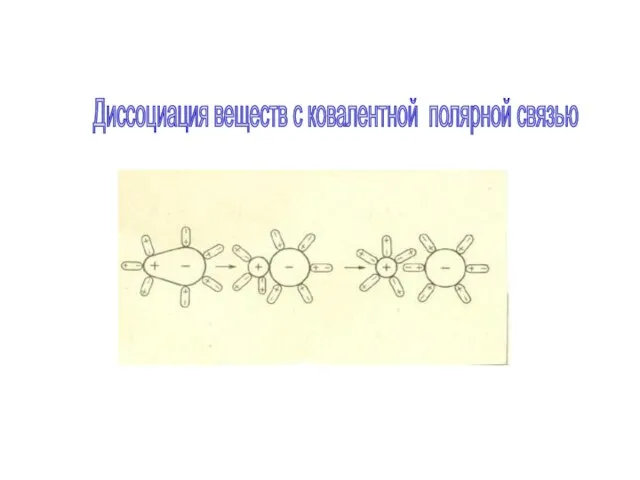
- 11. Диссоциация веществ с ковалентной полярной связью
- 13. Скачать презентацию






 Мой дом,моё жилищепрезентацию выполнили:Агеев.СУсов.А
Мой дом,моё жилищепрезентацию выполнили:Агеев.СУсов.А Терминология и судейство в бадминтоне
Терминология и судейство в бадминтоне Традиции и обычаи татар
Традиции и обычаи татар Презентация на тему American History (A few points)
Презентация на тему American History (A few points)  Я – парикмахер
Я – парикмахер Основы инновационной деятельности
Основы инновационной деятельности Разработка концепции и дизайна наручных коллекционных часов
Разработка концепции и дизайна наручных коллекционных часов 7
7 История развития вычислительной техники
История развития вычислительной техники Экономика и её участники
Экономика и её участники Электронные версии периодических изданий как новый вектор комплектования библиотеки: Плюсы и минусы замены "печатной" подписки "э
Электронные версии периодических изданий как новый вектор комплектования библиотеки: Плюсы и минусы замены "печатной" подписки "э Откуда берутся гении
Откуда берутся гении Перпендикулярные прямые в пространстве
Перпендикулярные прямые в пространстве С.Ю. Глазьев О стратегии экономического развития России
С.Ю. Глазьев О стратегии экономического развития России Пропала собака
Пропала собака История развития вычислительной техники
История развития вычислительной техники Алфавитный подход к определению информации
Алфавитный подход к определению информации Л 4 Основы мобилизационной подготовки и мобилизации здравоохранения
Л 4 Основы мобилизационной подготовки и мобилизации здравоохранения "Вишневый сад" А.П. Чехова - пьеса о Родине
"Вишневый сад" А.П. Чехова - пьеса о Родине В МИРЕ ГЕОМЕТРИИ
В МИРЕ ГЕОМЕТРИИ Загадки о животных
Загадки о животных Презентация на тему Решение систем неравенств
Презентация на тему Решение систем неравенств Пищевые цепи и поток энергии в них
Пищевые цепи и поток энергии в них Исаакиевский собор 8 класс
Исаакиевский собор 8 класс Добро Пожаловать
Добро Пожаловать Государственное Образовательное Учреждение
Государственное Образовательное Учреждение КЛУБ-У
КЛУБ-У Рисунок семьи
Рисунок семьи