Содержание
- 2. Как защититься? Многоклеточное в мире микробов и простейших
- 3. Встроенный в клеточные мембраны муцин – основной элемент гликокаликса – создает преграду, трудно преодолимую для любых
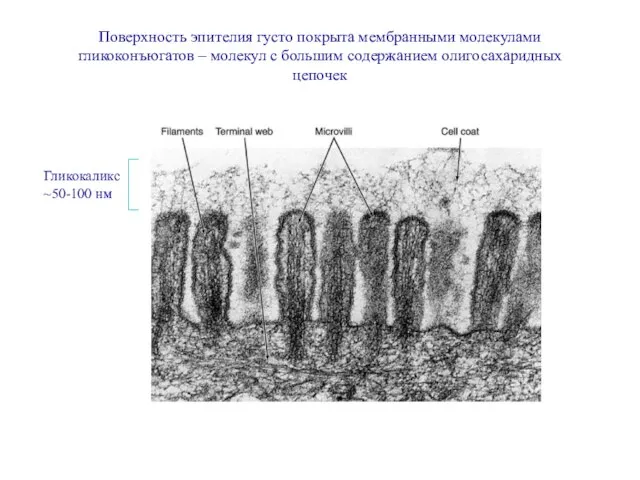
- 4. Гликокаликс ~50-100 нм Поверхность эпителия густо покрыта мембранными молекулами гликоконъюгатов – молекул с большим содержанием олигосахаридных
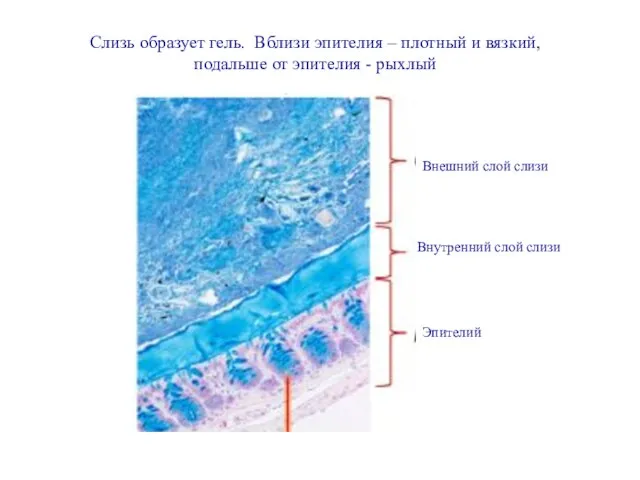
- 5. Внешний слой слизи Внутренний слой слизи Эпителий Слизь образует гель. Вблизи эпителия – плотный и вязкий,
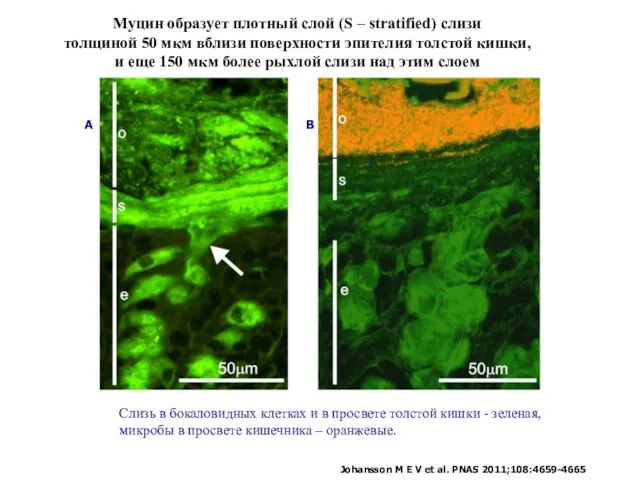
- 6. Муцин образует плотный слой (S – stratified) слизи толщиной 50 мкм вблизи поверхности эпителия толстой кишки,
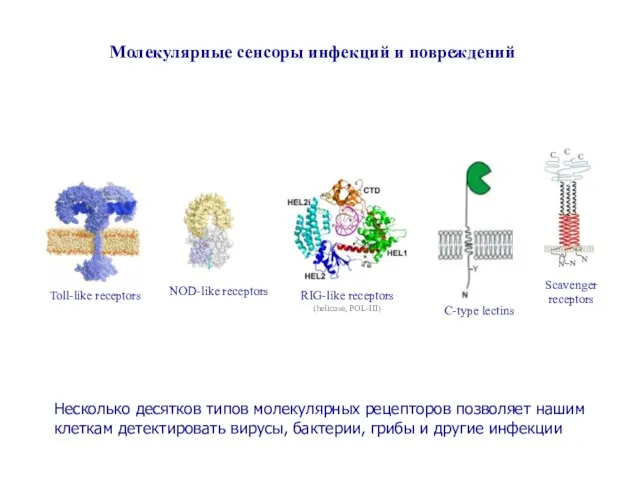
- 7. Молекулярные сенсоры инфекций и повреждений Toll-like receptors NOD-like receptors RIG-like receptors (helicase, POL-III) C-type lectins Scavenger
- 8. Если инфекция обнаружена, наши клетки выбрасывают вещества, токсичные для микробов
- 9. Дефенсины Кателицидины Гистатины Лактоферрин Лизоцим Псориазин Дермцидин и многие другие… Эндогенные антибиотики – защитные вещества белковой
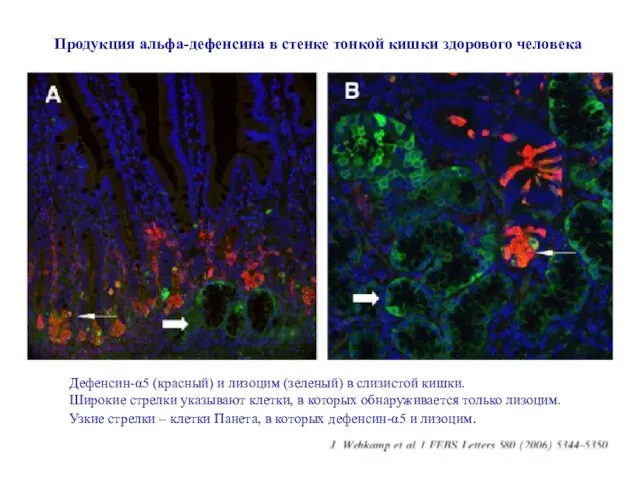
- 10. Дефенсин-α5 (красный) и лизоцим (зеленый) в слизистой кишки. Широкие стрелки указывают клетки, в которых обнаруживается только
- 11. Клетки эпителия, обнаружившие инфекцию, сообщают соседним клеткам (под эпителием) о том, что произошло вторжение инфекции Сообщения
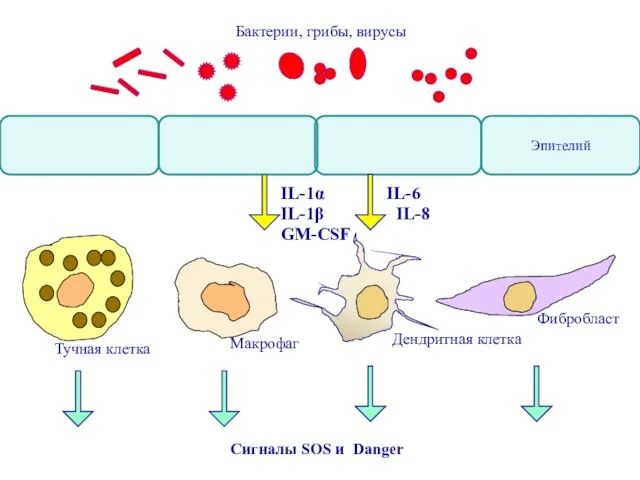
- 12. IL-1α IL-1β IL-6 IL-8 GM-CSF Фибробласт Макрофаг Дендритная клетка Тучная клетка Сигналы SOS и Danger Бактерии,
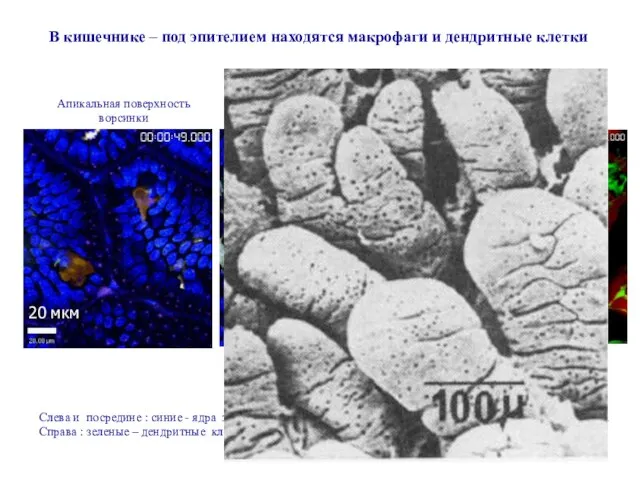
- 13. В кишечнике – под эпителием находятся макрофаги и дендритные клетки 20 мкм 20 мкм 50 мкм
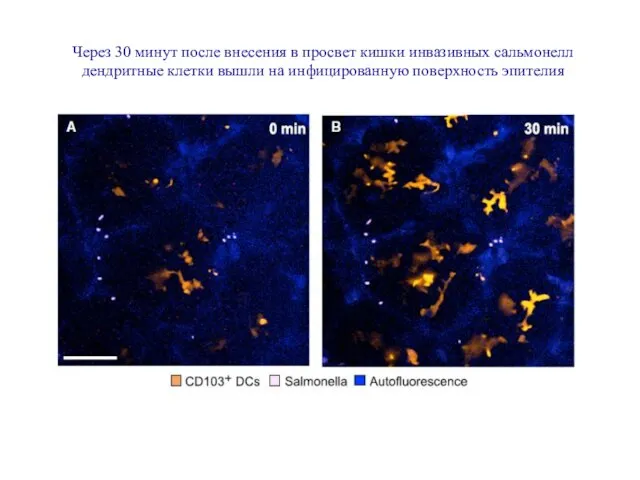
- 14. Через 30 минут после внесения в просвет кишки инвазивных сальмонелл дендритные клетки вышли на инфицированную поверхность
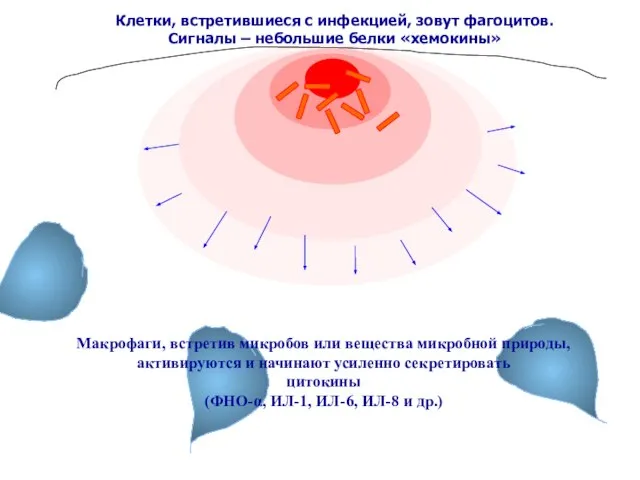
- 15. Макрофаги, встретив микробов или вещества микробной природы, активируются и начинают усиленно секретировать цитокины (ФНО-α, ИЛ-1, ИЛ-6,
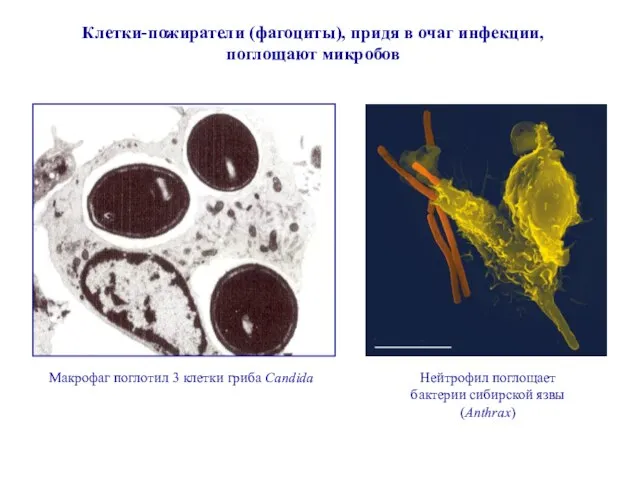
- 16. Клетки-пожиратели (фагоциты), придя в очаг инфекции, поглощают микробов Макрофаг поглотил 3 клетки гриба Candida Нейтрофил поглощает
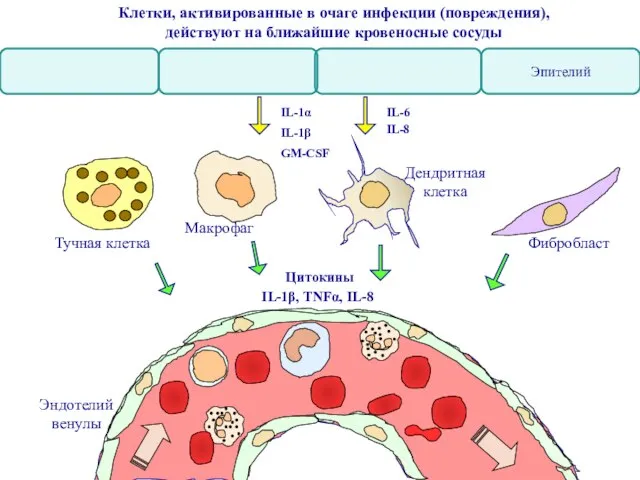
- 17. Фагоциты, активированные при контакте с инфекцией, выделяют цитокины (ИЛ-1, ФНО, ИЛ-6, ИЛ-8). Эти цитокины действуют на
- 18. Эндотелий венулы IL-1α IL-1β IL-6 IL-8 GM-CSF Фибробласт Макрофаг Дендритная клетка Тучная клетка Клетки, активированные в
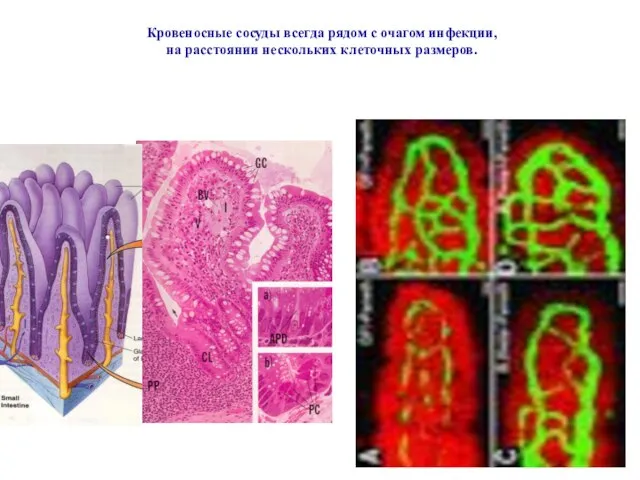
- 19. Кровеносные сосуды всегда рядом с очагом инфекции, на расстоянии нескольких клеточных размеров.
- 20. Два следствия активации эндотелия кровеносных сосудов вблизи очага инфекции: Повышение проницаемости стенки сосуда для крупных молекул
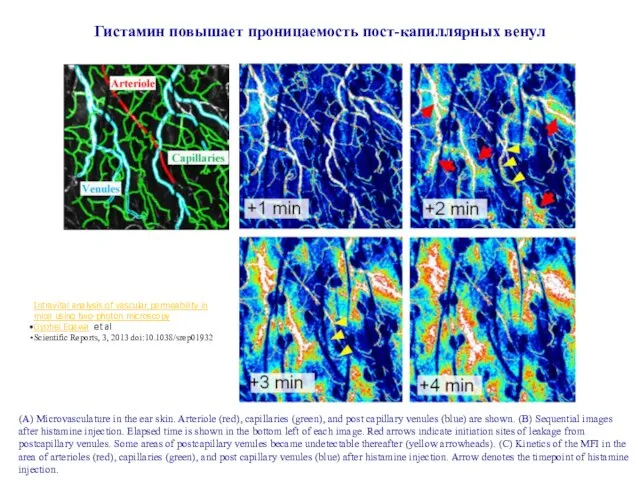
- 21. Вещества, которые выделяют тучные клетки (гистамин), повышают проницаемость стенки кровеносных сосудов. В течение нескольких минут через
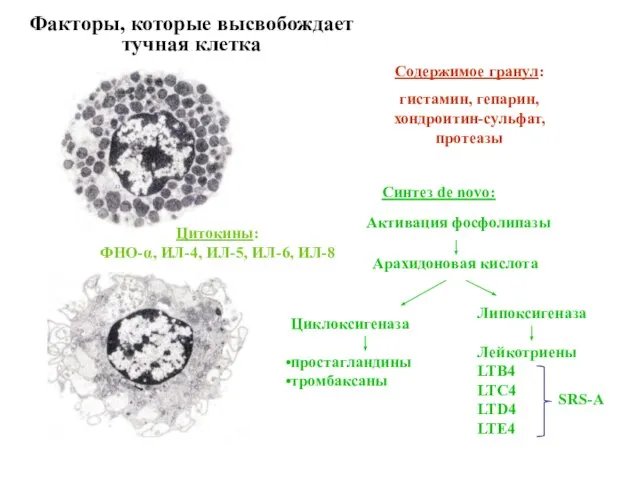
- 22. Факторы, которые высвобождает тучная клетка Содержимое гранул: гистамин, гепарин, хондроитин-сульфат, протеазы Синтез de novo: Активация фосфолипазы
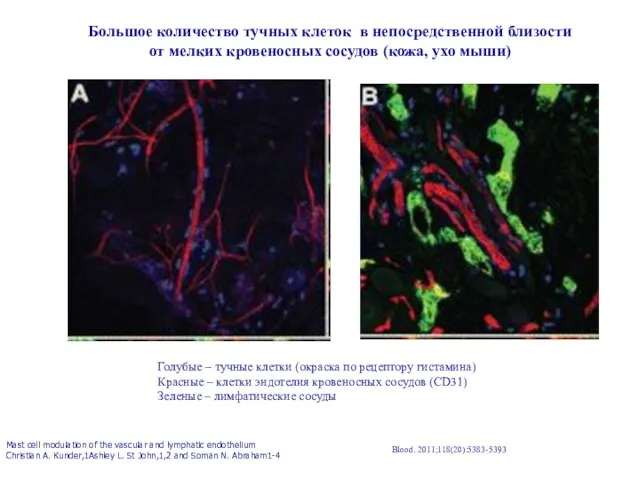
- 23. Большое количество тучных клеток в непосредственной близости от мелких кровеносных сосудов (кожа, ухо мыши) Голубые –
- 24. (A) Microvasculature in the ear skin. Arteriole (red), capillaries (green), and post capillary venules (blue) are
- 25. Крупные молекулы, выходя из кровотока в очаг инфекции, защищают нас от инфекции. Среди защитных молекул, имеющих
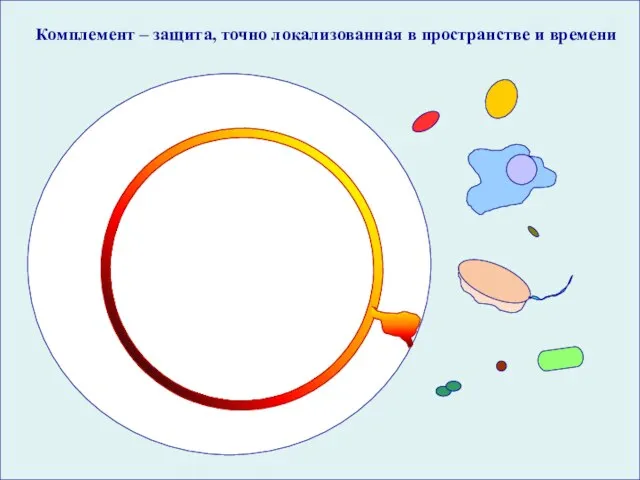
- 26. вирусов и Комплемент – защита, точно локализованная в пространстве и времени
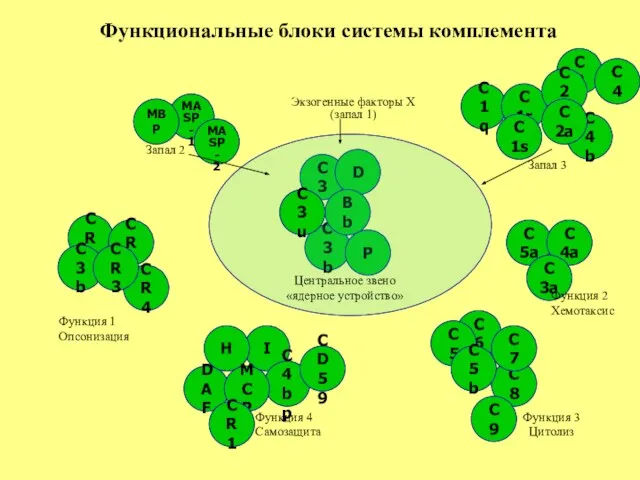
- 27. С3 С1q С8 С2 С1r С6 С4 С1s С3b С2b С4b С5 С5a С5b С9 С7
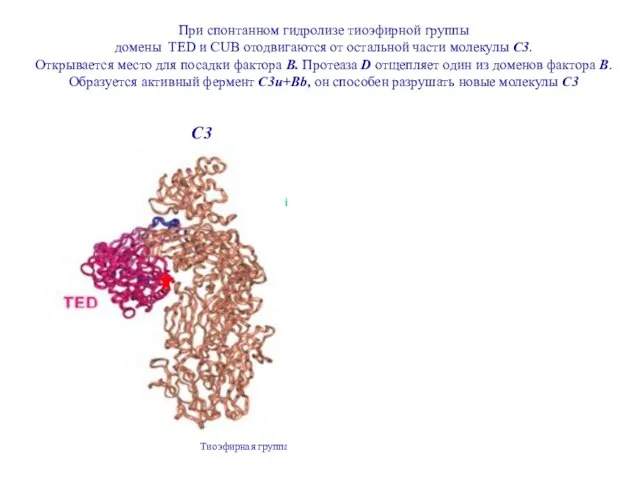
- 28. При спонтанном гидролизе тиоэфирной группы домены TED и CUB отодвигаются от остальной части молекулы C3. Открывается
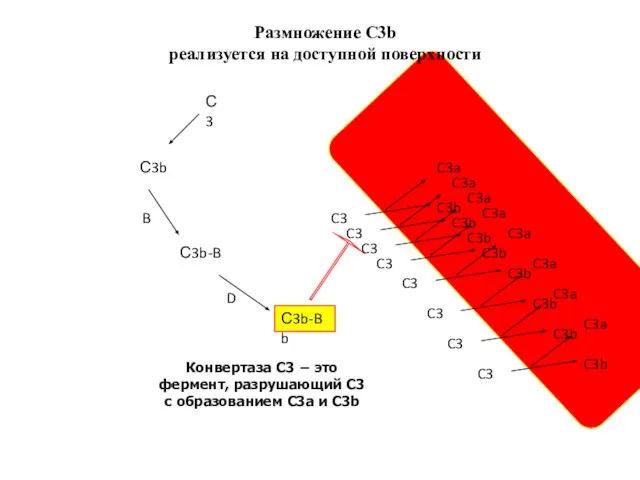
- 29. С3 С3b С3b-B D B С3b-Bb Размножение С3b реализуется на доступной поверхности Конвертаза С3 − это
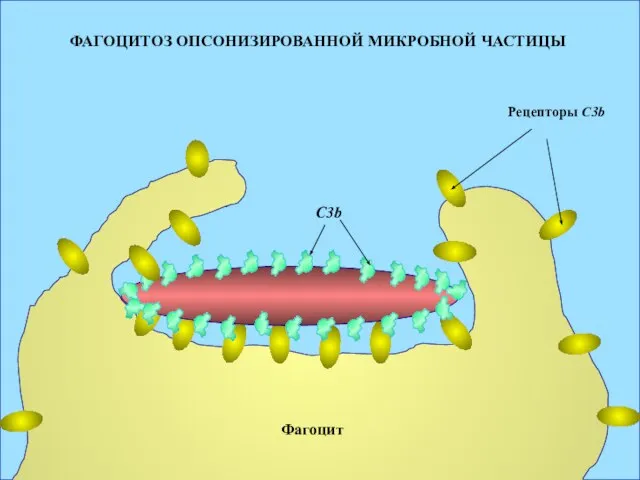
- 30. Три защитных действия комплемента: 1. ОПСОНИЗАЦИЯ ЧАСТИЦ (например, бактериальная частица), на которых активировался комплемент. Поверхность модифицируется
- 31. ФАГОЦИТОЗ ОПСОНИЗИРОВАННОЙ МИКРОБНОЙ ЧАСТИЦЫ Рецепторы С3b Фагоцит
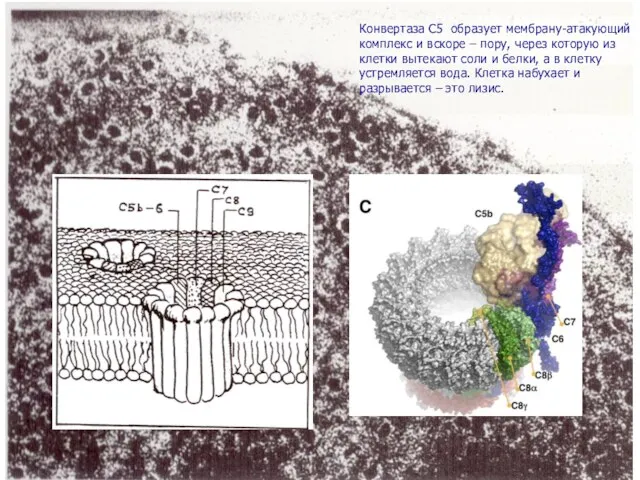
- 32. Конвертаза C5 образует мембрану-атакующий комплекс и вскоре – пору, через которую из клетки вытекают соли и
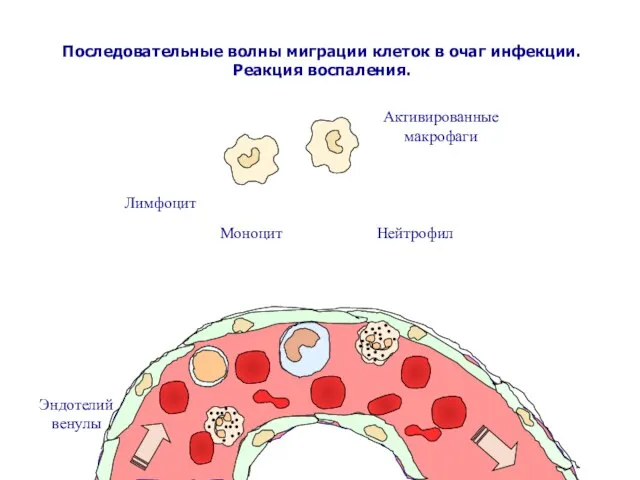
- 33. Второе следствие активации эндотелия кровеносных сосудов вблизи очага инфекции – это выход лейкоцитов из кровотока
- 34. Активированные макрофаги Нейтрофил Эндотелий венулы Лимфоцит Моноцит Последовательные волны миграции клеток в очаг инфекции. Реакция воспаления.
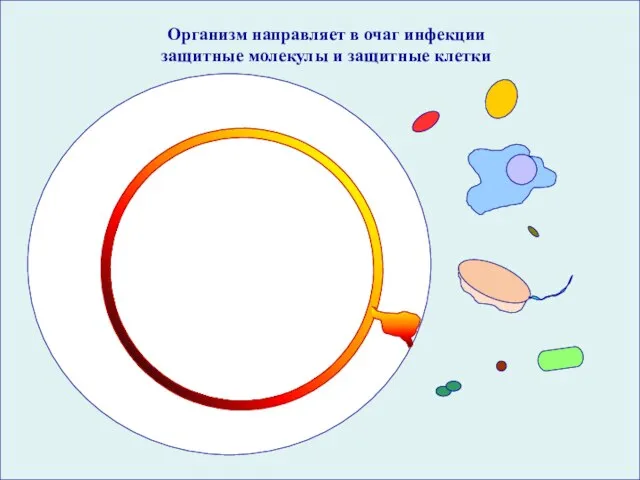
- 35. вирусов и Организм направляет в очаг инфекции защитные молекулы и защитные клетки
- 36. Если микробы или вещества микробной природы с током тканевой жидкости проникли в лимфатический узел или еще
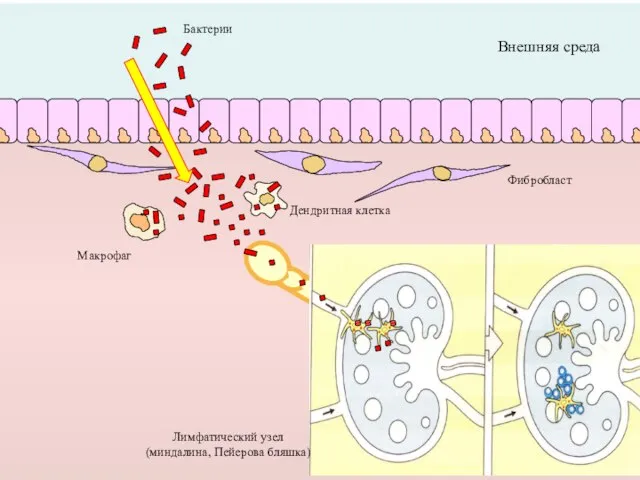
- 37. Внешняя среда Макрофаг Дендритная клетка Фибробласт Лимфатический узел (миндалина, Пейерова бляшка) Бактерии
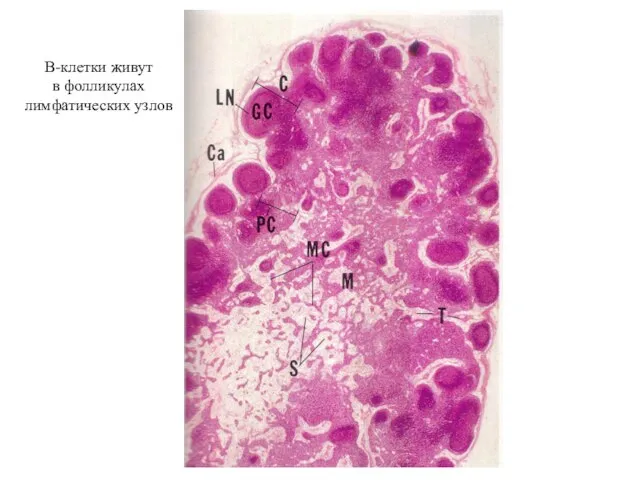
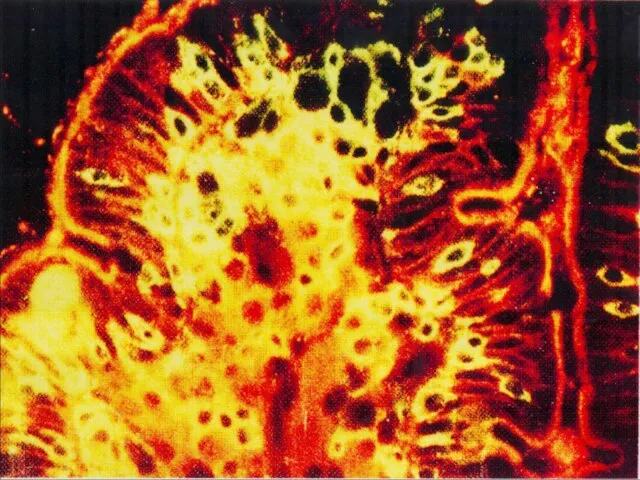
- 38. В-клетки живут в фолликулах лимфатических узлов
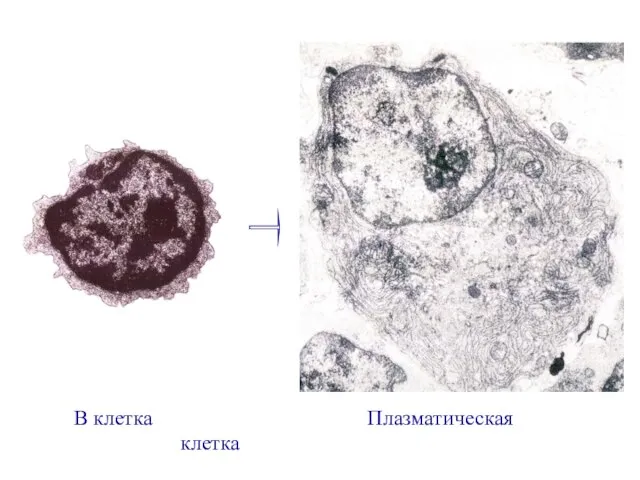
- 39. В клетка Плазматическая клетка
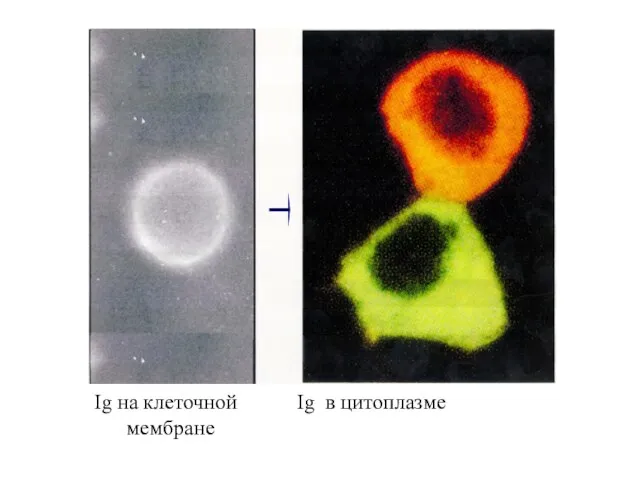
- 40. Ig на клеточной Ig в цитоплазме мембране
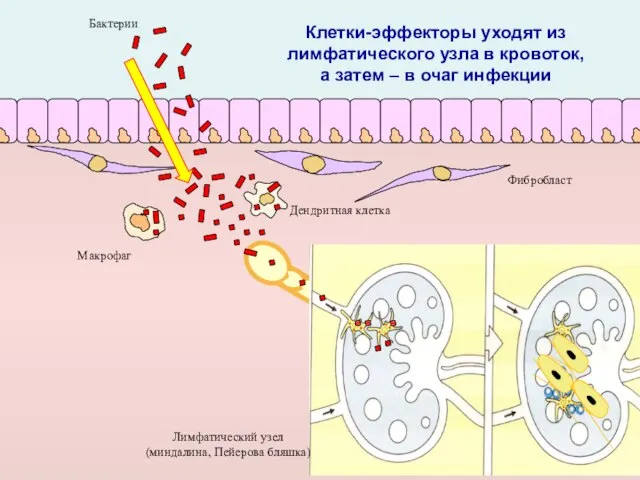
- 41. Макрофаг Дендритная клетка Фибробласт Лимфатический узел (миндалина, Пейерова бляшка) Бактерии Клетки-эффекторы уходят из лимфатического узла в
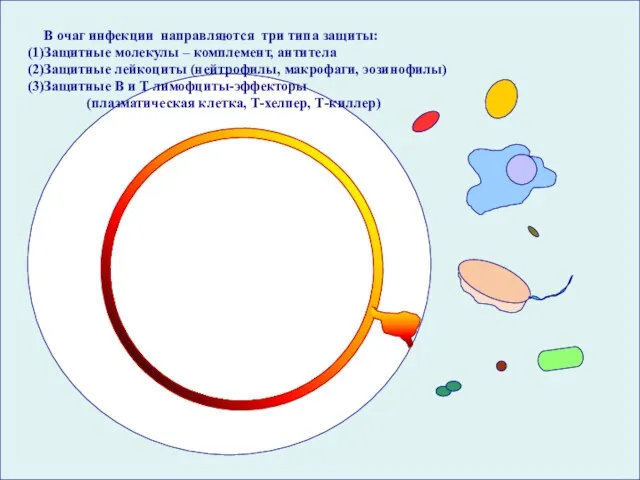
- 43. вирусов и В очаг инфекции направляются три типа защиты: Защитные молекулы – комплемент, антитела Защитные лейкоциты
- 44. Инфекция не уступает нам в оснащенности. Это – сильный, динамичный, умный и даже социально организованный противник
- 45. СТРАТЕГИЧЕСКИЕ ЦЕЛИ ИНФЕКЦИИ Использовать макроорганизм в качестве среды обитания Размножиться Инфицировать следующий макроорганизм
- 46. ТАКТИЧЕСКИЕ ЗАДАЧИ ИНФЕКЦИИ Проникнуть в макроорганизм Избежать ударов иммунной защиты или защититься от них Выжить и
- 47. СТРАТЕГИЧЕСКАЯ ЦЕЛЬ МАКРООРГАНИЗМА Не допустить вторжения инфекции Эффективно защититься от инфекции, если вторжение произошло
- 48. ЗАДАЧИ ИММУНИТЕТА В ОТНОШЕНИЯХ С ИНФЕКЦИЕЙ Не впустить инфекцию Убить инфекцию Удалить инфекцию из организма Залечить
- 49. АРСЕНАЛ ИНФЕКЦИИ Факторы, позволяющие проникать в клетки хозяина Факторы, способные убивать клетки хозяина Факторы, разрушающие тканевой
- 50. АРСЕНАЛ ИММУННОЙ ЗАЩИТЫ ОТ ИНФЕКЦИИ Эндогенные антибиотики (около 100 веществ) Комплемент Интерфероны Фагоциты Натуральные киллеры (NK)
- 51. ИММУННАЯ СИСТЕМА 1. Изобретает принципиальные виды защиты в процессе эволюции биологических видов 2. Нарабатывает огромное разнообразие
- 52. Инфекция тоже активно генерирует разнообразие факторов защиты, чтобы ускользнуть от иммунной атаки
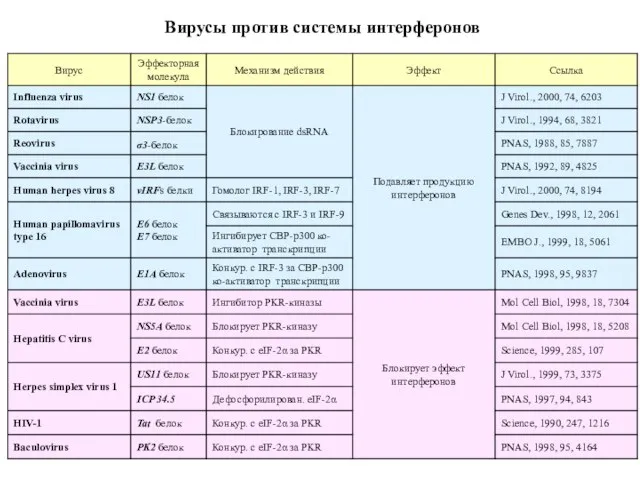
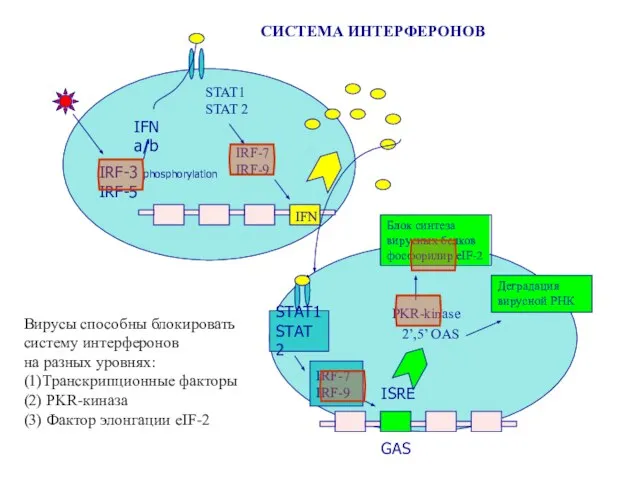
- 53. Вирусы против системы интерферонов
- 54. IFN a/b IRF-3 phosphorylation IRF-5 IRF-7 IRF-9 STAT1 STAT 2 STAT1 STAT 2 IRF-7 IRF-9 ISRE
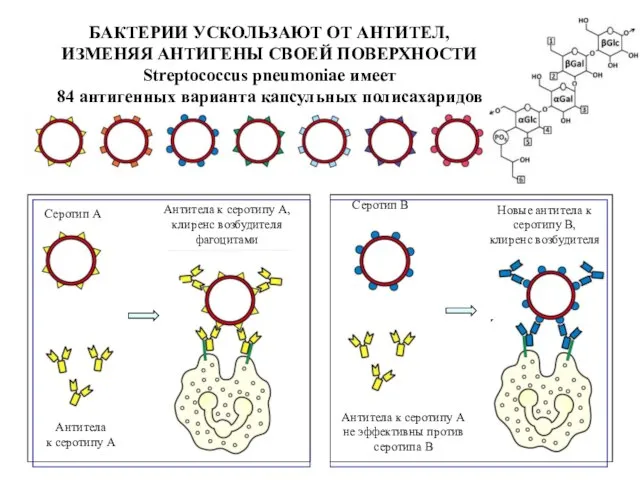
- 55. БАКТЕРИИ УСКОЛЬЗАЮТ ОТ АНТИТЕЛ, ИЗМЕНЯЯ АНТИГЕНЫ СВОЕЙ ПОВЕРХНОСТИ Streptococcus pneumoniae имеет 84 антигенных варианта капсульных полисахаридов
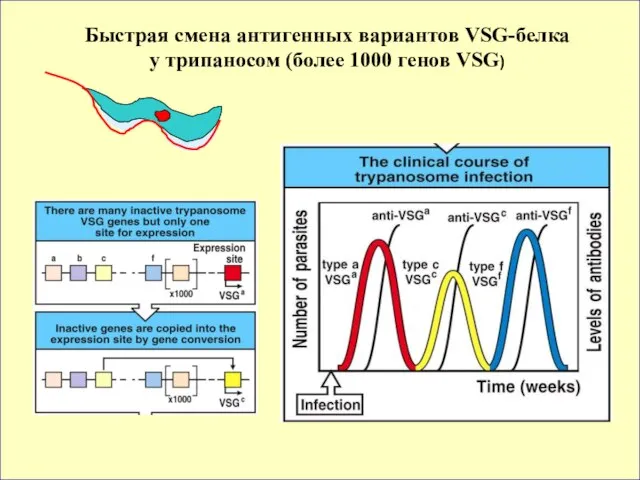
- 56. Быстрая смена антигенных вариантов VSG-белка у трипаносом (более 1000 генов VSG)
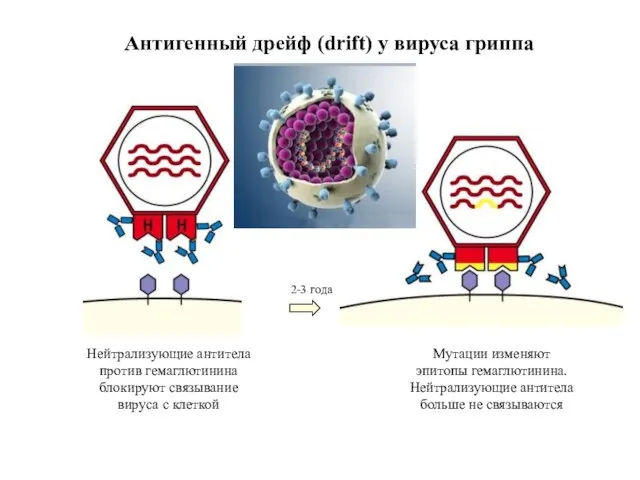
- 57. Антигенный дрейф (drift) у вируса гриппа Нейтрализующие антитела против гемаглютинина блокируют связывание вируса с клеткой Мутации
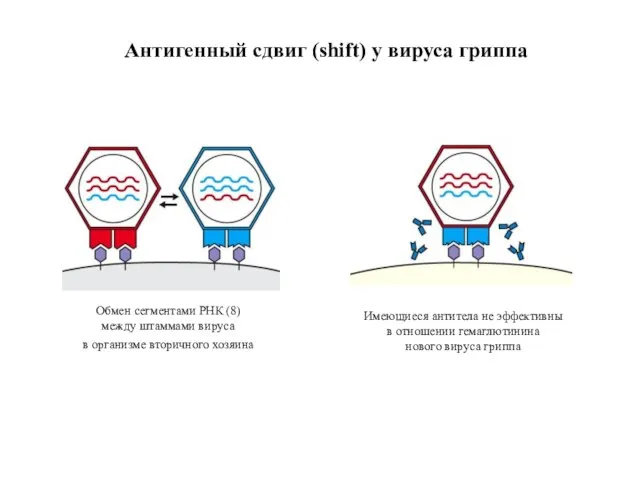
- 58. Антигенный сдвиг (shift) у вируса гриппа Обмен сегментами РНК (8) между штаммами вируса в организме вторичного
- 60. ИНФЕКЦИЯ И ИММУНИТЕТ ИСПОЛЬЗУЮТ ИДЕНТИЧНЫЙ ГЕНЕТИЧЕСКИЙ КОНСТРУКТОР ДЛЯ СОЗДАНИЯ СРЕДСТВ НАПАДЕНИЯ И ЗАЩИТЫ 1. Сегментарное устройство
- 61. Обе системы – иммунитет и инфекция – очень «интеллектуальны». Они гибко и адекватно используют имеющиеся средства
- 62. Бактерии, как люди, объединяются в коллективы для достижения своей цели
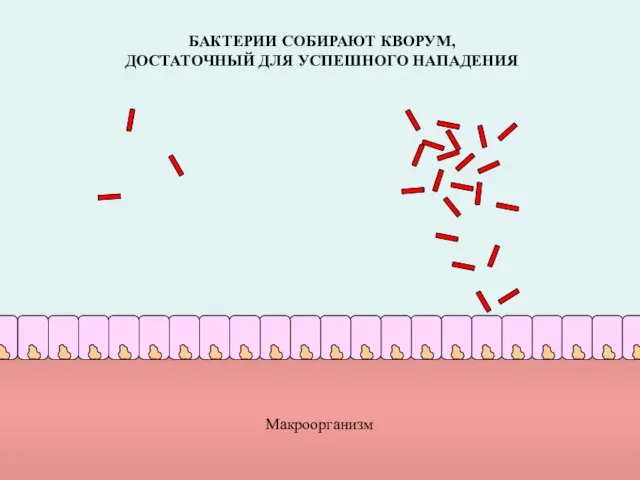
- 63. Макроорганизм БАКТЕРИИ СОБИРАЮТ КВОРУМ, ДОСТАТОЧНЫЙ ДЛЯ УСПЕШНОГО НАПАДЕНИЯ
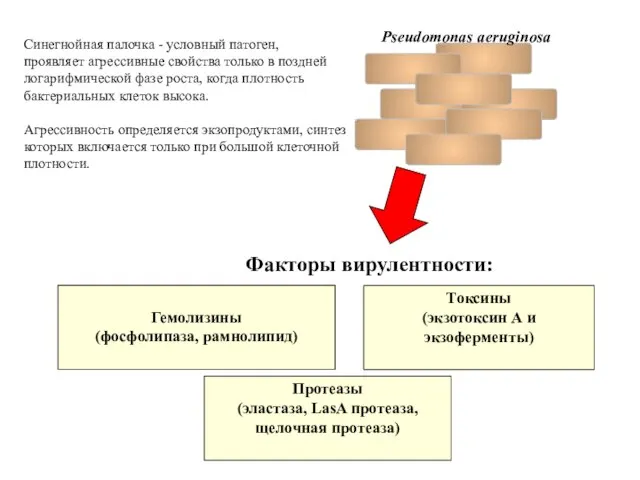
- 64. Синегнойная палочка - условный патоген, проявляет агрессивные свойства только в поздней логарифмической фазе роста, когда плотность
- 65. КАК БАКТЕРИИ ОЩУЩАЮТ КВОРУМ
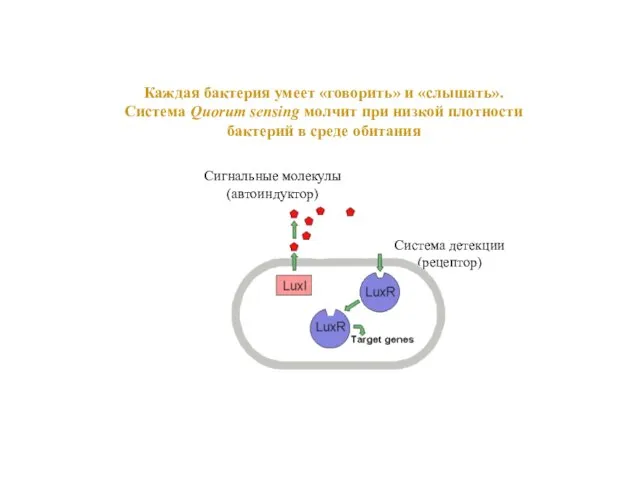
- 66. Каждая бактерия умеет «говорить» и «слышать». Система Quorum sensing молчит при низкой плотности бактерий в среде
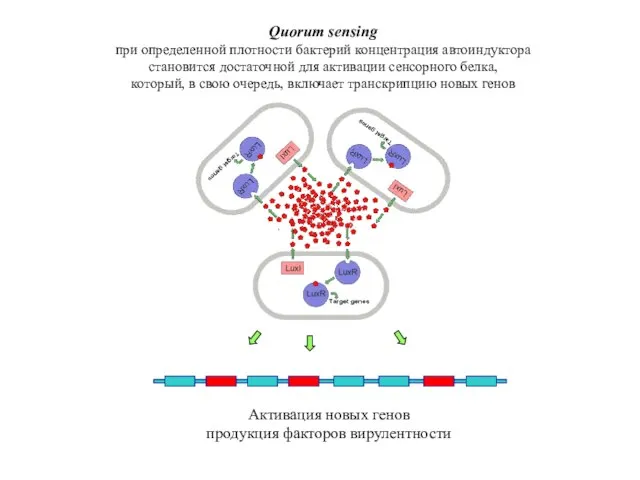
- 67. Активация новых генов продукция факторов вирулентности Quorum sensing при определенной плотности бактерий концентрация автоиндуктора становится достаточной
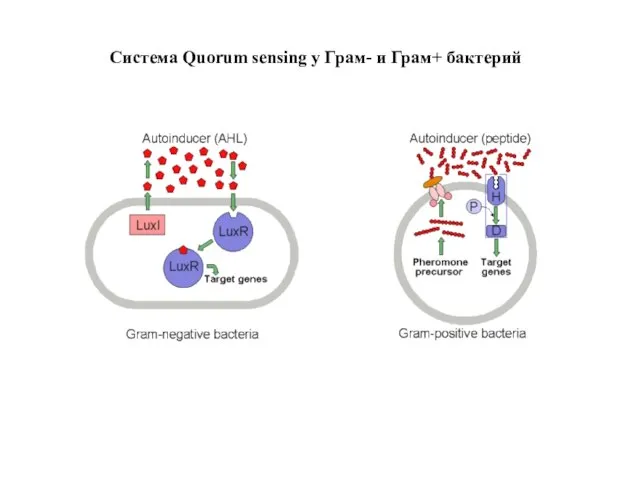
- 68. Система Quorum sensing у Грам- и Грам+ бактерий
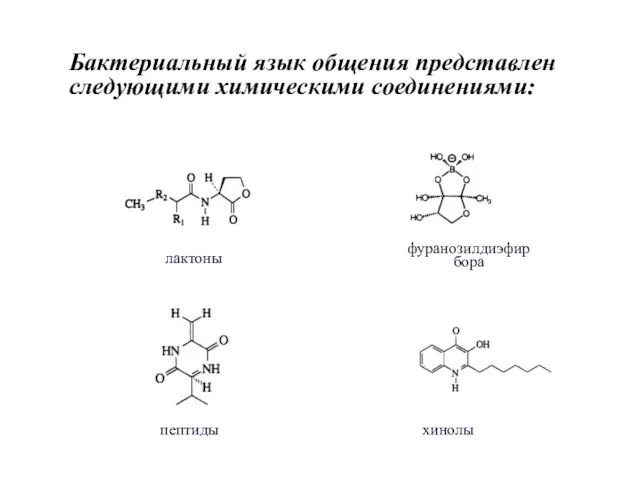
- 69. Бактериальный язык общения представлен следующими химическими соединениями: лактоны хинолы пептиды фуранозилдиэфир бора
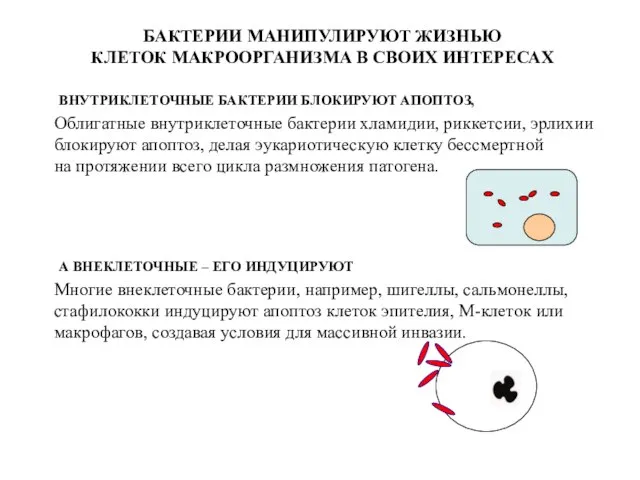
- 70. «Механизмы QS позволяют патогенным бактериям очень рационально использовать свой болезнетворный потенциал. Бактрии не атакуют эукариотическую клетку
- 71. Облигатные внутриклеточные бактерии хламидии, риккетсии, эрлихии блокируют апоптоз, делая эукариотическую клетку бессмертной на протяжении всего цикла
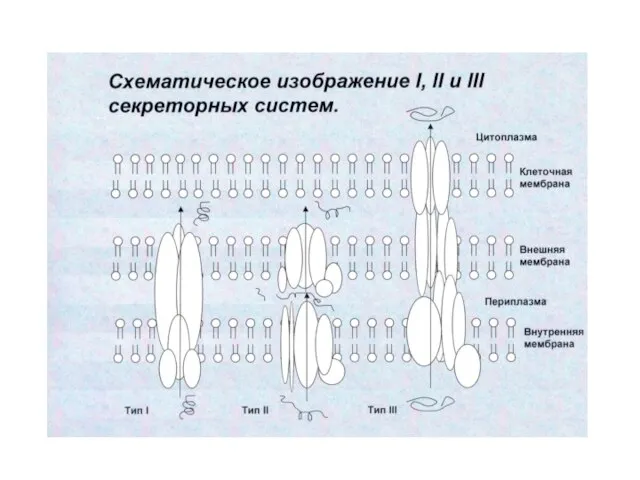
- 72. Для манипуляций с нашими клетками бактерии используют молекулярный шприц (называется «секреторная система»)
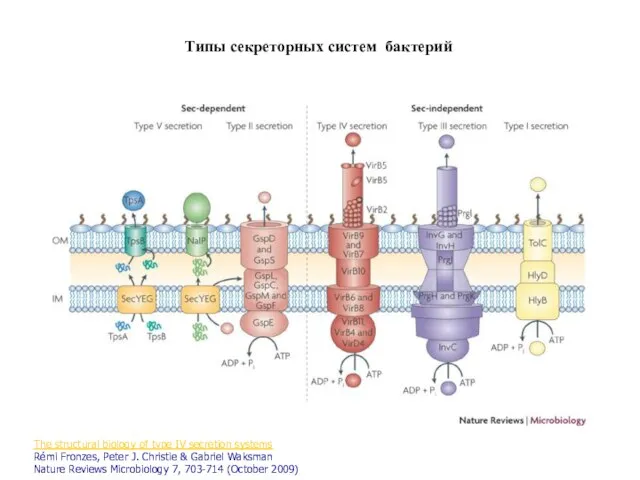
- 74. Типы секреторных систем бактерий The structural biology of type IV secretion systems Rémi Fronzes, Peter J.
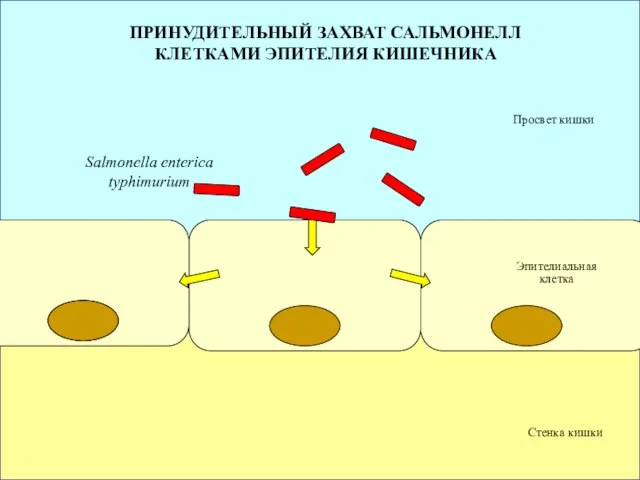
- 75. Просвет кишки Стенка кишки Salmonella enterica typhimurium Эпителиальная клетка ПРИНУДИТЕЛЬНЫЙ ЗАХВАТ САЛЬМОНЕЛЛ КЛЕТКАМИ ЭПИТЕЛИЯ КИШЕЧНИКА
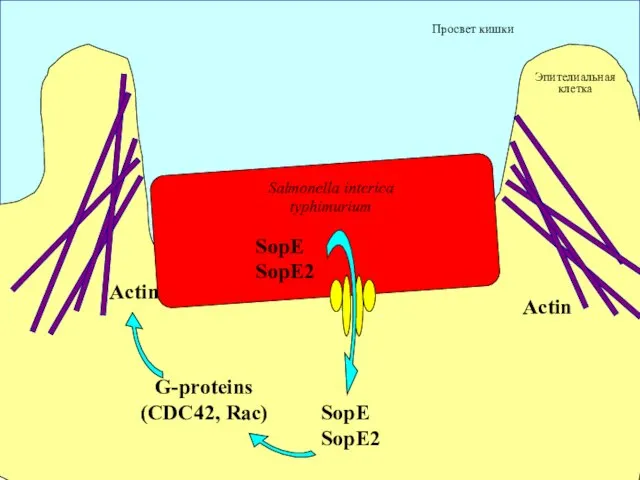
- 76. Эпителиальная клетка Просвет кишки SopE SopE2 Actin Actin Salmonella interica typhimurium G-proteins (CDC42, Rac) SopE SopE2
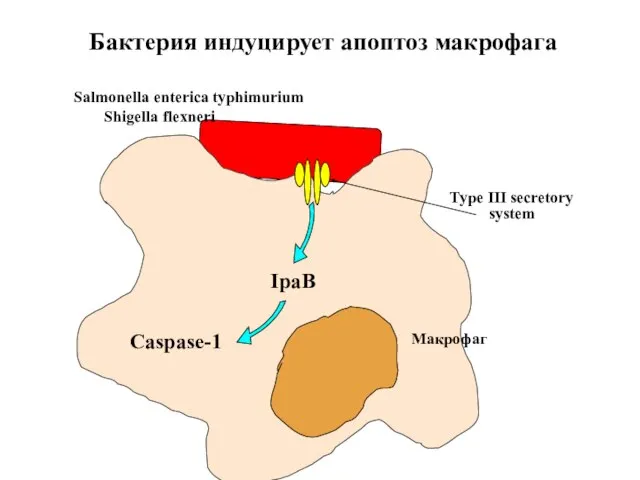
- 77. Макрофаг Salmonella enterica typhimurium Shigella flexneri IpaB Caspase-1 Бактерия индуцирует апоптоз макрофага Type III secretory system
- 78. Динамическое противостояние двух живых систем на примере взаимоотношений вирусной инфекции и иммунитета
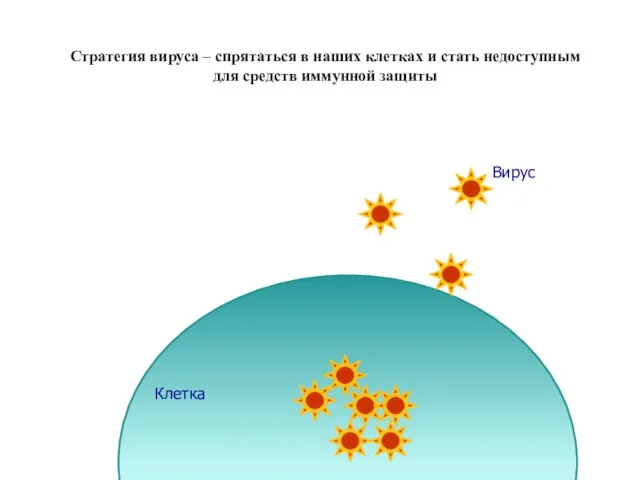
- 79. Стратегия вируса – спрятаться в наших клетках и стать недоступным для средств иммунной защиты Вирус Клетка
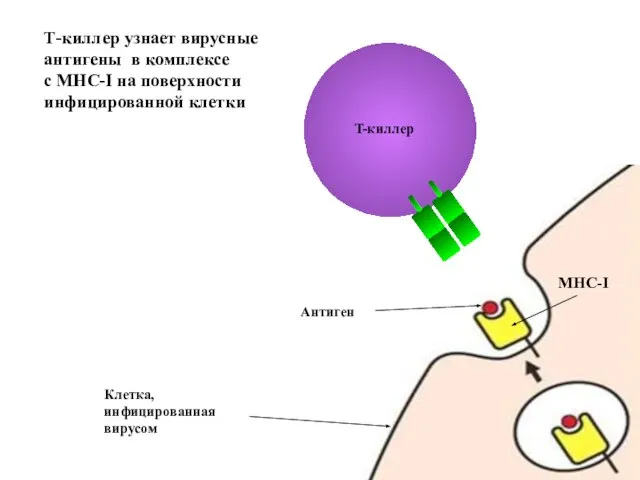
- 80. MHC-I Антиген Т-киллер узнает вирусные антигены в комплексе с МНС-I на поверхности инфицированной клетки Клетка, инфицированная
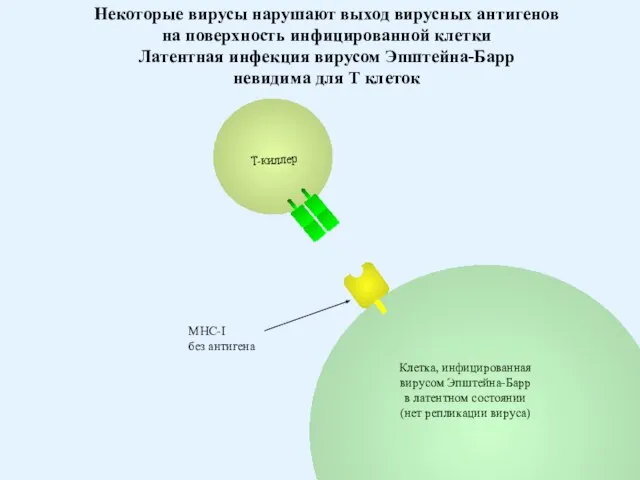
- 81. Клетка, инфицированная вирусом Эпштейна-Барр в латентном состоянии (нет репликации вируса) Некоторые вирусы нарушают выход вирусных антигенов
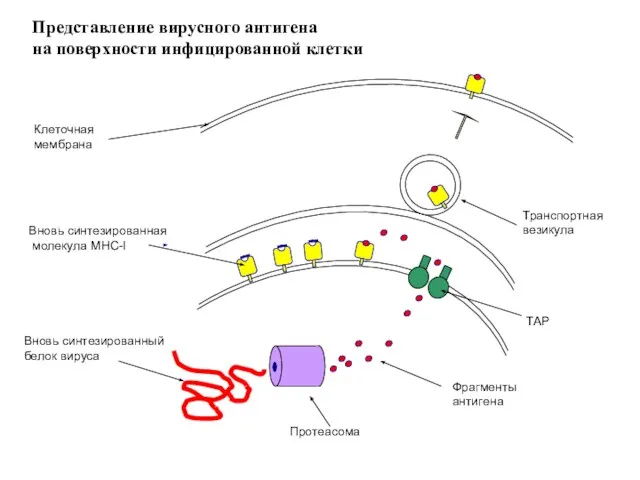
- 82. Вновь синтезированная молекула МНС-I Вновь синтезированный белок вируса Фрагменты антигена Транспортная везикула TAP Клеточная мембрана Представление
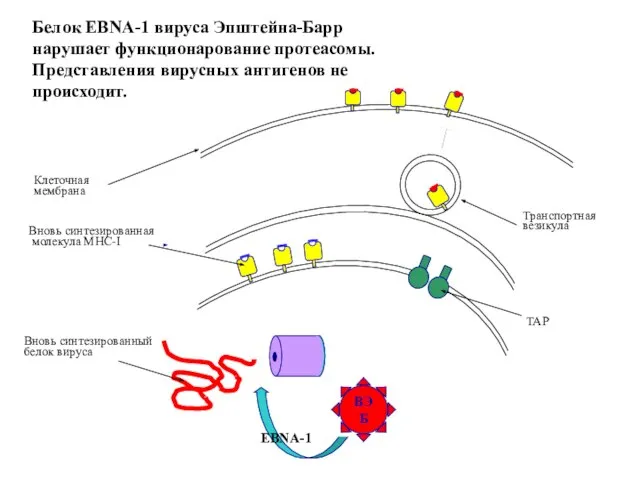
- 83. Вновь синтезированная молекула МНС-I Вновь синтезированный белок вируса Транспортная везикула TAP Клеточная мембрана Белок EBNA-1 вируса
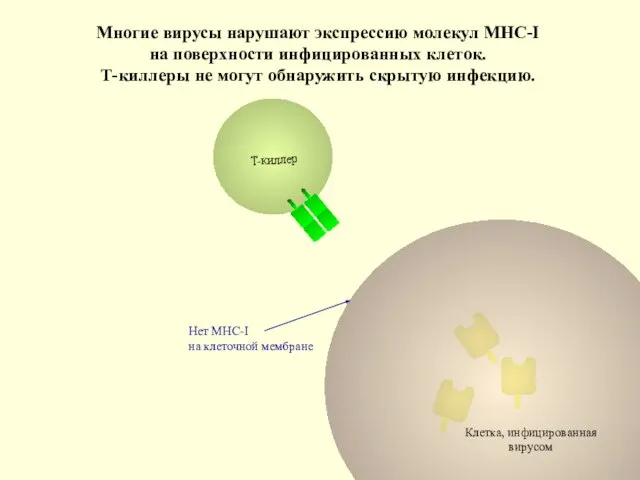
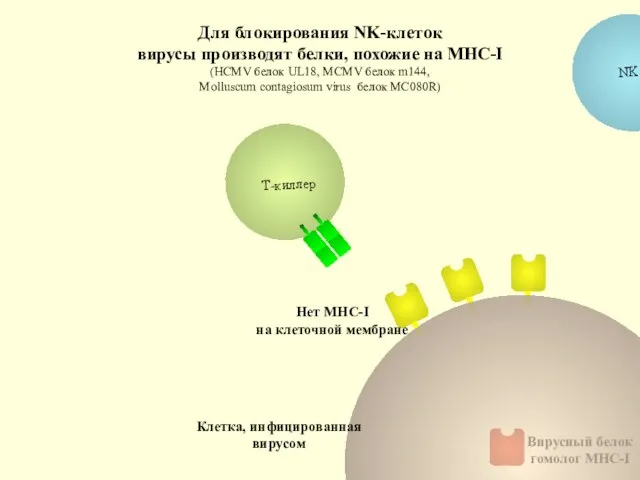
- 84. Клетка, инфицированная вирусом Нет МНС-I на клеточной мембране Многие вирусы нарушают экспрессию молекул МНС-I на поверхности
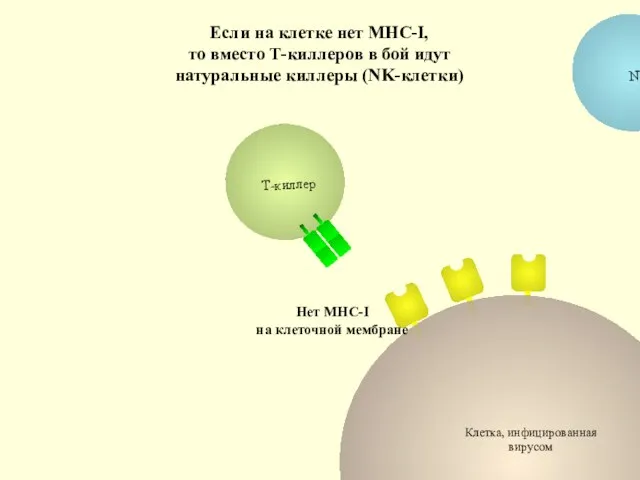
- 85. Клетка, инфицированная вирусом Нет МНС-I на клеточной мембране Если на клетке нет МНС-I, то вместо Т-киллеров
- 86. Для блокирования NK-клеток вирусы производят белки, похожие на МНС-I (HCMV белок UL18, MCMV белок m144, Molluscum
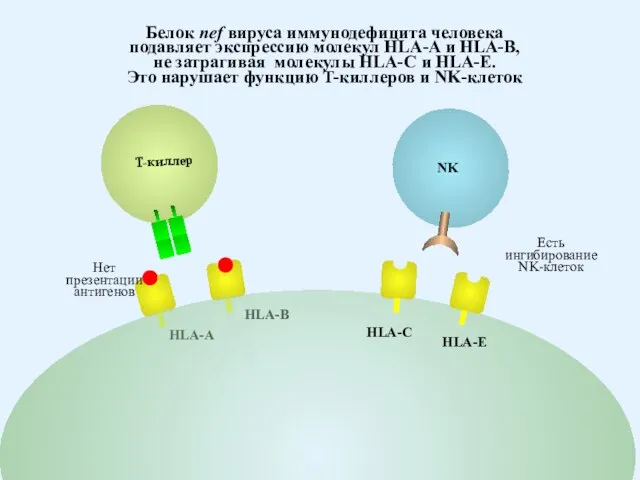
- 87. T-киллер Белок nef вируса иммунодефицита человека подавляет экспрессию молекул HLA-A и HLA-B, не затрагивая молекулы HLA-C
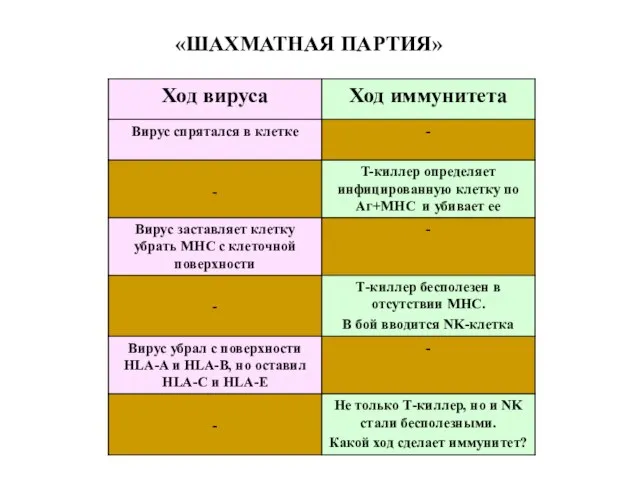
- 88. «ШАХМАТНАЯ ПАРТИЯ»
- 89. УРОКИ: ИММУНИТЕТ И ИНФЕКЦИЯ - ДИНАМИЧНЫЕ И РАЦИОНАЛЬНЫЕ ЖИВЫЕ СИСТЕМЫ, НЕПРЕРЫВНО ИЗМЕНЯЮЩИЕСЯ АДЕКВАТНО ВОЗНИКАЮЩИМ УСЛОВИЯМ. ИНФЕКЦИЯ
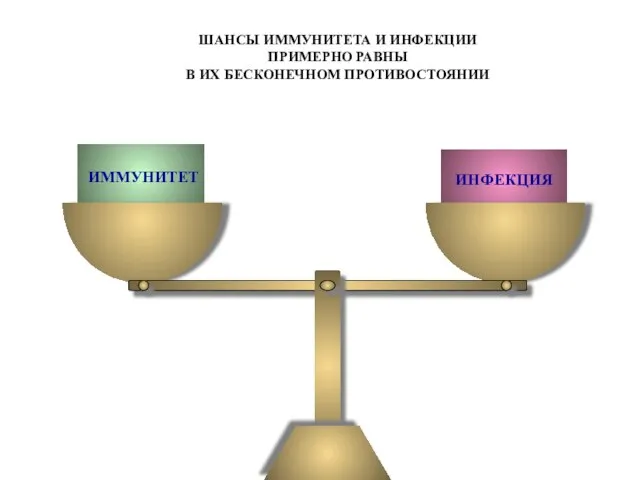
- 90. ИНФЕКЦИЯ ИММУНИТЕТ ШАНСЫ ИММУНИТЕТА И ИНФЕКЦИИ ПРИМЕРНО РАВНЫ В ИХ БЕСКОНЕЧНОМ ПРОТИВОСТОЯНИИ
- 91. ИНФЕКЦИЯ ИММУНИТЕТ ЭТИОТРОПНОЕ ЛЕЧЕНИЕ ДЕЗИНТОКСИКАЦИЯ ОСЛАБЛЕНИЕ ИММУНИТЕТА ВАКЦИНЫ
- 93. Скачать презентацию






























 Об организации отдыха и оздоровления учащихся
Об организации отдыха и оздоровления учащихся Использование методов педагогической квалиметрии как средства оценки качества образования
Использование методов педагогической квалиметрии как средства оценки качества образования Порядок организации оздоровления и отдыха детей города Перми в 2012 году
Порядок организации оздоровления и отдыха детей города Перми в 2012 году П п
П п Готовимся к сочинению на лингвистическую тему
Готовимся к сочинению на лингвистическую тему 3 июля 2009 Тула Зона отдыха «Петушки» Пролетарский район
3 июля 2009 Тула Зона отдыха «Петушки» Пролетарский район Методика оценки дебиторской задолженности Национальной коллегии оценщиков
Методика оценки дебиторской задолженности Национальной коллегии оценщиков Presentation
Presentation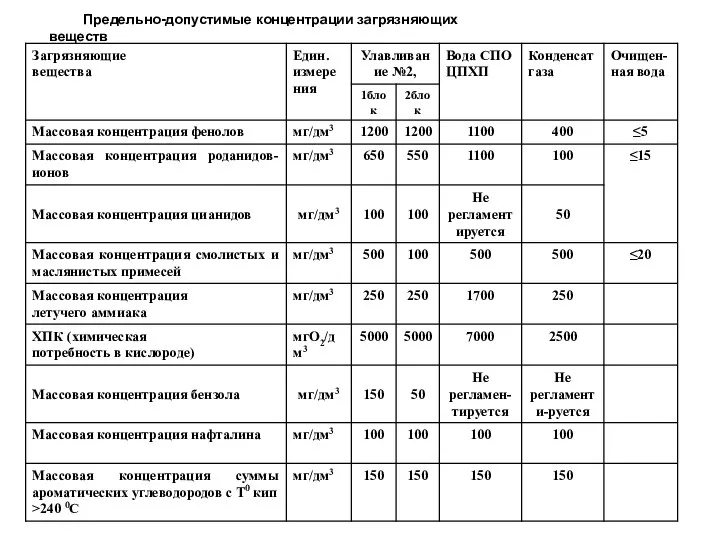 Предельно-допустимые концентрации загрязняющих веществ. Технологическая схема биохимической очистки сточных вод КХП
Предельно-допустимые концентрации загрязняющих веществ. Технологическая схема биохимической очистки сточных вод КХП Определение оптимального режима работы парогенератора АЭС с ВВЭР-1000
Определение оптимального режима работы парогенератора АЭС с ВВЭР-1000 Язык современной Интернет - субкультуры
Язык современной Интернет - субкультуры Сравнение интернета как рекламоносителя с другими медиа
Сравнение интернета как рекламоносителя с другими медиа Политическая деятельность
Политическая деятельность Портфоліо дізайнера
Портфоліо дізайнера Реализация федерального закона от 05.05.2014 №116-ФЗ О внесении изменений в отдельные законодательные акты РФ
Реализация федерального закона от 05.05.2014 №116-ФЗ О внесении изменений в отдельные законодательные акты РФ Участие граждан в решении проблем местных сообществ.Центры Активных Людей
Участие граждан в решении проблем местных сообществ.Центры Активных Людей Почему в России не будет работать закон о коррупции И.И. Елисеева, член-корреспондент РАН Социологический институт РАН
Почему в России не будет работать закон о коррупции И.И. Елисеева, член-корреспондент РАН Социологический институт РАН Правописание согласных в корне слова
Правописание согласных в корне слова Презентация на тему Знание и понимание
Презентация на тему Знание и понимание Теория справедливости Адамса
Теория справедливости Адамса Особенности истории информатики
Особенности истории информатики Отражение моего внутреннего мира в творчестве. Галичина Мария
Отражение моего внутреннего мира в творчестве. Галичина Мария Натуральное число
Натуральное число Система комплексной автоматизации Globus Professional v2.3.
Система комплексной автоматизации Globus Professional v2.3. «Готовность младших школьников к обучению в среднем звене»
«Готовность младших школьников к обучению в среднем звене» Республике Карелия
Республике Карелия Этюды о природе. Зима
Этюды о природе. Зима Генетика. Основные закономерности наследственности
Генетика. Основные закономерности наследственности