Содержание
- 2. КАТАЛИЗ - процесс, заключающийся в изменении скорости химических реакций в присутствии веществ, называемых катализаторами. Катализатор —
- 3. Катализ Положительный Отрицательный
- 4. Механизм действия катализатора К в реакции А + В = АВ можно схематически показать так: А
- 5. Существуют 3 вида катализаторов: а) Гомогенный - когда реакционная смесь и катализатор находятся или в жидком
- 6. Ферменты – биологические катализаторы Ферменты состоят из аминокислот, соединенных в полипептидные цепи различной длины и в
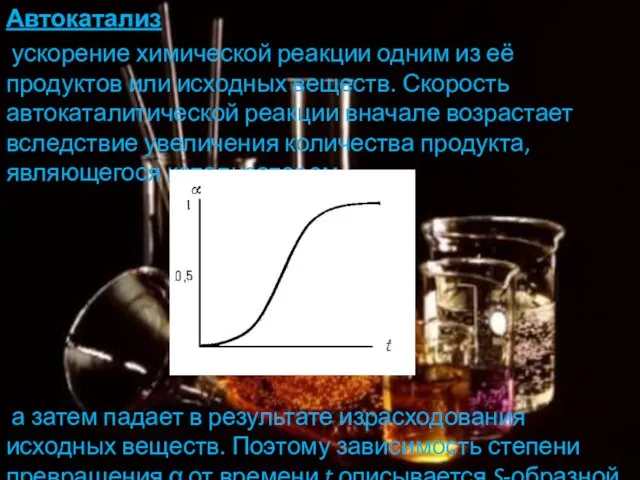
- 7. Автокатализ ускорение химической реакции одним из её продуктов или исходных веществ. Скорость автокаталитической реакции вначале возрастает
- 8. Одним из наиболее широко известных примеров автокатализа является окисление щавелевой кислоты перманганатом калия: 2MnO4- + 5C2O42-
- 9. Промоторы (или активаторы) - вещества, повышающие активность катализатора. При этом промоторы могут сами и не обладать
- 10. Ингибиторы - вещества, замедляющие химической реакции. Существуют различные типы ингибиторов. Их классифицируют следующим образом: 1) пассиваторы
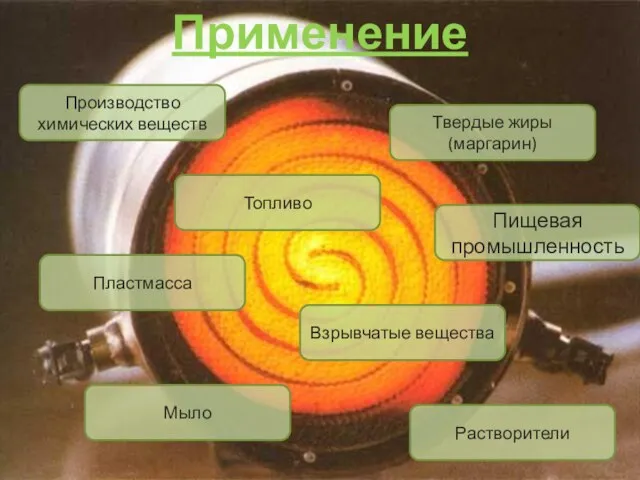
- 11. Применение Твердые жиры (маргарин) Пищевая промышленность Растворители Взрывчатые вещества Топливо Мыло Пластмасса Производство химических веществ
- 12. Роль катализа в экологии Созданы специальные устройства для дожигания выхлопных газов автомобилей, работающие на основе каталитического
- 13. . 1835 г. Берцелиус ввел впервые общее название «катализ» от греческого слова «каталоо» - разрушать Первые
- 15. Скачать презентацию










 Основы цветоведения
Основы цветоведения Культурная практика по Древней Руси
Культурная практика по Древней Руси Развитие речи
Развитие речи Презентация на тему Культура речи Синтаксические нормы
Презентация на тему Культура речи Синтаксические нормы Ресурсы повышения эффективности индивидуальной профилактической деятельности
Ресурсы повышения эффективности индивидуальной профилактической деятельности Государство
Государство Поверхности. Начертательная геометрия
Поверхности. Начертательная геометрия Особенности современного проектирования
Особенности современного проектирования Дети, как известно, наша боль, наша радость
Дети, как известно, наша боль, наша радость Электронные платежные системы России: игроки, состояние и проблемы
Электронные платежные системы России: игроки, состояние и проблемы Faisons connaissence. Leçon 9
Faisons connaissence. Leçon 9 "Вопорсы дядюшки Светофора"
"Вопорсы дядюшки Светофора" Конструкция There is/there are-There was/there were
Конструкция There is/there are-There was/there were ИРЛАНДИЯ
ИРЛАНДИЯ Сервировка стола к завтраку
Сервировка стола к завтраку Главная улица Москвы Если вы пройдете через Александровский сад и повернете налево,
Главная улица Москвы Если вы пройдете через Александровский сад и повернете налево, Как научить ребёнка сознательно относиться к собственному здоровью
Как научить ребёнка сознательно относиться к собственному здоровью Итоги повышения квалификации специалистов учреждений МСЭ по МКФ в рамках государственной программы «Доступная среда» на 2011-2015 го
Итоги повышения квалификации специалистов учреждений МСЭ по МКФ в рамках государственной программы «Доступная среда» на 2011-2015 го Понятие и содержание законности
Понятие и содержание законности Условия назначения страховой пенсии по старости
Условия назначения страховой пенсии по старости Юрист
Юрист Пассивные операции банков, их характеристика
Пассивные операции банков, их характеристика Презентация на тему Треугольники (5 класс)
Презентация на тему Треугольники (5 класс)  Техника мраморирования в современном дизайне
Техника мраморирования в современном дизайне Речевые секреты
Речевые секреты ВОЗРОЖДЕНИЕ (Ренессанс) Торговая площадь (Гроте-маркт) и ратуша —
ВОЗРОЖДЕНИЕ (Ренессанс) Торговая площадь (Гроте-маркт) и ратуша —  Батьківський комітет. Благодійний внесок
Батьківський комітет. Благодійний внесок Сетевая лаборатория проектного предпринимательского образования
Сетевая лаборатория проектного предпринимательского образования