Содержание
- 2. В.И.Вернадский: « Свободный кислород – самый могущественный деятель из всех известных нам химических тел земной коры».
- 3. Джозеф Пристли, Англия, 1774 год Антуан Лоран Лавуазье, Франция, 1777 год
- 4. « Экспресс – диагностика» 1. Воздух – это: А) смесь газов; Б) чистое вещество; 2. Газ
- 5. Порядковый номер атома кислорода - ……………….. 2. ………………… - 16 а.е.м. 3. Период -…………………… ………………………… -
- 6. РАСШИФРОВКА ТАЙНОПИСИ Порядковый номер атома кислорода - 8 2. Относительная атомная масса - 16 а.е.м. 3.
- 7. ХАРАКТЕРИСТИКА КИСЛОРОДА КАК ПРОСТОГО ВЕЩЕСТВА: Химическая формула – О2 , Mr (О2) = 32; М =
- 8. СПОСОБЫ ПОЛУЧЕНИЯ КИСЛОРОДА В ЛАБОРАТОРИИ 1. Разложение перманганата калия при нагревании:
- 9. СПОСОБЫ ПОЛУЧЕНИЯ КИСЛОРОДА В ЛАБОРАТОРИИ 2. Разложения пероксида водорода в присутствии катализатора — оксида марганца (IV).
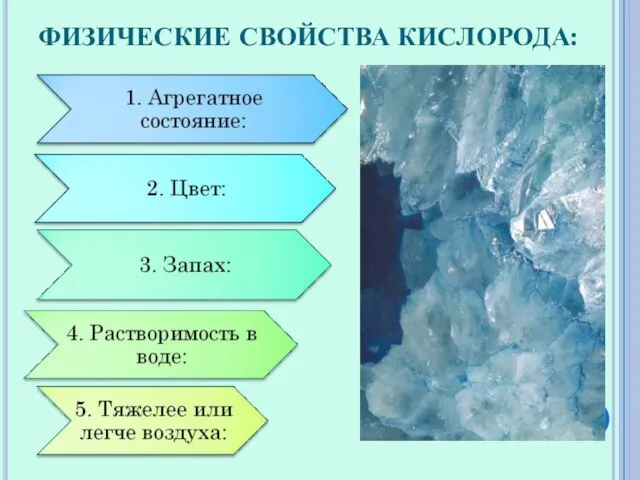
- 10. ФИЗИЧЕСКИЕ СВОЙСТВА КИСЛОРОДА:
- 11. СПОСОБЫ ПОЛУЧЕНИЯ КИСЛОРОДА В ПРОМЫШЛЕННОСТИ 1. Электролиз воды 2. Сжижение воздуха.
- 12. Состав воздуха Постоянными компонентами воздуха являются азот (78,09%), кислород (20,95%), инертные газы (0,93%). Переменные компоненты :
- 13. ИНФОРМАЦИЯ ИЗ ПОДЛИННЫХ ИСТОЧНИКОВ ИНФОРМАЦИЯ ИЗ ПОДЛИННЫХ ИСТОЧНИКОВ
- 14. ДЖОЗЕФ ПРИСТЛИ, АНГЛИЯ, 1774 ГОД При нагревании оксида ртути Дж.Пристли получил бесцветный газ, который мало растворялся
- 15. КАРЛ ШЕЕЛЕ, ШВЕЦИЯ опыты с 1768 по 1773: «Исследования воздуха являются в настоящее время важнейшим предметом
- 16. АНТУАН ЛОРАН ЛАВУАЗЬЕ, ФРАНЦИЯ, 1777 ГОД Подлинная природа этого газа была установлена во Франции. Название Oxygenium
- 17. ОСНОВНЫЕ СОЕДИНЕНИЯ КИСЛОРОДА самый распространённый оксид: оксид водорода (вода) – H2O
- 18. Оксид кремния – SiO2
- 19. ОКСИД АЛЮМИНИЯ - AL2O3
- 20. ЗНАЧЕНИЕ КИСЛОРОДА: Кислород- это сознание человека. Он особенно необходим мозгу. Клетки мозга умирают без кислорода гораздо
- 21. КИСЛОРОД ВХОДИТ В СОСТАВ ОРГАНИЧЕСКИХ ВЕЩЕСТВ 62% массы тела млекопитающих– это масса всех атомов кислорода, входящих
- 22. ВЫБЕРИТЕ ПРАВИЛЬНЫЙ ОТВЕТ: 1.В 1774 году один учёный после проведённого эксперимента написал: «Но что поразило меня
- 23. ВЫБЕРИТЕ ПРАВИЛЬНЫЙ ОТВЕТ: 5.Оксид железа (III) имеет формулу: А) Fe2O3 В) FeO3 С) Fe3O4 6.В каком
- 25. Скачать презентацию





















 Заболевания роговицы
Заболевания роговицы  Презентация на тему Международное сотрудничество в сфере уголовного судопроизводства
Презентация на тему Международное сотрудничество в сфере уголовного судопроизводства Духовное и физическое состояние молодёжи в Нерюнгринском районе
Духовное и физическое состояние молодёжи в Нерюнгринском районе Здоровый образ жизни: творчество и долголетие
Здоровый образ жизни: творчество и долголетие Оқы, еске түсір, айт
Оқы, еске түсір, айт Презентация на тему Королевство Норвегия
Презентация на тему Королевство Норвегия Презентация на тему Юганский заповедник
Презентация на тему Юганский заповедник Развивайка Природа
Развивайка Природа Влияние мультфильмов на психику детей
Влияние мультфильмов на психику детей Интерференция света в тонких пленках
Интерференция света в тонких пленках Презентация на тему Как человек использует свойства воды
Презентация на тему Как человек использует свойства воды  Святки. Традиции
Святки. Традиции Деление клетки.Митоз.Амитоз.Мейоз
Деление клетки.Митоз.Амитоз.Мейоз ПРАВИТЕЛЬСТВО САНКТ-ПЕТЕРБУРГАЖИЛИЩНЫЙ КОМИТЕТСанкт-Петербургское государственное учреждение «ГОРЖИЛОБМЕН»
ПРАВИТЕЛЬСТВО САНКТ-ПЕТЕРБУРГАЖИЛИЩНЫЙ КОМИТЕТСанкт-Петербургское государственное учреждение «ГОРЖИЛОБМЕН» Структура форм, пластика тела объекта. Фактура, текстура. Базовые упражнения
Структура форм, пластика тела объекта. Фактура, текстура. Базовые упражнения Структура компьютера и принципы его функционирования
Структура компьютера и принципы его функционирования PPF ЗВЕЗДОЧКА
PPF ЗВЕЗДОЧКА Ольга Парфенова - свадебный церемониймейстер
Ольга Парфенова - свадебный церемониймейстер Виды изобразительного искусства: живопись, графика, скульптура. 2 класс
Виды изобразительного искусства: живопись, графика, скульптура. 2 класс Одно решение для всех платежей или как еще получить деньги от клиента
Одно решение для всех платежей или как еще получить деньги от клиента Твой новый взгляд на свободу
Твой новый взгляд на свободу В районе Ясенево ведётся капитальный ремонт 4-х спортивных площадок по адресам: Вильнюсская ул., 17, Голубинская ул., 7-5, Литовский б-р.
В районе Ясенево ведётся капитальный ремонт 4-х спортивных площадок по адресам: Вильнюсская ул., 17, Голубинская ул., 7-5, Литовский б-р. ФИЗИКА – 9 класс
ФИЗИКА – 9 класс Строение и функции нервной системы
Строение и функции нервной системы  Презентация на тему БАКТЕРИИ
Презентация на тему БАКТЕРИИ  Выборочный контроль товаров на основе управления рисками Боб Олсон Консультант по таможенным вопросам Подготовлено Робертом Х
Выборочный контроль товаров на основе управления рисками Боб Олсон Консультант по таможенным вопросам Подготовлено Робертом Х Подвижные игры на уроке физической культуры
Подвижные игры на уроке физической культуры Система образов романа «Евгений Онегин»
Система образов романа «Евгений Онегин»