Содержание
- 2. характерные признаки: металлы тяжелее воды
- 3. Ga Cs Hg Большинство - твердые вещества при комнатной температуре, но есть и жидкие:
- 4. Большинство имеют металлический блеск, серые или белые Cs кристаллы Cu самородок Au самородок
- 5. КЛАССИФИКАЦИЯ МЕТАЛЛОВ 1. Черные и цветные 2. Тяжелые (ƍ≥5 г\см3) и легкие (ƍ≤5г\см3) 3. Драгоценные 4.
- 6. Черные Получено электро-лизом, чистота 99,97% Fe
- 7. Цветные Ag Bi Rb Sn Ti
- 8. Тяжелые Fe Hg Pb Bi
- 9. Тяжелые Co Sb Ni 99,99% Медленный электролиз
- 10. Легкие Li, K, Na, Rb, Cs, Fr, Be, Mg, Ca, Sr, Ba, Al, Sn Al Ca
- 11. ДРАГОЦЕННЫЕ Ag Au
- 12. Платиновые металлы Os Rh Pt
- 13. Редкоземельные La
- 14. Eu Y Sc
- 15. Металлы: s-, d-, f- элементы, а также небольшое количество p- элементов – Al, Ga, In, Tl,
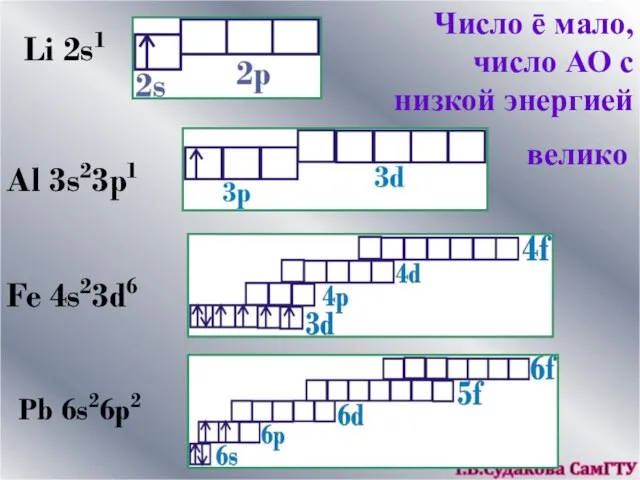
- 16. Li 2s1 Al 3s23p1 Fe 4s23d6 Pb 6s26p2 Число ē мало, число АО с низкой энергией
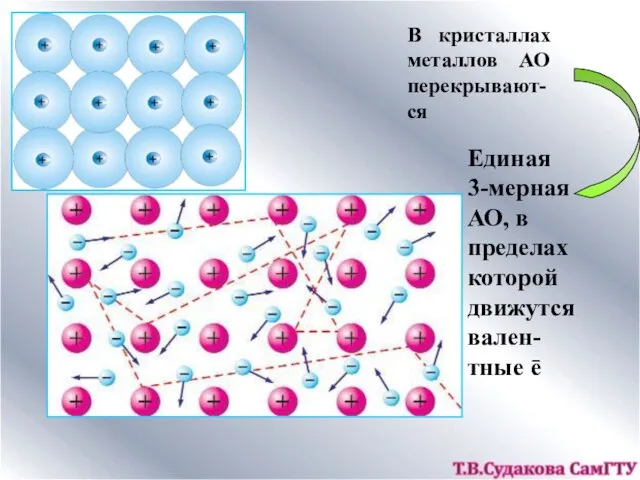
- 17. В кристаллах металлов АО перекрывают-ся Единая 3-мерная АО, в пределах которой движутся вален-тные ē
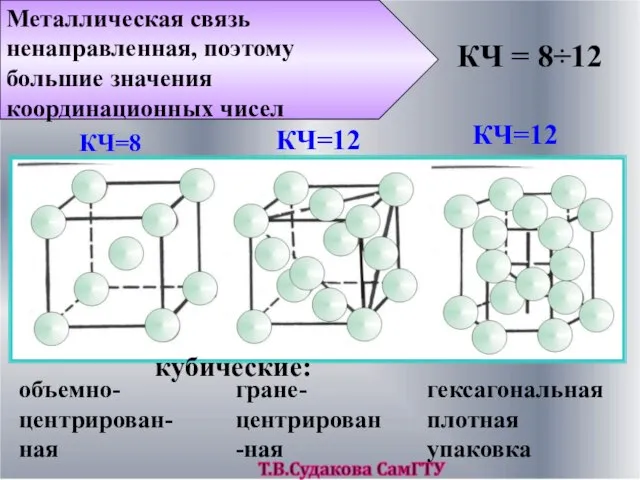
- 19. КЧ = 8÷12 Металлическая связь ненаправленная, поэтому большие значения координационных чисел объемно-центрирован-ная кубические: гране-центрирован-ная гексагональная плотная
- 20. ХИМИЧЕСКИЕ СВОЙСТВА Общие: 1. Малая электроотрицательность (ЭО). 2. Ме в реакциях образуют только катионы: Me0 ─
- 21. Металлы p- и d-элементы: Низшая СО +1, +2 Основные оксиды и гидроксиды Промежуточ-ная СО +3, +4
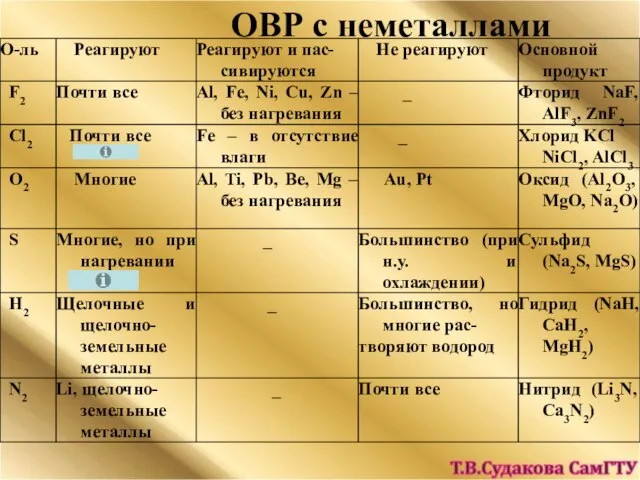
- 22. ОВР с неметаллами
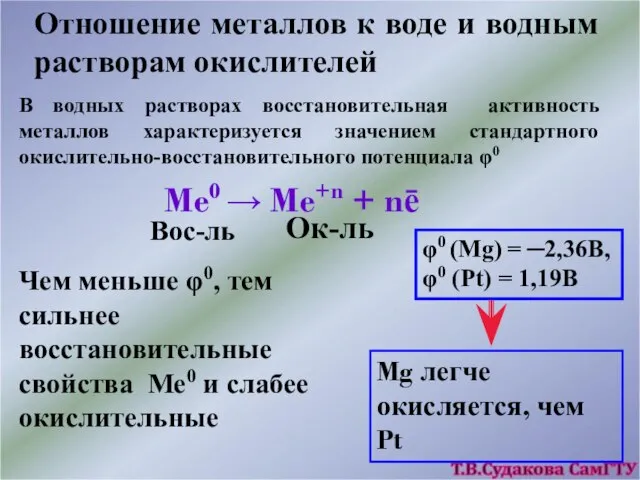
- 23. Отношение металлов к воде и водным растворам окислителей В водных растворах восстановительная активность металлов характеризуется значением
- 24. взаимодействие с водой - это ОВР, где окислитель Н+ φ(2Н+/Н2) = - 0,059•рН = 0,059•7 =
- 25. Ме0 + ОН– → МеО2– + Н2 Ме0 + Н2О + ОН– → [Ме(ОН)4]– + Н2
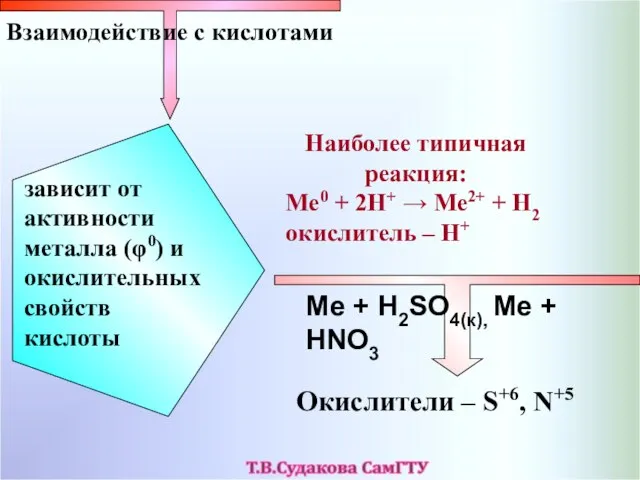
- 26. Наиболее типичная реакция: Ме0 + 2Н+ → Ме2+ + Н2 окислитель – Н+ Взаимодействие с кислотами
- 27. Оксидные: Fe2O3 - гематит, Fe2O3•H2O – гетит, Al2O3 – боксит, TiO2 – рутил, SnO2 – касситерит;
- 28. гематит Fe2O3 боксит Al2O3 касситерит SnO2
- 29. пирит FeS2 халькопирит Cu2S•FeS2
- 30. Общие методы получения: Вытеснение металла более активным металлом. Восстановление металлов неметаллами - газообразными СО и Н2
- 31. 3V2O5 (к) + 10Al(к) →5Al2O3(к) + 6V(к) TiCl4 (к) + 4Na (к) → Ti (к) +
- 32. Восстановление неметаллами - пирометаллургия -только при высоких температурах MgO + C = CO + Mg Sb2O4
- 33. электролиз водных растворов или расплавов: NaCl → Na+ + Cl─ катод─: анод+: Na+ + ē =
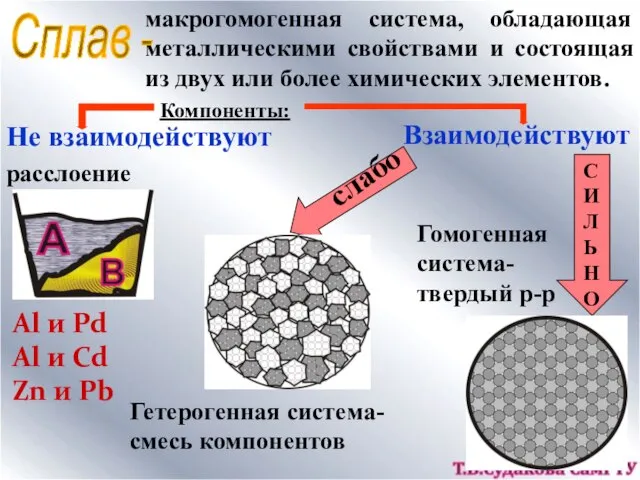
- 34. макрогомогенная система, обладающая металлическими свойствами и состоящая из двух или более химических элементов. Сплав - Компоненты:
- 35. однородное (гомогенное) кристал-лическое вещество переменного состава, в кристаллическую решетку которого входят атомы или ионы нескольких компонентов.
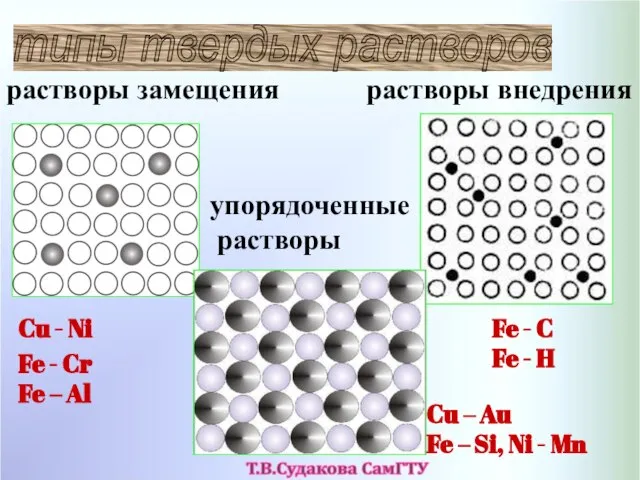
- 36. типы твердых растворов растворы замещения растворы внедрения упорядоченные растворы Cu - Ni Fe - C Fe
- 37. Очень сильное взаимодействие между атомами металлов Интерметаллические соединения (интерметаллиды)- Соединения металлов между собой и с неметаллами
- 38. Манганин – сплав 11% Mn, 2,5-3,5% Ni и 86% Cu; Примеры сплавов: Чугун – сплав Fe
- 40. сплав Fe с С (3,5-5,5%) и Mn (5-20%); На изломе – зеркальный блеск используется в произ-водстве
- 41. Обычная углеродистая нержавеющая Кровля, до 25 лет
- 42. литье Сталь 35Г Повышенная твердость и износостойкость щеки дробилок башня танка
- 43. высокое электрическое сопротивление, самые «тихие» сплавы: 70% Mn и 30% Cu демпфирование - поглощение энергии механических
- 44. Бронза: оловянная – Cu-Sn алюминиевая – Cu-Al бериллиевая – Cu-Be и т.п. Самая древняя !
- 45. Нейзильбер: Cu(50- 60%) –Ni(20-25%) –Zn(18-22%) Фехраль: Al-Cr (15-30%)-Fe (70% и более)
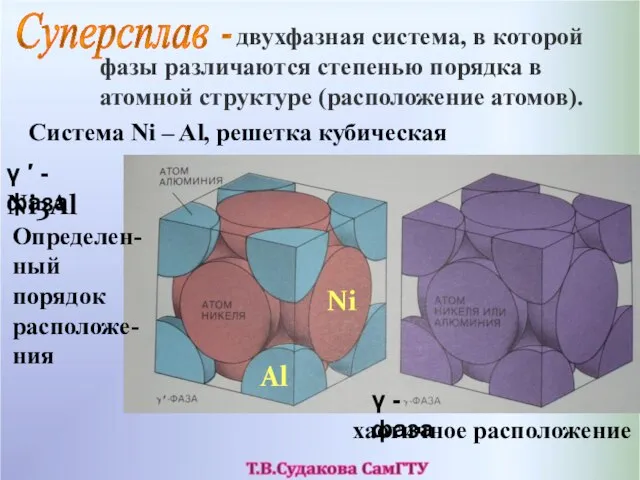
- 46. двухфазная система, в которой фазы различаются степенью порядка в атомной структуре (расположение атомов). Суперсплав - Система
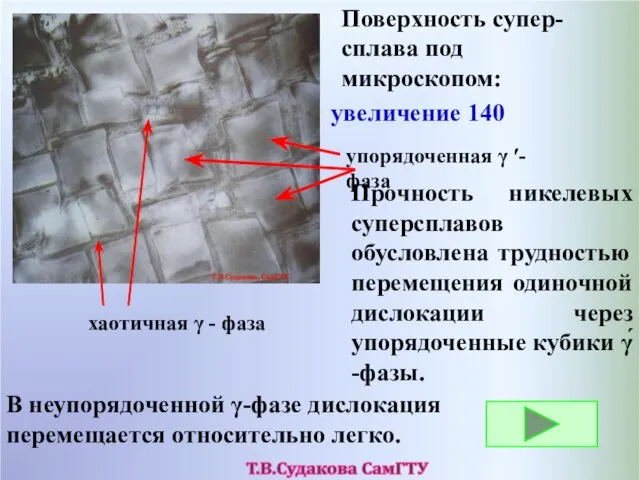
- 47. Поверхность супер-сплава под микроскопом: упорядоченная γ ′-фаза хаотичная γ - фаза Прочность никелевых суперсплавов обусловлена трудностью
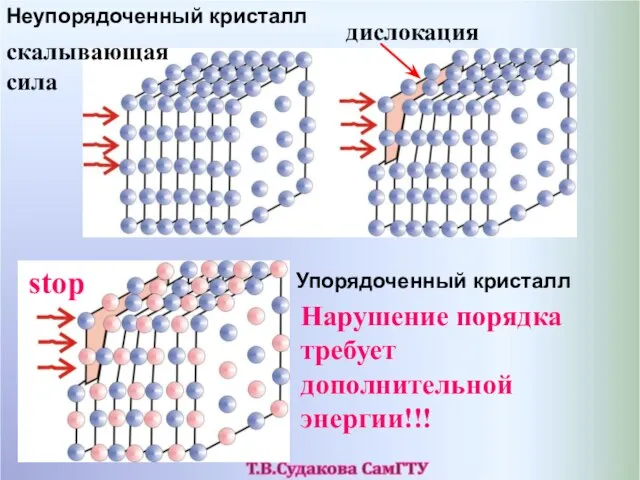
- 48. скалывающая сила дислокация stop Нарушение порядка требует дополнительной энергии!!! Неупорядоченный кристалл Упорядоченный кристалл
- 49. Сверхпластичность зерна Чем мельче зерно, тем выше скорость деформации. Причина - деформация металлических связей в контактах
- 50. Чем больше S поверхности частиц (наноразмеры), тем больше поверхностная G Сплав не устойчив! При ↑ Т
- 51. аморфные металлы Сверхбыстрое охлаждение Только ближний порядок в структуре
- 52. 1976г. - лента аморфного магнитного сплава Ni-Fe-P-B 1960г. -первый аморфный сплав Au75Si25 свойства: нет кристаллической решетки
- 53. тарелки с нагревательным контуром из тонких металлических лент: подогрев пищи прямо в тарелке. Металл для нагреватель-ного
- 55. Скачать презентацию








































 Разработка рекламной кампании продвижения бренда «Erdal»
Разработка рекламной кампании продвижения бренда «Erdal» Всемирный день психического здоровья
Всемирный день психического здоровья Действия туристской группы в ЧС по организации поиска туриста, отставшего от группы
Действия туристской группы в ЧС по организации поиска туриста, отставшего от группы Аппарат Государственной Думы Федерального Собрания Российской Федерации
Аппарат Государственной Думы Федерального Собрания Российской Федерации Общество и человек
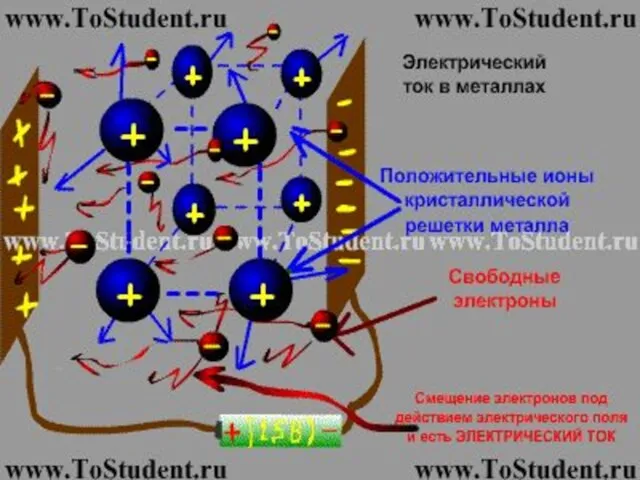
Общество и человек Электрический ток
Электрический ток  К.М. Симонова
К.М. Симонова Презентация на тему Загадки по ПДД
Презентация на тему Загадки по ПДД  Царства живой природы
Царства живой природы Потенциально-смертельные инциденты
Потенциально-смертельные инциденты Китай на пути модернизации и реформирования
Китай на пути модернизации и реформирования Природа в жизни человека
Природа в жизни человека Завоевание Обетованной земли
Завоевание Обетованной земли Национальная научно-техническая конференция
Национальная научно-техническая конференция Семинар сети пилотных ОУ по введению ФГОС Дорожная карта создания информационно-образовательной среды начальной ступени гимна
Семинар сети пилотных ОУ по введению ФГОС Дорожная карта создания информационно-образовательной среды начальной ступени гимна Тема исследования: Атака сотовых телефонов Авторы : Учащиеся 9 –го класса ОГОУ «Школа-интернат для д
Тема исследования: Атака сотовых телефонов Авторы : Учащиеся 9 –го класса ОГОУ «Школа-интернат для д Преемственность в обучении математике в Образовательной системе «Школа 2100»
Преемственность в обучении математике в Образовательной системе «Школа 2100» Верховный суд РФ
Верховный суд РФ Интернет технологии в образовании
Интернет технологии в образовании АКСАКОВ КОНСТАНТИН СЕРГЕЕВИЧ (1817–1860)
АКСАКОВ КОНСТАНТИН СЕРГЕЕВИЧ (1817–1860) Тест. Виды и жанры изобразительного искусства
Тест. Виды и жанры изобразительного искусства Выпускная квалификационная работа (дипломный проект)
Выпускная квалификационная работа (дипломный проект) Терроризм угроза обществу
Терроризм угроза обществу Презентация на тему Селекция животных
Презентация на тему Селекция животных  Презентация на тему Жизнь и творчество Александра Сергеевича Пушкина
Презентация на тему Жизнь и творчество Александра Сергеевича Пушкина  La journée des dictionnaires
La journée des dictionnaires Оружейная палата Московского Кремля
Оружейная палата Московского Кремля Александр Флеминг
Александр Флеминг