Содержание
- 2. Химические реакции – химические процессы, в результате которых из одних веществ образуются другие отличающиеся от них
- 3. По числу и составу реагирующих веществ: Реакции, идущие без изменения состава веществ В неорганической химии к
- 4. Реакции, идущие с изменением состава вещества Реакции соединения – это такие реакции, при которых из двух
- 5. Реакция соединения кислотного оксида фосфора(V) с водой: Р2 О5 + 3H2O = 2 H3PO4
- 6. Реакции разложения – это такие реакции, при которых из одного сложного вещества образуется несколько новых веществ.
- 7. Разложение перманганата калия при нагревании: Усиление горения тлеющей лучины свидетельствует от том, что происходит выделение кислорода:
- 8. Реакции замещения – это такие реакции, в результате которых атомы простого вещества замещают атомы какого-нибудь элемента
- 9. Реакции обмена – это такие реакции, при которых два сложных вещества обмениваются своими составными частями Эти
- 10. Взаимодействие сульфата хрома(III) с гидроксидом калия: Cr2(SO4)3 + 6KOH = 2Cr(OH)3 + 3K2SO4
- 11. По изменению степеней окисления химических элементов, образующих вещества: Окислительно-восстановительные реакции: Окислительно-восстановительные реакции – реакции, идущие с
- 12. Не окислительно-восстановительные реакции: К ним относятся все реакции ионного обмена, например: Na2CO3 + 2HCl = 2NaCl
- 13. По участию катализатора: Катализаторы – это вещества, участвующие в химической реакции и изменяющие ее скорость или
- 14. По агрегатному состоянию реагирующих веществ (фазовому составу): Гетерогенные реакции: Гетерогенные реакции – реакции, в которых реагирующие
- 15. По тепловому эффекту: Экзотермические реакции: Экзотермические реакции – реакции, протекающие с выделением энергии во внешнюю среду.
- 16. Эндотермические реакции: Эндотермические реакции – реакции, протекающие с поглощением энергии во внешнюю среду. К ним относятся
- 17. По направлению: Необратимые реакции: Необратимые реакции протекают в данных условиях только в одном направлении. К таким
- 19. Скачать презентацию
















 Основные направления инвестирования в Российской Федерации
Основные направления инвестирования в Российской Федерации  Учебная дисциплина. Психология
Учебная дисциплина. Психология Ачинск – город с историей
Ачинск – город с историей Презентация на тему Государства и народы доколумбовой Америки
Презентация на тему Государства и народы доколумбовой Америки  Сочинение с элементами описания внутреннего состояния по картине Н. Богданова-Бельского «У дверей школы»
Сочинение с элементами описания внутреннего состояния по картине Н. Богданова-Бельского «У дверей школы» Откройте для себя здоровую, юную кожу
Откройте для себя здоровую, юную кожу ПРАВАЧЕЛОВЕКА
ПРАВАЧЕЛОВЕКА Принципы организации судебной власти
Принципы организации судебной власти « У нас много замечательных и любимых не только нами, но и всем миром, писателей. Чехов занимает одно из первых мест среди них ». К. А.
« У нас много замечательных и любимых не только нами, но и всем миром, писателей. Чехов занимает одно из первых мест среди них ». К. А.  Музыкальная живопись и живописная музыка. Импрессионизм.
Музыкальная живопись и живописная музыка. Импрессионизм. Установка для повторного нанесения покрытия на аноды компании Каустик
Установка для повторного нанесения покрытия на аноды компании Каустик Rome Model United Nations Rome International Careers
Rome Model United Nations Rome International Careers  История Российского самодержавия
История Российского самодержавия Добро пожаловать на час общения «Поговорим о любви»
Добро пожаловать на час общения «Поговорим о любви» Технология моделирования в начальной школе Сложным является сообщение учащимся знаний, так как их объем из года в год увеличивает
Технология моделирования в начальной школе Сложным является сообщение учащимся знаний, так как их объем из года в год увеличивает Рациональное питание. Расчет меню
Рациональное питание. Расчет меню Планета дорог
Планета дорог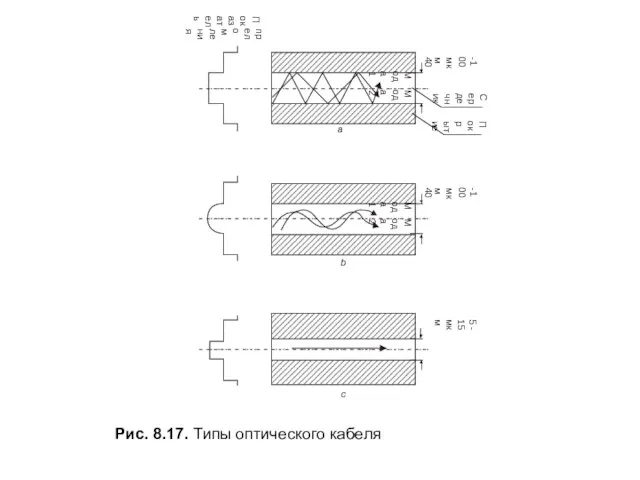 Рис. 8.17. Типы оптического кабеля
Рис. 8.17. Типы оптического кабеля Обширный информационный сервис по Европейскому Союзу, странам Европы и актульным событиям, происходящим в Европе
Обширный информационный сервис по Европейскому Союзу, странам Европы и актульным событиям, происходящим в Европе Идеал человеческого единства
Идеал человеческого единства Конкурс «Роялти – педагогу новатору»
Конкурс «Роялти – педагогу новатору» Современное состояние классовой борьбы в Австралии и Новой Зеландии
Современное состояние классовой борьбы в Австралии и Новой Зеландии Фото_Чек_лист_08_09_2022_ПВЗ_Октябрьское_поле
Фото_Чек_лист_08_09_2022_ПВЗ_Октябрьское_поле Причастия действительные и страдательные
Причастия действительные и страдательные Презентация на тему Природная зона тайги
Презентация на тему Природная зона тайги Multilayer model in optics. New analitic results.
Multilayer model in optics. New analitic results. Синтаксическая стилистика
Синтаксическая стилистика Презентация на тему Совесть и раскаяние (4 класс)
Презентация на тему Совесть и раскаяние (4 класс)