Содержание
- 2. Деление на минеральные и органические вещества В начале XIX века ученые разделяли все вещества в природе
- 3. Многочисленность органических веществ В настоящее время человечеству известно более 10 млн. веществ, из них около 70%
- 4. Определение класса органических соединений Наличие тех или иных функциональных групп либо атомов элементов определяет принадлежность соединения
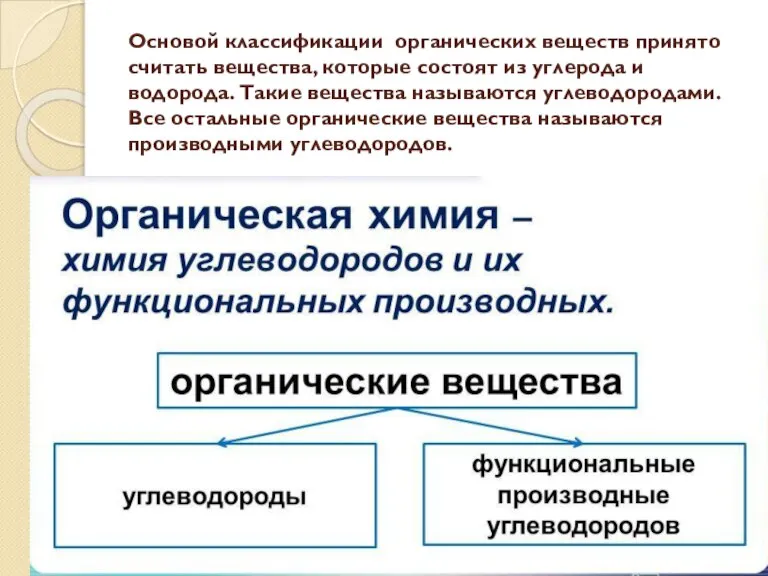
- 5. Основой классификации органических веществ принято считать вещества, которые состоят из углерода и водорода. Такие вещества называются
- 6. Классификация органических соединений Для классификации органических соединений по типам и построения их названий в молекуле органического
- 7. Углеродный скелет Углеродный скелет представляет собой последовательность химически связанных между собой атомов углерода. Функциональные группы образуют
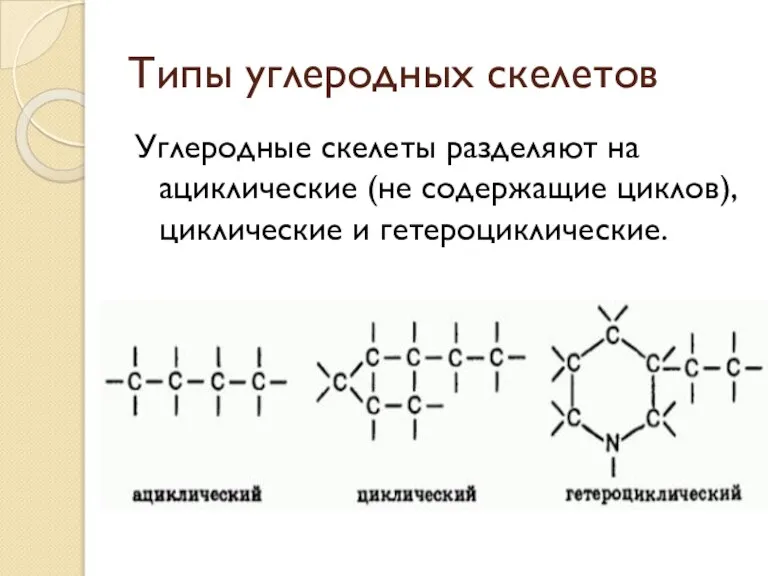
- 8. Типы углеродных скелетов Углеродные скелеты разделяют на ациклические (не содержащие циклов), циклические и гетероциклические.
- 9. Функциональные группы В большинстве органических соединений, кроме атомов углерода и водорода, содержатся атомы других элементов (не
- 10. Важнейшие функциональные группы
- 11. Номенклатура органических соединений В настоящее время для наименования органических соединений применяются три типа номенклатуры: тривиальная, рациональная
- 12. Тривиальная (историческая) номенклатура первая номенклатура, возникшая в начале развития органической химии, когда не существовало классификации и
- 13. Рациональная номенклатура по этой номенклатуре за основу наименования органического соединения обычно принимают название наиболее простого (чаще
- 14. Систематическая номенклатура ИЮПАК (IUPAC — Международный союз теоретической и прикладной химии) международная единая химическая номенклатура. Систематическая
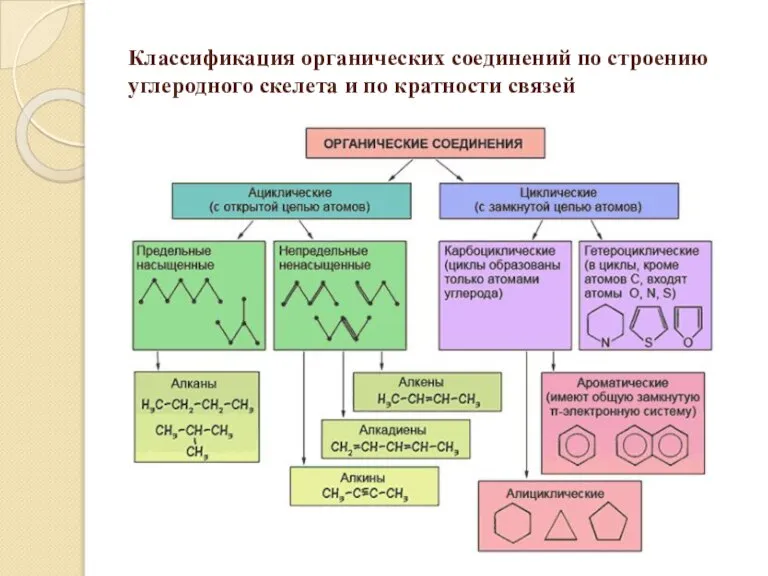
- 15. Классификация органических соединений по строению углеродного скелета и по кратности связей
- 16. Список основных классов органических веществ Алканы Алкины Алкены Бензолы Нитросоединения Нитрозопроизводные Галогенпроизводные Пероксиды Сульфиды Простые эфиры
- 17. План разбора класса органических веществ 1. Общая формула 2.Строение 3.Гомологический ряд. 4. Изомерия 5. Физические свойства
- 18. Теория химического строения Теория химического строения - учение о строении молекулы, описывающее все те её характеристики,
- 19. Основные положения теории химического строения органических соединений 1. Все атомы, образующие молекулы органических веществ, связаны в
- 20. АЛКАНЫ
- 21. Определение алканов Алканы (парафины) – алифатические (нециклические) предельные углеводороды, в которых атомы углерода связаны между собой
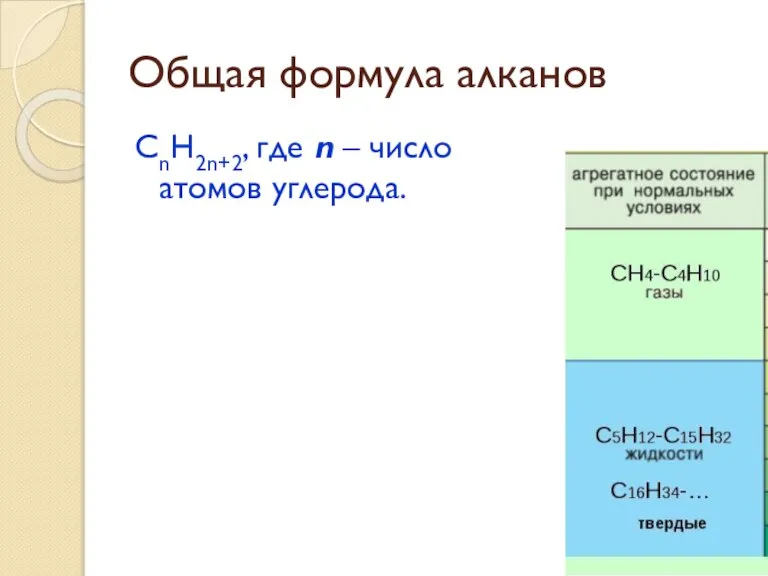
- 22. Общая формула алканов CnH2n+2, где n – число атомов углерода.
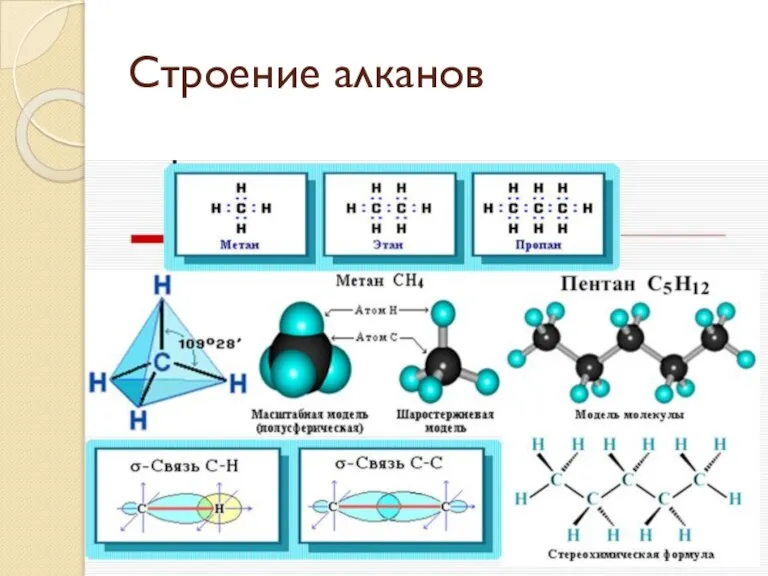
- 23. Строение алканов
- 24. Определение гомологического ряда Ряд химических соединений одного структурного типа, отличающихся друг от друга на одну или
- 25. Гомологический ряд алканов Простейший его представитель – метан СН4. Гомологами метана являются: этан C2H6; пропан C3H8;
- 26. Гомологический ряд алканов
- 27. Изомерия алканов: углеродного скелета и поворотная (конформационная) изомерия
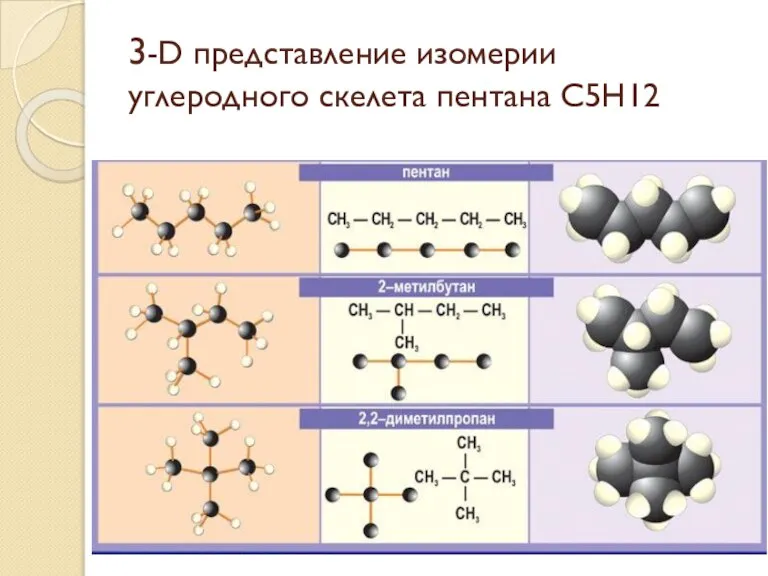
- 28. 3-D представление изомерии углеродного скелета пентана С5H12
- 30. Вопрос по таблице:
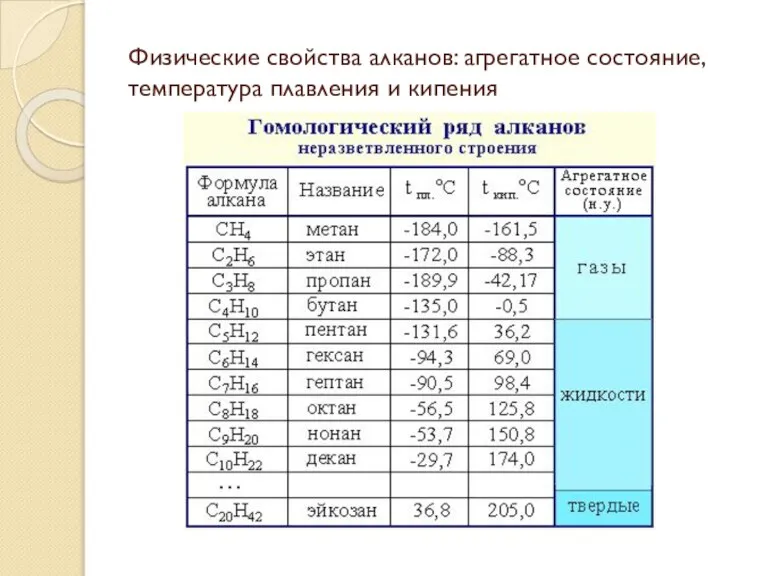
- 31. Физические свойства алканов: агрегатное состояние, температура плавления и кипения
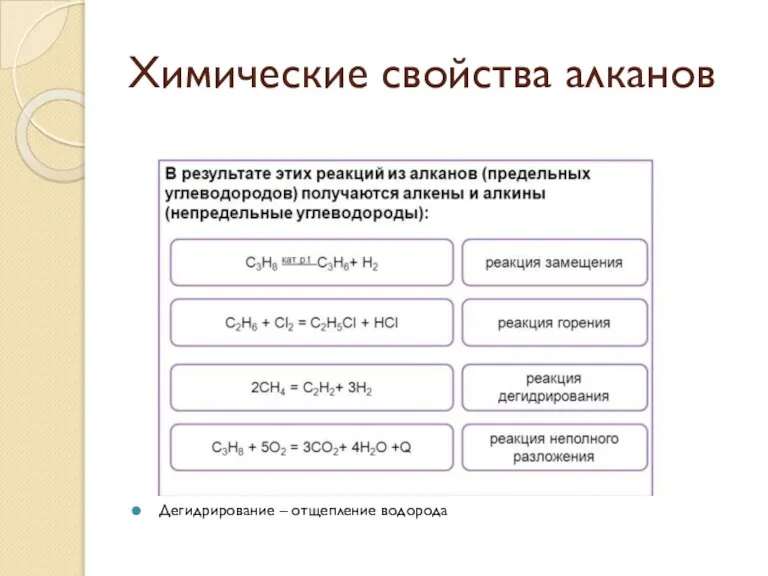
- 32. Химические свойства алканов Дегидрирование – отщепление водорода
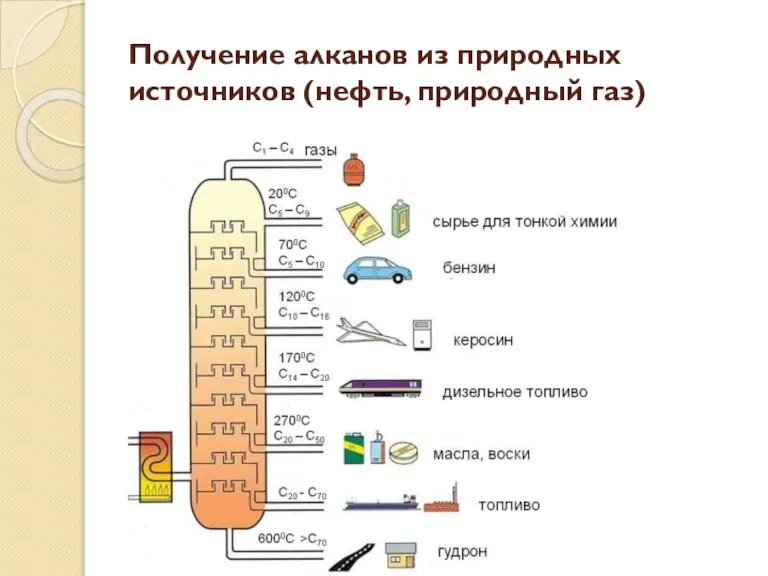
- 33. Получение алканов из природных источников (нефть, природный газ)
- 34. Получение и применение алканов
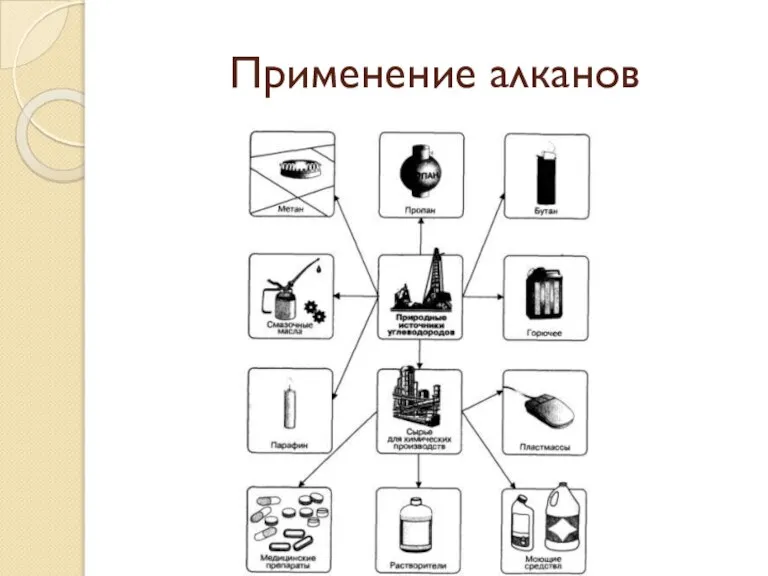
- 35. Применение алканов
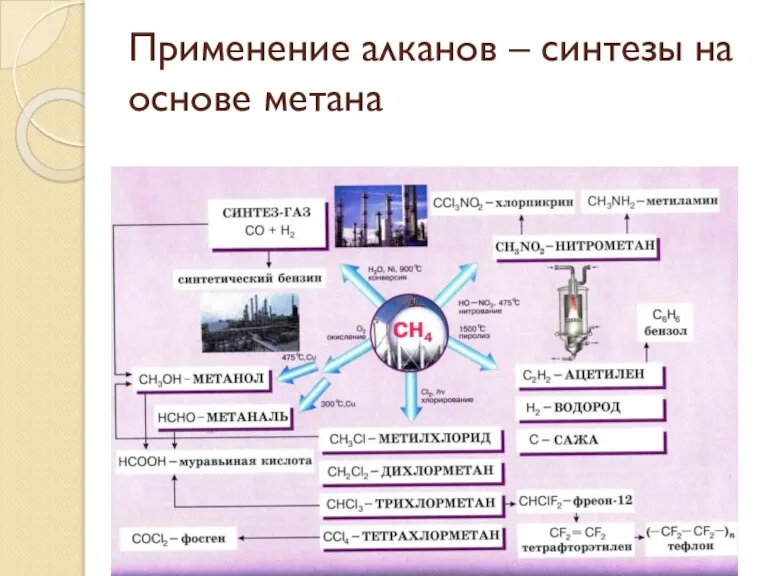
- 36. Применение алканов – синтезы на основе метана
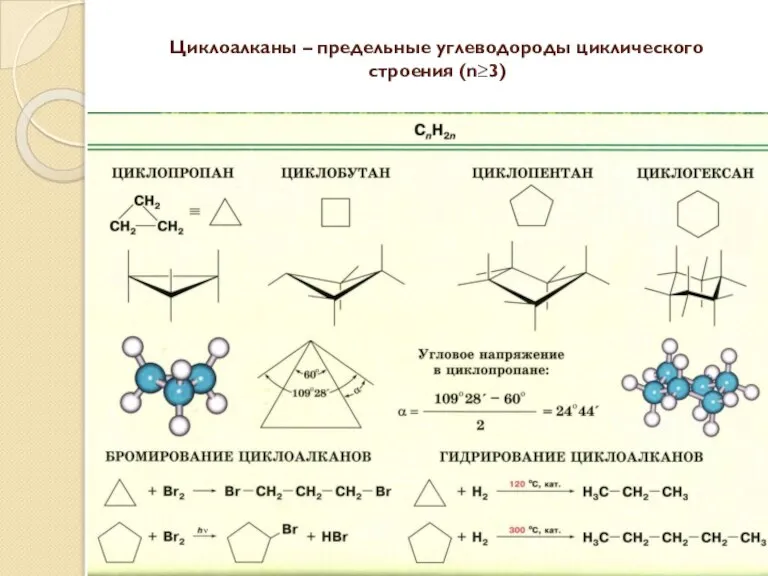
- 37. Циклоалканы – предельные углеводороды циклического строения (n≥3)
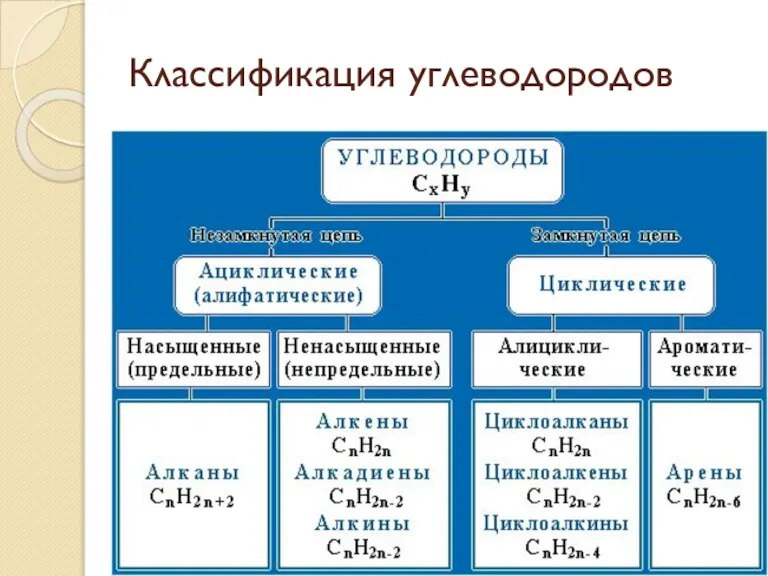
- 38. Классификация углеводородов
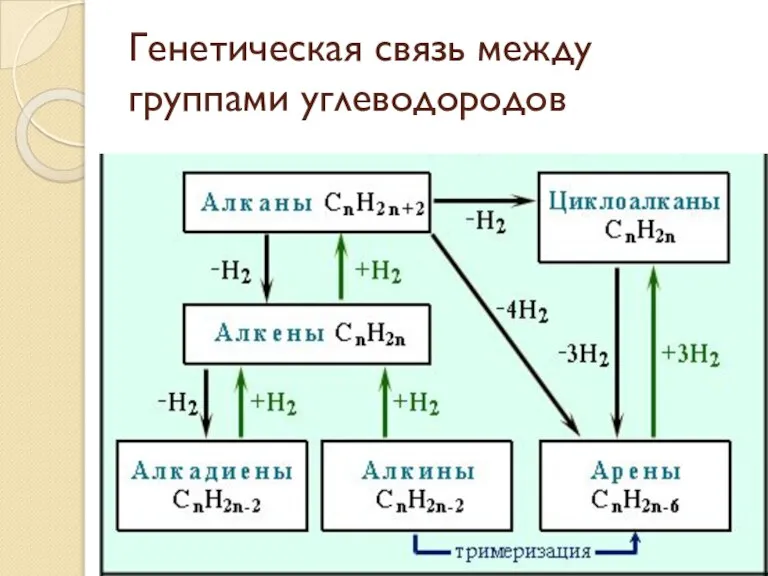
- 39. Генетическая связь между группами углеводородов
- 40. Непредельные углеводороды Непредельные углеводороды - это углеводороды, содержащие кратные связи в углеродном скелете молекулы. Кратными называются
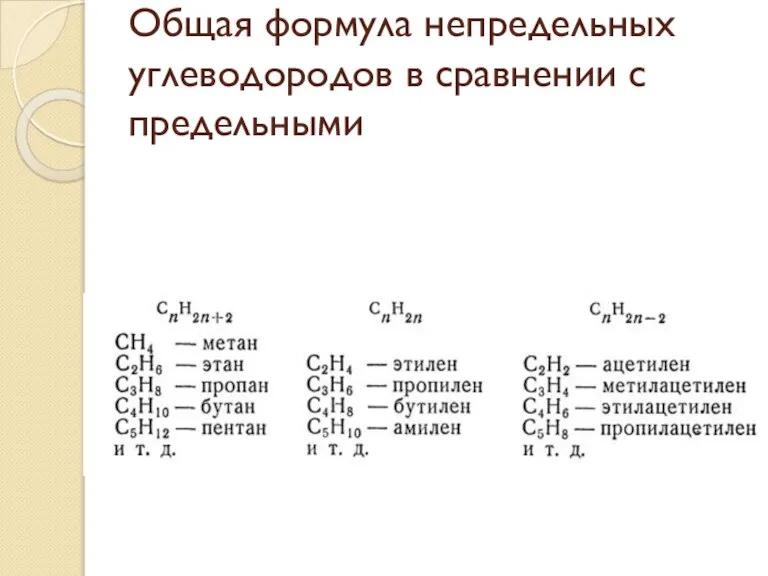
- 41. Общая формула непредельных углеводородов в сравнении с предельными
- 42. Определение алкенов Углеводородами ряда этилена, или этиленовыми углеводородами (олефинами или алкенами) называют ненасыщенные углеводороды, строение которых
- 43. Строение непредельных углеводородов Алкены CnH2n -одна двойная (- и -) связь Алкины CnH2n-2 - одна тройная
- 44. Изомерия непредельных углеводородов Структурная: изомерия углеродного скелета, изомерия положения заместителя или кратной связи. Пространственная (геометрическая или
- 45. Физические свойства алкенов С2 – С4 (газы) С5 – С18 (жидкости) С19 … – (твёрдые) Алкены
- 46. Химические свойства алкенов
- 47. Как и предельные углеводороды, алкены горят на воздухе: C2H4 + 3O2 t→ 2CO2 + 2H2O +
- 48. Получение алкенов 1. Действие спиртовых растворов едких щелочей на галогенпроизводные H3C-CH2-CH2BrH3C-CH=CH2+NaBr+H2O 2.Действие на спирты водоотнимающих средств
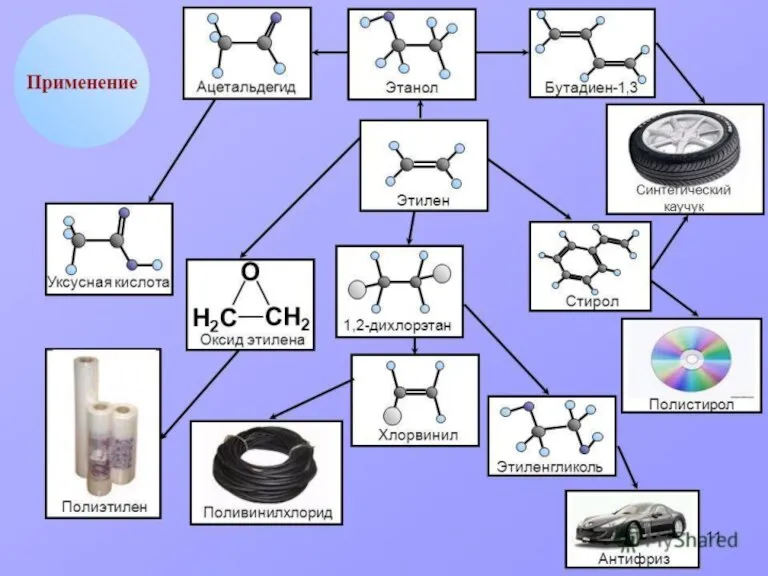
- 49. Применение этилена Этилен является одним из базовых продуктов промышленной химии и стоит в основании ряда цепочек
- 50. Применение этилена (2 часть) Этилен - исходное соединение для получения полиэтилена высокого и низкого давления и
- 51. Применение этилена (3 часть) Этилен применяют как исходный материал для производства ацетальдегида и синтетического этилового спирта.
- 52. Применение этилена (4 часть) Этилен используют для ускорения созревания плодов — например, помидоров, дынь, апельсинов, мандаринов,
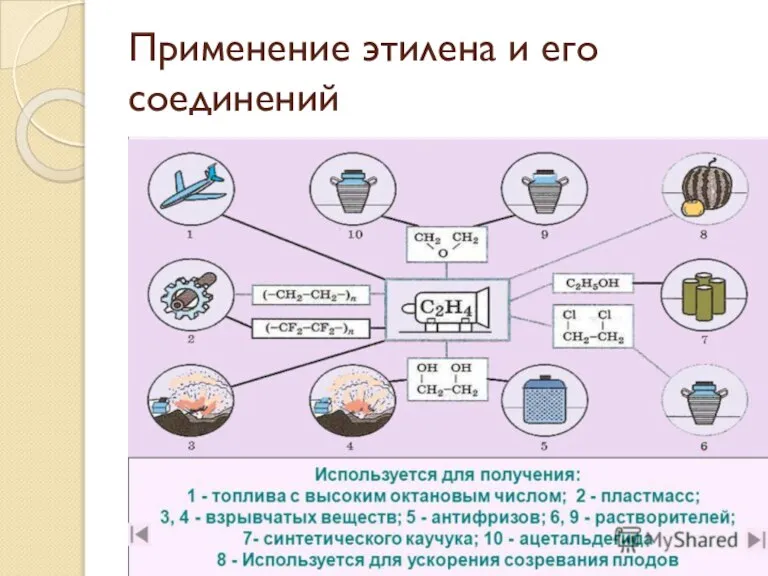
- 53. Применение этилена и его соединений
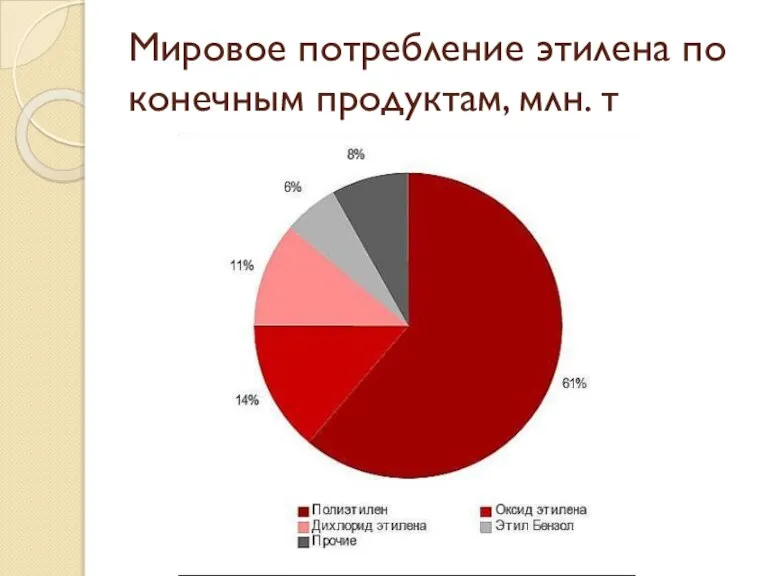
- 55. Мировое потребление этилена по конечным продуктам, млн. т
- 56. Ацетилен и ацетиленовые углеводороды (алкины)
- 57. Определение ацетиленовых углеводородов (алкинов) Ацетиленовыми углеводородами (алкинами) называются непредельные (ненасыщенные) углеводороды, содержащие в молекуле одну тройную
- 58. Ацетилен С2Н2 – Ацетилен – бесцветный газ, легче воздуха, мало растворим в воде, в чистом виде
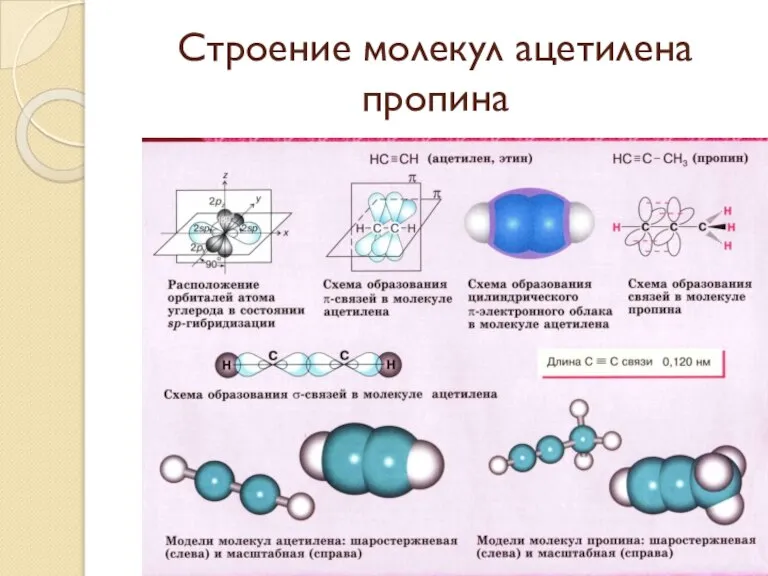
- 59. Строение молекул ацетилена пропина
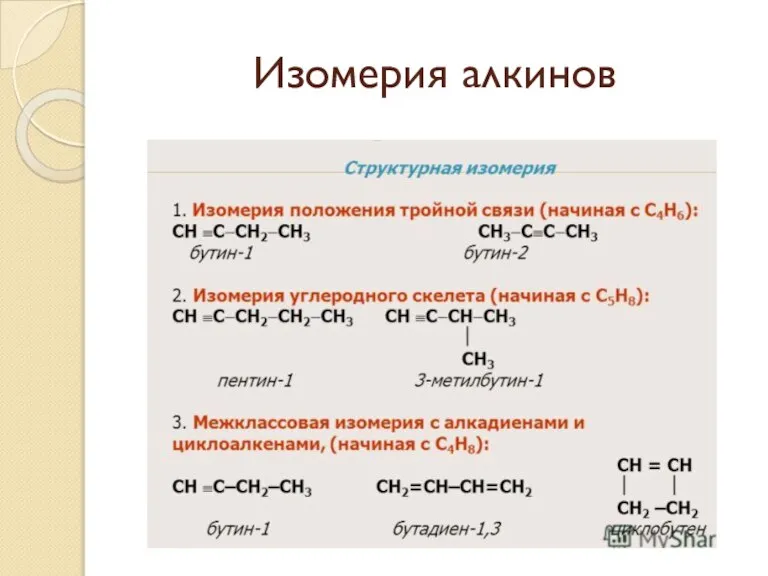
- 60. Изомерия алкинов
- 61. Физические свойства ацетилена С2Н2 – газ без цвета и почти без запаха, технический ацетилен обладает неприятным
- 62. Химические свойства алкинов 1.Присоединение галогенов 2.Присоединение водорода 3.Присоединение галогенводородов 4.Присоединение воды 5.Присоединение спиртов 6.Присоединение кислот 7.Присоединение
- 63. Свойства гомологов Свойства гомологов изменяются аналогично алкенам. По физическим свойствам алкины напоминают алкены и алканы. Температуры
- 64. Изомерия алкинов
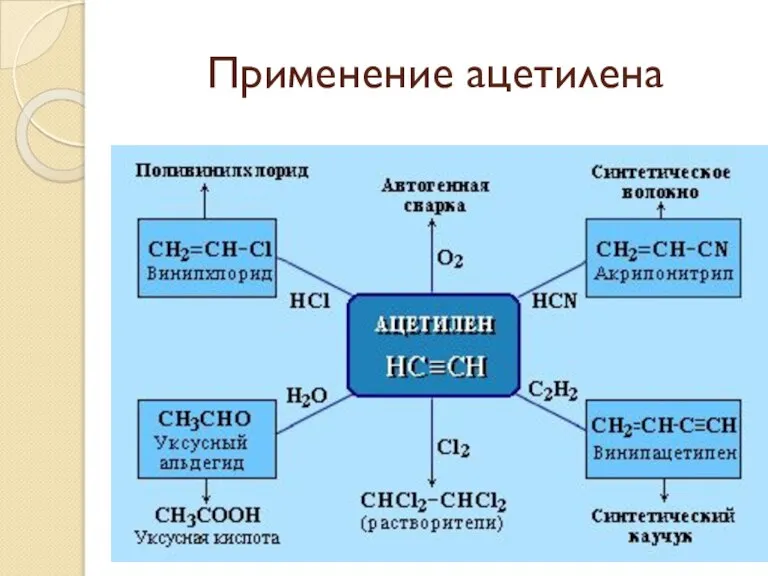
- 65. Применение ацетилена Из всех ацетиленовых углеводородов серьёзное промышленное значение имеет только ацетилен, который является важнейшим химическим
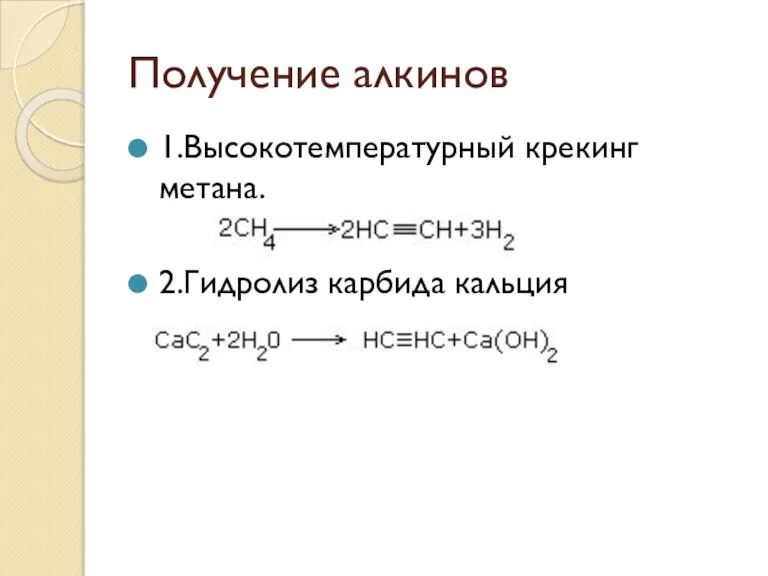
- 66. Получение алкинов 1.Высокотемпературный крекинг метана. 2.Гидролиз карбида кальция
- 67. Применение ацетилена
- 68. ДИЕНОВЫЕ УГЛЕВОДОРОДЫ (АЛКАДИЕНЫ) Диеновые углеводороды или алкадиены – это непредельные углеводороды, содержащие две двойные углерод -
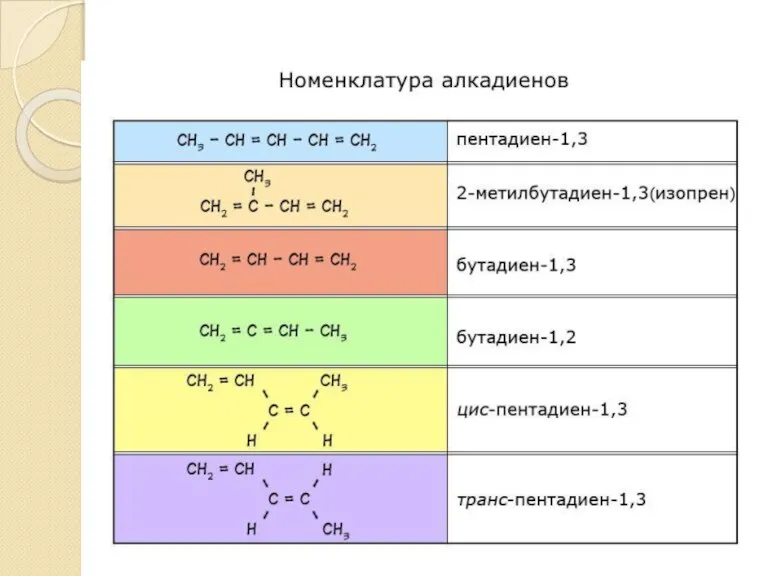
- 69. Алкадиены
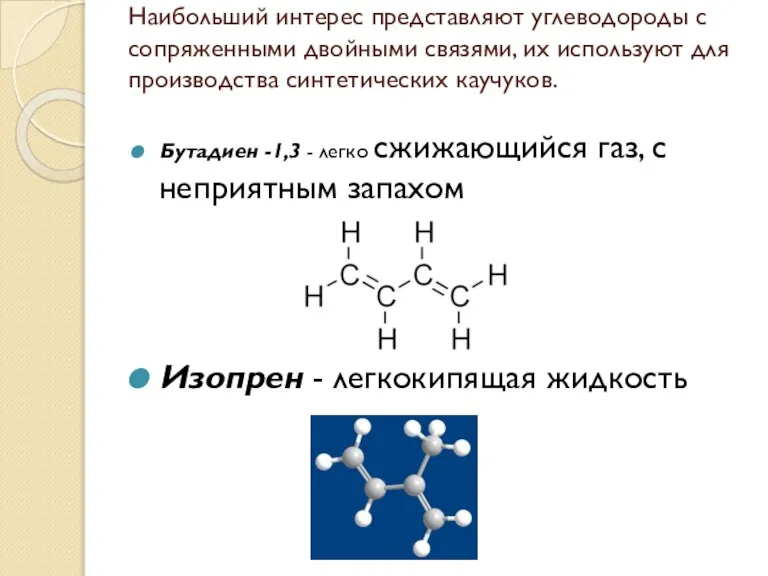
- 70. Наибольший интерес представляют углеводороды с сопряженными двойными связями, их используют для производства синтетических каучуков. Бутадиен -1,3
- 72. Физические свойства алкадиенов Бутадиен -1,3 – легко сжижающийся газ с неприятным запахом, t°пл.= -108,9°C, t°кип.= -4,5°C;
- 73. Химические свойства алкадиенов
- 74. Способы получения бутадиена Известно много способов получения бутадиена, но промышленное значение имеют лишь некоторые из них.
- 75. Первый способ получения бутадиена Способ получения бутадиена, являющегося исходным веществом ( мономером) для изготовления синтетического каучука,
- 76. Получение бутадиена из этилового спирта Этот способ получения бутадиена был осуществлен в СССР в промышленном масштабе.
- 78. Скачать презентацию



















































 Результаты независимой оценки учебных достижений обучающихся 5–8-х классов на примере регионального мониторинга по математике
Результаты независимой оценки учебных достижений обучающихся 5–8-х классов на примере регионального мониторинга по математике Красота родной природы пейзаж в графике
Красота родной природы пейзаж в графике Искусство шрифта. 7 класс
Искусство шрифта. 7 класс Взаимодействие Страховых Компаний и КМК Астана Моторс Расторгуев Денис Викторович Директор Департамента послепродажного
Взаимодействие Страховых Компаний и КМК Астана Моторс Расторгуев Денис Викторович Директор Департамента послепродажного  Апробация процедуры государственного контроля качества образования в образовательных учреждениях Санкт-Петербурга с использов
Апробация процедуры государственного контроля качества образования в образовательных учреждениях Санкт-Петербурга с использов РИНЦ для авторов
РИНЦ для авторов Море. Картины
Море. Картины Программный комплекс Rapid SCADA
Программный комплекс Rapid SCADA Служба образовательной деятельности и научно-методического сопровождения
Служба образовательной деятельности и научно-методического сопровождения Механизм внимания и его привлечения
Механизм внимания и его привлечения АЗБУКА БЕЗОПАСНОСТИ
АЗБУКА БЕЗОПАСНОСТИ Разходите на държавното обществено осигуряване през 2021 г
Разходите на държавното обществено осигуряване през 2021 г Выборы президента республики ЛЭКОН
Выборы президента республики ЛЭКОН Свистулька из веток
Свистулька из веток Гели-эликсиры Botolux
Гели-эликсиры Botolux Культура Западной и Центральной Европы
Культура Западной и Центральной Европы Реши задачи.
Реши задачи.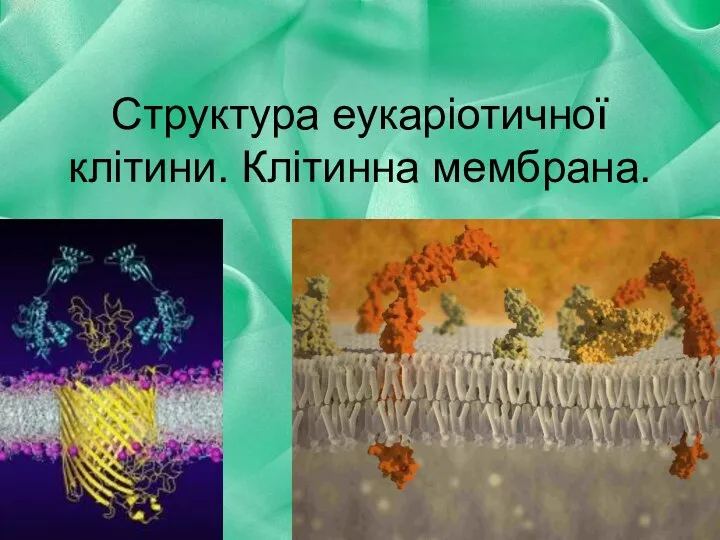 Урок 13-9.клітинна мембрана
Урок 13-9.клітинна мембрана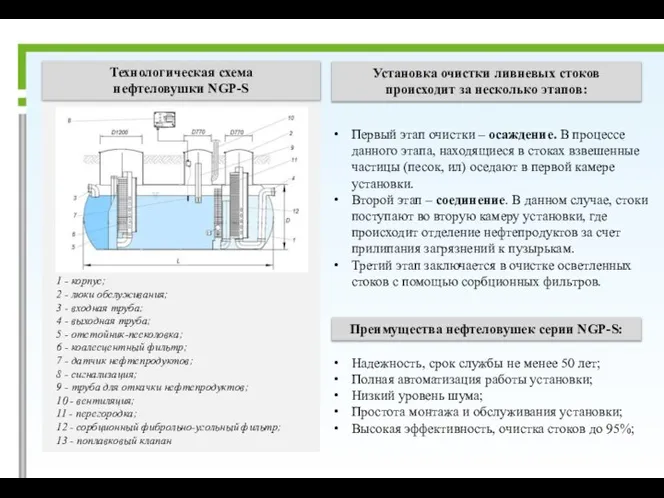 Технологическая схема нефтеловушки NGP-S
Технологическая схема нефтеловушки NGP-S Презентация на тему: Перевод с русского на русский
Презентация на тему: Перевод с русского на русский Цикл закупок проектов международных финансовых учреждений. Базовый обзор определения и оценки проектов
Цикл закупок проектов международных финансовых учреждений. Базовый обзор определения и оценки проектов Информационное моделирование
Информационное моделирование Первый снег
Первый снег Степень с целым отрицательным показателем (8 класс)
Степень с целым отрицательным показателем (8 класс) Параллельное расследование в зарубежных юрисдикциях
Параллельное расследование в зарубежных юрисдикциях Основные направления по формированию ИКТ-компетентности
Основные направления по формированию ИКТ-компетентности "праздник плуга".
"праздник плуга". Спутниковая связь
Спутниковая связь