Слайд 3Коррозия металлов
Введение
Химическая коррозия
Электрохимическая коррозия
Сущность процессов коррозии
Способы защиты от коррозии
Атмосферная коррозия стали
Ингибиторы коррозии

металлов
Слайд 4Введение
Слово коррозия происходит от латинского «corrodere», что означает разъедать. Хотя коррозию чаще

всего связывают с металлами, но ей подвергаются также камни, пластмассы и другие полимерные материалы и дерево. Например, в настоящее время мы являемся свидетелями большого беспокойства широких слоев людей в связи с тем, что от кислотных дождей катастрофически страдают памятники (здания и скульптуры), выполненные из известняка или мрамора.
Таким образом, коррозией называют самопроизвольный процесс разрушения материалов и изделий из них под химическим воздействием окружающей среды. Процессы физического разрушения к коррозии не относят, хотя часто они наносят не меньший вред памятникам культуры. Их называют истиранием, износом, эрозией.
Слайд 5Металлы составляют одну из основ цивилизации на планете Земля. Среди них как

конструкционный материал явно выделяется железо. Объем промышленного производства железа примерно в 20 раз больше, чем объем производства всех остальных металлов, вместе взятых. Широкое внедрение железа в промышленное строительство и транспорт произошло на рубеже XVIII...XIX вв. В это время появился первый чугунный мост, спущено на воду первое судно, корпус которого был изготовлен из стали, созданы первые железные дороги. Однако начало практического использования человеком железа относят к IX в. до н.э. Именно в этот период человечество из бронзового века перешло в век железный. Тем не менее история свидетельствует о том, что изделия из железа были известны в Хеттском царстве (государство Малой Азии), а его расцвет относят к XIV...XIII вв. до н.э.
Слайд 6В природе, хотя и очень редко, но встречается самородное железо. Его происхождение

считают метеоритным, т.е. космическим, а не земным. Поэтому первые изделия из железа (они изготавливались из самородков) ценились очень высоко – гораздо выше, чем из серебра и даже золота.
Слайд 7Несмотря на широкое внедрение в нашу сегодняшнюю жизнь полимерных материалов, стекла, керамики,

основным конструкционным материалом продолжает оставаться железо и сплавы на его основе. С изделиями из железа мы на каждом шагу встречаемся в быту и знаем, как много хлопот доставляют его ржавление и сама ржавчина. Ржавлением называют только коррозию железа и его сплавов. Другие металлы коррозируют, но не ржавеют. Хотя коррозируют практически все металлы, в повседневной жизни человек чаще всего сталкивается с коррозией железа.
Слайд 8Химическая коррозия
Химическую коррозию стали вызывают сухие газы и жидкости, не
имеющие характера электролитов,

например органические соединения или
растворы неорганических веществ в органических растворителях, Химическая
коррозия не сопровождается возникновением электрического тока. Она основана
на реакции между металлом и агрессивным реагентом. Этот вид коррозии
протекает в основном равномерно по всей поверхности металла. В связи с этим
химическая коррозия менее опасна, чем электрохимическая.
Слайд 9Продукты коррозии могут образовывать на поверхности металла плотный
защитный слой, затормаживающий её дальнейшее

развитие, или же пористый
слой, не защищающий поверхность от разрушающего воздействия среды. В
этом случае процесс коррозии продолжается до полного разрушения
материала или период времени пока будет действовать агрессивная среда.
Наиболее часто на практике встречается газовая коррозия
стали, вызванная воздействием О2 , SO2 , H2S, CI, НС1,
NO3 ,CO2 ,CO и H2 .
Слайд 10Электрохимическая коррозия
Электрохимическая коррозия происходит при взаимодействии металлов с
жидкими электролитами, в основном растворами

кислот, оснований и
солей. Механизм процесса коррозии зависит от структуры металла, а так же
от типа электролита. Сталь, как всякий металл, имеет кристаллическое
строение, при котором атомы располагаются в соответствующем порядке,
образуя характерную пространственную решетку. Кристаллы железа имеют
строение, значительно отличающиеся от идеальной схемы, так как имеются
пустоты, не занятые атомами металла, трещины, включения примесей к
газов .
Слайд 11Металлы обладают хорошей электропроводностью, что обусловлено
наличием свободных электронов, движение которых создает электрический
ток.

Числу свободных электронов соответствует эквивалентное число ион-
атомов, т.е. атомов, утративших один или более электрон. В случае
возникновения на концах металлического стержня разности потенциалов
электроны движутся от полюса с высшим потенциалом к противоположному
полюсу. Металлы, обладающие электронной проводимостью, являются
проводниками первого рода, а электролиты которые имеют ионную
проводимость проводниками второго рода.
Слайд 12В зависимости от типа и содержания растворённых в воде
солей изменению подвергаются не

только нормальные потенциалы, но даже
положение металла в ряду потенциалов.
Слайд 13Сущность процессов коррозии
Коррозия металлов чаще всего сводится к их окислению и превращению

в оксиды. В частности, коррозия железа может быть описана упрощенным уравнением
4Fe + 3O2 + 2H2О = 2Fe2O3·H2О
Гидратированный оксид железа Fе2O3·H2О и является тем, что люди называют ржавчиной. Это рыхлый порошок светло-коричневого цвета. Многие металлы при коррозии покрываются плотной, хорошо скрепленной с металлами оксидной пленкой, которая не позволяет кислороду воздуха и воде проникнуть в более глубокие слои и потому предохраняет металл от дальнейшего окисления. Например, алюминий – очень активный металл и теоретически с водой должен был бы взаимодействовать в соответствии с уравнением
2Al + 3H2О = Al2O3 + 3H2
Слайд 14Строго отделить химическую коррозию от электрохимической трудно, а иногда и невозможно. Дело

в том, что электрохимическая коррозия часто связана с наличием в металле случайных примесей или специально введенных легирующих добавок.
Слайд 15Способы защиты от коррозии
Проблема защиты металлов от коррозии возникла почти в самом

начале их использования. Люди пытались защитить металлы от атмосферного воздействия с помощью жира, масел, а позднее и покрытием другими металлами и прежде всего легкоплавким оловом (лужением). В трудах древнегреческого историка Геродота (V в. до н.э.) уже имеется упоминание о применении олова для защиты железа от коррозии.
Слайд 16Для защиты чугунных и стальных водяных труб от коррозии используют цементные покрытия.

Поскольку коэффициенты теплового расширения портландцемента и стали близки, а стоимость цемента невысокая, то он довольно широко применяется для этих целей. Недостаток портландцементных покрытий тот же, что и эмалевых, – высокая чувствительность к механическим ударам.
Слайд 17Широко распространенным способом защиты металлов от коррозии является покрытие их слоем других

металлов. Покрывающие металлы сами коррозируют с малой скоростью, так как покрываются плотной оксидной пленкой. Покрывающий слой наносят различными методами: кратковременным погружением в ванну с расплавленным металлом (горячее покрытие), электроосаждением из водных растворов электролитов (гальваническое покрытие), напылением (металлизация), обработкой порошками при повышенной температуре в специальном барабане (диффузионное покрытие), с помощью газофазной реакции, например 3CrCl2 + 2Fe – [1000°C] → 2FeCl3 + 3Cr (в сплаве с Fe).
Слайд 18Имеются и другие методы нанесения металлических покрытий, например, разновидностью диффузионного способа защиты

металлов является погружение изделий в расплав хлорида кальция CaCl2, в котором растворены наносимые металлы.
Слайд 19Атмосферная коррозия стали
Наиболее часто встречающимся на практике типом коррозии стали
является образование ржавчины

под влиянием атмосферных воздействий
(чаще всего кислорода и влажности), В сухом атмосферном воздухе сталь
практически не подвергается коррозии. Атмосферная коррозия носит
электрохимический характер, причем электролитом является слой влаги,
имеющийся на поверхности металла.
Слайд 20Протекание процессов коррозии в атмосферных условиях аналогично коррозии
стали в воде, содержащей кислород.

Продукты коррозии, покрывающие металл,
представляют собой гидра тированные окиси железа с составом, определяемым
формулой
Скорость атмосферной коррозии зависит от содержания влаги в воздухе.
Повышение относительной влажности воздуха до 70-75% приводит к сравнительно
небольшим потерям стали. При влажности, превышающей эти значения,
наблюдается интенсивное ускорение процессов коррозии .
Загрязнение воздуха агрессивными продуктами такими, как СО2, SО2, CI2,
H2S, дым и сажа, усиливает коррозию. Сталь, в течение нескольких лет
подвергавшаяся воздействию промышленной атмосферы, имеет значительно
большие потери, чем сталь в условиях сельской местности .
Слайд 21Ингибиторы
Применение ингибиторов – один из эффективных способов борьбы с коррозией металлов в

различных агрессивных средах (в атмосферных, в морской воде, в охлаждающих жидкостях и солевых растворах, в окислительных условиях и т.д.). Ингибиторы – это вещества, способные в малых количествах замедлять протекание химических процессов или останавливать их. Название ингибитор происходит от лат. inhibere, что означает сдерживать, останавливать. Ингибиторы взаимодействуют с промежуточными продуктами реакции или с активными центрами, на которых протекают химические превращения. Они весьма специфичны для каждой группы химических реакций. Коррозия металлов – это лишь один из типов химических реакций, которые поддаются действию ингибиторов. По современным представлениям защитное действие ингибиторов связано с их адсорбцией на поверхности металлов и торможением анодных и катодных процессов.
Слайд 22Первые ингибиторы были найдены случайно, опытным путем, и часто становились клановым секретом.

Известно, что дамасские мастера для снятия окалины и ржавчины пользовались растворами серной кислоты с добавками пивных дрожжей, муки, крахмала. Эти примеси были одними из первых ингибиторов. Они не позволяли кислоте действовать на оружейный металл, в результате чего растворялись лишь окалина и ржавчина.





















 Оптические иллюзии
Оптические иллюзии Северо-западный экономический район
Северо-западный экономический район Презентация на тему Альтернативные источники энергии С точки зрения географии
Презентация на тему Альтернативные источники энергии С точки зрения географии  Металлообрабатывающие станки
Металлообрабатывающие станки Построение бизнес-моделей
Построение бизнес-моделей SENSOR+TEST 2009 ВЫСТАВКА ИЗМЕРИТЕЛЬНОЙ ТЕХНИКИ The Measurement Fair Нюрнберг, Германия 26 – 28 мая 2009
SENSOR+TEST 2009 ВЫСТАВКА ИЗМЕРИТЕЛЬНОЙ ТЕХНИКИ The Measurement Fair Нюрнберг, Германия 26 – 28 мая 2009 Управление Федерального казначейства по г. Санкт-Петербургу
Управление Федерального казначейства по г. Санкт-Петербургу давл тв тел
давл тв тел Проект по технологии РАЗДЕЛОЧНАЯ ДОСКА
Проект по технологии РАЗДЕЛОЧНАЯ ДОСКА Семь бед – один ответ
Семь бед – один ответ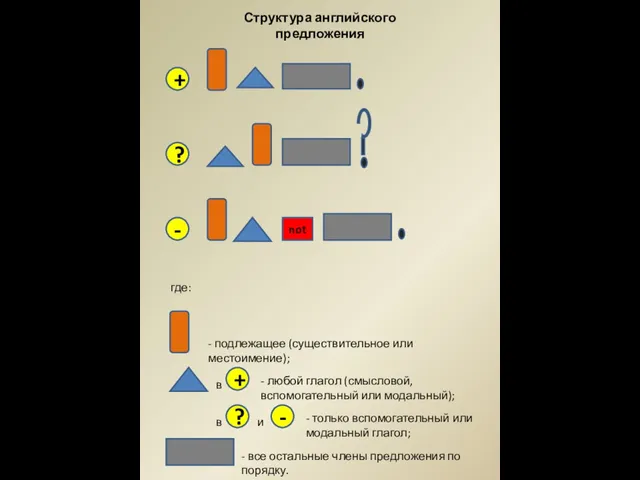 Структура английского предложения
Структура английского предложения Главная книга страны – Конституция Российской Федерации
Главная книга страны – Конституция Российской Федерации Основание Санкт-Петербурга
Основание Санкт-Петербурга Вітання з нагоди професійного свята!
Вітання з нагоди професійного свята! Цветотипы
Цветотипы ЛР № 2 7класс
ЛР № 2 7класс Политические режимы
Политические режимы Рецепты салатов из сырых овощей
Рецепты салатов из сырых овощей Таможенные сборы
Таможенные сборы Презентация на тему Фазиль Абдулович Искандер
Презентация на тему Фазиль Абдулович Искандер  Общежитие №3
Общежитие №3 Наша Родина на карте мира.
Наша Родина на карте мира. Аргентина (7 класс)
Аргентина (7 класс)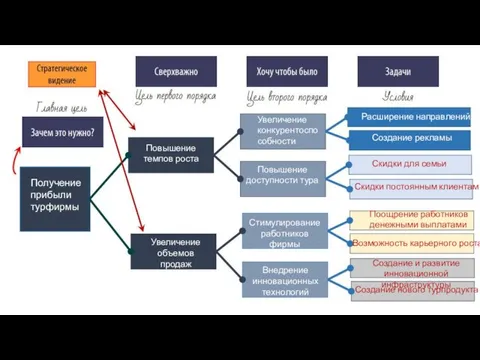 Стратегическое видение. Получение прибыли турфирмы
Стратегическое видение. Получение прибыли турфирмы Государственный строй Ногайской Орды
Государственный строй Ногайской Орды Презентация на тему История денежных знаков России
Презентация на тему История денежных знаков России  Происхождение жизни на земле
Происхождение жизни на земле Агентство маркетинговых исследований
Агентство маркетинговых исследований