Слайд 2Цель работы.
Цель работы:
Изучить процессы коррозии металлов, в зависимости от различных условий.

Провести классификацию коррозии.
Рассмотреть, какие способы защиты металлов наиболее эффективны.
Объяснить применение этого явления металлов в очень важных исторических событиях
Слайд 3 Экспериментальная часть исследовательской работы.
Цель экспериментальной части.
1) Изучить химическую сущность процесса

коррозии.
2) Исследовать какие факторы определяют протекание
коррозии,
3) Изучить действия антикоррозийных способов защиты
металлов, выяснить действие ингибитора в процессе
коррозии,
4) Выяснить влияние электролитов на процесс коррозии.
Слайд 6Выводы экспериментальной части.
скорость коррозии загрязнённого металла выше чем скорость коррозии чистого металла
на

скорость разрушения влияет однородность поверхности металла, металл с шероховатой поверхностью будет разрушаться быстрее.
в случае покрытия железа более активным металлом коррозия железа не наблюдается, а в случае покрытия менее активным металлом скорость химического процесса становится выше.
скорость коррозии зависит от активности металла.
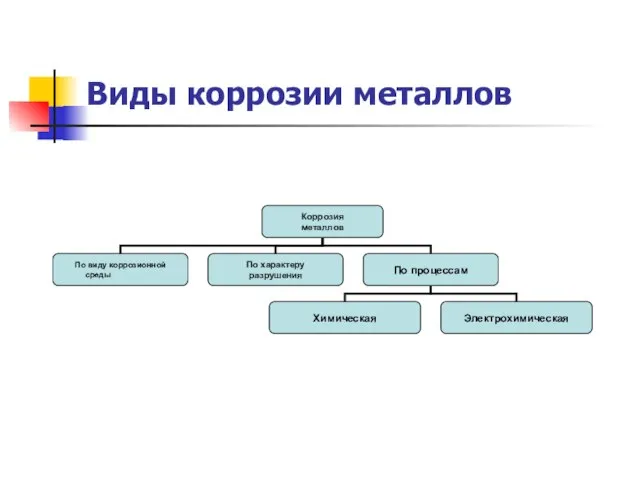
Слайд 8Электрохимическая коррозия
Это такая коррозия, в результате которой наряду с химическими процессами (отдача

электронов атомами коррозируемого металла — процесс окисления) протекают электрические (перенос электронов от одного участка изделия к другому).
Слайд 9 Химическая коррозия
Кислородная коррозия стали
связана с образованием
оксидной пленки,
состоящей

из
FeO, Fe2O3, Fe3O4.
Слайд 10Классификация коррозии по виду коррозионной среды
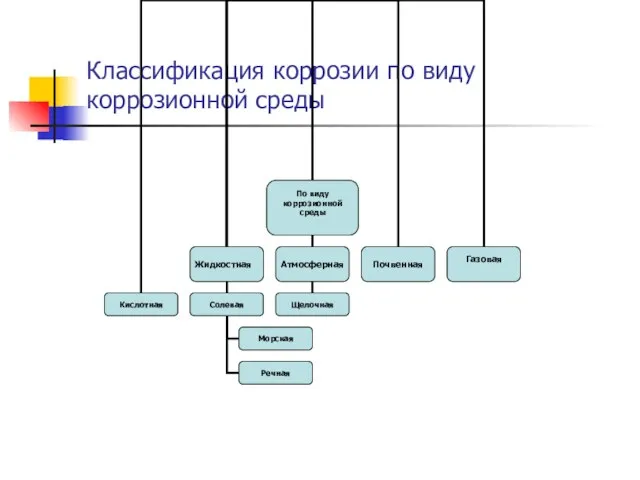
Слайд 11 Классификация
коррозии по характеру разрушения
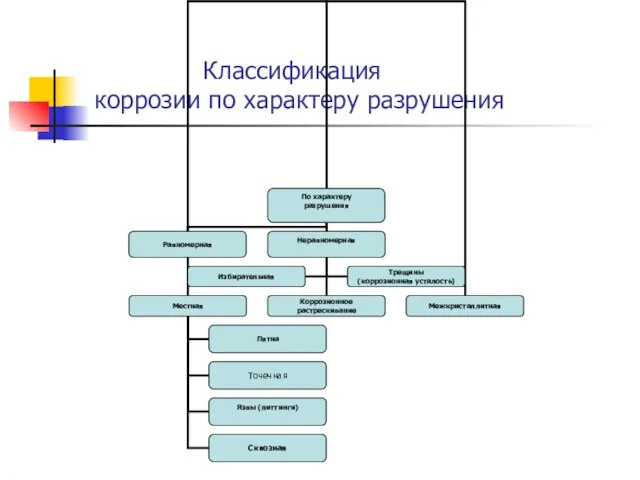
Слайд 134. Первый коррозионист Фемистокл
500 - 449 годы до н. э.
Еще

древние столкнулись с обрастанием подводной части морских судов - отложением толстых (до 30 - 40 см) слоев, образованных поселениями водных организмов-обрастателей . Из-за обрастания корабли резко (на 30 - 40 %) теряли скорость хода. Эмпирически было найдено средство против обрастания - медная обшивка. Сейчас механизм действия такой защиты нам предельно ясен: в морскую воду переходят ионы меди, которые токсичны для большинства обрастателей.
Фемистокл предлагает способ защиты от контактной коррозии железных гвоздей в медной обшивке. По его указанию при строительстве судов гвозди предварительно погружали в расплавленный свинец. Освинцованные, они значительно лучше и надежнее держали обшивку.
350 легких греческих трирем, которые отличались быстротой хода нанесли поражение превосходящим силам противника: персидский флот насчитывал свыше 800 , значительно более тяжело вооруженных и крупных кораблей.
Слайд 14Сражение латунных трубок
31 мая 1916 г. встретились две гигантские армады Великобритании

и Германии. По грубому счету потопленных кораблей сражение закончилось «вничью». Немецкие адмиралы решили вывести свои корабли из сражения.
Все попытки англичан догнать флот противника из-за значительно большей быстроходности и маневренности немецких судов.
Британские корабли не могли развивать полной мощности — значительная часть латунных конденсаторных трубок вышла из строя из-за коррозии.
В начале XX века немецкие металлурги установили, что присадка олова замедляет обесцинкование. В 1912 г. в глубокой тайне в Германии был начат выпуск конденсаторных трубок из так называемой морской латуни.Именно этому сплаву и обязан был германский флот благополучным исходом сражения.
В 1929 г. английские коррозионисты нашли еще более эффективный способ защиты а-латуни от обесцинкования — небольшими (0,01—0,04 %) добавками мышьяка, фосфора, сурьмы; они создали новый сплав — «адмиралтейскую» латунь, содержащую 29 % цинка, 1 % олова и 0,02—0,04 % мышьяка.












 Конструирование Тема: «Лазерный светотелефон»
Конструирование Тема: «Лазерный светотелефон» Подготовка финансовых отчетов и исполнение налоговых обязательств
Подготовка финансовых отчетов и исполнение налоговых обязательств Многообразие клеток
Многообразие клеток Образовательная программа дошкольного образования
Образовательная программа дошкольного образования Команда 9 Бизнесмены
Команда 9 Бизнесмены Знай правила движения! 4 класс
Знай правила движения! 4 класс XXXIX расширенное заседание коллегии Министерства транспорта и дорожного хозяйства Республики Татарстан
XXXIX расширенное заседание коллегии Министерства транспорта и дорожного хозяйства Республики Татарстан Класификация типов запросов и ее влияние на стратегию продвижения сайтов
Класификация типов запросов и ее влияние на стратегию продвижения сайтов Лаборатория Бионанофизики представляет уникальный проект
Лаборатория Бионанофизики представляет уникальный проект Истоки холодной войны. Военно-политические блоки
Истоки холодной войны. Военно-политические блоки Музыка ландшафта
Музыка ландшафта Бренды. Вещи. Люди
Бренды. Вещи. Люди Церковь Иль-Джезу
Церковь Иль-Джезу Школа костюма
Школа костюма Презентация на тему Планеты солнечной системы Сатурн
Презентация на тему Планеты солнечной системы Сатурн  Пушкин в Михайловском
Пушкин в Михайловском Национально – государственное устройство
Национально – государственное устройство Христианская семья. 2 урок
Христианская семья. 2 урок Триединая цель урока
Триединая цель урока ДЕТИ и ДЕНЬГИ
ДЕТИ и ДЕНЬГИ Презентация на тему What would you like to see in the USA
Презентация на тему What would you like to see in the USA Basic Concepts of Real Estate Marketability Analysis
Basic Concepts of Real Estate Marketability Analysis Природа в стихах русских поэтов
Природа в стихах русских поэтов К нам пришел гость Много бед таят леса. Волк, медведь там и лиса! Наш зверек живет в тревоге, От беды уносит ноги... Ну-ка, быстро отгад
К нам пришел гость Много бед таят леса. Волк, медведь там и лиса! Наш зверек живет в тревоге, От беды уносит ноги... Ну-ка, быстро отгад Российские нобелевские лауреаты в области физики
Российские нобелевские лауреаты в области физики Правовые основы природопользования и охраны окружающей среды
Правовые основы природопользования и охраны окружающей среды Питание –необходимое условие для жизни человека
Питание –необходимое условие для жизни человека Порядок приема и учета замечаний к промежуточным отчетным документам
Порядок приема и учета замечаний к промежуточным отчетным документам